文档内容
期中考测试(提升)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2023·黑龙江鹤岗 )下列各组离子在给定条件下一定能大量共存的是
A.无色溶液:Na+、Cu2+、Cl−、
B.加入锌生成氢气的溶液: 、Fe3+、 、
C.遇酚酞变红的溶液:Na+、K+、 、
D.加酚酞显红色的溶液:K+、H+、 、
2.(2023秋·云南曲靖 )下列各组内的离子,在溶液中能大量共存的是
A.H+、Ba2+、SO 、NO B.H+、OH-、Cl-、SO
C.Na+、Ca2+、Mg2+、Cl- D.NH 、Ba2+、OH-、NO
3.(2023·广西 )下列反应既是离子反应,又是氧化还原反应的是
A.实验室用KMnO 制O B.工业上用C还原Fe O
4 2 2 3
C.NaOH和稀H SO 反应 D.Na和盐酸反应
2 4
4.(2022秋·江西抚州·高一统考学业考试)配制80mL NaOH溶液的操作如图所示。下列说法正
确的是A.操作1前需称取3.2g NaOH B.操作1固体溶解后立即进行操作2
C.操作3和操作5分别为转移和摇匀 D.操作4俯视刻度线定容会使所配溶液浓度偏高
5.(2023·河南信阳 )FeCl 溶液、Fe(OH) 胶体和Fe(OH) 浊液是重要的分散系。下列叙述中不正确的是
3 3 3
A.三种分散系中分散质粒子的直径:Fe(OH) 浊液>Fe(OH) 胶体>FeCl 溶液
3 3 3
B.可通过过滤的方式从Fe(OH) 浊液中分离Fe(OH)
3 3
C.Fe(OH) 胶体区别于其他分散系的本质特征是丁达尔效应
3
D.Fe(OH) 胶体中逐滴滴入HI溶液至过量,最终可以得到棕色溶液
3
6.(2023·辽宁大连 )下列关于Na的化合物之间转化反应的离子方程式书写不正确的是
A.碱转化为酸式盐:OH-+CO +H O =
2 2
B.碱转化为两种盐:2OH-+Cl =ClO-+Cl-+H O
2 2
C.过氧化物转化为碱:2 +2H O=4OH-+O ↑
2 2
D.正盐转化酸式盐:2Na+ + +CO +H O=NaHCO ↓
2 2 3
7.(2023春·云南大理·高一大理市大理第一中学校考阶段练习)将0.015mol四氧化三铁完全溶解在
100mL1mol/L硫酸中,然后加K Cr O 溶液25mL,恰好使溶液中Fe2+全部转为Fe3+,Cr O 全部转化为Cr3+,
2 2 7 2
则K Cr O 溶液物质的量浓度是
2 2 7
A.0.05mol/L B.0.3mol/L C.0.2mol/L D.0.1mol/L
8.(2023秋·云南曲靖·高一会泽县实验高级中学校校考开学考试)电视节目《中国诗词大会》显示了中国
传统文化的博大精深,下列诗词中涉及化学变化的是
A.八月秋高风怒号,卷我屋上三重茅 B.梅须逊雪三分白,雪却输梅一段香
C.无边落木萧萧下,不尽长江滚滚来 D.千锤万出深山,烈火焚烧若等闲
9.(2022秋·河南信阳·高一信阳高中校考阶段练习)在复杂的体系中,确认化学反应先后顺序有利于解决
问题,下列化学反应先后顺序判断正确的是A.在含 、 、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、 、
B.含等量的FeBr 、FeI 的溶液中,缓慢通入氯气:I-、Br-、Fe2+
2 2
C.含等量的Ba(OH) 、KOH的溶液中,缓慢通入CO :KOH、Ba(OH)
2 2 2
D.在含Fe3+、H+、 的溶液中逐滴加入烧碱溶液:H+、Fe3+、
10.(2023·江苏盐城 )实验室制氯气,既可用浓盐酸与MnO 在加热条件下反应,又可用浓盐酸与KClO
2 3
直接反应制取。关于氯气的制取,下列说法正确的是
A.在浓盐酸中加入足量的二氧化锰,充分加热后HCl能完全反应
B.实验室制取法中HCl只做还原剂
C.浓盐酸与KClO 直接反应,氯气只是氧化产物
3
D.实验室制取法中KClO 、MnO 均为氧化剂
3 2
11.(2023春·云南大理·高一大理市大理第一中学校考阶段练习)设N 为阿伏伽德罗常数的值,下列说法
A
正确的是
A.标准状况下,11.2L四氯化碳中含有的分子数0.5N
A
B.常温常压下,18.0g水所含的电子数为10N
A
C.300mL0.1mol/L的NaCl溶液含有0.03N 个NaCl分子
A
D.密闭容器内投入2molSO 和1molO ,一定条件下充分反应后SO 的分子数为2N
2 2 3 A
12.(2022秋·浙江宁波·高一宁波市同济中学校联考期中)下列对实验操作分析错误的是
A.配制0.1mol·L-1 NaCl溶液时,若没有洗涤烧杯和玻璃棒,则所得溶液物质的量浓度偏低
B.NH NO 溶解吸热,若配制0.5mol·L-1 NH NO 溶液时直接将溶解后的溶液转移到容量瓶中,则所得
4 3 4 3
溶液的物质的量浓度偏低
C.配制一定物质的量浓度溶液时,若所用砝码放在左盘,则所得溶液的物质的量浓度一定偏低
D.配制一定物质的量浓度溶液时,若定容中不小心加水超过刻度线,立刻将超出的水吸出,则所得溶
液的物质的量浓度偏低
13.(2023·河南信阳 )高锰酸钾(KMnO )是一种常用的氧化剂。不同条件下高锰酸钾可发生如下反应:
4+5e-+8H+→Mn2++4H O; +3e-+2H O→MnO +4OH-; +e-→ 。高锰酸钾溶液与硫化亚铁
2 2 2
有如下反应:FeS+KMnO +H SO →K SO +MnSO +Fe (SO ) +S+H O(未配平)。下列有关说法正确的是
4 2 4 2 4 4 2 4 3 2
A.由上面的反应可知,高锰酸根离子( )反应后的产物与溶液的酸碱性有关
B.高锰酸钾可代替二氧化锰用来制取Cl ,氧化剂和还原剂物质的量之比为1∶8
2
C.在高锰酸钾溶液与硫化亚铁的反应中,将硫酸换成浓盐酸,对反应不影响
D.高锰酸钾溶液也可与H O 溶液发生反应,其中H O 是氧化剂
2 2 2 2
14.(2023·黑龙江鹤岗 )已知 溶液与NaCl溶液混合无现象, 溶液与盐酸混合可发生反应:
,下列说法不正确的是
A.反应中每生成1个Cl ,转移2个电子
2
B.反应中氧化剂与还原剂个数之比为1:5
C.向 和NaCl混合溶液中滴加稀硫酸也能生成
D.反应 可以发生
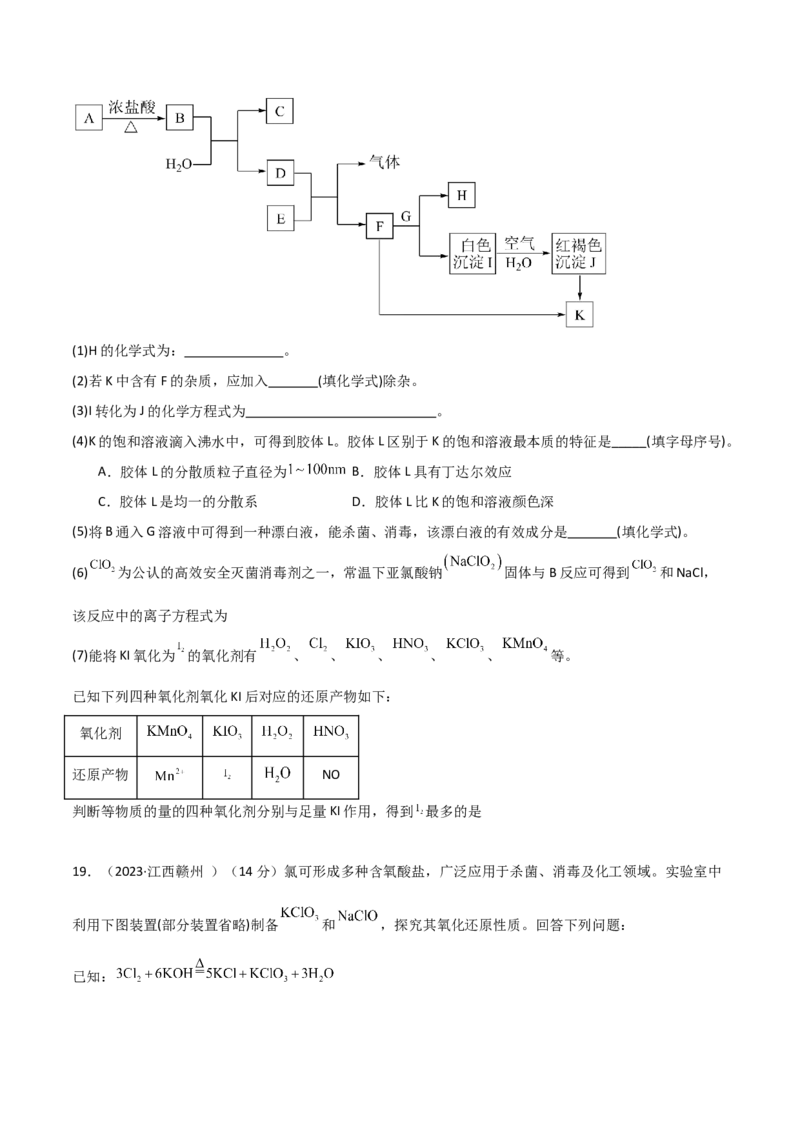
15.(2023秋·甘肃酒泉·高一统考期末)某化学小组欲通过测定混合气体中 的含量来计算 已变质的
样品中 的含量。实验装置如下图( 为弹性良好的气囊)。已知:①过氧化钠与硫酸反应的总化学方程式为:
②忽略气体在I和IV中的溶解。下列说法正确的是
A.b的作用是为了除去气体中的 ,故b中应装有无水
B.测定气体总体积必须关闭 ,打开
C.量筒I用于测量产生气体的 体积,量筒II用于测量产生氧气的体积
D.若量筒II收集的气体折算为标准状况下是 ,则 已变质的样品中的 质量为
16.(2023春·湖南长沙·高一校联考阶段练习)向FeI 、FeBr 的混合溶液中通入适量氯气,溶液中某些离
2 2
子的物质的量变化情况如图所示。则下列说法中正确的是
A.还原性:I-<Fe2+<Br-
B.原混合溶液中Br-的物质的量为4mol
C.线段BC表示Cl-的物质的量变化
D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
二、非选择题:共56分。
17.(2023·江西赣州)(14分)回答下列问题:
Ⅰ.某学校实验室从化学试剂商店买回的浓度为 的浓硫酸。现用该浓酸硫配制
的稀硫酸。可供选用的仪器有:①胶头滴管;②烧杯;③玻璃棒;④药匙;⑤量筒;⑥托盘天平。请回答
下列问题:
(1)配制稀硫酸时,还缺少的仪器有 。
(2)经计算,配制上述的稀硫酸需要用量筒量取上述浓硫酸的体积为 mL,量取硫酸时应选用
规格的量筒;A.10mL B.50mL C.100mL D.200mL
(3)在烧杯中稀释浓硫酸的实验操作为 。
(4)对所配制的稀硫酸进行测定,发现其浓度大于 ,配制过程中下列各项操作可能引起该误差的原
因 。
①用量筒量取浓硫酸时,仰视刻度线
②容量瓶用蒸馏水洗涤后未经干燥
③将稀释后的稀硫酸立即转入容量瓶后,立即进行后面的实验操作
④定容后,把容量瓶倒置摇匀,正放后发现液面低于刻度线,又补充几滴水至刻度处
Ⅱ.海水中含有大量 、 、等物质,在 由 、 、组成的混合液中,部分离子浓度
大小如下图所示(不考虑溶液中 和 浓度)。请回答下列问题:
(5)该混合液中 的物质的量为 mol。
18.(2023秋·辽宁沈阳·高一校联考期末)(14分)高中化学课本必修一中出现的部分物质间的转化关系
如图所示(部分物质已省略。已知 是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完
成下列填空。(1)H的化学式为: 。
(2)若K中含有F的杂质,应加入 (填化学式)除杂。
(3)I转化为J的化学方程式为 。
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_____(填字母序号)。
A.胶体L的分散质粒子直径为 B.胶体L具有丁达尔效应
C.胶体L是均一的分散系 D.胶体L比K的饱和溶液颜色深
(5)将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是 (填化学式)。
(6) 为公认的高效安全灭菌消毒剂之一,常温下亚氯酸钠 固体与B反应可得到 和NaCl,
该反应中的离子方程式为
(7)能将KI氧化为 的氧化剂有 、 、 、 、 、 等。
已知下列四种氧化剂氧化KI后对应的还原产物如下:
氧化剂
还原产物 NO
判断等物质的量的四种氧化剂分别与足量KI作用,得到 最多的是
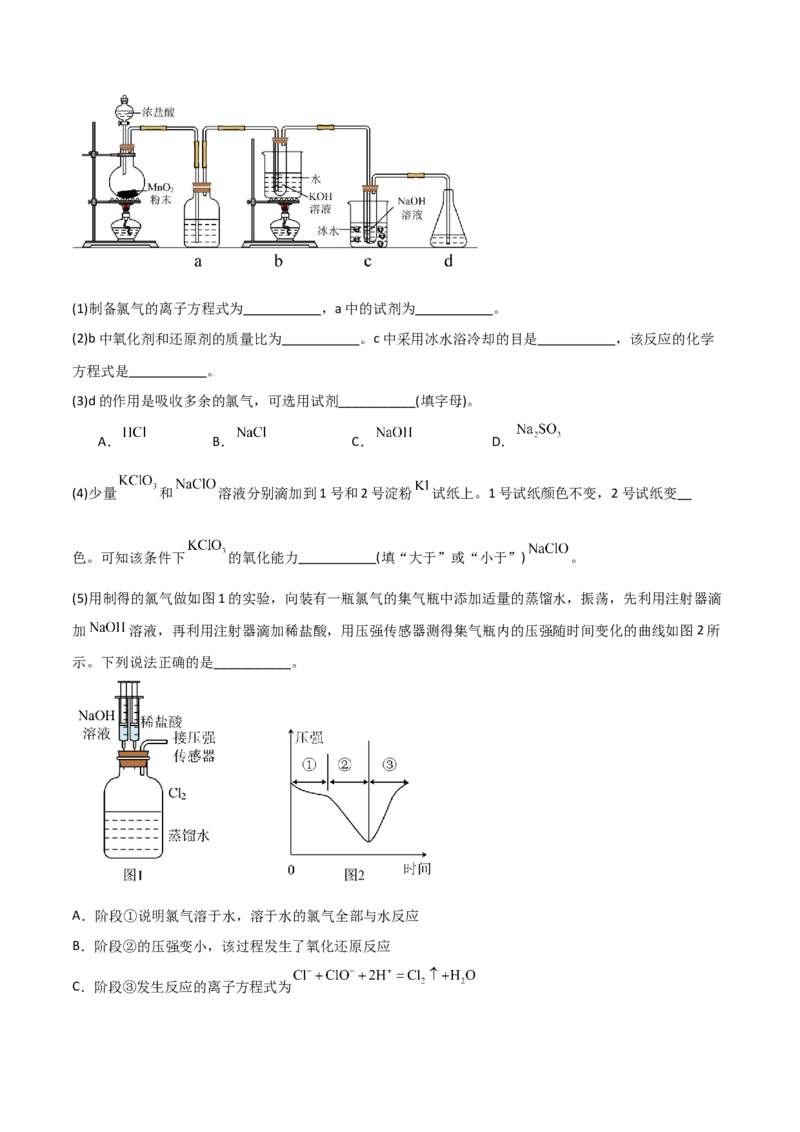
19.(2023·江西赣州 )(14分)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中
利用下图装置(部分装置省略)制备 和 ,探究其氧化还原性质。回答下列问题:
已知:(1)制备氯气的离子方程式为 ,a中的试剂为 。
(2)b中氧化剂和还原剂的质量比为 。c中采用冰水浴冷却的目是 ,该反应的化学
方程式是 。
(3)d的作用是吸收多余的氯气,可选用试剂___________(填字母)。
A. B. C. D.
(4)少量 和 溶液分别滴加到1号和2号淀粉 试纸上。1号试纸颜色不变,2号试纸变
色。可知该条件下 的氧化能力 (填“大于”或“小于”) 。
(5)用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴
加 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所
示。下列说法正确的是___________。
A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段②的压强变小,该过程发生了氧化还原反应
C.阶段③发生反应的离子方程式为D.若将 换成 ,所得的压强变化趋势与图2相似
20.(2023秋·云南曲靖·高一会泽县实验高级中学校校考开学考试)(14分)过氧化钠(Na O )可以作供氧
2 2
剂,某学习小组的同学对过氧化钠的性质进行如下探究。
【查阅资料】
①Na O 是一种淡黄色固体,能与CO 发生反应生成一种气体和另一种物质;
2 2 2
② ;
③NH Cl溶液呈酸性。
4
【探究一】二氧化碳与过氧化钠反应生成的气体。
设计收集生成气体的实验装置如图所示(图中铁架台未画出)。
(1)B中氢氧化钠溶液的作用是 ,当观察到C中澄清石灰水不变浑浊,说明二氧化碳已经除尽。写出
澄清石灰水中溶质的化学式 。
(2)检验气体:将带火星的小木条伸入收集气体的D中,发现木条复燃,证明二氧化碳与过氧化钠反应生成
的气体是 。
【探究二】二氧化碳与过氧化钠反应生成的另一种物质。
【猜想与假设】对反应生成的另一种物质提出了3种猜想。
猜想一:是氢氧化钠
猜想二:是碳酸钠
猜想三:是碳酸氢钠
(3)同学们对反应物中有关元素的组成分析,一致认为猜想一和猜想三不正确的,理由是 。
【进行实验】
(4)排除错误猜想后通过以下实验验证了另一种物质,完成实验报告。
实验操作 实验现象 实验结论
用试管取少量CO 与Na O 反应后的固体溶于蒸馏水中,加入 溶 产生 猜想二正
2 2 2液,振荡,观察现象。 。 确。
【交流反思】
(5)若向NH Cl溶液中加入一定量的Na O ,充分反应,产生的气体有 (填化学式)。
4 2 2