文档内容
化学反应与热能
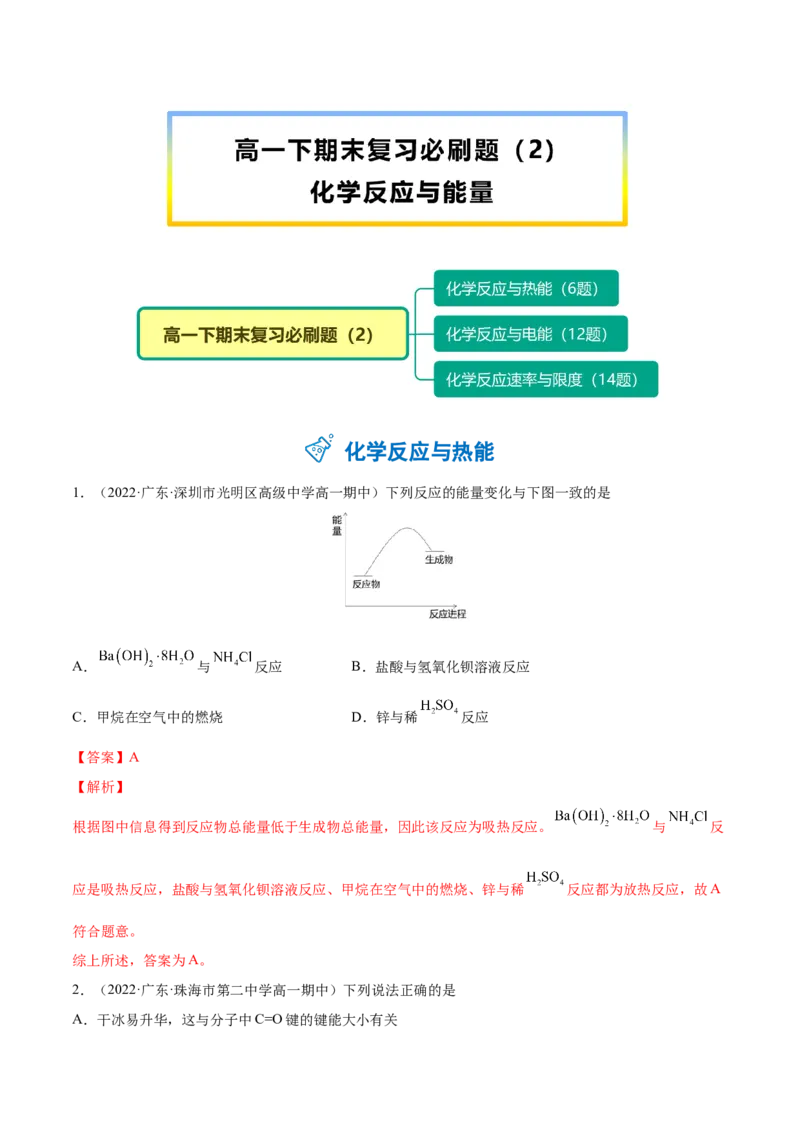
1.(2022·广东·深圳市光明区高级中学高一期中)下列反应的能量变化与下图一致的是
A. 与 反应 B.盐酸与氢氧化钡溶液反应
C.甲烷在空气中的燃烧 D.锌与稀 反应
【答案】A
【解析】
根据图中信息得到反应物总能量低于生成物总能量,因此该反应为吸热反应。 与 反
应是吸热反应,盐酸与氢氧化钡溶液反应、甲烷在空气中的燃烧、锌与稀 反应都为放热反应,故A
符合题意。
综上所述,答案为A。
2.(2022·广东·珠海市第二中学高一期中)下列说法正确的是
A.干冰易升华,这与分子中C=O键的键能大小有关B.吸热反应一定需要加热的条件才能进行
C.灼热的炭与CO 的反应既是氧化还原反应又是放热反应
2
D.已知石墨转化为金刚石是吸热反应,所以石墨比金刚石更稳定
【答案】D
【解析】
A.干冰易升华,是其分子间作用力较小,沸点温度低于熔点温度导致,与分子中C=O键的键能大小无关,
A错误;
B.吸热反应不一定需要加热的条件也能进行,例如氢氧化钡晶体和氯化铵反应,B错误;
C.灼热的炭与CO 反应生成CO,是氧化还原反应,也是吸热反应,C错误;
2
D.石墨转化为金刚石是吸热反应,则金刚石能量高于石墨,体系能量较低的比较稳定,所以石墨比金刚
石更稳定,D正确;
故选D。
3.(2021·安徽·涡阳县第九中学高一期末)下列说法错误的是
A.化学反应中形成化学键会放出能量
B.化学反应中拆开反应物的化学键需要吸收能量
C.化学反应中放出或吸收的热量与反应物或生成物的状态无关
D.化学反应中若反应物的总能量大于生成物的总能量,则该反应是放热反应
【答案】C
【解析】
A.形成新的化学键,能量降低,会释放能量,故A正确;
B.断裂化学键需要能量,吸收能量,所以化学反应中拆开反应物的化学键需要吸收能量,故B正确;
C.反应物或生成物的状态不同,能量不同,则化学反应中放出或吸收的热量与反应物或生成物的状态有
关,故C错误;
D.反应物总能量大于生成物总能量,化学反应中要释放能量,则该反应是放热反应,故D正确;
故选C。
4.(2021·贵州贵阳·高一期末)N 和H 在催化剂表面合成氨的微观历程图如下,用 、 、
2 2
分别表示N、H、NH ,已知: ,该反应属于放热反应。下列说法正确的是
2 2 3A.②→③过程,是放热过程
B.该反应中若生成等量的NH (l),则放出的热量较少
3
C.合成氨反应中,反应物总能量低于生成物总能量
D.③→④过程,形成的NH 为共价化合物
3
【答案】D
【解析】
A.②→③为N≡N键、H-H键的断裂过程,断裂化学键吸热、形成化学键放热,则②→③过程是吸热过程,
故A错误;
B.气态转化为液体放热,则该反应中若生成等量的NH (l),则放出的热量较多,故B错误;
3
C. ,该反应属于放热反应,说明反应物总能量大于生成物总能量,故C错
误;
D.由图可知,③→④的过程是N原子和H原子形成NH 的过程,NH 中只含有共价键,属于共价化合物,
3 3
故D正确;
故选D。
5.(2021·广东·高一期末)氮气与氟气在一定条件下可以化合得到三氟化氮(NF )。三氟化氮在半导体加工、
3
太阳能电池的制造中都有广泛应用。生成三氟化氮的过程中,形成或断裂化学键需要放出或吸收的能量如
图:
下列说法错误的是
A.该反应是一个放热反应
B.该反应中发生了共价键的断裂和形成
C.该反应的化学方程式为
D.断裂1 mol N-F键吸收的能量小于断裂1 mol F-F键吸收的能量
【答案】D【解析】
A.根据图示可知:1 mol N 与3 mol F 反应产生2 mol NF 能量变化为(941.7 kJ+3×154.8 kJ)-6×283.0
2 2 3
kJ=-291.9 kJ,说明该反应是放热反应,A正确;
B.该反应发生时,断裂反应物中的共价键,同时产生了生成物中的共价键,B正确;
C.该反应发生时,有1 mol N 和3 mol F 发生,产生了2 mol NF ,故反应方程式为: ,C
2 2 3
正确;
D.断裂1 mol N-F需吸收283.0 kJ热量,而断裂1 mol F-F键稀吸收热量154.8 kJ的热量,故断裂1 mol N-
F键吸收的能量大于断裂1 mol F-F键吸收的能量,D错误;
故合理选项是D。
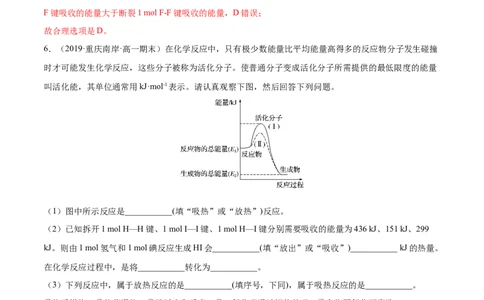
6.(2019·重庆南岸·高一期末)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞
时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量
叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答下列问题。
(1)图中所示反应是___________(填“吸热”或“放热”)反应。
(2)已知拆开1 mol H—H键、1 mol I—I键、1 mol H—I键分别需要吸收的能量为436 kJ、151 kJ、299
kJ。则由1 mol氢气和1 mol碘反应生成HI会___________(填“放出”或“吸收”)___________ kJ的热量。
在化学反应过程中,是将___________转化为___________。
(3)下列反应中,属于放热反应的是___________(填序号,下同),属于吸热反应的是___________。
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥Ba(OH) ·8H O与NH Cl反应 ⑦铁粉与稀盐酸反应
2 2 4
【答案】 放热 放出 11 化学能 热能
①②③⑤⑦ ④⑥
【解析】
(1)由题图可知反应物的总能量高于生成物的总能量,故该反应为放热反应。
(2)H(g)+I(g)===2HI(g),断裂1 mol H—H键和1 mol I—I键需要吸收436 kJ+151 kJ=587 kJ热量,生
2 2成2 mol HI放出2×299 kJ=598 kJ热量,所以1 mol氢气和1 mol碘反应生成HI放出11 kJ的热量;在化学
反应过程中,将化学能转化为热能。
(3)应熟悉常见的吸热反应和放热反应:中和反应、燃料的燃烧、有氧参与的氧化还原反应、多数化合
反应等属于放热反应;多数分解反应(H O 分解除外)、二氧化碳通过炽热的碳、Ba(OH) ·8H O与NH Cl反
2 2 2 2 4
应等属于吸热反应。所以放热反应有:①②③⑤⑦;吸热反应有:④⑥.
化学反应与电能
1.(2019·浙江·绍兴市教育教学研究院高一期末)利用石墨、锌片、铜片、导线、电流计、橙汁、烧杯等
用品探究原电池的组成。下列结论不正确的是
A.原电池是将化学能转化成电能的装置
B.原电池由电极、电解质溶液和导线等组成
C.图中电极a为石墨、电极b为锌片时,导线中会产生电流
D.图中电极a为锌片、电极b为铜片时,电子由铜片通过导线流向锌片
【答案】D
【解析】
A.原电池是把化学能转化为电能的装置,A正确;
B.原电池由电解质溶液、电极、导线组成闭合回路,B正确;
C.因为橙汁为酸性,所以图中a极为石墨、b极为锌片时,则Zn作原电池的负极,石墨作原电池的正极,
导线中会产生电流,C正确;
D.图中a极为锌片、b极为铜片时,则Zn为负极,Cu为正极,电子从负极流向正极,所以电子从Zn片
流向Cu片,D错误;
答案选D。
2.(2021·安徽·蒙城第一中学高一期末)银具有诱人的白色光泽、较高的化学稳定性,深受人们的青睐,广
泛用于饰品、银器、礼品、奖章和纪念币。但银制品用久表面会生成Ag S而逐渐变黑。根据电化学原理,
2
某同学设计用如图方法除去银制品表面的黑色Ag S,使其恢复如初。下列说法正确的是
2A.用酒精代替NaCl溶液也同样有效 B.Fe盆一极发生还原反应
C.处理后Ag手镯质量增大 D.电子流向Ag手镯一极
【答案】D
【解析】
A.酒精不是电解质,不能构成原电池,因此不能用于除去银制品表面的黑色Ag S,使其恢复如初,A错
2
误;
B.由于电极活动性Fe>Ag,所以Fe为负极,Fe盆一极失去电子发生氧化反应,B错误;
C.用该方法处理银手镯时,Ag S变为Ag单质,因此银制品质量会减轻,C错误;
2
D.在原电池反应中,Fe为负极,Ag为正极,电子由负极Fe流向正极Ag手镯一极,D正确;
故合理选项是D。
3.(2021·广西·南宁市英华学校高一期末)微型纽扣电池在现代生活中有广泛应用,有种银锌电池,其电
极分别是Ag O和Zn,电解质溶液为KOH溶液,电极反应式为:Zn+2OH--2e-=ZnO+HO,Ag O+HO+
2 2 2 2
2e-=2Ag+2OH-,总反应式为:Ag O+Zn=ZnO+2Ag。根据上述反应式,判断下列叙述中正确的是
2
A.在使用过程中,电池负极区溶液的pH增大
B.在使用过程中,电子由Ag O经外电路流向Zn极
2
C.Zn是负极,Ag O是正极
2
D.Zn极发生还原反应,Ag O极发生氧化反应
2
【答案】C
【解析】
A.根据元素化合价变化知,Zn失电子而作负极,负极上OH-参加反应导致其浓度减小,溶液的碱性降低,
pH减小,故A错误;
B.该原电池中,Zn是负极、Ag O是正极,电子从负极Zn沿导线流向正极Ag O,故B错误;
2 2
C.电池反应中Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极、Ag O
2
是正极,负极上发生氧化反应、正极上发生还原反应,故C正确;
D.Zn失电子发生氧化反应、Ag O得电子发生还原反应,故D错误;
2
故选:C。
4.(2021·湖南·高一期末)常见锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为,下列说法错误的是
A.该电池属于一次电池
B.电池工作时,电子由锌筒通过外电路流向石墨棒
C.电池负极上发生失去电子的还原反应
D.外电路中每通过0.4mol电子,锌的质量理论上减小13.0g
【答案】C
【解析】
A.锌—锰碱性电池是一次电池,故A正确;
B.电池工作时,电子由负极通过外电路流向正极,故B正确;
C.负极失电子,发生氧化反应,故C错误;
D.由电极反应式为 可知,外电路中每通过0.4mol电子时,Zn反应0.2mol,减
少质量为 ,故D正确;
故选:C。
5.(2021·安徽安庆·高一期末)铅蓄电池是一种典型的可充电电池,其放电时的电池总反应Pb+PbO+4H+
2
+2SO =PbSO+H O,则下列说法不正确的是
4 2
A.电池工作时,负极反应:Pb-2e-=Pb2+
B.铅蓄电池是二次电池,放电时是化学能转化为电能
C.电池工作时,电子由Pb板通过导线流向PbO 板
2
D.电池工作时,溶液中H+移向PbO 板
2
【答案】A
【解析】
A.电池工作时,负极Pb失去电子与SO 结合生成PbSO ,所以电极反应式为Pb-2e-+SO =PbSO,故A
4 4
错误;
B.铅蓄电池是可充电电池、是二次电池,充电时作为电解池,将电能转化为化学能储存,放电时是化学
能转化为电能,故B正确;
C.电池工作时,电子从负极Pb沿导线流向正极PbO ,故C正确;
2D.电池工作时,内电路中阳离子H+移向正极PbO ,阴离子SO 移向负极Pb,故D正确;
2
故选A。
6.(2021·陕西宝鸡·高一期末)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢
氧燃料电池的说法正确的是
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H+O= 2H O
2 2 2
【答案】D
【解析】
A.燃料电池是将化学能转化为电能,A项错误;
B.a极通入H 发生氧化反应,是电池的负极,B项错误;
2
C.外电路中电子由负极流向正极,即由电极a通过导线流向电极b,C项错误;
D.氢氧燃料电池酸性和碱性条件下生成物都是水,故该电池的总反应:2H+O= 2H O,故D正确;
2 2 2
故答案为D。
7.(2019·广西桂林·高一期末)有A、B、C、D四种金属。当A、B组成原电池时,电子流动方向为
导线 ;把A、D用导线连接后同时浸入稀硫酸中,A上有气泡产生;C与D构成原电池时,
电极反应式为 , ,则A、B、C、D金属性由强到弱的顺序为
A. B.
C. D.
【答案】D【解析】
当A、B组成原电池时,电子流动方向为 导线 ,则金属性A>B;把A、D用导线连接后同
时浸入稀硫酸中,A上有气泡产生,则金属性D>A;C与D构成原电池时,电极反应式为 ,
,则金属性C>D;所以 。
故选D。
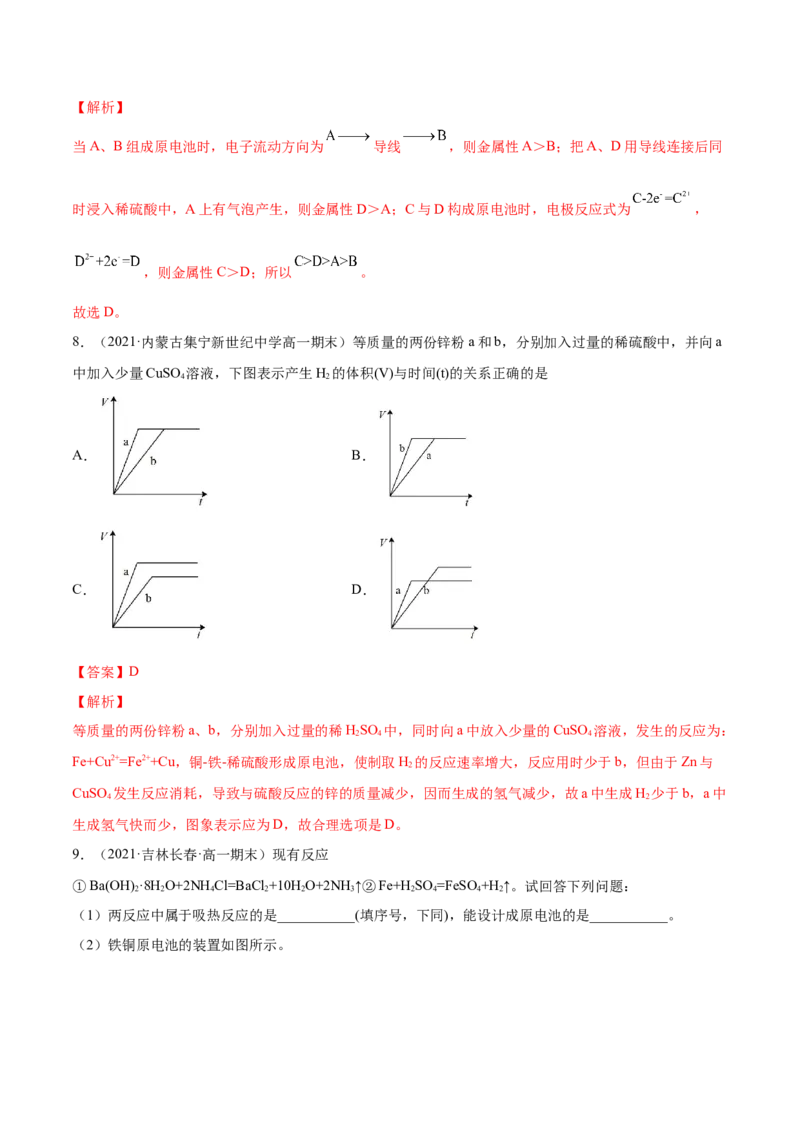
8.(2021·内蒙古集宁新世纪中学高一期末)等质量的两份锌粉a和b,分别加入过量的稀硫酸中,并向a
中加入少量CuSO 溶液,下图表示产生H 的体积(V)与时间(t)的关系正确的是
4 2
A. B.
C. D.
【答案】D
【解析】
等质量的两份锌粉a、b,分别加入过量的稀HSO 中,同时向a中放入少量的CuSO 溶液,发生的反应为:
2 4 4
Fe+Cu2+=Fe2++Cu,铜-铁-稀硫酸形成原电池,使制取H 的反应速率增大,反应用时少于b,但由于Zn与
2
CuSO 发生反应消耗,导致与硫酸反应的锌的质量减少,因而生成的氢气减少,故a中生成H 少于b,a中
4 2
生成氢气快而少,图象表示应为D,故合理选项是D。
9.(2021·吉林长春·高一期末)现有反应
①Ba(OH) ·8H O+2NH Cl=BaCl +10H O+2NH ↑②Fe+H SO =FeSO+H ↑。试回答下列问题:
2 2 4 2 2 3 2 4 4 2
(1)两反应中属于吸热反应的是___________(填序号,下同),能设计成原电池的是___________。
(2)铁铜原电池的装置如图所示。①铁作___________(填“正极”或“负极”),溶液中的H+向___________(填“铁”或“铜”)电极方向移
动。
②正极的现象是___________。负极的电极方程式为___________。
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为___________ L。
【答案】(1) ① ②
(2) 负极 铜 有气泡产生 Fe-2e-=Fe2+ 2.24
【解析】
(1)Ba(OH) ·8H O+2NH Cl═2NH ↑+BaCl +10H O是吸热反应,Fe+H SO ═FeSO +H ↑属自发的氧化还原
2 2 4 3 2 2 2 4 4 2
反应,可以设计成原电池;答案为①;②。
(2)①Fe-Cu原电池中,铁的金属性强于铜,所以铁为负极,Cu为正极,溶液中H+向正极铜电极方向移
动;答案为负极;铜。
②正极发生还原反应,电极反应为2H++2e-=H ↑,现象是有气泡产生,负极的电极反应式为Fe-2e-=Fe2+;答
2
案为有气泡产生;Fe-2e-=Fe2+。
③由正极电极反应为2H++2e-=H ↑可知,反应过程中有0.2mol电子发生转移,产生0.1molH,在标准状况
2 2
下的体积为2.24L;答案为2.24。
10.(2021·广东潮州·高一期末)完成下列问题。
(1)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如下图所示的原电池装置。则A(正极)极材料为___________,
B(负极)极材料为___________,溶液C为___________,A(正极)电极上发生反应的类型为___________(填
“氧化”或“还原”)反应,B(负极)电极上发生的电极反应为___________,当有1.6g铜溶解时,通过外电
路的电子的物质的量为___________。
(2)某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如下图。则电极a是电池的___________(填
“正”或“负”)极,该电池正极的电极反应式为___________。【答案】(1) 石墨 Cu FeCl 溶液 还原 Cu-2e-=Cu2+ 0.05 mol
3
(2) 负 O+4H++4e-=2H O
2 2
【解析】
(1)要将反应:Cu+2Fe3+=Cu2++2Fe2+设计成原电池,在该反应中Cu失去电子发生氧化反应;Fe3+得到电
子发生还原反应产生Fe2+,若A为正极,则A电极材料应该是活动性比Cu的导体,可以是石墨电极;B
电极为负极,电极材料是Cu,溶液C为含有Fe3+的溶液,可以是FeCl 溶液;A电极为正极,发生还原反
3
应;B电极为负极,失去电子,发生氧化反应,电极反应式为:Cu-2e-=Cu2+;1.6 g Cu的物质的量是
n(Cu)= ,由于Cu是+2价金属,因此电池工作过程中电子转移的物质的量为n(e-)=0.025
mol×2=0.05 mol;
(2)根据图示可知:a电极通入H,失去电子发生氧化反应,所以a电极为负极,a电极反应式为:H-2e-
2 2
=2H+;b电极上通入O,O 得到电子,发生还原反应,所以b电极为正极,正极上O 得到电子后与溶液中
2 2 2
的H+结合形成HO,故正极的电极反应式为:O+4H++4e-=2H O。
2 2 2
11.(2019·浙江·诸暨市教育研究中心高一期末)根据下列原电池的装置图,回答问题:
(1)若C为稀HSO 溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反
2 4
应式为___________;反应进行一段时间后溶液C的pH将___________(填“升高”“降低”或“基本不
变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如上图所示的原电池装置,则负极A极材料为___________,
正极B极材料为___________,溶液C为___________。
(3)用CH 和O 组合形成的质子交换膜燃料电池的结构示意图如下:
4 2①则d电极是___________(填“正极”或“负极”),c电极的反应方程式为___________。
②若线路中转移2mol电子,则上述燃料电池,消耗的O 在标准状况下的体积为___________L。
2
(4)熔融盐电池具有高的发电效率,因而受到重视。可用LiCO 和NaCO 的熔融盐混合物作电解质,
2 3 2 3
CO为负极燃料气,空气与CO 的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极电极反应
2
式为2CO+2 -4e-=4CO ,则正极电极反应式为___________。
2
【答案】(1) 2H++2e-=H ↑ 升高
2
(2) Cu 石墨(其他合理答案也可) FeCl 溶液(其他合理答案也可)
3
(3) 正 CH-8e-+2H O=CO+8H+ 11.2L
4 2 2
(4)O+2CO +4e-=2C
2 2
【解析】
(1)铁作负极,则该原电池反应是铁与稀硫酸置换H 的反应,所以正极反应是H+得电子生成H,电极反
2 2
应式为2H++2e-=H ↑;溶液中H+放电,导致溶液中H+浓度减小, pH升高。
2
(2)Cu+2Fe3+=Cu2++2Fe2+设计成如题图所示的原电池装置,根据方程式中物质发生反应类型判断,Cu发
生氧化反应,作原电池的负极,所以A极材料是Cu,B极材料是比铜不活泼的导电物质如石墨、Ag等即
可。溶液C中含有Fe3+,如FeCl 溶液。
3
(3)①根据图中的电子流向知,d电极是电子流入的电极,c电极是电子流出的电极,说明d电极是正极,
c电极是负极,甲烷在负极发生氧化反应生成CO,电极反应式为CH-8e-+2H O=CO+8H+。
2 4 2 2
②线路中转移2mol电子,消耗的O 为0.5mol,在标准状况下的体积为22.4L/mol 0.5mol=11.2L。
2
(4)
该熔融盐燃料电池中,正极上氧气得电子和二氧化碳反应生成碳酸根离子,电极反应式为O+2CO +4e-=2C
2 2
。
12.(2021·四川遂宁·高一期末)任何化学反应都伴随着能量的变化,通过化学反应化学能可转化为热能、
电能等不同形式的能量。(1)H 可用于工业合成氨气,已知拆开1mol H-H键、1molN≡N键分别需要吸收的能量为436kJ、946kJ,
2
形成1molN-H键会放出能量391kJ,则在反应N+3H 2NH 中,每生成2molNH ___________(填
2 2 3 3
“吸收”或“放出”)热量___________kJ。当在相同的条件下向容器中充入1molN 和3molH 时,它们反
2 2
应对应的热量___________(填“大于”、“等于”或“小于”)你所计算出的值。
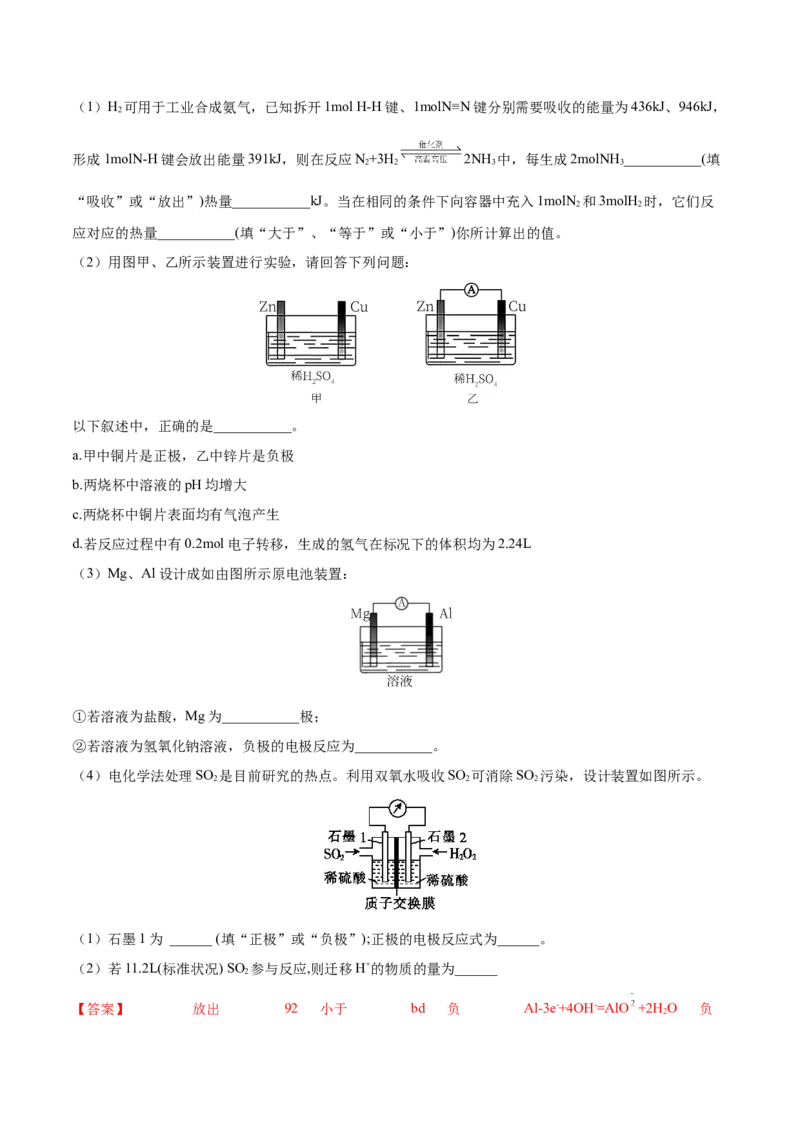
(2)用图甲、乙所示装置进行实验,请回答下列问题:
以下叙述中,正确的是___________。
a.甲中铜片是正极,乙中锌片是负极
b.两烧杯中溶液的pH均增大
c.两烧杯中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标况下的体积均为2.24L
(3)Mg、Al设计成如由图所示原电池装置:
①若溶液为盐酸,Mg为___________极;
②若溶液为氢氧化钠溶液,负极的电极反应为___________。
(4)电化学法处理SO 是目前研究的热点。利用双氧水吸收SO 可消除SO 污染,设计装置如图所示。
2 2 2
(1)石墨1为 ______ (填“正极”或“负极”);正极的电极反应式为______。
(2)若11.2L(标准状况) SO 参与反应,则迁移H+的物质的量为______
2
【答案】 放出 92 小于 bd 负 Al-3e-+4OH-=AlO +2H O 负
2极 HO+2e-+2H+=2H O 1mol
2 2 2
【解析】
(1)拆1molH-H键、1molN≡N、1molN-H键分别需要吸收的能量为436kJ、946kJ、391kJ,在反应
N+3H 2NH 中,断裂3mol H-H键,1mol N≡N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol
2 2 3
NH ,共⇌形成6molN-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放
3
热反应,放出的热量为:2346kJ-2254kJ=92kJ,当在相同的条件下向容器中充入1molN 和3molH 时,反应
2 2
物不能完全反应,所以它们反应对应的热量会小于92kJ,故答案为:放出; 92;小于.
(2)甲池中锌与稀硫酸反应,锌表面产生气泡,反应离子方程式为Zn+2H+=Zn2++H ↑,铜与稀硫酸不反应;
2
乙池中形成原电池,锌比铜活泼,锌作负极,电极反应式为Zn-2e-=Zn2+,铜作正极,电极反应式为2H+
+2e-=H ↑,总反应为Zn+2H+=Zn2++H ↑,据此作答;
2 2
a.由分析可知,甲装置不能形成原电池,则甲不存在正极,故A错误;
b.由分析可知,两池中氢离子均被消耗,pH增大,故b正确;
c.甲池中铜表面无明显现象,乙池中铜表面产生气泡,故c错误;
d.甲、乙的总反应均为Zn+2H+=Zn2++H ↑,有0.2mol电子转移,生成氢气0.1mol,在标况下的体积为
2
0.1mol×22.4L/mol=2.24L,,故d正确;
故答案为:bd;
(3)①Mg、Al均能与盐酸反应,Mg更活泼,Mg作负极,Al作正极;
②Mg与氢氧化钠溶液不反应,Al与氢氧化钠溶液反应,故Al作负极,Mg作正极;电极反应式为Al-3e-
+4OH-=AlO +2H O;
2
(4)(1)该原电池中,通入二氧化硫的电极上失电子发生氧化反应,则通入二氧化硫的电极是负极、通
入双氧水的电极是正极,正极上双氧水得电子生成水,电极反应式为HO+2e-+2H+=2H O;
2 2 2
(2)n(SO )= ,该反应的负极反应式为SO +2H O-2e-=SO +4H+,正极电极反应式
2 2 2
为HO+2e-+2H+=2H O,有0.5mol二氧化硫参加反应,有2mol氢离子在正极上发生反应,则迁移H+的物
2 2 2
质的量为反应的二氧化硫的2倍,为1mol。
化学反应速率与限度
1.(2021·广东潮州·高一期末)下列说法正确的是A.可逆反应的化学反应限度不会随反应条件的改变而改变
B.化学反应的限度决定了反应物在该条件下的最大转化率
C.化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率
D.在可逆反应中,正反应的化学反应速率是正值,逆反应的化学反应速率是负值
【答案】B
【解析】
A.可逆反应的化学反应限度是在一定条件下限度,当外界条件发生改变时,化学平衡被破坏,就会建立
新条件下的新的平衡状态,因此反应限度会随反应条件的改变而改变,A错误;
B.当反应在一定条件下达到限度时,反应物转化率达到最大值,因此化学反应的限度决定了反应物在该
条件下的最大转化率,B正确;
C.化学反应速率表示的是化学反应进行的快慢程度,与化学反应类型是否是可逆反应无关,C错误;
D.化学反应速率表示的是化学反应进行的快慢程度,是单位时间内反应物浓度减少值或生成物浓度的增
大值,因此正反应、逆反应的化学反应速率都是正值,D错误;
故合理选项是B。
2.(2021·吉林·延边二中高一期末)已知 ,反应速率分别用 、 、
、 表示,正确的是
A. B.
C. D.
【答案】A
【解析】
A.由于v(O ):v(NO)=5:4,所以 ,A正确;
2
B.由于v(O ):v(H O)=5:6,所以 ,B错误;
2 2
C.由于v(NH ):v(H O)=4:6=2:3,所以 ,C错误;
3 2
D.由于v(NH ):v(O )=4:5,所以 ,D错误;
3 2
故合理选项是A。3.(2021·河南·柘城县第四高级中学高一期末)反应 在四种不同情况下的反
应速率分别为:
① ②
③ ④
下列有关反应速率的比较中正确的是
A.④<③=②<① B.④>③>②>① C.④>③=②>① D.①>②>③>④
【答案】C
【解析】
不同物质表示的速率之比等于其化学计量数之比,故各物质表示的反应速率与其化学计量数之比越大,反
应速率越快,① =0.0075mol•(L•s)-1② =0.20mol•(L•s)-1③ =0.20mol•(L•s)-1④
=0.2255mol•(L•s)-1反应速率④>③=②>①,故D正确;
答案:C。
4.(2021·广东·高一期末)某温度下,起始浓度均为1 mol/L的两种气体X 和Y,在恒容密闭容器中反应
2 2
仅生成气体Z,反应2 min后,测得c(X )=0.4 mol/L,c(Z)=0.4 mol/L,用Y 表示的化学反应速率为
2 2
v(Y )=0.1 mol/(L·min),则该反应的化学方程式可能为
2
A. B.
C. D.
【答案】A
【解析】
2 min后测得反应消耗X 的浓度为0.6 mol/L,v(X )= mol/(L·min);v(Y )=0.1 mol/(L·min),
2 2 2
v(Z)= mol/(L·min),则v(X ):v(Y ):v(Z)= 3:1:2,根据质量守恒定律可知Z化学式为
2 2
XY。由于用不同物质表示的反应速率比等于化学方程式中的计量数的比,故该反应的化学方程式可能为
3
,合理选项是A。
5.(2021·重庆·高一期末)某校化学社同学研究影响0.1 mol/LNa SO 溶液与0.1 mol/LHSO 溶液反应速
2 2 3 2 4率的因素,设计实验如下:
序 NaSO 溶液体 HSO 溶液体 加入水的体 混合前各溶液和水的 混合后开始出现浑
2 2 3 2 4
号 积/mL 积/mL 积/mL 温度/℃ 浊的时间
① 2 2 0 20
② 1 2 V 20
1
③ 1 2 V 40
2
④ 2 2 0 40
下列说法不正确的是A.①和②研究的是浓度对反应速率的影响
B.②和③研究的是温度对反应速率的影响
C.V=V =1
1 2
D.出现浑浊时间最短的是第③组实验
【答案】D
【解析】
A.①和②温度相同,加入的硫酸体积相同,NaSO 溶液体积不同,所以研究的是NaSO 浓度对反应速
2 2 3 2 2 3
率的影响,故A正确;
B.②和③只有温度不同,其他条件都相同,所以研究的是温度对反应速率的影响,故B正确;
C.由以上分析可知,V=V=1,故C正确;
1 2
D.实验③的温度虽然比①和②中高,但NaSO 溶液的浓度没有实验④大,所以速率最快的是实验④,出
2 2 3
现浑浊时间最短的是第④组实验,故D错误;
故选D。
6.(2021·山东聊城·高一期末)化学在生活中的应用随处可见,下列措施不是为了改变化学反应速率的是
A.将食物存放在冰箱中 B.加工馒头时添加膨松剂
C.糕点包装袋内放置除氧剂 D.冶铁时将铁矿石粉碎
【答案】B
【解析】
A.食物存放在冰箱中,可降低温度,减缓食物氧化速率,与减小反应速率有关,故A不符合;
B.加工馒头时添加膨松剂,可使馒头疏松柔软,与改变反应速率无关,故B符合;
C.包装袋内放置除氧剂,可防止糕点被氧化,减缓食物氧化速率,与减小反应速率有关,故C不符合;
D.将铁矿石粉碎,可增大接触面积,可加快反应速率,与增大反应速率有关,故D不符合;
故选B。
7.(2021·甘肃·永昌县第一高级中学高一期末)在C(s)+CO(g)=2CO(g)的反应中,现采取下列措施:①缩
2
小体积,增大压强②增加碳的量③通入CO ④恒容下充入N ⑤恒压下充入N,上述能够使反应速率增大
2 2 2的措施是
A.①④ B.②③⑤ C.①③ D.①②④
【答案】C
【解析】
①缩小体积,增大压强,浓度增大,反应速率加快;
②碳是固体,增加碳的量,反应速率不变;
③通入CO,反应物浓度增大,反应速率加快;
2
④恒容下充入N,反应物浓度不变,反应速率不变;
2
⑤恒压下充入N,容器容积增大,浓度减小,反应速率减小;
2
答案选C。
8.(2021·新疆伊犁·高一期末)少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢。为了加快此
反应速率而不改变H 的产量,可以使用如下方法中的
2
①加HO②适当升温③加NaOH固体④加NaCl溶液⑤滴入几滴硫酸铜溶液⑥改用10mL0.1mol/L盐酸
2
A.①③⑥ B.②⑥ C.③⑥ D.④⑤⑥
【答案】B
【解析】
①加水,稀释了盐酸的浓度,反应速率变慢,故①不符合题意;
②适当升温(不考虑盐酸挥发),反应速率加快,但铁的物质的量不变,所以生成氢气的物质的量不变,故
②符合题意;
③加氢氧化钠固体,与盐酸反应,减少了盐酸的浓度,反应速率变慢,故③不符合题意;
④加NaCl溶液,相当于稀释盐酸浓度,反应速率变慢;故④不符合题意;
⑤滴入几滴硫酸铜溶液,铁把铜置换出来,形成原电池,反应速率加快,但与盐酸反应的铁减少,减少了
产生氢气的量,故⑤不符合题意;
⑥改用10mL0.1mol/L盐酸,即增加了盐酸的浓度,反应速率加快,但铁的物质的量不变,所以生成氢气
的物质的量不变,故⑥符合题意;
由上分析可知,②⑥符合加快反应速率而不改变H 的产量,B选项符合题意;答案为B。
2
9.(2021·重庆·高一期末)一定温度下,向2L恒容密闭容器中充入0.4molNH 和0.5molO 发生反应:
3 2
4NH (g)+5O(g) 4NO(g)+6H O(g)。2min末,NO的物质的量为0.2mol。下列有关说法不正确的是
3 2 2
A.2min末,NH 的浓度为0.1mol·L-1
3
B.0~2min内,用NH 表示的平均反应速率为v(NH )=0.05mol·L-1·min-1
3 3C.2min末,生成的水物质的量为0.3 mol
D.继续反应达平衡后,NO的浓度可以达到为0.2mol·L-1
【答案】D
【解析】
A.2min末,NO的物质的量为0.2mol,则消耗NH 0.2mol,则2min末,NH 的物质的量为
3 3
0.4mol-0.2mol=0.2mol,容器体积为2L,则NH 的浓度为0.1mol/L,故A正确;
3
B.0~2min内,用NH 表示的平均反应速率为v(NH )= =0.05mol·L-1·min-1,故B正确;
3 3
C.根据反应方程式,生成0.2mol NO的同时生成0.3mol水,故C正确;
D.若0.4mol NH 完全反应,则生成NO 0.4mol,浓度为0.2mol/L,但该反应是可逆反应,不能进行到底,
3
所以达平衡后,NO的浓度不能达到0.2mol·L-1,故D错误;
故选D。
10.(2019·重庆·高一期末)将6molA气体和3molB气体在2L的容器中混合,并在一定条件下发生如下
反应:2A(g)+B(g)=xC(g),若经2s后测得A的物质的量浓度为2.4mol/L,C的物质的量浓度为0.6mol/L。
下列叙述正确的是
A.x=1
B.2s内用物质A表示的反应的平均速率为0.3mol·L-1·s-1
C.2s时,物质B的物质的量浓度为0.6mol·L-1
D.2s时物质A的转化率为40%
【答案】B
【解析】
A.初始时A的浓度为 =3mol/L,所以2s后∆c(A)=3mol/L-2.4mol/L=0.6mol/L,C的物质的量浓度为
0.6mol/L,即∆c(C)=0.6mol/L,相同时间内∆c(A):∆c(C)=1:1,所以x=2,A错误;
B.2s内∆c(A)=0.6mol/L,所以平均反应速率为 =0.3mol·L-1·s-1,B正确;
C.根据方程式可知相同时间内∆c(A):∆c(B)=2:1,所以∆c(B)=0.3mol/L,B的初始浓度为
=1.2mol/L,所以2s时,物质B的物质的量浓度为1.5mol/L-0.3mol/L=1.2mol/L,C错误;
D.2s时物质A的转化率为 ×100%=20%,D错误;
综上所述答案为B。11.(2019·浙江·绍兴市教育教学研究院高一期末)在一定温度下的定容容器中,有反应
。当下列的物理量不再发生变化时,表明已达到平衡状态的是
A.混合气体的密度 B.混合气体的压强
C.气体的总物质的量 D.物质A的物质的量浓度
【答案】A
【解析】
A.因为A为固体,所以反应中气体的总质量一直在变化,当混合气体的密度不变,说明气体的质量不变,
反应达平衡状态,故A正确;
B.方程式两边气体的计量数相等,所以混合气体的压强一直不变,故B错误;
C.混合气体的总物质的量一直不变,故C错误;
D.A为纯固体、物质的量浓度是常数,故D正确;
答案:A
12.(2020·广东梅县东山中学高一期末)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进
行探究。
实验一:甲同学利用Al、Fe、Mg和2mol/L的稀硫酸,设计实验方案探究影响反应速率的因素。实验报告
如下表:
实验步骤 现象 结论
①分别取等体积的2mol/L的硫酸于试管中; 反应物的性质越活
②分别投入大小、形状相同的Al、Fe、Mg 泼,反应速率越快
(1)该同学观察到的实验现象:反应快慢依次是___________。根据控制变量法,要得出正确的实验结论,
还需控制的实验条件是保持___________相同。
(2)乙同学为了更精确地探究浓度对反应速率的影响,利用如图所示装置在同温下进行定量实验。用大
小、形状相同的Fe分别和0.5mol/L及2mol/L的足量稀硫酸反应。图中仪器A的名称是___________;Fe
与稀硫酸反应的离子方程式为__________;通过___________可以说明浓度对化学反应速率的影响。
实验二:已知:2KMnO +5H C O+3H SO =K SO +2MnSO +8H O+10CO↑,酸性KMnO 溶液和HC O 溶
4 2 2 4 2 4 2 4 4 2 2 4 2 2 4
液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(3)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是___________的影响。
(4)若用实验证明你的猜想,除酸性KMnO 溶液、HC O 溶液外,可以在反应一开始时加入
4 2 2 4
___________(填标号)。A.KSO B.MnSO C.MnCl D.HO
2 4 4 2 2
【答案】(1) Mg>Al>Fe 温度
(2) 锥形瓶 Fe+2H+=Fe2++H↑ 测定和比较相同时间内产生氢气的体积(或测定和
2
比较产生相同体积氢气所需的时间)
(3)Mn2+的催化作用(或催化剂)
(4)B
【解析】
(1)
金属活动性:Mg>Al>Fe,根据实验结论“反应物的性质越活泼,反应速率越快”可知,实验现象为:反
应快慢Mg>Al>Fe;温度对化学反应速率的影响较大,根据控制变量法,要得出正确的实验结论,还需
控制的实验条件是保持温度相同,故答案为:Mg>Al>Fe;温度;
(2)
仪器A为锥形瓶,用大小形状相同的Fe分别和0.5mol/L及2mol/L的足量稀硫酸反应,方程式为
Fe+H SO =FeSO+H ↑,离子方程式为Fe+2H+=Fe2++H ↑,可通过测定和比较相同时间内产生氢气的体积,
2 4 4 2 2
以判断浓度对化学反应速率的影响,故答案为:锥形瓶;Fe+2H+=Fe2++H ↑;相同时间内产生氢气的体积;
2
(3)
反应生成Mn2+,则Mn2+的催化作用使反应速率明显增大,故答案为:Mn2+的催化作用;
(4)
反应方程式2KMnO +5H C O+3H SO =K SO +2MnSO +8H O+10CO↑中,浓度变化较大的为锰离子,因
4 2 2 4 2 4 2 4 4 2 2
MnCl 中的Cl-能与KMnO 反应造成干扰,所以选择的可作催化剂的试剂应该是硫酸盐,故B正确,故答
2 4
案为:B。
13.(2021·山东·沂水县教育局高一期末)SO 和NO 是主要的大气污染物。某学习小组认为一定条件下,
2 x
用NH 与NO 反应转化为无污染物质可进行汽车尾气无害化处理。
3 2
(1)写出实验室制取氨气的化学方程式为____。
(2)将NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO (两端用夹子K、K 夹好),烧
3 2 1 2
杯Z中盛装NaOH溶液(已知:2NO +2NaOH=NaNO +NaNO +H O),在一定温度下按如图装置进行实验。
2 3 2 2①打开K,推动注射器活塞,使X中的气体缓慢通入Y管中,红棕色气体慢慢变浅。发生反应的化学方
1
程式为_____。
②将注射器活塞退回原处并固定,待装置恢复到室温。打开K,Z中NaOH溶液产生倒吸现象,原因是
2
_____。
(3)利用(2)中装置探究SO 能否与NaO 发生氧化还原反应。将Y中的药品更换为少量NaO,将注射
2 2 2 2 2
器X中SO 缓慢推入Y中,Y装置中的现象为_____。
2
(4)100℃时,在2L密闭容器中发生反应NO(g) 2NO (g),各气体浓度随时间变化的情况如图所示。
2 4 2
①当NO 的浓度为0.06mol·L-1'时,反应时间为ts,则0~ts时,用NO 气体的浓度变化量表达该反应的平均
2 4 2
速率为____。
②已知NO (g)与SO (g)发生可逆反应:NO (g)+SO(g) SO (g)+NO(g)(该反应正向为放热反应)。在一定
2 2 2 2 3
条件下,向1L密闭容器中充入4molNO (g)和2molSO (g)充分反应,下列说法正确的是____。
2 2
a.只要经过足够长的时间,可使c(SO )=0
2
b.每消耗1molSO ,同时生成1molNO ,说明该反应达到平衡状态
2 2
c.达到平衡状态时,各物质的物质的量浓度相等
d.当气体颜色不再变化时,若升高温度,气体的颜色会发生变化
【答案】(1)2NH Cl+Ca(OH) CaCl +2H O+2NH ↑
4 2 2 2 3
(2) 6NO +8NH 7N+12H O 反应后气体分子数减少,Y管中压强小于外界大气压,
2 3 2 2故产生倒吸现象
(3)淡黄色粉末颜色变成白色
(4) bd
【解析】
【分析】
本实验为通过验证NO 与NH 的反应,以及SO 与NaO 的反应,探究由SO 和NO 是主要的大气污染物
2 3 2 2 2 2 x
转化为无污染物质的过程,据此分析回答问题。
(1)
实验室用氯化铵和氢氧化钙在加热情况下反应生成氯化钙、水和氨气,化学方程式为2NH Cl+Ca(OH)
4 2
CaCl +2H O+2NH ;
2 2 3
(2)
①由题干可知,二氧化氮和氨气反应生成氮气和水,化学方程式为6NO +8NH 7N+12H O;
2 3 2 2
②室温下水为液态,由化学反应方程式可知反应后气体分子数减少,Y管中压强小于外界大气压,故产生
倒吸现象;
(3)
过氧化钠与二氧化硫反应生成硫酸钠,故Y装置中的现象为淡黄色粉末颜色变成白色;
(4)
①反应的过程中NO 不断减少,NO 不断增加,故①为NO ,②为NO,当NO 的浓度为0.06mol·L-1'时,
2 4 2 2 2 4 2 4
NO 变化的浓度为 ,由化学反应方程式可知,NO 变化的浓度为
2 4 2
,故平均速率为 ;
②a.因反应是可逆反应,反应物与生成物共存,故c(SO )不等于0,a错误;
2
b.每消耗1molSO ,同时生成1molNO ,正反应速率和逆反应速率相等,反应达到平衡状态,b正确;
2 2
c.二氧化氮与二氧化硫的物质的量不相等,根据化学反应方程式可知,二氧化氮与二氧化硫按照1:1发
生反应,故达到平衡状态时,各物质的物质的量浓度不相等,c错误;
d.二氧化氮是红棕色的气体,当颜色不变说明反应达到平衡状态,反应正向为放热反应,升高温度平衡,
逆向移动气体的颜色会变深,d正确;故选bd。
14.(2021·重庆·高一期末)近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、CO 和
2
H)在催化剂的作用下合成甲醇(CHOH)是其中的一个研究项目。该研究发生的主要反应如下:
2 3
Ⅰ.CO与H 反应合成甲醇:CO(g)+2H(g) CHOH(g)
2 2 3
Ⅱ.CO 与H 反应合成甲醇:CO(g)+3H(g) CHOH(g)+H O(g)
2 2 2 2 3 2
(1)上述反应符合原子经济性的是反应___________(I或II)。
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
A.恒温恒容下,再充入CO B.升高温度
C.恒温恒容下,向其中充入Ar D.恒温恒压下,向其中充入Ar
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是
___________。
A.单位时间内消耗3molH ,同时生成1mol的CHOH
2 3
B.CHOH的体积分数不再发生变化
3
C.3v(CO)=v(H )
2 2
D.容器内气体密度不再改变
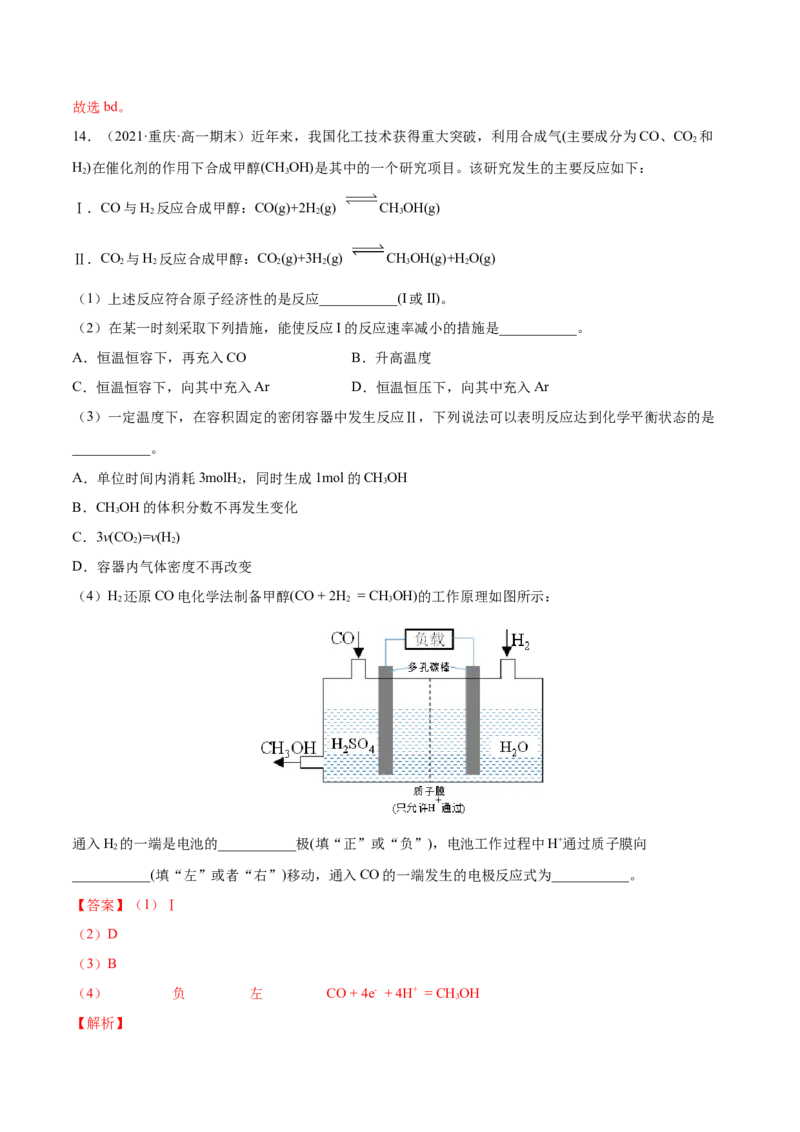
(4)H 还原CO电化学法制备甲醇(CO + 2H = CHOH)的工作原理如图所示:
2 2 3
通入H 的一端是电池的___________极(填“正”或“负”),电池工作过程中H+通过质子膜向
2
___________(填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________。
【答案】(1)Ⅰ
(2)D
(3)B
(4) 负 左 CO + 4e- + 4H+ = CHOH
3
【解析】(1)
原子经济性指的是反应物原子全部转移到生成物中,原子利用率是100%。反应Ⅰ和Ⅱ中 符合原子经济性
的是反应Ⅰ。
(2)
A.恒温恒容下,再充入CO,增大了反应物浓度,反应速率加快,故A不选;
B.升高温度可以加快反应速率,故B不选;
C.恒温恒容下,向其中充入Ar,各物质浓度均无改变,反应速率不变,故C不选;
D.恒温恒压下,向其中充入Ar,容器体积扩大,各物质浓度降低,反应速率减慢,故D选;
故选D。
(3)
A.无论平衡与否,单位时间内消耗3molH ,一定同时同时生成1mol的CHOH,所以该说法不能判断是
2 3
否平衡,故A不选;
B.CHOH的体积分数不再发生变化可以说明反应达到了平衡状态,故B选;
3
C.平衡时正逆反应速率相等,3v(CO)=v(H )不能表示出正逆反应速率相等,故C不选;
2 2
D.该反应的反应物和生成物均为气体,气体总质量是不变的,容器体积也是固定的,所以容器内气体密
度是一直不变的,所以当容器内气体密度不再改变时不能说明反应达到了平衡状态,故D不选;
故选B。
(4)
该装置是原电池,根据总反应:CO+2H=CH OH可知,C的化合价降低,CO在正极得到电子,H的化合
2 3
价升高,H 在负极失去电子,所以通入H 的一端是负极;电池工作过程中阳离子移向正极,所以H+向左
2 2
移动;通入CO的一端为正极,CO在酸性溶液中得到电子转变为CHOH,电极反应式为:CO + 4e- + 4H+
3
= CHOH。
3倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育