文档内容
高一下期中复习必刷题
题型一:硫及其化合物
【题1】(2021·玉岩中学)二氧化硫能使溴水褪色,说明二氧化硫具有( )
A. 还原性 B. 氧化性 C. 漂白性 D. 酸性
【题2】(2021·玉岩中学)下列实验报告记录的实验现象正确的是
实验
A 无色 无色 白色沉淀 无色溶液
B 红色 无色 白色沉淀 白色沉淀
记
录
C 红色 无色 无色溶液 白色沉淀
D 无色 无色 无色溶液 无色溶液
A. A B. B C. C D. D
【题3】(2021·深圳中学)下列反应产生的气体,通入NaSO 溶液不反应的是
2 3
A. Al与NaOH溶液 B. MnO 和浓盐酸共热
2C. 浓硝酸和铜片 D. 铜片和浓硫酸共热
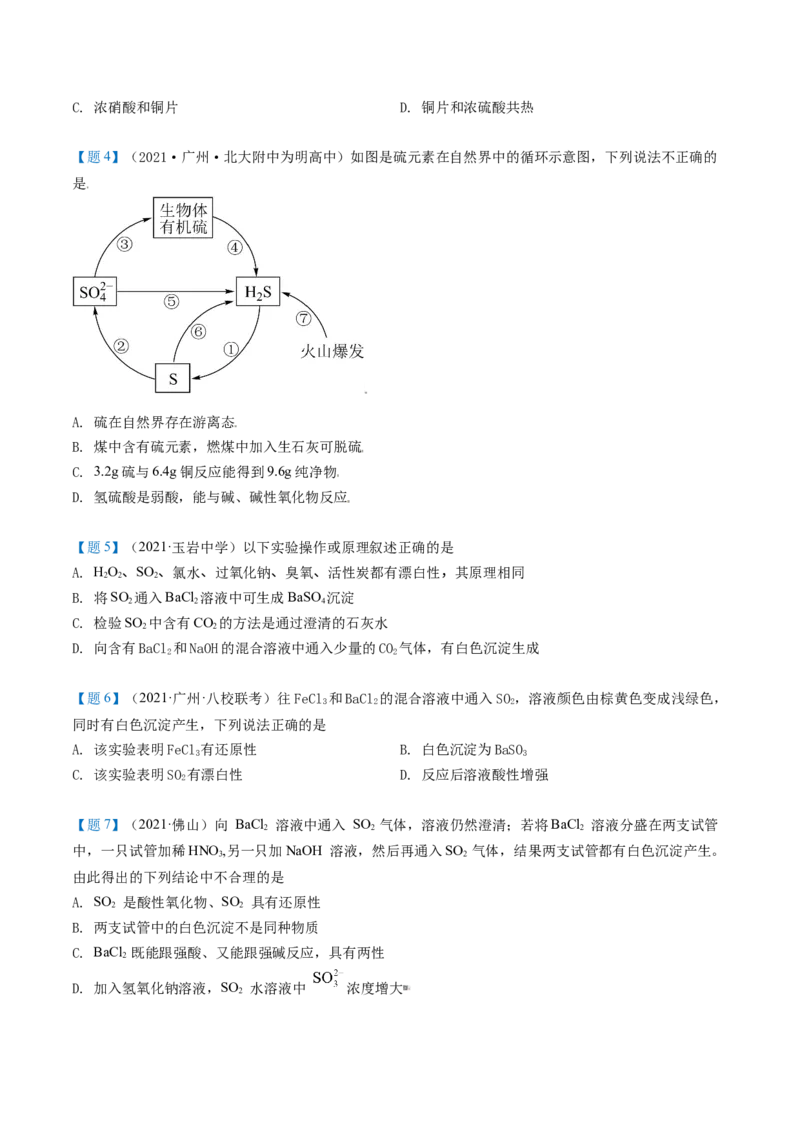
【题4】(2021·广州·北大附中为明高中)如图是硫元素在自然界中的循环示意图,下列说法不正确的
是
A. 硫在自然界存在游离态
B. 煤中含有硫元素,燃煤中加入生石灰可脱硫
C. 3.2g硫与6.4g铜反应能得到9.6g纯净物
D. 氢硫酸是弱酸,能与碱、碱性氧化物反应
【题5】(2021·玉岩中学)以下实验操作或原理叙述正确的是
A. HO、SO 、氯水、过氧化钠、臭氧、活性炭都有漂白性,其原理相同
2 2 2
B. 将SO 通入BaCl 溶液中可生成BaSO 沉淀
2 2 4
C. 检验SO 中含有CO 的方法是通过澄清的石灰水
2 2
D. 向含有BaCl 和NaOH的混合溶液中通入少量的CO 气体,有白色沉淀生成
2 2
【题6】(2021·广州·八校联考)往FeCl 和BaCl 的混合溶液中通入SO ,溶液颜色由棕黄色变成浅绿色,
3 2 2
同时有白色沉淀产生,下列说法正确的是
A. 该实验表明FeCl 有还原性 B. 白色沉淀为BaSO
3 3
C. 该实验表明SO 有漂白性 D. 反应后溶液酸性增强
2
【题7】(2021·佛山)向 BaCl 溶液中通入 SO 气体,溶液仍然澄清;若将BaCl 溶液分盛在两支试管
2 2 2
中,一只试管加稀HNO,另一只加NaOH 溶液,然后再通入SO 气体,结果两支试管都有白色沉淀产生。
3 2
由此得出的下列结论中不合理的是
A. SO 是酸性氧化物、SO 具有还原性
2 2
B. 两支试管中的白色沉淀不是同种物质
C. BaCl 既能跟强酸、又能跟强碱反应,具有两性
2
D. 加入氢氧化钠溶液,SO 水溶液中 浓度增大
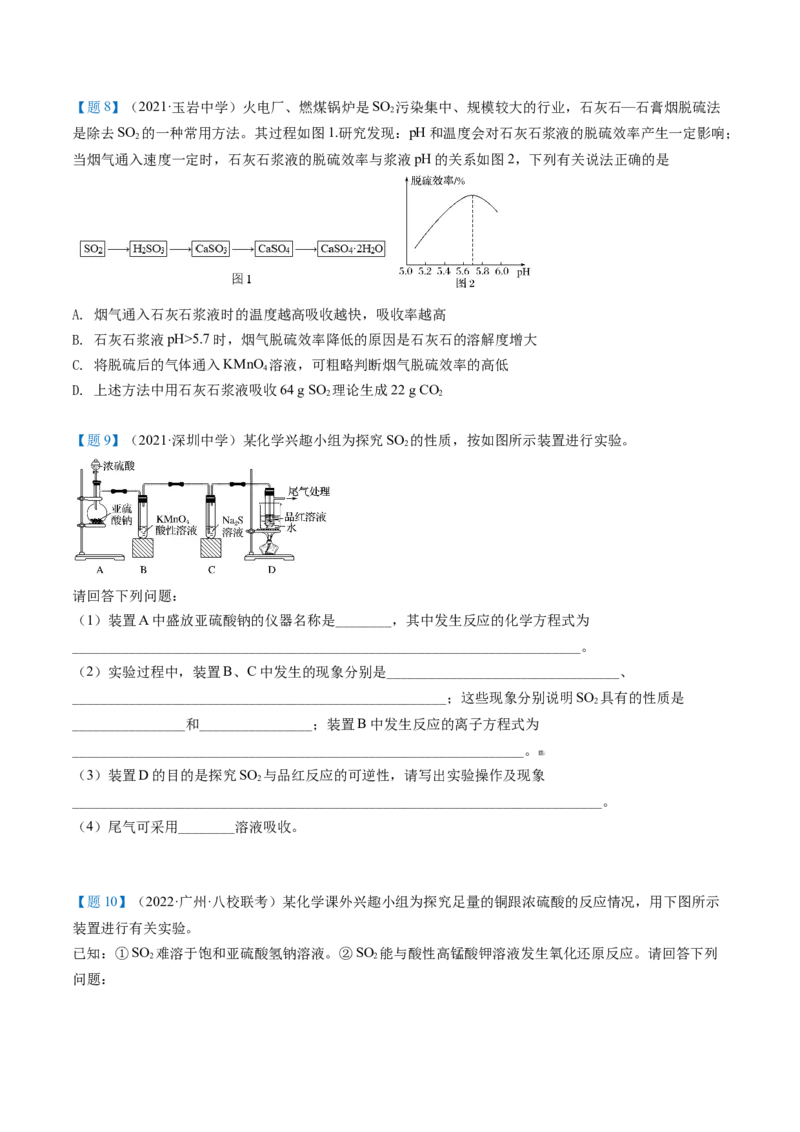
2【题8】(2021·玉岩中学)火电厂、燃煤锅炉是SO 污染集中、规模较大的行业,石灰石—石膏烟脱硫法
2
是除去SO 的一种常用方法。其过程如图1.研究发现:pH和温度会对石灰石浆液的脱硫效率产生一定影响;
2
当烟气通入速度一定时,石灰石浆液的脱硫效率与浆液pH的关系如图2,下列有关说法正确的是
A. 烟气通入石灰石浆液时的温度越高吸收越快,吸收率越高
B. 石灰石浆液pH>5.7时,烟气脱硫效率降低的原因是石灰石的溶解度增大
C. 将脱硫后的气体通入KMnO 溶液,可粗略判断烟气脱硫效率的高低
4
D. 上述方法中用石灰石浆液吸收64 g SO 理论生成22 g CO
2 2
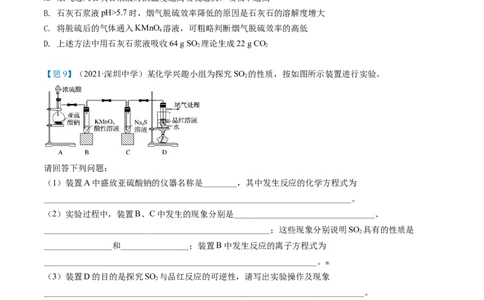
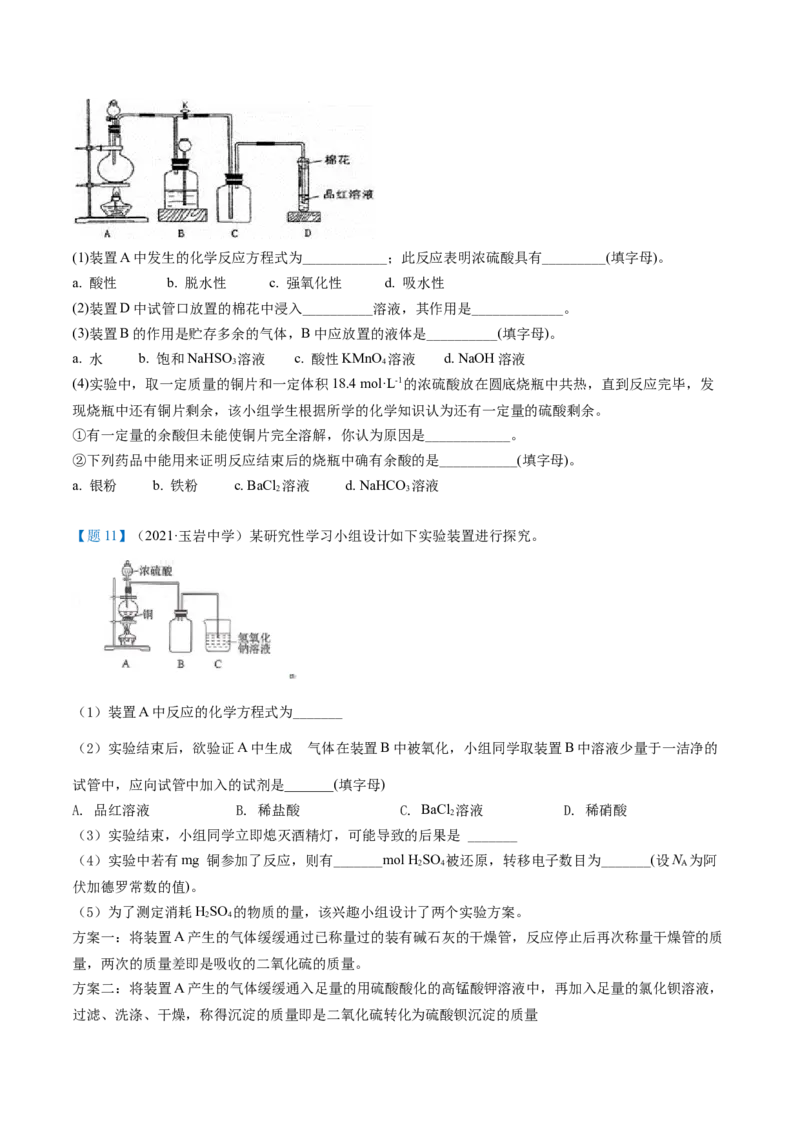
【题9】(2021·深圳中学)某化学兴趣小组为探究SO 的性质,按如图所示装置进行实验。
2
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为
________________________________________________________________________。
(2)实验过程中,装置B、C中发生的现象分别是_________________________________、
_____________________________________________________;这些现象分别说明SO 具有的性质是
2
________________和________________;装置B中发生反应的离子方程式为
________________________________________________________________。
(3)装置D的目的是探究SO 与品红反应的可逆性,请写出实验操作及现象
2
___________________________________________________________________________。
(4)尾气可采用________溶液吸收。
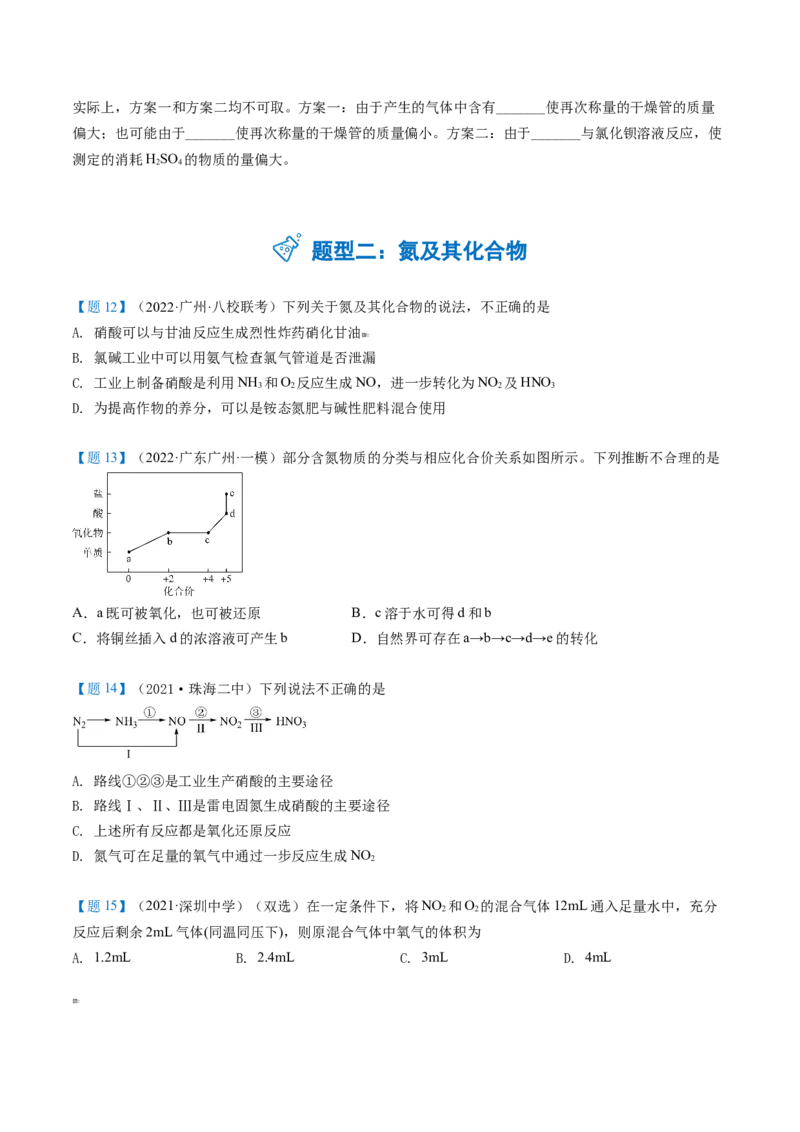
【题10】(2022·广州·八校联考)某化学课外兴趣小组为探究足量的铜跟浓硫酸的反应情况,用下图所示
装置进行有关实验。
已知:①SO 难溶于饱和亚硫酸氢钠溶液。②SO 能与酸性高锰酸钾溶液发生氧化还原反应。请回答下列
2 2
问题:(1)装置A中发生的化学反应方程式为____________;此反应表明浓硫酸具有_________(填字母)。
a. 酸性 b. 脱水性 c. 强氧化性 d. 吸水性
(2)装置D中试管口放置的棉花中浸入__________溶液,其作用是_____________。
(3)装置B的作用是贮存多余的气体,B中应放置的液体是__________(填字母)。
a. 水 b. 饱和NaHSO 溶液 c. 酸性KMnO 溶液 d. NaOH溶液
3 4
(4)实验中,取一定质量的铜片和一定体积18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发
现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是____________。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________(填字母)。
a. 银粉 b. 铁粉 c. BaCl 溶液 d. NaHCO 溶液
2 3
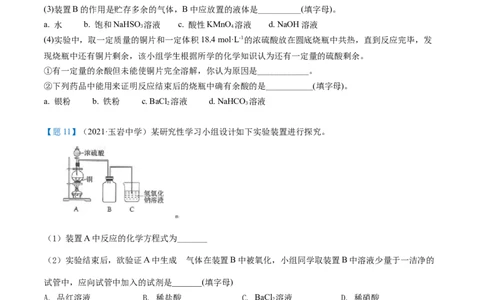
【题11】(2021·玉岩中学)某研究性学习小组设计如下实验装置进行探究。
(1)装置A中反应的化学方程式为_______
的
(2)实验结束后,欲验证A中生成 气体在装置B中被氧化,小组同学取装置B中溶液少量于一洁净的
试管中,应向试管中加入的试剂是_______(填字母)
A. 品红溶液 B. 稀盐酸 C. BaCl 溶液 D. 稀硝酸
2
(3)实验结束,小组同学立即熄灭酒精灯,可能导致的后果是 _______
(4)实验中若有mg 铜参加了反应,则有_______mol HSO 被还原,转移电子数目为_______(设N 为阿
2 4 A
伏加德罗常数的值)。
(5)为了测定消耗HSO 的物质的量,该兴趣小组设计了两个实验方案。
2 4
方案一:将装置A 产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量干燥管的质
量,两次的质量差即是吸收的二氧化硫的质量。
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液中,再加入足量的氯化钡溶液,
过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量实际上,方案一和方案二均不可取。方案一:由于产生的气体中含有_______使再次称量的干燥管的质量
偏大;也可能由于_______使再次称量的干燥管的质量偏小。方案二:由于_______与氯化钡溶液反应,使
测定的消耗HSO 的物质的量偏大。
2 4
题型二:氮及其化合物
【题12】(2022·广州·八校联考)下列关于氮及其化合物的说法,不正确的是
A. 硝酸可以与甘油反应生成烈性炸药硝化甘油
B. 氯碱工业中可以用氨气检查氯气管道是否泄漏
C. 工业上制备硝酸是利用NH 和O 反应生成NO,进一步转化为NO 及HNO
3 2 2 3
D. 为提高作物的养分,可以是铵态氮肥与碱性肥料混合使用
【题13】(2022·广东广州·一模)部分含氮物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.a既可被氧化,也可被还原 B.c溶于水可得d和b
C.将铜丝插入d的浓溶液可产生b D.自然界可存在a→b→c→d→e的转化
【题14】(2021·珠海二中)下列说法不正确的是
A. 路线①②③是工业生产硝酸的主要途径
B. 路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C. 上述所有反应都是氧化还原反应
D. 氮气可在足量的氧气中通过一步反应生成NO
2
【题15】(2021·深圳中学)(双选)在一定条件下,将NO 和O 的混合气体12mL通入足量水中,充分
2 2
反应后剩余2mL气体(同温同压下),则原混合气体中氧气的体积为
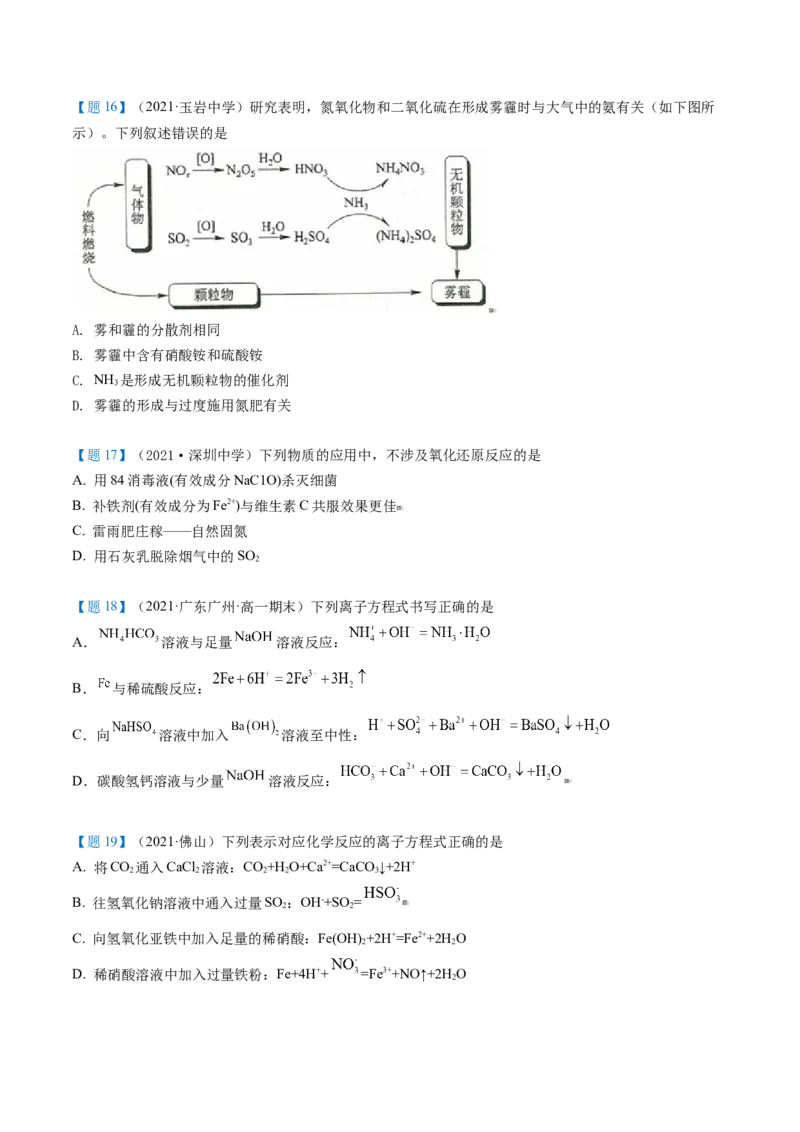
A. 1.2mL B. 2.4mL C. 3mL D. 4mL【题16】(2021·玉岩中学)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所
示)。下列叙述错误的是
A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH 是形成无机颗粒物的催化剂
3
D. 雾霾的形成与过度施用氮肥有关
【题17】(2021·深圳中学)下列物质的应用中,不涉及氧化还原反应的是
A. 用84消毒液(有效成分NaC1O)杀灭细菌
B. 补铁剂(有效成分为Fe2+)与维生素C共服效果更佳
C. 雷雨肥庄稼——自然固氮
D. 用石灰乳脱除烟气中的SO
2
【题18】(2021·广东广州·高一期末)下列离子方程式书写正确的是
A. 溶液与足量 溶液反应:
B. 与稀硫酸反应:
C.向 溶液中加入 溶液至中性:
D.碳酸氢钙溶液与少量 溶液反应:
【题19】(2021·佛山)下列表示对应化学反应的离子方程式正确的是
A. 将CO 通入CaCl 溶液:CO+H O+Ca2+=CaCO ↓+2H+
2 2 2 2 3
B. 往氢氧化钠溶液中通入过量SO :OH-+SO=
2 2
C. 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH) +2H+=Fe2++2H O
2 2
D. 稀硝酸溶液中加入过量铁粉:Fe+4H++ =Fe3++NO↑+2HO
2【题20】(2021·玉岩中学)关于SO 与NO 的下列说法错误的是
2 2
A. 都能与NaOH溶液反应生成两种盐 B. 都能使石蕊试液变红
C. 都是引起光化学烟雾的大气污染物 D. 工业制硫酸、硝酸时要用到它们
【题21】(2021·玉岩中学)下列有关实验的操作,正确的是
实验 操作
A. 除去NaHCO 固体中混有的NHCl 直接将固体加热
3 4
B. 实验室收集Cu与稀硝酸反应生成的NO 向上排空气法收集
C. 检验非金属性Cl>Si 在NaSiO 溶液中加入足量HCl
2 3
取该溶液于干净的试管中,加NaOH浓溶液加热,
D. 检验某溶液中是否含有NH+
4
并用湿润的红色石蕊试纸检验
A. A B. B C. C D. D
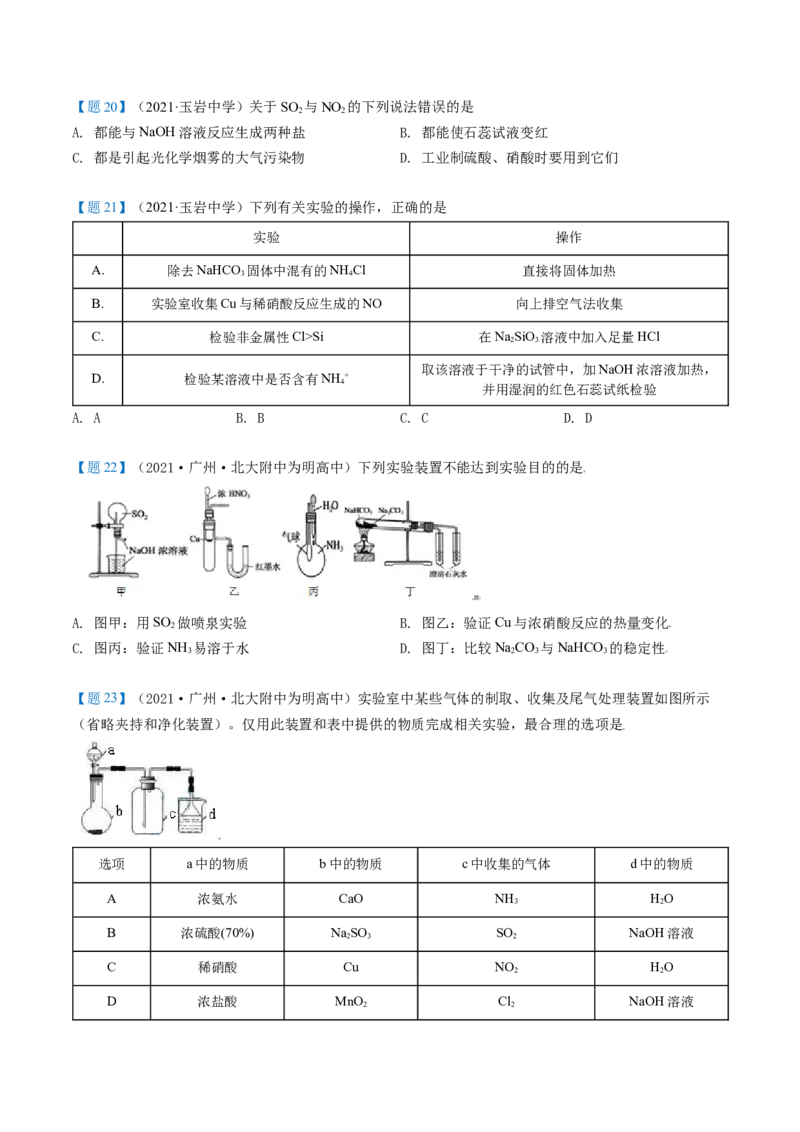
【题22】(2021·广州·北大附中为明高中)下列实验装置不能达到实验目的的是
A. 图甲:用SO 做喷泉实验 B. 图乙:验证Cu与浓硝酸反应的热量变化
2
C. 图丙:验证NH 易溶于水 D. 图丁:比较NaCO 与NaHCO 的稳定性
3 2 3 3
【题23】(2021·广州·北大附中为明高中)实验室中某些气体的制取、收集及尾气处理装置如图所示
(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO NH HO
3 2
B 浓硫酸(70%) NaSO SO NaOH溶液
2 3 2
C 稀硝酸 Cu NO HO
2 2
D 浓盐酸 MnO Cl NaOH溶液
2 2A. A B. B C. C D. D
【题24】(2021·深圳中学)利用如图所示装置进行实验,将液体X逐滴加入到固体Y中。下列有关实验
现象或结论正确的是
选项 X Y Z 实验现象或结论 装置
A 稀硫酸 亚硫酸钠 品红溶液 SO 能氧化品红
2
B 浓盐酸 KMnO 氢硫酸溶液 产生浑浊
4
C 浓盐酸 石灰石 硅酸钠溶液 非金属性:C>Si
D 浓硝酸 Cu 水 试管中液体变红
A. A B. B C. C D. D
【题25】(2021·珠海二中)下列各实验的现象及结论都正确的是
选项 实验 现象 结论
浓硫酸滴入蔗糖中,产生的气体导入 蔗糖变黑、体积膨胀, 使澄清石灰水变浑浊的气体是
A
澄清石灰水 澄清石灰水变浑浊 CO
2
过量铁粉加入稀硝酸中,充分反应 有无色气泡产生,溶液
B 稀硝酸能将Fe氧化成Fe3+
后,滴加KSCN溶液 呈血红色
向1mL0.1mol/LFeCl 溶液中滴加
3
C 2mL0.1mol/LKI溶液,充分反应后, 溶液变为红色 Fe3+和I-的反应为可逆反应
滴加几滴KSCN溶液
D 向FeCl 溶液中加入铜粉 溶液由棕黄色变蓝色 Cu与FeCl 发生了置换反应
3 3
A. A B. B C. C D. D
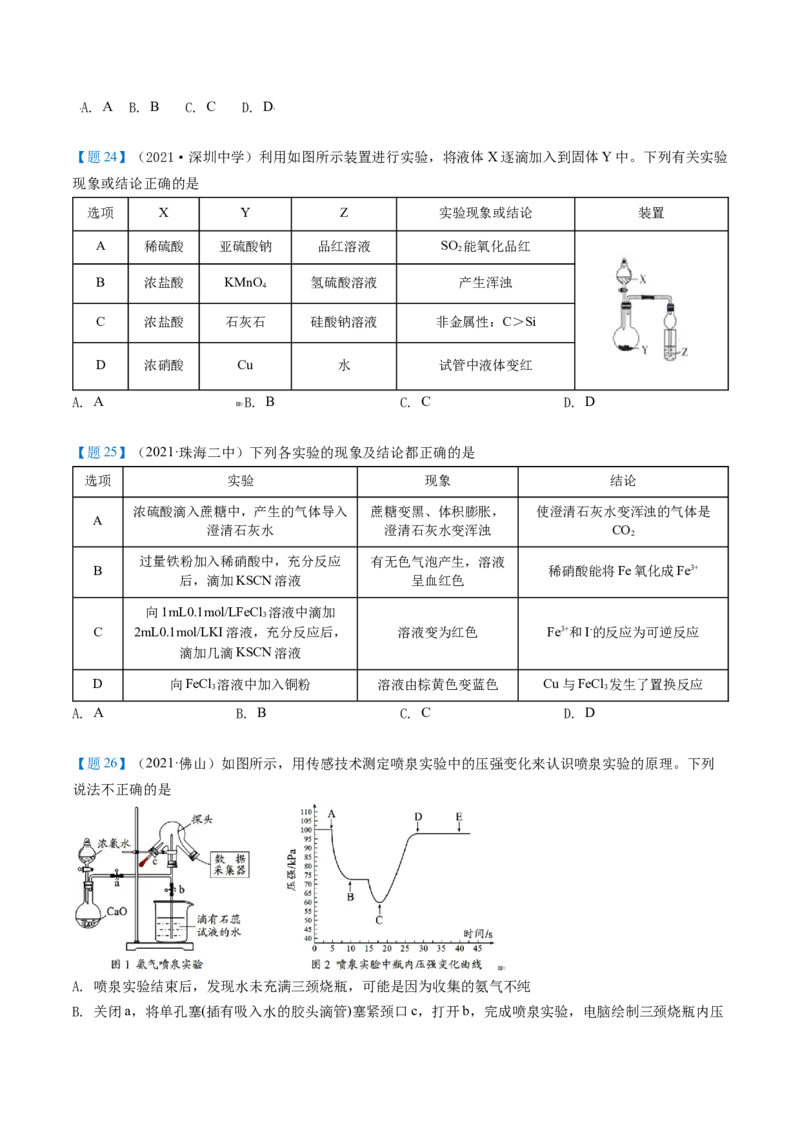
【题26】(2021·佛山)如图所示,用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。下列
说法不正确的是
A. 喷泉实验结束后,发现水未充满三颈烧瓶,可能是因为收集的氨气不纯
B. 关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈烧瓶内压强变化曲线如图2,则C点时喷泉最剧烈
C. 工业上,可用蘸有浓盐酸或者液氯的玻璃棒检验液氨是否泄漏
D. 三颈烧瓶中充满NH 形成的氨水与换成NO 形成的HNO 溶液的溶质的物质的量浓度不同
3 2 3
【题27】(2021·玉岩中学)硝酸与金属反应后所得还原产物与硝酸的浓度和金属的活泼性有关。10 mL
0.5 mol·L-1HNO 与0.048 g Mg恰好完全反应。若氮元素只被还原到一种价态,下列说法不正确的是
3
A. HNO 作还原剂
3
B. HNO 浓度越低,N元素还原价态越低
3
C. 反应中转移电子数为0.004 mol
D. 还原产物可能为NH NO
4 3
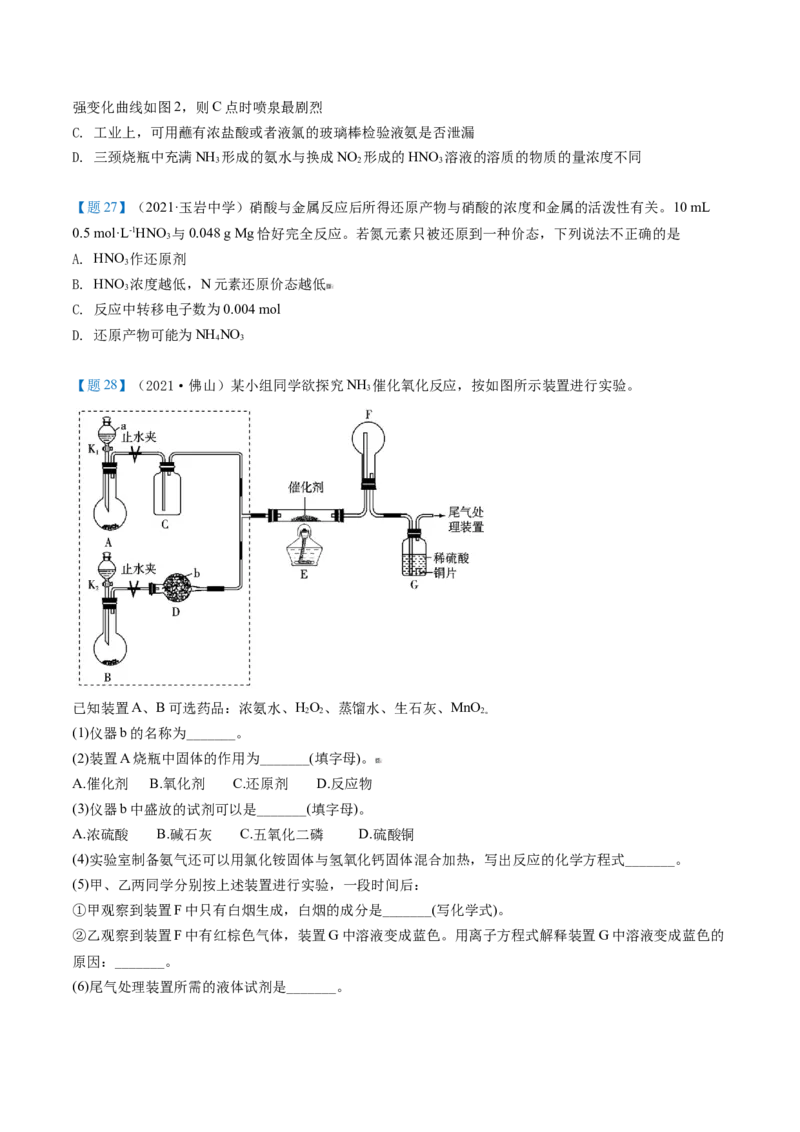
【题28】(2021·佛山)某小组同学欲探究NH 催化氧化反应,按如图所示装置进行实验。
3
已知装置A、B可选药品:浓氨水、HO、蒸馏水、生石灰、MnO
2 2 2。
(1)仪器b的名称为_______。
(2)装置A烧瓶中固体的作用为_______(填字母)。
A.催化剂 B.氧化剂 C.还原剂 D.反应物
(3)仪器b中盛放的试剂可以是_______(填字母)。
A.浓硫酸 B.碱石灰 C.五氧化二磷 D.硫酸铜
(4)实验室制备氨气还可以用氯化铵固体与氢氧化钙固体混合加热,写出反应的化学方程式_______。
(5)甲、乙两同学分别按上述装置进行实验,一段时间后:
①甲观察到装置F中只有白烟生成,白烟的成分是_______(写化学式)。
②乙观察到装置F中有红棕色气体,装置G中溶液变成蓝色。用离子方程式解释装置G中溶液变成蓝色的
原因:_______。
(6)尾气处理装置所需的液体试剂是_______。【题29】(2021·佛山)某校化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测试。
Ⅰ.第一组,取刚降到地面的酸雨水样,进行了如下实验:
①向雨水试样中滴加氯化钡溶液,有白色浑浊出现;
②每隔一段时间测定其 ,数据如下表所示:
测定时间/小时 0 1 2 3
pH 4.73 4.62 4.56 4.55
(1)出现白色浑浊的离子方程式为___________。
(2)分析上述 变化数据,你认为可能的原因是(用化学方程式表示) ___________。
Ⅱ.第二组,用下列装置定量分析空气中 的含量:
(3)通入空气前应进行的实验操作是___________。 溶液中导管末端做成球状多孔结构的作用是
___________。
(4)随着空气的不断通入,酸性 溶液颜色逐渐变浅直至褪色。已知 变成 , 变成
,写出此离子方程式___________,说明 具有___________性。
(5)若实验中气体流速为 、酸性 溶液的体积 ,其浓度为 ,从气体通入到紫
色恰好褪去,用时 。则此次取样处的空气中二氧化硫含量为___________ 。
【题30】(2021·广东·广州市玉岩中学高一期中)氮氧化物(NO、NO )、SO 是大气污染物。回答下列问题:
2 2
(1)以上污染物会造成的环境问题有_______(写一种即可)。
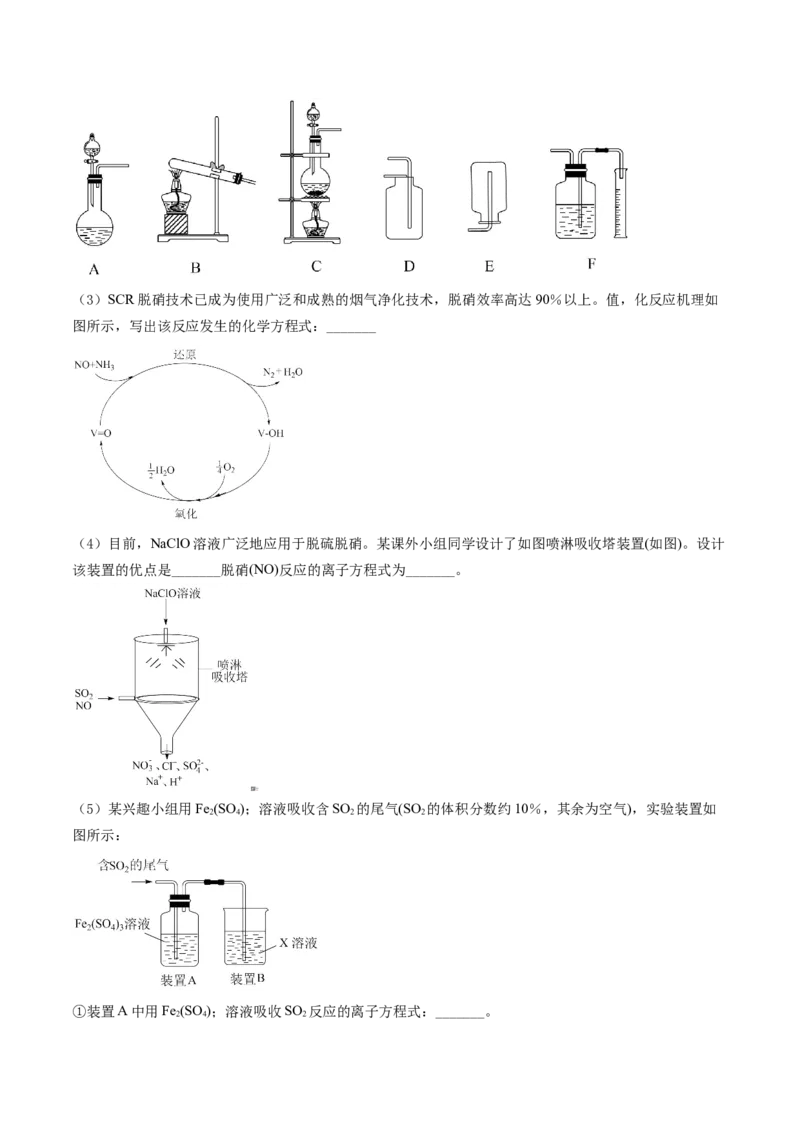
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO 反应制备
3
并收集NO ,应选择的装置是_______(填字母)。
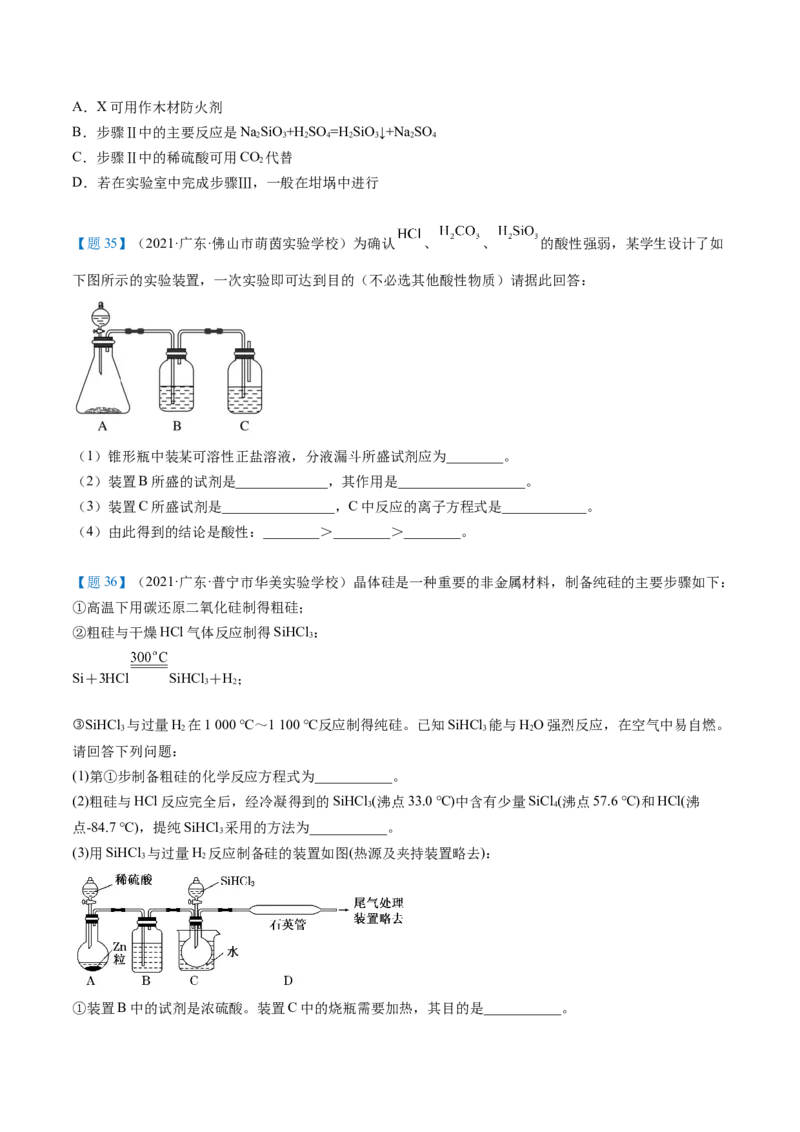
2(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。值,化反应机理如
图所示,写出该反应发生的化学方程式:_______
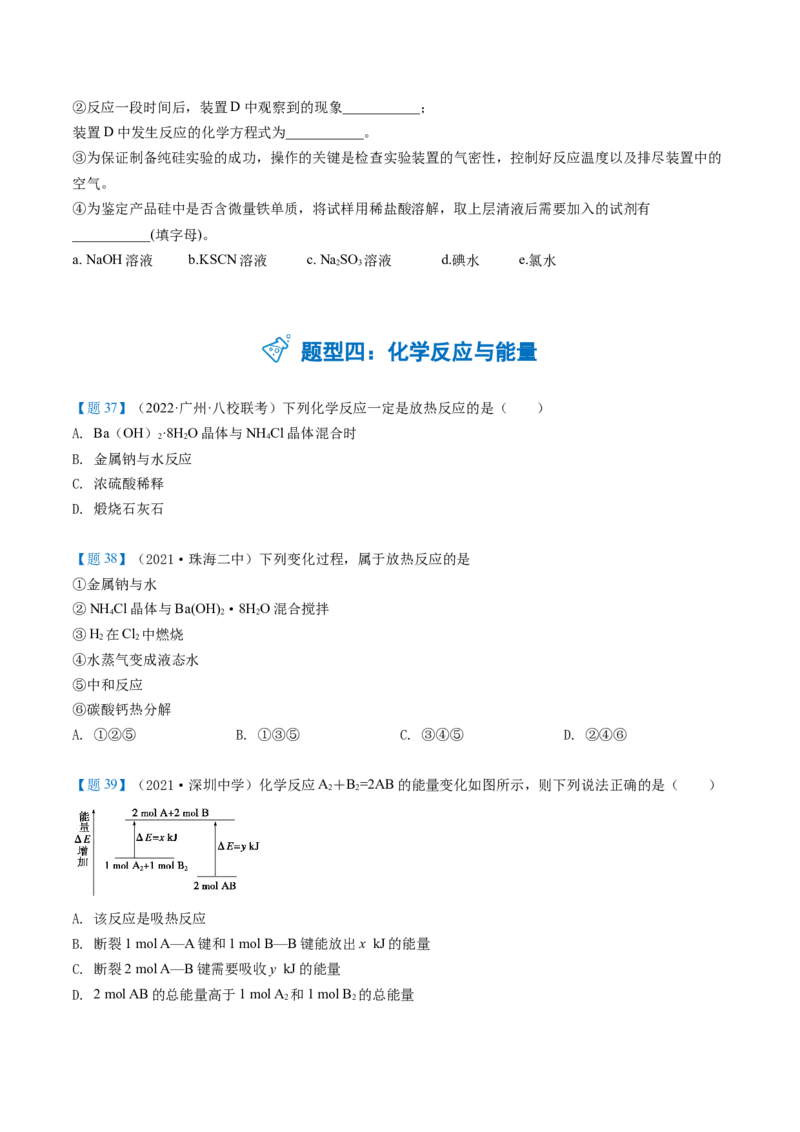
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计
该装置的优点是_______脱硝(NO)反应的离子方程式为_______。
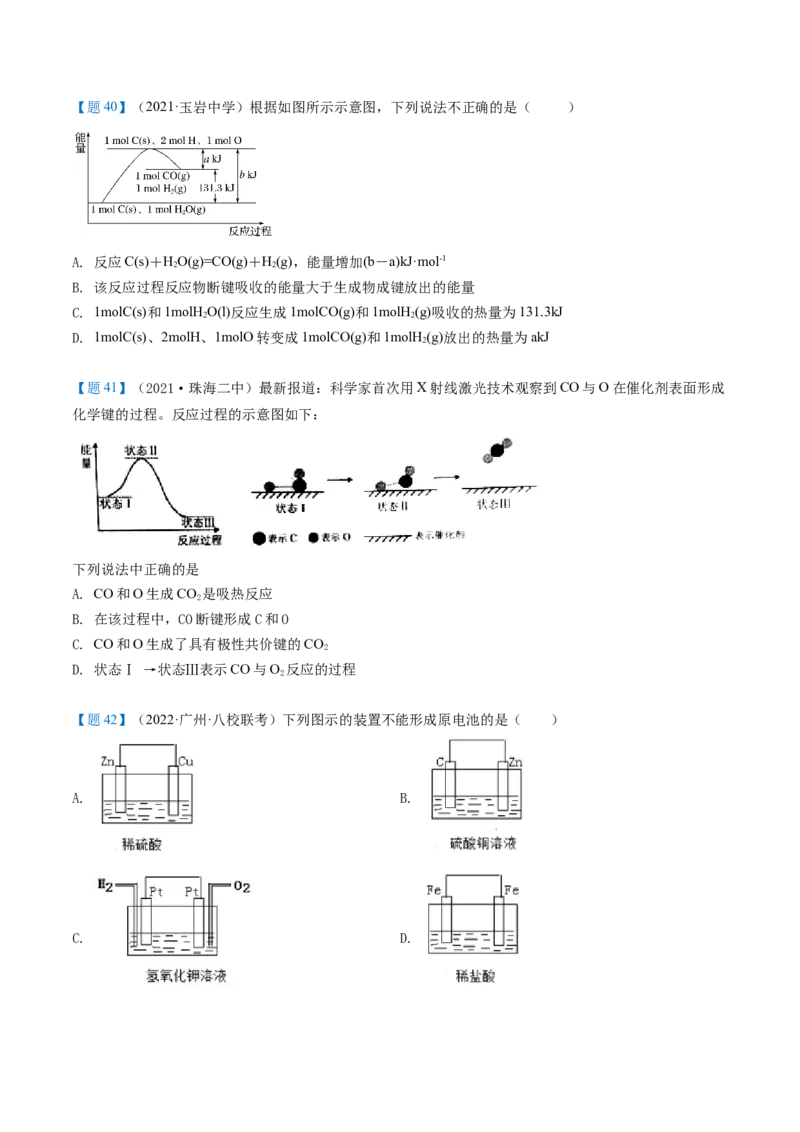
(5)某兴趣小组用Fe (SO );溶液吸收含SO 的尾气(SO 的体积分数约10%,其余为空气),实验装置如
2 4 2 2
图所示:
①装置A中用Fe (SO );溶液吸收SO 反应的离子方程式:_______。
2 4 2②反应后,若要检验SO 是否过量,可用试剂为_______。
2
③若实验测得反应后的装置A中不含有SO ,为测定其中所含FeSO 的物质的量浓度,现进行如下实验:
2 4
取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO) 溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当
4 2
反应恰好完全时,共消耗Ce(SO) 溶液18.00mL。请通过计算确定FeSO 的物质的量浓度_______。
4 2 4
题型三:硅及其化合物
【题31】(2021·广东实验中学高一期中)关于硅及其化合物用途的叙述中,不正确的有
A.NaSiO 可用作助燃剂
2 3
B.SiO 可用于制造光导纤维
2
C.单晶硅可用于制造太阳能电池
D.石灰石是生产玻璃的原料
【题32】(2021·佛山)半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是硅,下列有关硅
及其化合物叙述正确的是
A. 陶瓷、玻璃、水泥的主要成分都是硅酸盐
B. 光导纤维的主要成分是高纯硅
C. 可用石英坩埚加热熔融氢氧化钠固体
D. 二氧化硅不和任何酸反应
【题33】(2021·珠海二中)下列化学或离子方程式正确的是
A. NaOH与NH Cl溶液混合加热:OH-+ NH ·H O
4 3 2
B. SO 通入NaClO溶液中:SO +2ClO-+H O= +2HClO
2 2 2
C. 强碱溶液吸收HNO 工业尾气:2NO +2OH-= + +H O
3 2 2
D. 粗硅的冶炼:SiO+C Si+CO ↑
2 2
【题34】(2021·广东·肇庆二中)由粗SiO(含少量Fe O、Al O 杂质)制备纯SiO 的流程如图所示,下列
2 2 3 2 3 2
说法错误的是A.X可用作木材防火剂
B.步骤Ⅱ中的主要反应是NaSiO+H SO =H SiO↓+Na SO
2 3 2 4 2 3 2 4
C.步骤Ⅱ中的稀硫酸可用CO 代替
2
D.若在实验室中完成步骤Ⅲ,一般在坩埚中进行
【题35】(2021·广东·佛山市萌茵实验学校)为确认 、 、 的酸性强弱,某学生设计了如
下图所示的实验装置,一次实验即可达到目的(不必选其他酸性物质)请据此回答:
(1)锥形瓶中装某可溶性正盐溶液,分液漏斗所盛试剂应为________。
(2)装置B所盛的试剂是_____________,其作用是__________________。
(3)装置C所盛试剂是________________,C中反应的离子方程式是____________。
(4)由此得到的结论是酸性:________>________>________。
【题36】(2021·广东·普宁市华美实验学校)晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl :
3
Si+3HCl SiHCl +H;
3 2
③SiHCl 与过量H 在1 000 ℃~1 100 ℃反应制得纯硅。已知SiHCl 能与HO强烈反应,在空气中易自燃。
3 2 3 2
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为___________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl (沸点33.0 ℃)中含有少量SiCl (沸点57.6 ℃)和HCl(沸
3 4
点-84.7 ℃),提纯SiHCl 采用的方法为___________。
3
(3)用SiHCl 与过量H 反应制备硅的装置如图(热源及夹持装置略去):
3 2
①装置B中的试剂是浓硫酸。装置C中的烧瓶需要加热,其目的是___________。②反应一段时间后,装置D中观察到的现象___________;
装置D中发生反应的化学方程式为___________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及排尽装置中的
空气。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需要加入的试剂有
___________(填字母)。
a. NaOH溶液 b.KSCN溶液 c. Na SO 溶液 d.碘水 e.氯水
2 3
题型四:化学反应与能量
【题37】(2022·广州·八校联考)下列化学反应一定是放热反应的是( )
A. Ba(OH)·8H O晶体与NH Cl晶体混合时
2 2 4
B. 金属钠与水反应
C. 浓硫酸稀释
D. 煅烧石灰石
【题38】(2021·珠海二中)下列变化过程,属于放热反应的是
①金属钠与水
②NH Cl晶体与Ba(OH) ·8HO混合搅拌
4 2 2
③H 在Cl 中燃烧
2 2
④水蒸气变成液态水
⑤中和反应
⑥碳酸钙热分解
A. ①②⑤ B. ①③⑤ C. ③④⑤ D. ②④⑥
【题39】(2021·深圳中学)化学反应A+B =2AB的能量变化如图所示,则下列说法正确的是( )
2 2
A. 该反应是吸热反应
B. 断裂1 mol A—A键和1 mol B—B键能放出x kJ的能量
C. 断裂2 mol A—B键需要吸收y kJ的能量
D. 2 mol AB的总能量高于1 mol A 和1 mol B 的总能量
2 2【题40】(2021·玉岩中学)根据如图所示示意图,下列说法不正确的是( )
A. 反应C(s)+HO(g)=CO(g)+H(g),能量增加(b-a)kJ·mol-1
2 2
B. 该反应过程反应物断键吸收的能量大于生成物成键放出的能量
C. 1molC(s)和1molH O(l)反应生成1molCO(g)和1molH (g)吸收的热量为131.3kJ
2 2
D. 1molC(s)、2molH、1molO转变成1molCO(g)和1molH (g)放出的热量为akJ
2
【题41】(2021·珠海二中)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成
化学键的过程。反应过程的示意图如下:
下列说法中正确的是
A. CO和O生成CO 是吸热反应
2
B. 在该过程中,CO断键形成C和O
C. CO和O生成了具有极性共价键的CO
2
D. 状态Ⅰ →状态Ⅲ表示CO与O 反应的过程
2
【题42】(2022·广州·八校联考)下列图示的装置不能形成原电池的是( )
A. B.
C. D.【题43】(2022·广州·八校联考) 、 两根金属棒插入 溶液中构成如图所示装置,实验中电流表指针
发生偏转,同时 棒变粗, 棒变细,则 、 、 溶液可能是下列中的
编号 溶液
A 稀硫酸
B 硝酸银溶液
C 硫酸铜溶液
D 稀硫酸
A. A B. B C. C D. D
【题44】(2021·佛山)铅蓄电池是一种典型的可充电电池,其放电时的电池总反应式为Pb+PbO+4H+
2
+2SO2- =2PbSO +2H O,则下列说法不正确的是
4 4 2
A. 电池工作时,负极反应为:Pb-2e- = Pb2+
B. 铅蓄电池是二次电池,充电时电能转化为化学能
C. 电池工作时,电子由Pb板通过导线流向PbO 板
2
D. 电池工作时,溶液中H+移向PbO 板
2
【题45】(2021·珠海二中)有一种被称为“软电池”的纸质电池,其总反应为:
Zn+2MnO +H O=ZnO+2MnOOH。下列说法正确的是
2 2
A. 该电池中Zn作正极
B. 该电池工作时电流由Zn经导线流向MnO
2
C. 正极电极反应为:MnO +2e-+H O=MnOOH+OH-
2 2
D. 当6.5gZn完全溶解时,流经电路的电子个数约为1.204×1023
【题46】(2021·广州·北大附中为明高中)锂碘电池可用于心脏起搏器,电池反应可简化为:
2Li+I=2LiI。电池工作时,下列说法正确的是
2
A. 碘电极是电池的负极
B. 锂电极发生还原反应
C. 电池正极反应:Li-e-=Li+
D. 电流从碘电极经外电路流向锂电极
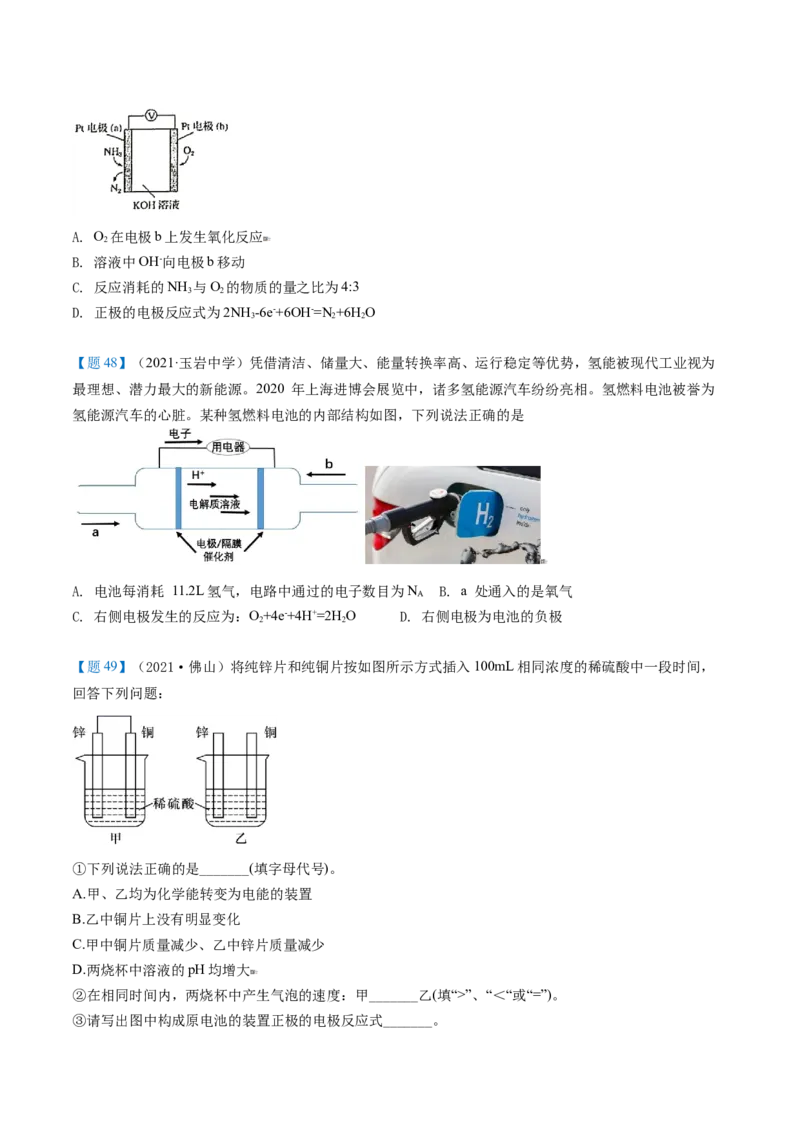
【题47】(2021·玉岩中学)电化学气敏传感器可用于监测环境中NH 的含量,其工作原理示意图如下。
3
下列说法正确的是( )A. O 在电极b上发生氧化反应
2
B. 溶液中OH-向电极b移动
C. 反应消耗的NH 与O 的物质的量之比为4:3
3 2
D. 正极的电极反应式为2NH -6e-+6OH-=N +6H O
3 2 2
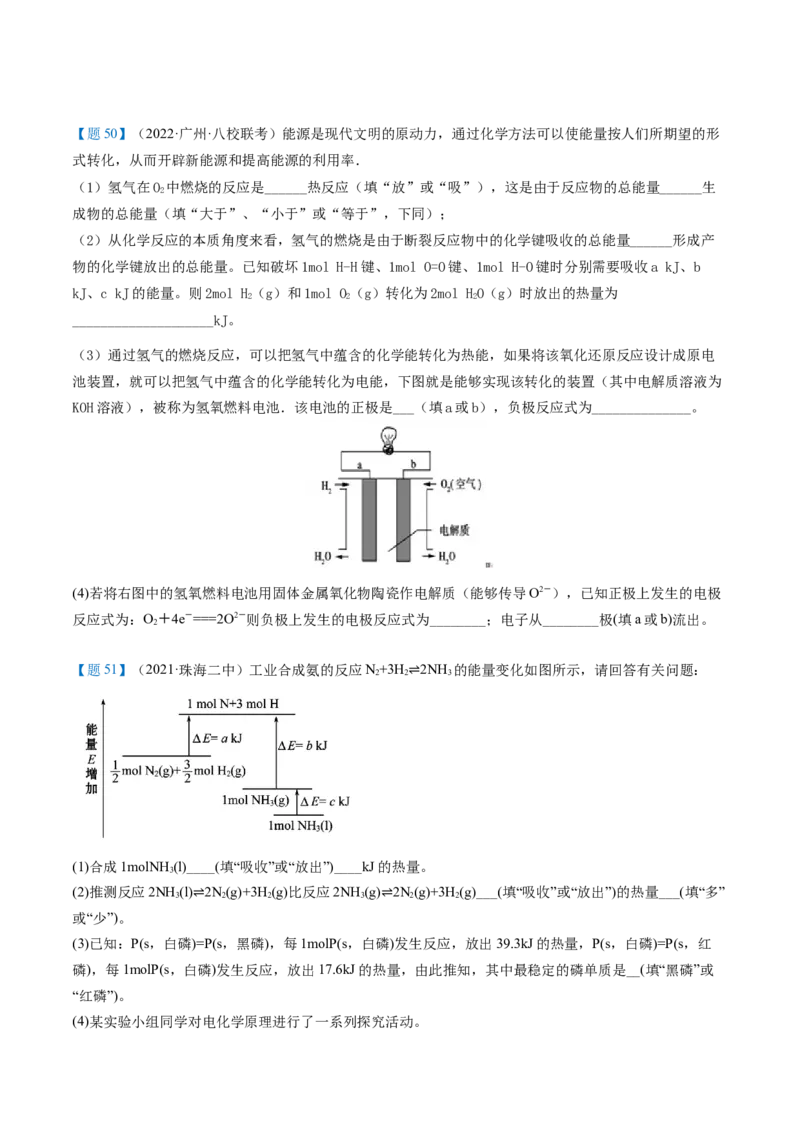
【题48】(2021·玉岩中学)凭借清洁、储量大、能量转换率高、运行稳定等优势,氢能被现代工业视为
最理想、潜力最大的新能源。2020 年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为
氢能源汽车的心脏。某种氢燃料电池的内部结构如图,下列说法正确的是
A. 电池每消耗 11.2L氢气,电路中通过的电子数目为N B. a 处通入的是氧气
A
C. 右侧电极发生的反应为:O+4e-+4H+=2H O D. 右侧电极为电池的负极
2 2
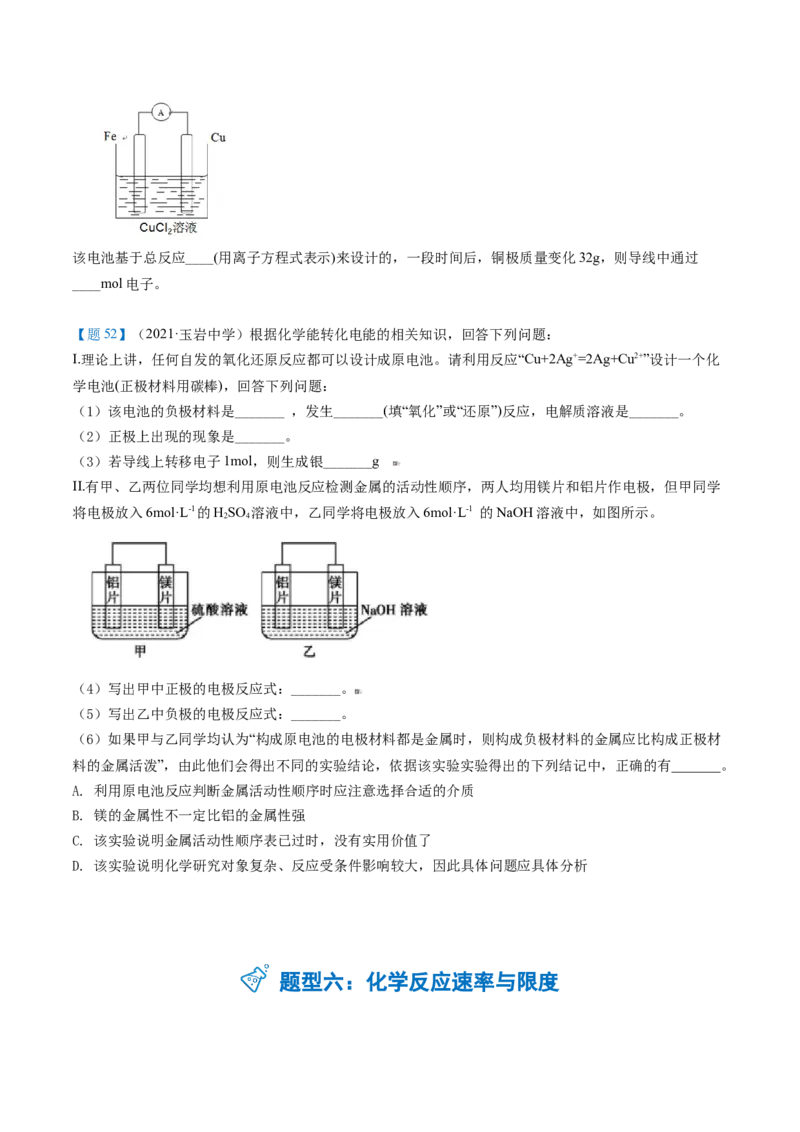
【题49】(2021·佛山)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸中一段时间,
回答下列问题:
①下列说法正确的是_______(填字母代号)。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置正极的电极反应式_______。【题50】(2022·广州·八校联考)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形
式转化,从而开辟新能源和提高能源的利用率.
(1)氢气在O 中燃烧的反应是______热反应(填“放”或“吸”),这是由于反应物的总能量______生
2
成物的总能量(填“大于”、“小于”或“等于”,下同);
(2)从化学反应的本质角度来看,氢气的燃烧是由于断裂反应物中的化学键吸收的总能量______形成产
物的化学键放出的总能量。已知破坏1mol H-H键、1mol O=O键、1mol H-O键时分别需要吸收a kJ、b
kJ、c kJ的能量。则2mol H(g)和1mol O(g)转化为2mol HO(g)时放出的热量为
2 2 2
____________________kJ。
(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电
池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的装置(其中电解质溶液为
KOH溶液),被称为氢氧燃料电池.该电池的正极是___(填a或b),负极反应式为______________。
(4)若将右图中的氢氧燃料电池用固体金属氧化物陶瓷作电解质(能够传导O2-),已知正极上发生的电极
反应式为:O+4e-===2O2-则负极上发生的电极反应式为________;电子从________极(填a或b)流出。
2
【题51】(2021·珠海二中)工业合成氨的反应N+3H 2NH 的能量变化如图所示,请回答有关问题:
2 2 3
⇌
(1)合成1molNH (l)____(填“吸收”或“放出”)____kJ的热量。
3
(2)推测反应2NH (l) 2N(g)+3H(g)比反应2NH (g) 2N(g)+3H(g)___(填“吸收”或“放出”)的热量___(填“多”
3 2 2 3 2 2
或“少”)。
⇌ ⇌
(3)已知:P(s,白磷)=P(s,黑磷),每1molP(s,白磷)发生反应,放出39.3kJ的热量,P(s,白磷)=P(s,红
磷),每1molP(s,白磷)发生反应,放出17.6kJ的热量,由此推知,其中最稳定的磷单质是__(填“黑磷”或
“红磷”)。
(4)某实验小组同学对电化学原理进行了一系列探究活动。该电池基于总反应____(用离子方程式表示)来设计的,一段时间后,铜极质量变化32g,则导线中通过
____mol电子。
【题52】(2021·玉岩中学)根据化学能转化电能的相关知识,回答下列问题:
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化
学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_______ ,发生_______(填“氧化”或“还原”)反应,电解质溶液是_______。
(2)正极上出现的现象是_______。
(3)若导线上转移电子1mol,则生成银_______g 。
II.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学
将电极放入6mol·L-1的HSO 溶液中,乙同学将电极放入6mol·L-1 的NaOH溶液中,如图所示。
2 4
(4)写出甲中正极的电极反应式:_______。
(5)写出乙中负极的电极反应式:_______。
(6)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材
料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结记中,正确的有_______。
A. 利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B. 镁的金属性不一定比铝的金属性强
C. 该实验说明金属活动性顺序表已过时,没有实用价值了
D. 该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
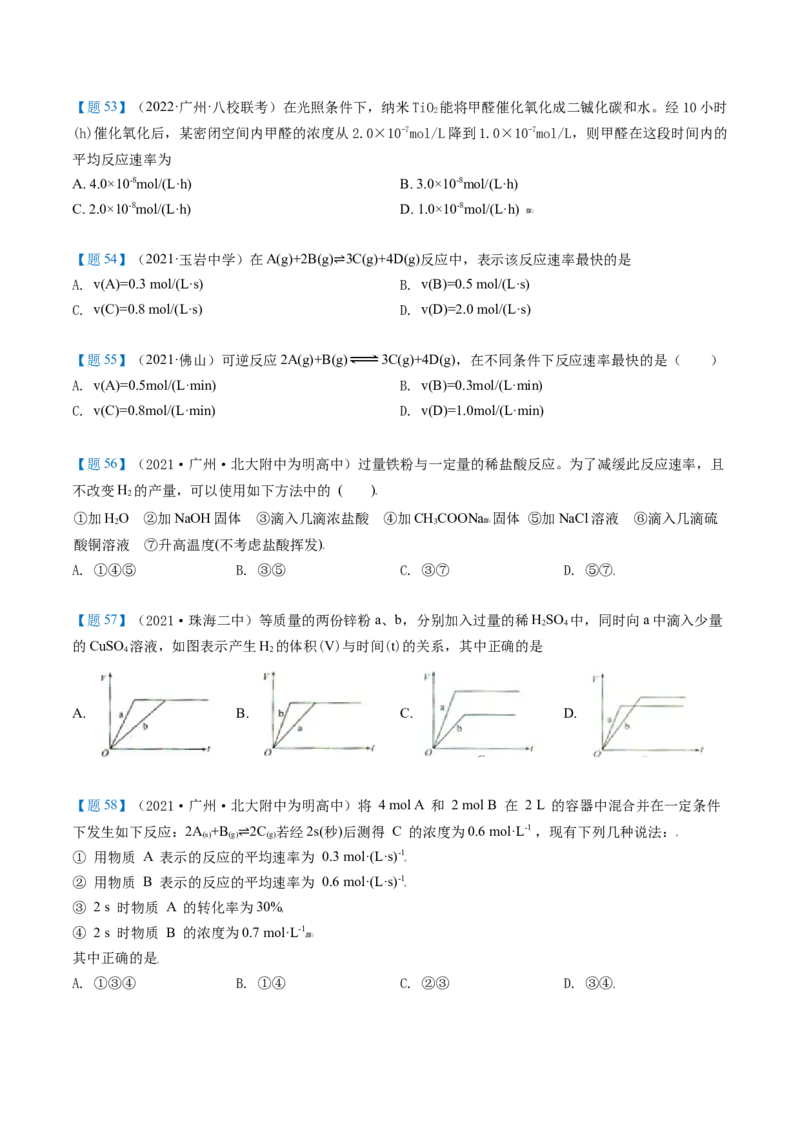
题型六:化学反应速率与限度【题53】(2022·广州·八校联考)在光照条件下,纳米TiO 能将甲醛催化氧化成二铖化碳和水。经10小时
2
(h)催化氧化后,某密闭空间内甲醛的浓度从2.0×10-7mol/L降到1.0×10-7mol/L,则甲醛在这段时间内的
平均反应速率为
A. 4.0×10-8mol/(L·h) B. 3.0×10-8mol/(L·h)
C. 2.0×10-8mol/(L·h) D. 1.0×10-8mol/(L·h)
【题54】(2021·玉岩中学)在A(g)+2B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是
A. v(A)=0.3 mol/(L·s) B. v(B)=0.5 mol/(L·s)
⇌
C. v(C)=0.8 mol/(L·s) D. v(D)=2.0 mol/(L·s)
【题55】(2021·佛山)可逆反应2A(g)+B(g) 3C(g)+4D(g),在不同条件下反应速率最快的是( )
A. v(A)=0.5mol/(L·min) B. v(B)=0.3mol/(L·min)
C. v(C)=0.8mol/(L·min) D. v(D)=1.0mol/(L·min)
【题56】(2021·广州·北大附中为明高中)过量铁粉与一定量的稀盐酸反应。为了减缓此反应速率,且
不改变H 的产量,可以使用如下方法中的 ( )
2
①加HO ②加NaOH固体 ③滴入几滴浓盐酸 ④加CHCOONa 固体 ⑤加NaCl溶液 ⑥滴入几滴硫
2 3
酸铜溶液 ⑦升高温度(不考虑盐酸挥发)
A. ①④⑤ B. ③⑤ C. ③⑦ D. ⑤⑦
【题57】(2021·珠海二中)等质量的两份锌粉a、b,分别加入过量的稀HSO 中,同时向a中滴入少量
2 4
的CuSO 溶液,如图表示产生H 的体积(V)与时间(t)的关系,其中正确的是
4 2
A. B. C. D.
【题58】(2021·广州·北大附中为明高中)将 4 mol A 和 2 mol B 在 2 L 的容器中混合并在一定条件
下发生如下反应:2A +B 2C 若经2s(秒)后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法:
(s) (g) (g)
① 用物质 A 表示的反应的平均速率为 0.3 mol·(L·s)-1
⇌
② 用物质 B 表示的反应的平均速率为 0.6 mol·(L·s)-1
③ 2 s 时物质 A 的转化率为30%
④ 2 s 时物质 B 的浓度为0.7 mol·L-1
其中正确的是
A. ①③④ B. ①④ C. ②③ D. ③④【题59】(2021·珠海二中)在一绝热(不与外界发生热交换)的恒容容器中,发生可逆反应:N(g)
2
+3H (g) 2NH (g),下列描述中不能说明反应已经达到平衡状态的标志是
2 3
A. 容器内温度不再变化
⇌
B. 用N、H、NH 表示反应速率的比为1:3:2的状态
2 2 3
C. 混合气体的平均相对分子质量不再变化
D. 有生成3molH 的同时,生成2molNH
2 3
【题60】(2021·玉岩中学)目前国际空间站处理CO 废气涉及的反应为CO+4H CH+
2 2 2 4
2HO。下列关于该反应的说法正确的是
2
A. 升高温度能减慢该反应的速率
B. 钌催化剂能加快该反应的速率
C. 达到平衡时,v(正)=v(逆)=0
D. 达到平衡时,CO 能100%转化为CH
2 4
【题61】(2021·广州·北大附中为明高中)对可逆反应4NH(g)+5O(g) 4NO(g)+6HO(g),下列叙
3 2 2
述中正确的是
A. 达到化学平衡时,5v (O)=4v (NO)
正 2 逆
B. 若单位时间内生成x mol NO的同时,消耗x mol NH,则反应达到平衡状态
3
C. 未达到化学平衡时,正反应速率一定不等于逆反应速率
D. 达到化学平衡时,3v (NH)=2v (HO)不成立
正 3 正 2
【题62】(2021·玉岩中学)一定温度下,向2L恒容密闭容器中充入0.4molNH 和0.5molO 发生反应
3 2
4NH (g)+5O(g) 4NO(g)+6H O(g)。2min后,NO的浓度为0.06mol·L-1。下列有关说法不正确的是
3 2 2
A. 2min末,用NO表示的反应速率为0.06mol·L-1·min-1
⇌
B. 2min末,NH 的浓度为0.14mol·L-1
3
C. 0~2min内,生成的水的质量为3.24g
D. 0~2min内,O 的物质的量减少了0.15mol
2
【题63】(2021·广州·北大附中为明高中)对于反应2HI(g) H(g)+I (g,紫色),下列叙述能够说明反
2 2
应已达到平衡状态的是
⇌
A. 混合气体的总质量不再变化
B. 温度和容积一定时,容器内压强不再变化
C. 1molH—H键断裂的同时有2molH—I键断裂
D. 各物质的物质的量浓度之比为2:1:1
【题64】(2021·广州·北大附中为明高中)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是_______________________。
(2)实验室中现有NaSO 、MgSO 、Ag SO 、KSO 等4种溶液,可与上述实验中CuSO 溶液起相似作用的
2 4 4 2 4 2 4 4
是____________。
(3)要加快上述实验中气体产生的速率,还可采取的措施有_____________________(答两种)。
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合
溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体。记录获得相同体积的气体所需时间。
实验
A B C D E F
混合溶液
4 mol·L-1 HSO/mL 30 V V V V V
2 4 1 2 3 4 5
饱和CuSO 溶液/mL 0 0.5 2.5 5 V 20
4 6
HO/mL V V V V 10 0
2 7 8 9 10
①请完成此实验设计,其中:V=________,V=________,V=______;
1 6 9
②该同学最后得出的结论为:当加入少量CuSO 溶液时,生成氢气的速率会大大提高。但当加入的CuSO
4 4
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:________。
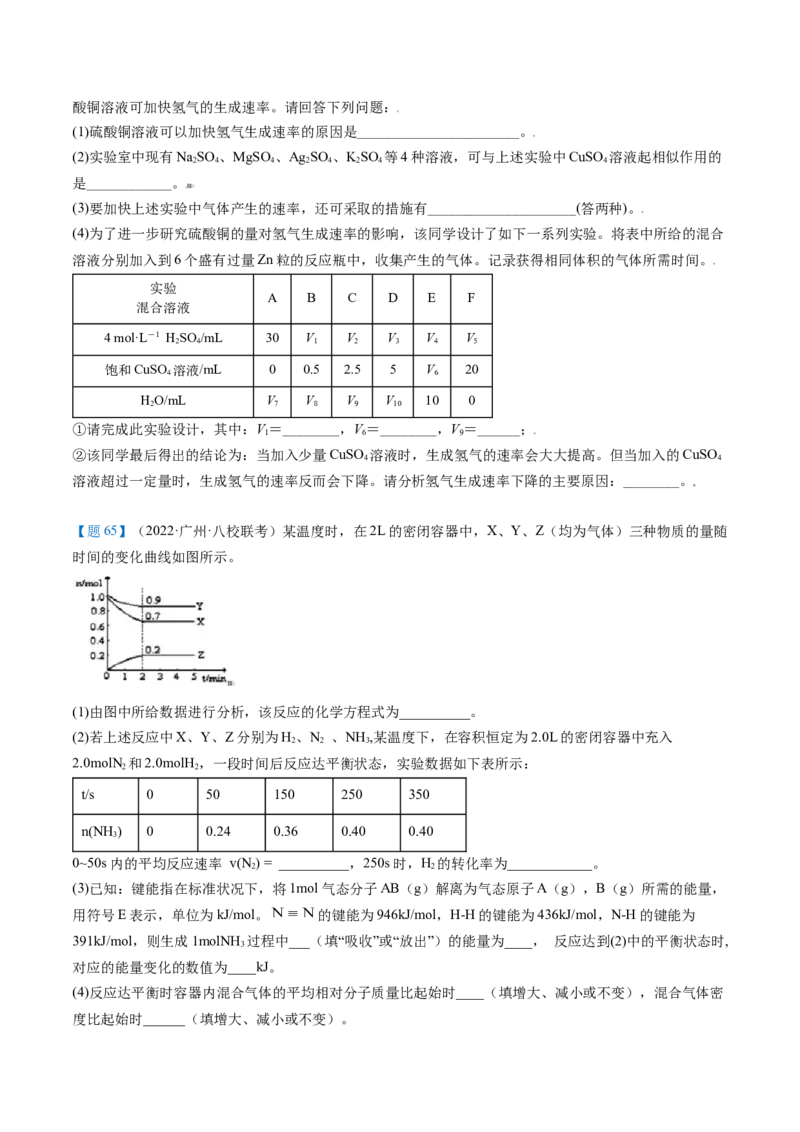
【题65】(2022·广州·八校联考)某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随
时间的变化曲线如图所示。
(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H、N 、NH ,某温度下,在容积恒定为2.0L的密闭容器中充入
2 2 3
2.0molN 和2.0molH,一段时间后反应达平衡状态,实验数据如下表所示:
2 2
t/s 0 50 150 250 350
n(NH ) 0 0.24 0.36 0.40 0.40
3
0~50s内的平均反应速率 v(N ) = __________,250s时,H 的转化率为____________。
2 2
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,
用符号E表示,单位为kJ/mol。 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为
391kJ/mol,则生成1molNH 过程中___(填“吸收”或“放出”)的能量为____, 反应达到(2)中的平衡状态时,
3
对应的能量变化的数值为____kJ。
(4)反应达平衡时容器内混合气体的平均相对分子质量比起始时____(填增大、减小或不变),混合气体密
度比起始时______(填增大、减小或不变)。(5)为加快反应速率,可以采取的措施是_______
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH
3
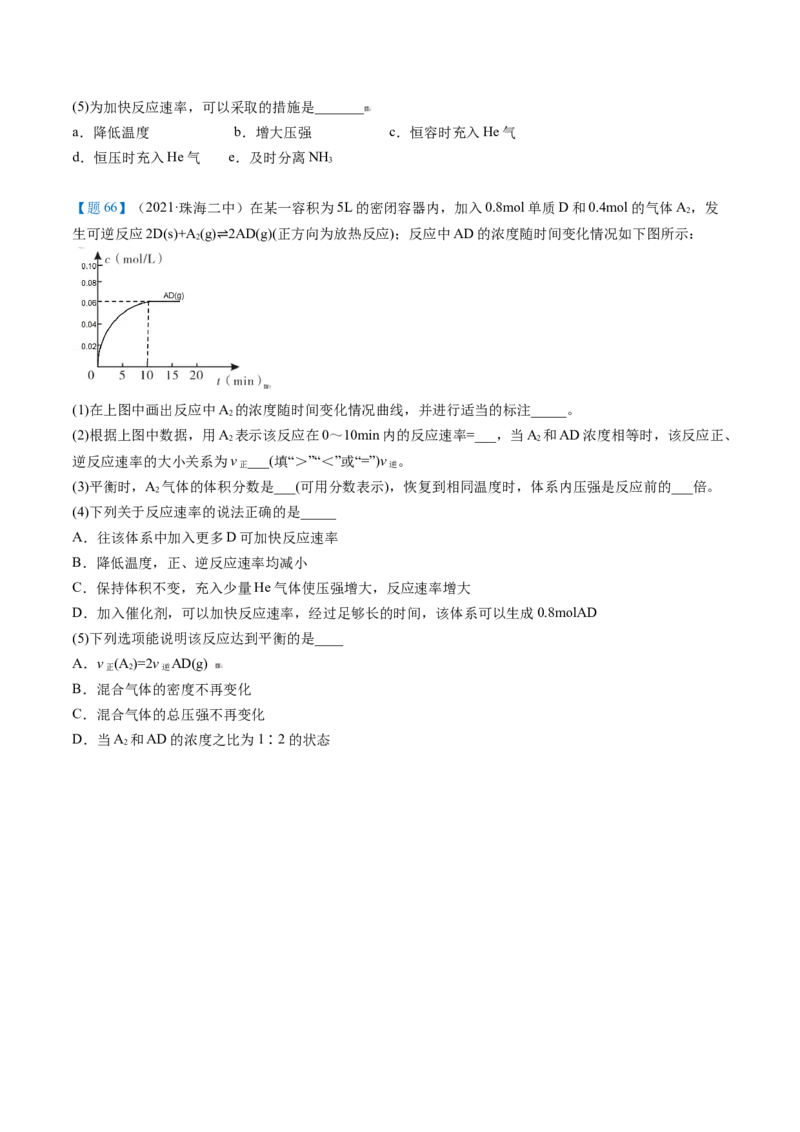
【题66】(2021·珠海二中)在某一容积为5L的密闭容器内,加入0.8mol单质D和0.4mol的气体A,发
2
生可逆反应2D(s)+A (g) 2AD(g)(正方向为放热反应);反应中AD的浓度随时间变化情况如下图所示:
2
⇌
(1)在上图中画出反应中A 的浓度随时间变化情况曲线,并进行适当的标注_____。
2
(2)根据上图中数据,用A 表示该反应在0~10min内的反应速率=___,当A 和AD浓度相等时,该反应正、
2 2
逆反应速率的大小关系为v ___(填“>”“<”或“=”)v 。
正 逆
(3)平衡时,A 气体的体积分数是___(可用分数表示),恢复到相同温度时,体系内压强是反应前的___倍。
2
(4)下列关于反应速率的说法正确的是_____
A.往该体系中加入更多D可加快反应速率
B.降低温度,正、逆反应速率均减小
C.保持体积不变,充入少量He气体使压强增大,反应速率增大
D.加入催化剂,可以加快反应速率,经过足够长的时间,该体系可以生成0.8molAD
(5)下列选项能说明该反应达到平衡的是____
A.v (A )=2v AD(g)
正 2 逆
B.混合气体的密度不再变化
C.混合气体的总压强不再变化
D.当A 和AD的浓度之比为1∶2的状态
2倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育