文档内容
第七章 有机化合物
第三节 乙醇与乙酸
第二课时 乙酸 官能团与有机化合物的分类
在初中化学中,只简单地介绍了乙酸的用途,没有从组成和结构角度认识其性质、存在和用途。
乙酸是学生比较熟悉的生活用品,又是典型的烃的衍生物,从这两种烃的衍生物的组成、结构和性
质出发,可以让学生知道官能团对有机物性质的重要影响,建立“(组成)结构一性质一用途”的
有机物学习模式。在学生的头脑中逐步建立烃基与官能团位置关系等立体结构模型,帮助学生打好
进一步学习的方法论基础,同时鼓励学生用学习到的知识解释常见有机物的性质和用途。
教学目标
1.知道乙酸的组成、结构、官能团、物理性质及用途。
2.会运用乙酸的结构分析其化学性质。
核心素养
1.微观探析:从官能团的角度认识乙酸的性质。
2.科学探究: 设计实验探究乙酸的性质。
重点:乙酸的组成、乙酸的酸性和酯化反应。
难点: 使学生建立乙酸分子的立体结构模型,并能从结构角度初步认识乙酸的酯化反应。
查找相关资料,准备课件准备资料。
教师讲述:我国是世界上谷物酿醋最早的国家,早在公元前8世纪就已有了醋的文字记载。春秋战
国时期,已有专门酿醋的作坊。到汉代时,醋开始普遍生产。南北朝时,食醋的产量和销量都已很
大,其时的名著《齐民要术》曾系统地总结了我国劳动人民从上古到北魏时期的制醋经验和成就,
书中共收载了22种制醋方法,这也是我国现存史料中,对粮食酿造醋的最早记载。
一、乙酸的物理性质教师讲述:无色刺激性气味液体,熔点16.6℃,低于16.6℃就凝结成冰状晶体,所以无水乙酸又称
冰醋酸。乙酸易溶于水和酒精。
二、乙酸的分子组成与结构
教师讲述:教师讲述乙酸的分子式、结构式、结构简式、官能团
C HO CHCOOH —COOH(羧基)
2 4 2 3
投影展示:乙酸球棍模型,比例模型
学生活动:思考与讨论:
(1)食醋可以清除水壶中的少量水垢(主要成分是碳酸钙),这是利用了乙酸的什么性质?请写
出相关反应的化学方程式
(2)如何比较乙酸与碳酸、盐酸的酸性强弱?请查阅资料,与同学讨论,根据生活经验设计实验
方案。
学生讨论展示交流成果,教师讲评。
三、乙酸的化学性质
教师小结:1、乙酸的弱酸性
电离方程式:CHCOOH CHCOO— + H+
3 3
Mg + 2CH COOH → (CH COO) Mg + H↑
3 3 2 2
CuO + 2CH COOH → (CH COO) Cu + H O
3 3 2 2
NaOH+ CH COOH → CH COONa + H O
3 3 2
CaCO + 2CHCOOH → (CH COO) Ca + CO ↑+HO
3 3 3 2 2 2
酸性比较:HCl>CH COOH > H CO >HClO
3 2 3
演示实验:实验7-6:在一支试管中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL
乙酸,再加入几片碎壳片。连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和
NaCO,溶液的液面上(如图7-22),观察现象。
2 3
学生活动:思考与交流:
1、装药品的顺序如何?
2、浓硫酸的作用是什么?3、如何提高乙酸乙酯的产率?
4、得到的反应产物是否纯净?主要杂质有哪
些?如何除去?
5、饱和NaCO 溶液有什么作用?
2 3
6、为什么导管不插入饱和NaCO 溶液中?有无其它防倒吸的方法?
2 3
学生讨论展示交流成果,教师讲评。
教师小结:
1、混合酸的顺序:先加乙醇再加浓HSO 最后加乙酸
2 4
2、浓HSO 作用:催化剂、吸水剂
2 4
3、加热的目的:提高反应速率
4、导管的作用:导气、冷凝
5、饱和NaCO 的作用: 中和乙酸、溶解乙醇、抑制乙酸乙酯在水中的溶解
2 3
注意:不能伸到液面下(防倒吸)
教师讲解:2、酯化反应
浓硫酸
CHCOOH + HOC H △ CHCOOC H+H O
3 2 5 3 2 5 2
定义:酸和醇起作用,生成酯和水的反应叫做酯化反应
学生活动:思考:酯化反应中酸和醇分子内的化学键怎样断裂?
学生活动:探究酯化反应可能的反应方式
可能一:
可能二:
学生讨论展示交流成果,教师讲评。
教师小结:根据同位素示踪方法,标记乙醇的氧原子,得到下列结果。
酯化反应实质:酸脱羟基醇脱羟基上的氢原子。
酯化反应形式:取代反应。四、官能团与有机物分类
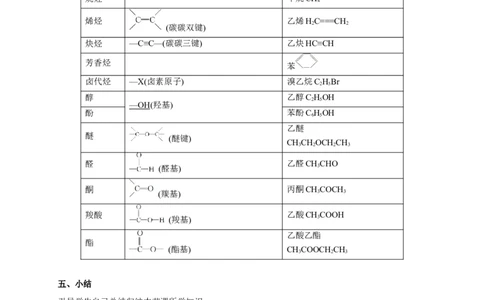
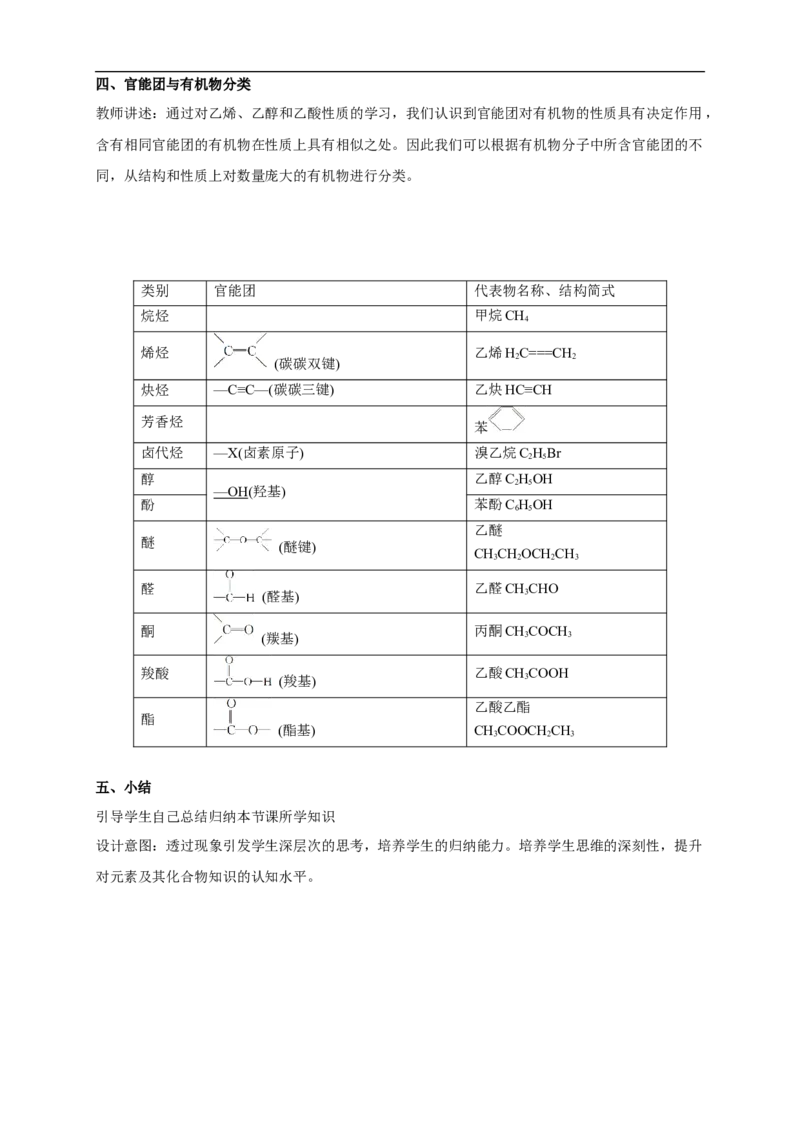
教师讲述:通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,
含有相同官能团的有机物在性质上具有相似之处。因此我们可以根据有机物分子中所含官能团的不
同,从结构和性质上对数量庞大的有机物进行分类。
类别 官能团 代表物名称、结构简式
烷烃 甲烷CH
4
烯烃 乙烯HC===CH
2 2
(碳碳双键)
炔烃 —C≡C—(碳碳三键) 乙炔HC≡CH
芳香烃
苯
卤代烃 —X(卤素原子) 溴乙烷C HBr
2 5
醇 乙醇C HOH
2 5
—OH(羟基)
酚 苯酚C HOH
6 5
乙醚
醚 (醚键)
CHCHOCH CH
3 2 2 3
醛 乙醛CHCHO
(醛基) 3
酮 丙酮CHCOCH
(羰基) 3 3
羧酸 乙酸CHCOOH
(羧基) 3
乙酸乙酯
酯
(酯基) CHCOOCH CH
3 2 3
五、小结
引导学生自己总结归纳本节课所学知识
设计意图:透过现象引发学生深层次的思考,培养学生的归纳能力。培养学生思维的深刻性,提升
对元素及其化合物知识的认知水平。