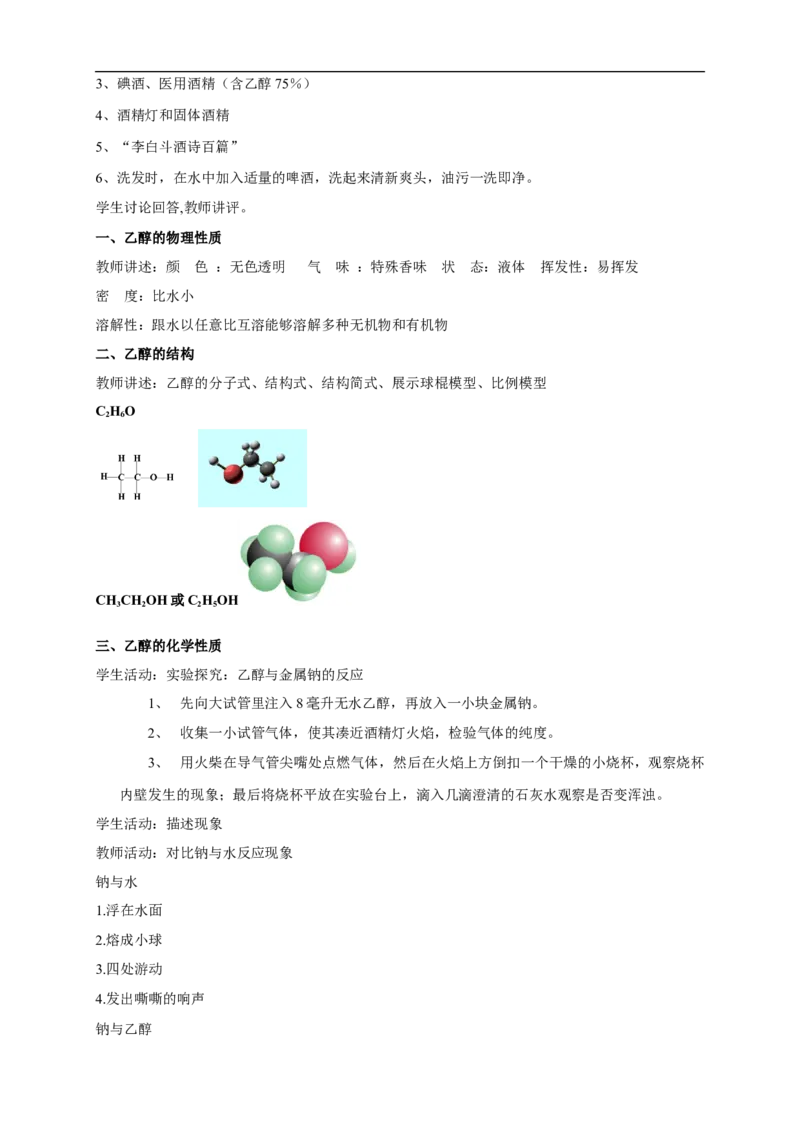文档内容
第七章 有机化合物
第三节 乙醇与乙酸
第一课时 乙醇
在初中化学中,只简单地介绍了乙醇和乙的用途,没有从组成和结构角度认识其性质、存在和
用途。乙醇是学生比较熟悉的生活用品,又是典型的烃的衍生物,从烃的衍生物的组成、结构和性
质出发,可以让学生知道官能团对有机物性质的重要影响,建立“(组成)结构一性质一用途”的
有机物学习模式。教学设计中,在学生初中知识的基础上,突出从烃到烃的衍生物的结构变化,强
调官能团与性质的关系,在学生的头脑中逐步建立烃基与官能团位置关系等立体结构模型,帮助学
生打好进一步学习的方法论基础,同时鼓励学生用学习到的知识解释常见有机物的性质和用途。
教学目标
1.知道乙醇的组成、结构、官能团、物理性质及用途。
2.了解烃的衍生物的概念及官能团与性质的关系。
3.会运用乙醇的结构分析其化学性质。
核心素养
1.微观探析:从官能团的角度认识乙醇的组成、结构、性质和变化,形成“结构决定性质”的观念。
2.科学探究:设计实验探究乙醇的结构与性质。
重点:乙醇、乙醇的取代反应与氧化反应。
难点:使学生建立乙醇的立体结构模型,并能从结构角度初步认识乙醇的氧化。
查找相关资料,准备课件准备资料。
学生活动:思考与交流:下列应用体现了乙醇的哪些性质和用途
1、用乙醇汽油替代普通汽油-“中国汽车要喝酒”
2、高烧病人擦拭酒精或白酒降温3、碘酒、医用酒精(含乙醇75%)
4、酒精灯和固体酒精
5、“李白斗酒诗百篇”
6、洗发时,在水中加入适量的啤酒,洗起来清新爽头,油污一洗即净。
学生讨论回答,教师讲评。
一、乙醇的物理性质
教师讲述:颜 色 :无色透明 气 味 :特殊香味 状 态:液体 挥发性:易挥发
密 度:比水小
溶解性:跟水以任意比互溶能够溶解多种无机物和有机物
二、乙醇的结构
教师讲述:乙醇的分子式、结构式、结构简式、展示球棍模型、比例模型
CHO
2 6
CH CH OH或CHOH
3 2 2 5
三、乙醇的化学性质
学生活动:实验探究:乙醇与金属钠的反应
1、 先向大试管里注入8毫升无水乙醇,再放入一小块金属钠。
2、 收集一小试管气体,使其凑近酒精灯火焰,检验气体的纯度。
3、 用火柴在导气管尖嘴处点燃气体,然后在火焰上方倒扣一个干燥的小烧杯,观察烧杯
内壁发生的现象;最后将烧杯平放在实验台上,滴入几滴澄清的石灰水观察是否变浑浊。
学生活动:描述现象
教师活动:对比钠与水反应现象
钠与水
1.浮在水面
2.熔成小球
3.四处游动
4.发出嘶嘶的响声
钠与乙醇1.开始时沉在乙醇底部
2.不熔成小球
3.四处游动
4.发出嘶嘶的响声
教师小结:1、乙醇与钠的反应
2CHCHOH+2Na→2CH CHONa+H ↑其它活泼金属如钾、钙、镁等也可与乙醇反应
3 2 3 2 2
学生活动:练习:写出乙醇与镁反应的化学方程式
学生书写,教师讲评:
2CHCHOH+Mg→(CH CHO) Mg+H↑
3 2 3 2 2 2
学生活动:思考与交流:钠与水、与乙醇反应对比
1、从二者均能反应放出氢气,可得出什么结论?
2、从二者反应剧烈程度不同分析,乙醇 和水分子的羟基中的H原子哪个较活泼?乙基对乙醇的性
质有无影响?
学生展示讨论结果,教师讲评:
[结论] 1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水
官能团决定有机物的性质,连接官能团的其它部分对性质也有所影响。
教师讲述:2、乙醇的氧化反应
(1)乙醇在空气中燃烧 :
现象:产生淡蓝色火焰,同时放出大量热。
点燃
C HOH + 3 O 2CO +3H O
2 5 2 2 2
学生活动: 探究实验:
①用小试管取2mL无水乙醇
②加热一端绕成螺旋状的铜丝至红热
③将铜丝趁热插到盛有乙醇的试管底部
④反复操作几次,观察铜丝颜色和液体气味的变化。
学生展示结果,教师讲评:
【实验现象】a.铜丝红色→黑色→红色反复变化
b.在试管口可以闻到刺激性气味
学生活动:[思考]铜丝在此实验中起什么作用?
教师小结:
催化剂
2CHOH+O △ 2CHCHO+2H O铜丝在实验中作催化剂
5 2 3 2四、小结
引导学生自己总结归纳本节课所学知识。