文档内容
第六章 化学反应与能量
第二节 化学反应速率与限度
第 1 课时 化学反应速率
本节是必修二第六章第二节第一课时化学反应的速率。《普通化学课程标准(2017版)》对
这一节的内容要求如下:体会从限度和快慢两个方面去认识和调控化学反应的重要性。了解可逆反
应的含义,知道可逆反应在一定条件下能达到化学平衡状态。知道化学反应平均速率的表示方法,
通过实验探究影响化学反应速率的因素。认识化学变化是有条件的,学习运用变量控制方法研究化
学反应,了解控制反应条件在生产和科学研究中的作用。
考虑到通过初中和高中的化学学习,学生对化学反应速率与反应条件相关,改变反应条件
(如使用催化剂)可调控反应速率等知识已有所了解。教材中化学反应速率影响因素的内容,以新
旧兼容、详略有别的方式编排。教材结合学生学过的相关知识,补充一些生活、生产中需要通过反
应条件调控反应速率的实例,说明认识化学反应速率影响因素的重要性,并借此体现调控反应速率
的意义和价值。在已知催化剂这一反应速率影响因素的基础上,通过“探究”,重点引导学生探讨
反应温度和反应物浓度对化学反应速率的影响,并结合浓度影响因素,针对气体反应说明压强的影
响。
“探究”中安排的两个实验和一个讨论,教材采取了学生自主参与度不同的设计。对反应温
度的影响的探究给出了具体步骤,学生只需自主操作并观察、比较;对反应物浓度的影响的探究只
给出探究设计提示,学生需要根据要求选择实验用品,设计并实施实验。“问题与讨论”则需要学
生自主提出问题、进行假设、设计实验方案。这种探究水平的进阶式设计,意在体现一定探究性的
前提下保证可操作性,同时也照顾到全国范围内化学教学的实际可行性。
除“探究”之外,教材还利用“思考与讨论”引导学生探讨得出影响化学反应速率的其他一
些因素,如反应物颗粒大小、反应物接触面积等。这样将教材中提及的各种不同影响因素分层次处
理,既突出浓度(压强)、温度、催化剂的影响因素等重点内容,又不局限于这几个因素,表明影
响化学反应速率的因素还有很多。
【学习目标】1、了解化学反应速率的概念和表示方法。
2、能够进行化学反应速率的简单计算。
3、理解影响化学反应速率的因素及规律。
【核心素养】
1、变化观念:认识反应条件对化学反应速率的影响(控制变量)。
2、模型认知:能用一定的理论模型说明外界条件改变对反应速率的影响。
重点:化学反应速率的概念及其影响因素;
难点:化学反应速率的影响因素。
多媒体、5%H O 溶液、1mol/LFeCl3溶液、0.1mol/L盐酸、1mol/L盐酸、大理石碎块、冷水、
2 2
热水、试管、试管夹、烧杯。
【引入】
在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现所期待的物质转化或能
量转化,还要关注化学反应进行的快慢和程度,以提高生产效率。
【思考与讨论】
在化学实验和日常生活中,我们经常观察到这样的现象:有的反应进行的快,有的进行的慢。
你了解下图涉及的化学反应进行的快慢吗?反应的快慢程度与我们有什么关系?
不同的化学反应进行的快慢千差万别,快和慢是相对而言的,我们以上的判断方法都是定性地
描述反应的快慢。而在科学研究和实际应用中,往往需要定量地描述一个反应的快慢。
什么是定性?什么是定量?
例如:我们学过物理都知道:
(1) 光的传播速度是很快的;
(2) 光在空气中的传播速度3×108 m/s。
【过渡】在物理中我们是如何定量地判断一个物体移动速度快慢的?用速度来描述:单位时间内物体移动的距离的大小。
那么化学上又是如何定量地判断一个化学反应的快慢的呢?
【讲解】
一、化学反应速率
1.定义
化学反应速率是用来衡量化学反应过程进行的快慢的物理量。通常用单位时间内反应物浓度的
减少量或生成物浓度的增加量(均取正值)表示。
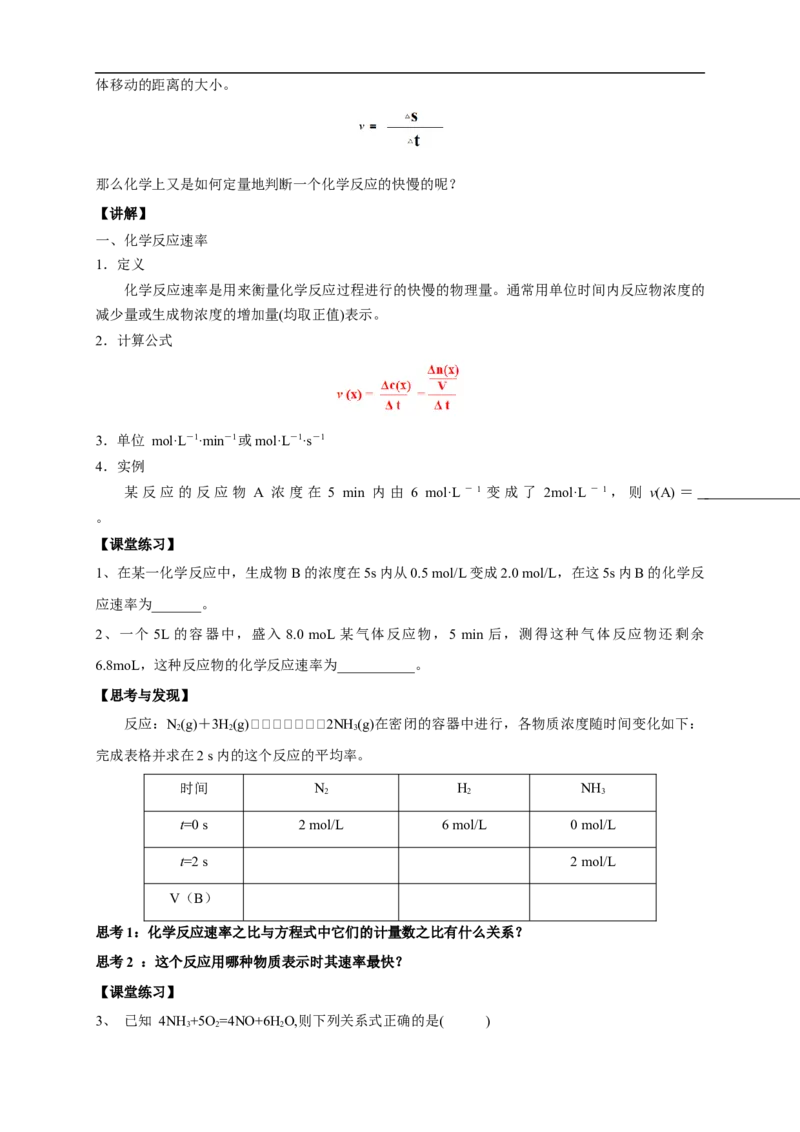
2.计算公式
3.单位 mol·L-1·min-1或mol·L-1·s-1
4.实例
某反应的反应物 A 浓度在 5 min 内由 6 mol·L -1 变成了 2mol·L -1,则 v(A) =
。
【课堂练习】
1、在某一化学反应中,生成物B的浓度在5s内从0.5 mol/L变成2.0 mol/L,在这5s内B的化学反
应速率为_______。
2、一个 5L 的容器中,盛入 8.0 moL 某气体反应物,5 min 后,测得这种气体反应物还剩余
6.8moL,这种反应物的化学反应速率为___________。
【思考与发现】
反应:N(g)+3H(g)2NH (g)在密闭的容器中进行,各物质浓度随时间变化如下:
2 2 3
完成表格并求在2 s内的这个反应的平均率。
时间 N H NH
2 2 3
t=0 s 2 mol/L 6 mol/L 0 mol/L
t=2 s 2 mol/L
V(B)
思考1:化学反应速率之比与方程式中它们的计量数之比有什么关系?
思考2 :这个反应用哪种物质表示时其速率最快?
【课堂练习】
3、 已知 4NH +5O =4NO+6HO,则下列关系式正确的是( )
3 2 2A. 4/5v(NH )=v(O) B.4/5v(NH )=v(HO)
3 2 3 2
C. 5/6v(O )=v(HO) D. 4/5v(O )=v(NO)
2 2 2
4、反应 A + 3B = 2C + 2D 在四种不同条件下的化学反应速率为:
(1)v(A)=0.3mol/L·s (2)v(B)=0.6mol/L·s
(3)v(C)=0.4mol/L·s (4)v(D)=0.45mol/L·s
则该反应速率的快慢顺序为 。
【思考与讨论】
对于下列反应,你是希望其反应速率越快越好还是越慢越好?
■钢铁腐蚀 ■ 食物腐坏 ■ 炼钢 ■ 合成氨
调控化学反应速率常常是决定化学实验成败或化工生产成本的关键。有哪些因素能够影响化学
反应速率呢?
【讲解】
二、影响化学反应速率的因素
【实验探究】
影响化学反应速率的因素
【问题】我们已经知道催化剂可以影响化学反应速率,此外,还有哪些反应条件会影响化学反应的
速率?
【假设】影响化学反应速率的因素可能有反应温度、反应物浓度等。
【用品】5%H O 溶液、1mol/LFeCl 溶液、0.1mol/L盐酸、1mol/L盐酸、大理石碎块、冷水、热水、
2 2 3
试管、试管夹、烧杯。
(1) 反应温度的影响
在两支大小相同的试管中均加入2mL5%H O 溶液,同时滴入2滴1mol/LFeCl ,溶液。待试管
2 2 3
中均有适量气泡出现时,将其中一支试管放入盛有冷水的烧杯中,另一支试管放入盛有热水的烧杯
中,观察现象并进行对比。
不同温度环境 实验现象
冷水
热水
结论1:当其它条件不变时,升高温度,化学反应速率增大;降低温度,化学反应速率减小
(2) 反应物浓度的影响
利用实验室提供的用品,设计实验方案并提请教师审阔,待教师同意后进行实验(提示:探究
某影响因素时,需保持其他条件因素相同)。步骤: 。
记录: 。
变量控制
科学研究中,对于多因素(多变量)的问题,常常采用只改变其中的某一个因素,控制其他因
素不变的研究方法,使多因素的问题变成几个单因素的问题分别加以研究,最后再将几个单因素问
题的研究结果加以综合。这种变量控制的方法是科学探究中常用的方法。例如,以上探究在比较不
同温度对化学反应速率的影响时,控制浓度和其他影响因素相同;而比较不同浓度对化学反应速率
的影响时,则控制温度和其他影响因素相同;最后综合得出影响化学反应速率的多种因素。
【实验探究】浓度对化学反应速率的影响
1、请预计大理石( CaCO )分别与0.1mol/L和1mol/L的盐酸反应的快慢。你能得出什么结论吗?
3
结论2:增大反应物的浓度反应速率加快,减小反应物的浓度反应速率减慢。
2、块状CaCO 、粉末状CaCO 与0.1 mol/L的盐酸反应谁快谁慢?为什么?
3 3
结论3:增大固体表面积可以加快反应速率(接触充分)。
【实验探究】催化剂对化学反应速率的影响
现象 结论
加入MnO
2
加入FeCl
3
不加其他试剂
结论4:加入催化剂(正)能加快化学反应的速率。
【实验探究】压强对反应速率的影响
压强对反应速率的影响
有气体参加的反应,改变压强对反应速率的影响实质是改变体积,使反应物的浓度改变。
(1)压缩体积或充入气态反应物,使压强增大,都能加快化学反应速率。
(2)体积不变,充入不参与反应的气体。虽然总的压强增大,但反应物浓度不发生变化,故化学反应
速率不变。
【总结】影响因素 规律
内 反应物本身的性 反应物的化学性质越活泼,化学反应速率越快;反之化学反应速
因 质 率越慢
增大反应物的浓度,化学反应速率增大;减小反应物的浓度,化
浓度
学反应速率减小
温度 升高温度,化学反应速率增大;降低温度,化学反应速率减小
外
因
催化剂 一般地,使用催化剂能极大地加快反应速率
固体的表面积 增大固体反应物的表面积,化学反应速率加快
其他 光照、溶剂、形成原电池等,也能影响化学反应速率
【思考与讨论】
下列调控反应速率的措施或实验中,分别利用或体现了哪些影响反应速率的因素?
(1)向炉膛内鼓风,用煤粉代替煤块可以使炉火更旺。
(2)把食物存放在冰箱里,在糕点包装内放置除氧剂可以延长食品保质期。
(3)做化学实验时,为加速反应的进行,通常将块状或颗粒状的固体药品研细并混匀,或者将固
体试剂溶于水配成溶液后再进行实验。
(4)铁在空气中和在纯氧中反应的剧烈程度明显不同。
科学·技术·社会
神奇的催化剂
催化剂是现代化学中关键而神奇的物质之一。据统计,有 80%以上的化工生产过程(如氨、硫
酸、硝酸的合成,乙烯、丙烯、苯乙烯的聚合,煤、石油、天然气的综合利用,等等)使用了催化
剂,目的是增大反应速率,提高生产效率。在资源利用、能源开发、医药制造、环境保护等领域,
催化剂有着广泛的应用。催化剂十分神奇,它能极大地提高化学反应速率(可使反应速率增大几个
到十几个数量级),而自身的组成、化学性质和质量在反应前后不发生变化;它和一些反应体系的
关系就像钥匙与锁的关系,具有一定的选择性。
生物体内几乎所有的化学反应(如淀粉、脂肪、蛋白质的水解,DNA的复制等)都是由生物
体内存在的特殊催化剂——酶所催化的。酶比一般的催化剂具有更高的选择性和催化效率,而且是
在正常体温的条件下发生作用,反应条件温和。受酶的启示,科学家开牌了设计和合成催化剂的新
途径,正在研制具有生物酶某些特性的化学酶,以期实现“仿酶催化”。催化剂的神奇面纱至今尚
未完全揭开,对催化剂的研究是当代化学一个极具魅力和应用前景的重要课题。【课堂练习】
1.下列关于化学反应速率的说法,不正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率的大小主要取决于反应物的性质
C.化学反应速率可以用单位时间内生成某物质的质量的多少来表示
D.化学反应速率常用单位有mol·L-1·s-1和mol·L-1·min-1
2.一定条件下,分别对反应C(s)+CO(g)2CO(g)进行如下操作(只改变该条件):①升高反应体
2
系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中
一定能使反应速率显著变大的是( )
A.①②③④ B.①③④
C.①② D.①③
3.已知合成氨反应N(g)+3H(g)2NH (g),其浓度数据如下:
2 2 3
N H NH
2 2 3
起始浓度/mol·L-1 1.0 3.0 0
2 s末浓度/mol·L-1 0.6 1.8 0.8
当用氨气浓度的增加来表示该化学反应的速率时,其速率为( )
A.0.2 mol·L-1·s-1 B.0.4 mol·L-1·s-1
C.0.6 mol·L-1·s-1 D.0.8 mol·L-1·s-1
4.把下列四种X溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此
时,X和盐酸缓慢地进行反应,其中反应最快的是( )
A.10 ℃ 20 mL 3 mol·L-1的X溶液
B.20 ℃ 30 mL 2 mol·L-1的X溶液
C.20 ℃ 10 mL 4 mol·L-1的X溶液
D.10 ℃ 10 mL 2 mol·L-1的X溶液
5.实验室用锌粒与2 mol·L-1硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
A.用锌粉代替锌粒
B.改用3 mol·L-1硫酸溶液
C.改用热的2 mol·L-1硫酸溶液
D.向该硫酸溶液中加入等体积的水本节课化学反应速率的概念和影响化学反应速率的因素是重点内容,而影响化学反应速率的
因素的影响的开放性很强,要求学生自己设计实验进行探究。所以用实验引起学生的兴趣是让学生
脑海中有初步印象的最佳方法。在教学活动中应该关注学生个体差异,发现与挖掘课堂教学资源。
课堂实施过程中学会倾听、欣赏、微笑、等待。注意课堂组织,自己的语言简练、艺术些,学生的
表达机会多些,活动丰富些。从而培养学生发展的核心素养。