文档内容
6.2.1 化学反应的速率(学案)
1.了解化学反应速率的概念和表示方法。
2.能够进行化学反应速率的简单计算。
3.理解影响化学反应速率的因素及规律。
重点:化学反应速率的概念及其影响因素。
难点:化学反应速率的概念及其影响因素。
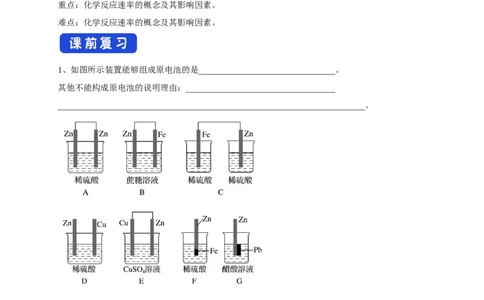
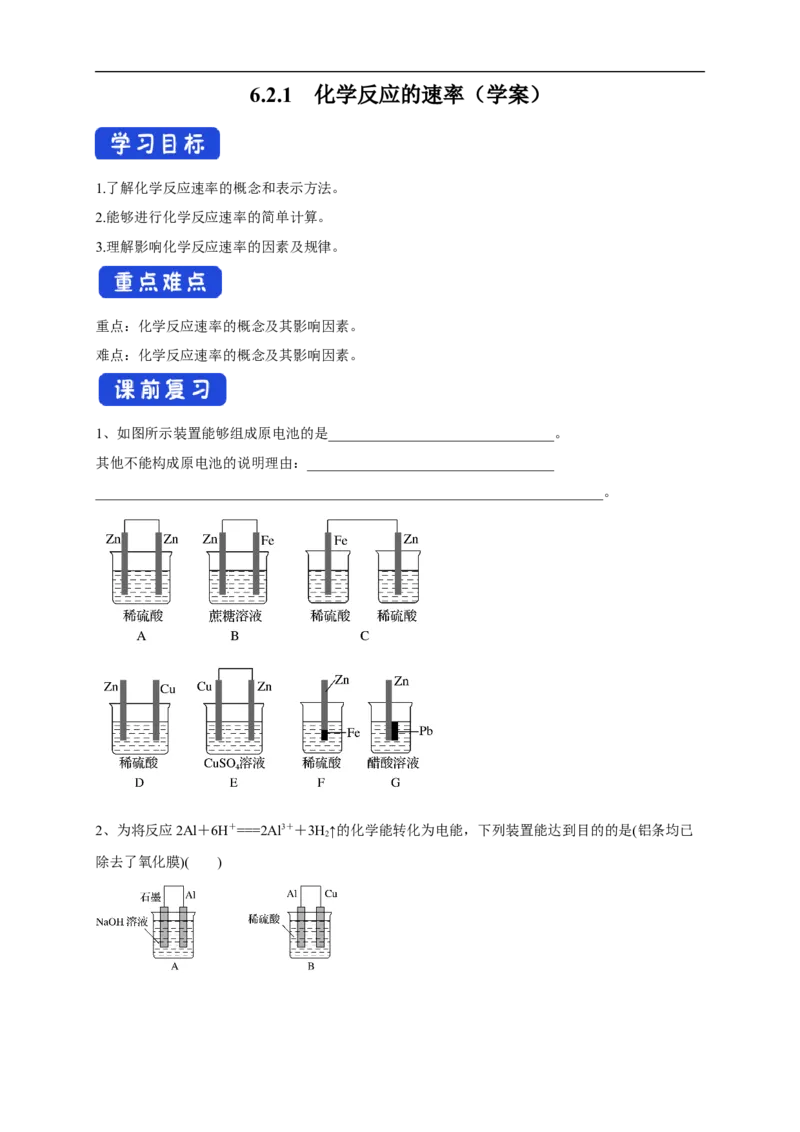
1、如图所示装置能够组成原电池的是________________________________。
其他不能构成原电池的说明理由:___________________________________
________________________________________________________________________。
2、为将反应2Al+6H+===2Al3++3H↑的化学能转化为电能,下列装置能达到目的的是(铝条均已
2
除去了氧化膜)( )1、思考与交流:化学反应的快慢是相对的!不同的化学反应,快慢不同。你了解下列化学变化过
程进行的快慢吗?反应的快慢与我们有什么关系?
2、化学反应速率是如何定义的呢?回忆一下物理中是怎么描述物体运动的快慢?
3、用∆t来表示时间,∆c表示浓度变化,v表示反应速率,你能用字母符号来表示化学反应速率吗?
4、在某一化学反应里,反应物A的浓度在10 s内从4.0 mol/L变成1.0 mol/L。在这10 s内A的化
学反应速率为多少?
5、在2 L的密闭容器中,加入1 mol N 和3 mol H ,发生 N+3H == 2NH ,在2s末时,测得容器
2 2 2 2 3
中含有0.4 mol的NH ,求该反应的化学反应速率。
3
6、探究温度对反应速率的影响:
【假设】
影响化学反应速率的因素可能有反应温度、反应物浓度等。
【用品】5%H,O,溶液、1mol/LFeCl,溶液、0.1mol/L盐酸、1mol/L盐酸、大理石碎块、冷水、热水、试
管、试管夹、烧杯。
【实验】
(1) 反应温度的影响
不同温度环境 实验现象
冷水
热水
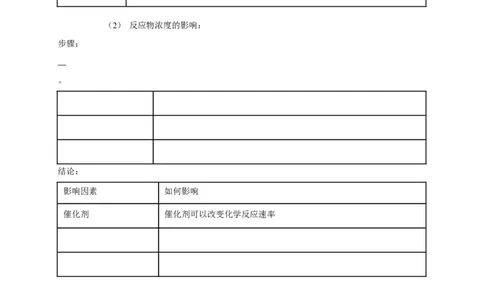
(2) 反应物浓度的影响:
步骤:
。
结论:
影响因素 如何影响
催化剂 催化剂可以改变化学反应速率
1.下列关于化学反应速率的说法,不正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率的大小主要取决于反应物的性质
C.化学反应速率可以用单位时间内生成某物质的质量的多少来表示D.化学反应速率常用单位有mol·L-1·s-1和mol·L-1·min-1
2.已知合成氨反应N (g)+3H (g)2NH (g),其浓度数据如下:
2 2 3
N H NH
2 2 3
起始浓度/mol·L-1 1.0 3.0 0
2 s末浓度/mol·L-
0.6 1.8 0.8
1
当用氨气浓度的增加来表示该化学反应的速率时,其速率为( )
A.0.2 mol·L-1·s-1 B.0.4 mol·L-1·s-1
C.0.6 mol·L-1·s-1 D.0.8 mol·L-1·s-1
3.把下列四种X溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释
到50 mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( )
A.10 ℃ 20 mL 3 mol·L-1的X溶液
B.20 ℃ 30 mL 2 mol·L-1的X溶液
C.20 ℃ 10 mL 4 mol·L-1的X溶液
D.10 ℃ 10 mL 2 mol·L-1的X溶液
4.实验室用锌粒与2 mol·L-1硫酸溶液制取氢气,下列措施不能增大化学反应速率的
是( )
A.用锌粉代替锌粒
B.改用3 mol·L-1硫酸溶液
C.改用热的2 mol·L-1硫酸溶液
D.向该硫酸溶液中加入等体积的水
5.在反应C(s)+CO (g)===2CO(g)中,可使反应速率增大的措施是( )
2
①增大压强 ②升高温度 ③通入CO ④增加碳的量 ⑤用等量炭粉代替焦炭
2
A.①②③ B.②③④⑤
C.①②③⑤ D.②③④
6.下列各组反应(表中物质均为反应物),反应刚开始时,放出H 的速率最大的是(
2
)
选项 金属(粉末状) 酸的浓度 体积 反应温度
A 0.1 mol Mg 6 mol·L-1 硝酸 10 mL 60 ℃
B 0.1 mol Mg 3 mol·L-1盐酸 10 mL 60 ℃
C 0.1 mol Fe 3 mol·L-1盐酸 10 mL 60 ℃D 0.1 mol Mg 3 mol·L-1硫酸 10 mL 60 ℃