文档内容
2021-2022 学年高二化学重难点专题突破
模块素养评价(一)
(75分钟 100分)
一、选择题(本题共15小题,每小题3分,共45分。
1.下列各项叙述中,正确的是( )
A.Br-的核外电子排布式:[Ar]4s24p6
B.Na的简化电子排布式: [Na]3s1
C.基态Cr原子的价层电子排布式:3d44s2
D.价层电子排布为 4s24p3的元素位于第四周期第ⅤA族,是 p区元素
2.下列说法不正确的是( )
A.某价层电子排布为4d25s2的基态原子,该元素位于周期表中第五周期第ⅣB族
B.在元素周期表中,s区、d区和ds区的元素都是金属元素
C.当碳原子的核外电子排布由 转变为 时,释放能量,由激发态转化成基态
D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8
3.X、Y、Z和W为原子序数依次增大的四种短周期主族元素。X的一种核素可用于测定文物的年代,基
态Y原子的电子总数是其最高能级电子数的2倍,Z是短周期中金属性最强的元素,W的单质为黄绿色气
体。下列说法正确的是( )
A.Z可与Y形成化合物ZY
2 2
B.原子半径:r(Z)>r(W)>r(Y)>r(X)
C.第一电离能:W>X>Y>Z
D.X的氢化物中不存在非极性共价键
4.下列说法中正确的是( )
A.单晶硅为分子晶体
B.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
C.键长H—F < H—Cl < H—Br < H—I,因此稳定性HF < HCl < HBr < HI
D.PH 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱
3
5.根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是( )
选项 分子式 中心原子杂化方式 价层电子对互斥模型 分子或离子的立体构型
A SO sp 直线形 直线形
2B HCHO sp2 平面三角形 三角锥形
C HO+ sp2 四面体形 平面三角形
3
D NH sp3 正四面体形 正四面体形
6.下列叙述中,正确的是( )
A.在同一能级上运动的电子,其运动状态肯定不同
B.如图所示银的晶胞中有14个银原子
C.11号到18号元素位于元素周期表中同一周期,所以元素的电负性逐渐增大
D.固态时能导电的晶体一定是金属晶体
7.冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶
点及面心,实心球所示原子位于立方体内)类似。有关冰晶胞的说法合理的是( )
A.冰晶胞内水分子间以共价键相结合
B.晶体冰与金刚石晶体硬度都很大
C.冰分子间的氢键具有方向性和饱和性,也是一种σ键
D.氢键的存在导致冰晶胞与金刚石晶胞微粒的排列方式类似
8.下列叙述中,不正确的是( )
A.微粒半径由小到大顺序是H+<Li+<H-
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
C.[Cu(NH )]2+中H提供接受孤电子对的空轨道
3 4
D.分子的中心原子通过sp3杂化轨道成键时,该分子不一定为四面体结构
9.石墨烯可看作将石墨的层状结构一层一层地剥开得到的单层碳原子;石墨炔是平面网状结构的全碳分
子,具有优良的化学稳定性和半导体性能,还可用于H 的提纯;将氢气氢化到石墨烯排列的六角晶格中,
2
使每个碳原子都增加一个氢原子可得最薄的绝缘新材料石墨烷。下列有关说法中不正确的是( )A.石墨烯和石墨炔互为同素异形体
B.石墨炔有望替代二氧化硅用作半导体材料
C.12 g石墨烯完全转变为石墨烷需标准状况下11.2 L氢气
D.石墨炔孔径略大于H 分子的直径,因此它是理想的H 提纯薄膜
2 2
10.短周期主族元素W、X、Y、Z的原子序数依次增大,基态W的原子2p轨道处于半充满状态,基态X
的原子的2p能级上只有一对成对电子,基态Y的原子的最外层电子运动状态只有1种,元素Z与W同主
族。下列说法错误的是( )
A.第一电离能:W>X>Y
B.电负性:Y>W>Z
C.简单离子半径:Z>X>Y
D.最简单氢化物的沸点:X>W>Z
11.毒奶粉主要是奶粉中含有有毒的三聚氰胺( )。下列关于三聚氰胺分子的说法中正确
的是( )
A.所有氮原子均采取sp3杂化
B.一个三聚氰胺分子中共含有15个σ键
C.属于极性分子
D.三聚氰胺分子中所有原子可能共平面
12.NH 和BF 可以通过配位键形成化合物NH ·BF,下列说法正确的是( )
3 3 3 3
A.NH 和BF 的立体构型都是三角锥形
3 3
B.NH 和BF 的中心原子的杂化方式相同
3 3
C.NH 和BF 形成的化合物NH ·BF 中各原子都达到8电子稳定结构
3 3 3 3
D.NH 和BF 形成的化合物NH ·BF 中N和B都采取的是sp3杂化
3 3 3 3
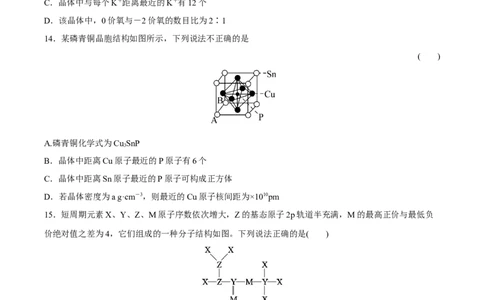
13.高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0,部分为-2。如图为超氧化钾晶体
的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )A.超氧化钾的化学式为KO ,每个晶胞含有4个K+和8个O
2
B.晶体中每个K+周围有8个O,每个O周围有8个K+
C.晶体中与每个K+距离最近的K+有12个
D.该晶体中,0价氧与-2价氧的数目比为2∶1
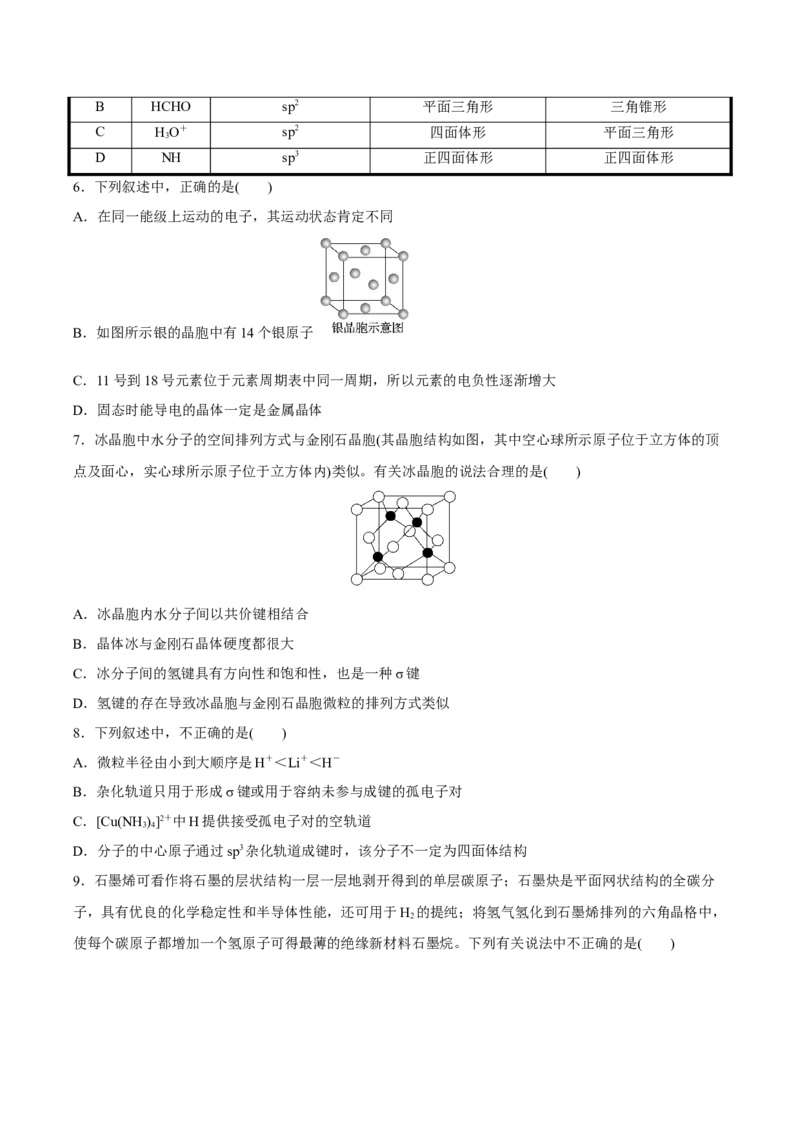
14.某磷青铜晶胞结构如图所示,下列说法不正确的是
( )
A.磷青铜化学式为Cu SnP
3
B.晶体中距离Cu原子最近的P原子有6个
C.晶体中距离Sn原子最近的P原子可构成正方体
D.若晶体密度为a g·cm-3,则最近的Cu原子核间距为×1010pm
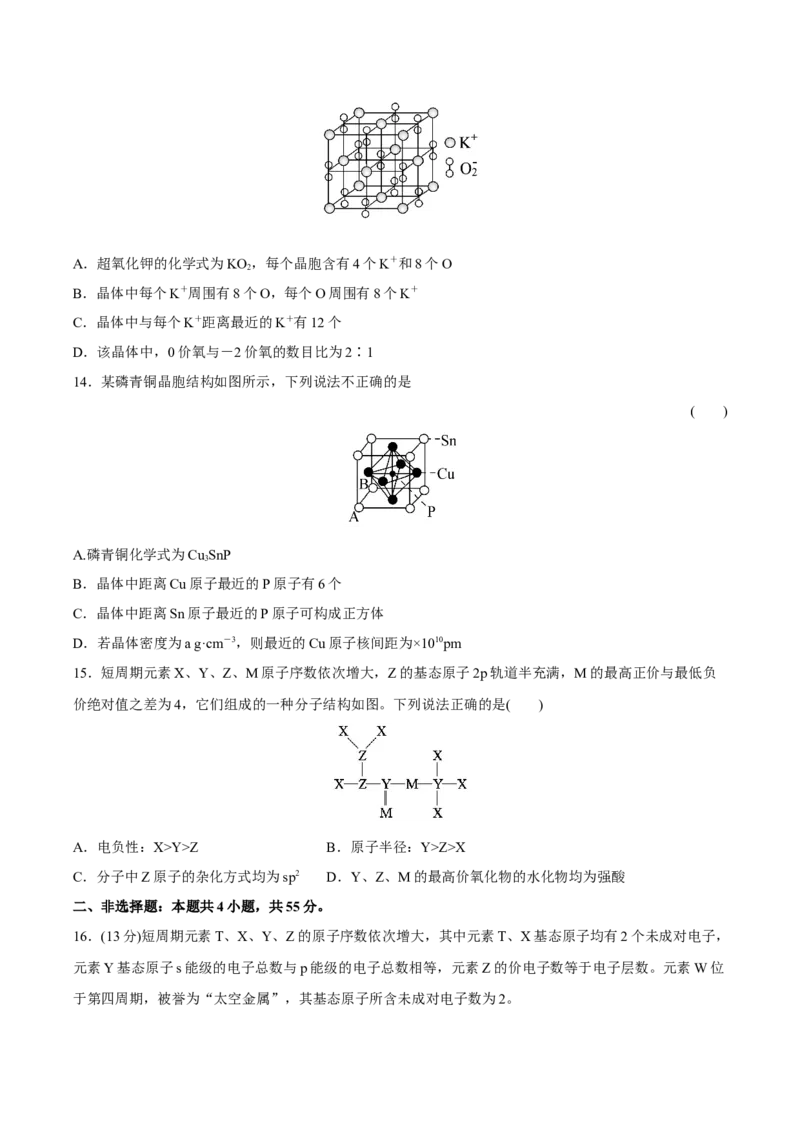
15.短周期元素X、Y、Z、M原子序数依次增大,Z的基态原子2p轨道半充满,M的最高正价与最低负
价绝对值之差为4,它们组成的一种分子结构如图。下列说法正确的是( )
A.电负性:X>Y>Z B.原子半径:Y>Z>X
C.分子中Z原子的杂化方式均为sp2 D.Y、Z、M的最高价氧化物的水化物均为强酸
二、非选择题:本题共4小题,共55分。
16.(13分)短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,
元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于电子层数。元素W位
于第四周期,被誉为“太空金属”,其基态原子所含未成对电子数为2。(1)①元素X、Y、Z的第一电离能由大到小的顺序为________(用元素符号表示)。
②元素W在周期表中的位置为________,元素Y在周期表________区。
(2)T、X分别与氢组成的TH 与HX 分子中,T、X原子轨道的杂化类型分别是________。
2 2 2 2
(3)T与X可形成TX离子,TX的空间构型为________(用文字描述)。
(4)有同学推测,YX的熔点比氯化钠高,其原因是________________。
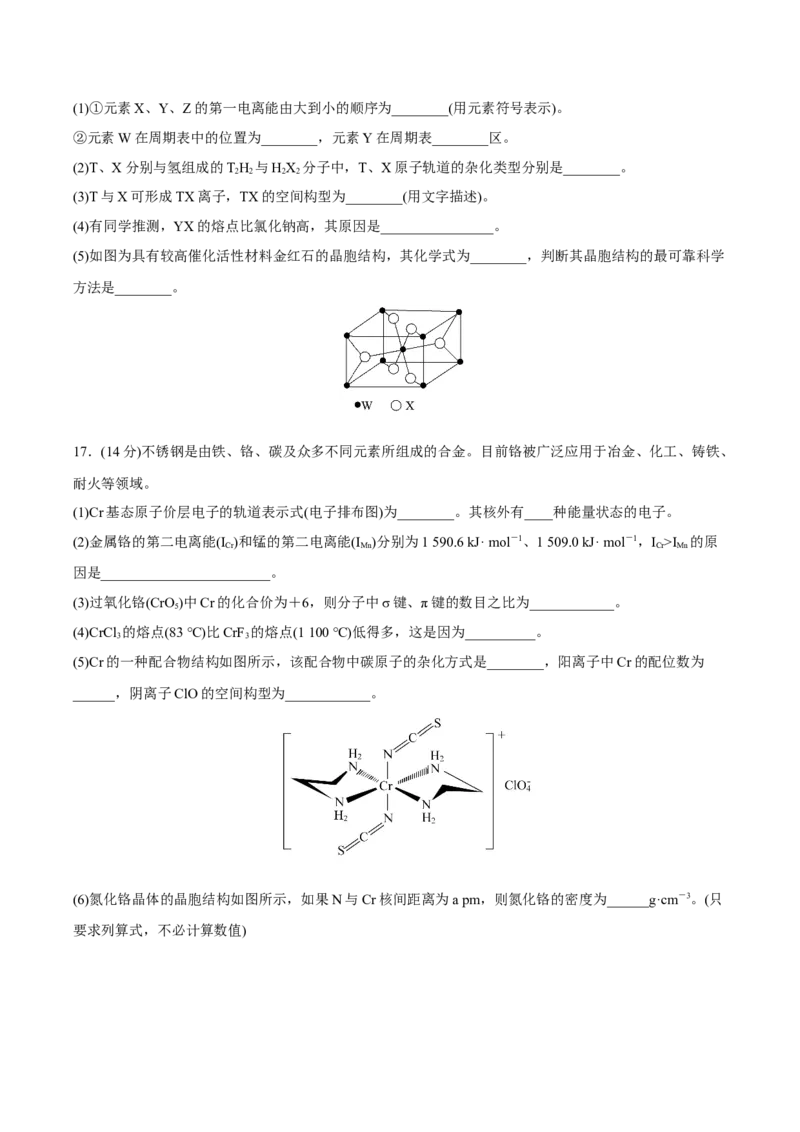
(5)如图为具有较高催化活性材料金红石的晶胞结构,其化学式为________,判断其晶胞结构的最可靠科学
方法是________。
17.(14分)不锈钢是由铁、铬、碳及众多不同元素所组成的合金。目前铬被广泛应用于冶金、化工、铸铁、
耐火等领域。
(1)Cr基态原子价层电子的轨道表示式(电子排布图)为________。其核外有____种能量状态的电子。
(2)金属铬的第二电离能(I )和锰的第二电离能(I )分别为1 590.6 kJ· mol-1、1 509.0 kJ· mol-1,I >I 的原
Cr Mn Cr Mn
因是________________________。
(3)过氧化铬(CrO )中Cr的化合价为+6,则分子中σ键、π键的数目之比为____________。
5
(4)CrCl 的熔点(83 ℃)比CrF 的熔点(1 100 ℃)低得多,这是因为__________。
3 3
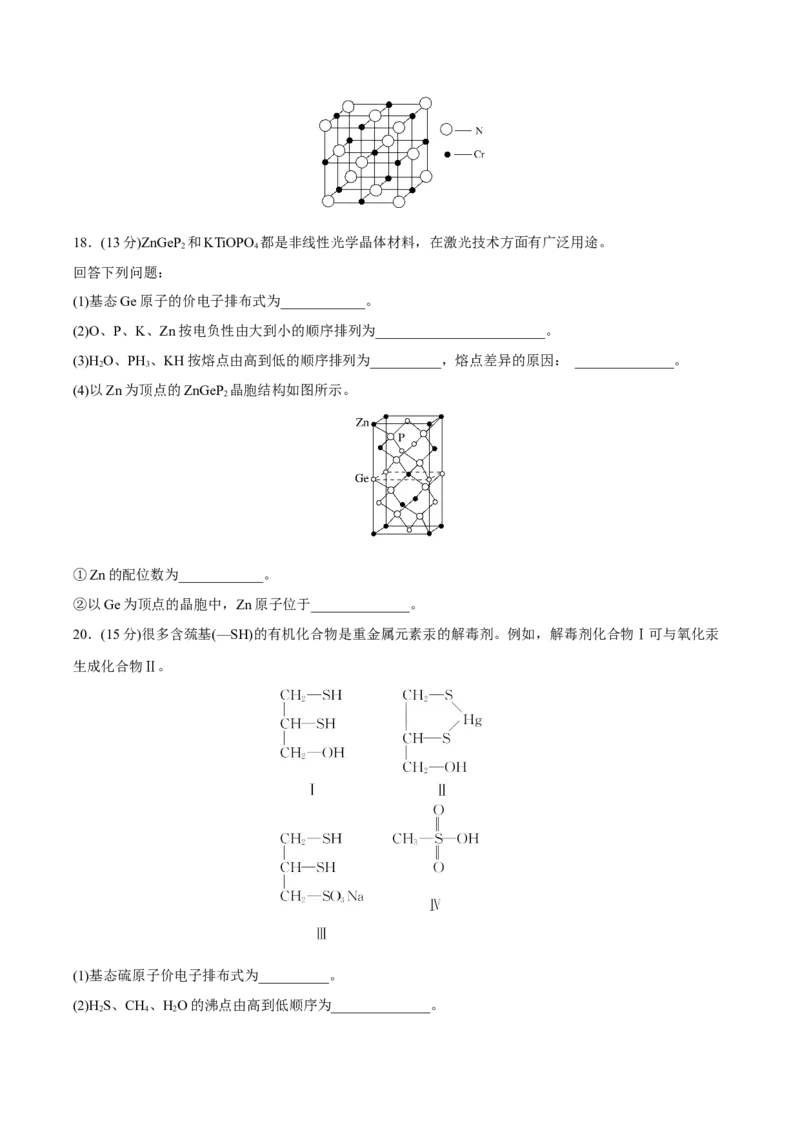
(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是________,阳离子中Cr的配位数为
______,阴离子ClO的空间构型为____________。
(6)氮化铬晶体的晶胞结构如图所示,如果N与Cr核间距离为a pm,则氮化铬的密度为______g·cm-3。(只
要求列算式,不必计算数值)18.(13分)ZnGeP 和KTiOPO 都是非线性光学晶体材料,在激光技术方面有广泛用途。
2 4
回答下列问题:
(1)基态Ge原子的价电子排布式为____________。
(2)O、P、K、Zn按电负性由大到小的顺序排列为________________________。
(3)H O、PH 、KH按熔点由高到低的顺序排列为__________,熔点差异的原因: ______________。
2 3
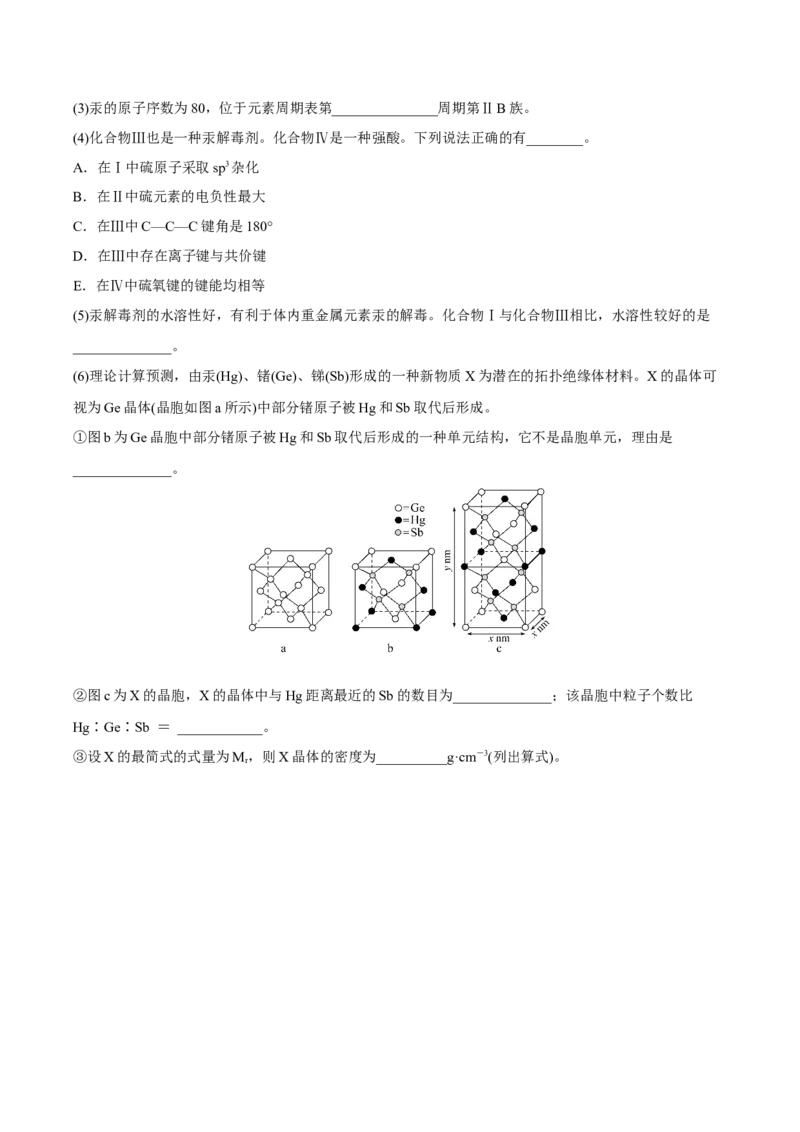
(4)以Zn为顶点的ZnGeP 晶胞结构如图所示。
2
①Zn的配位数为____________。
②以Ge为顶点的晶胞中,Zn原子位于______________。
20.(15分)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞
生成化合物Ⅱ。
(1)基态硫原子价电子排布式为__________。
(2)H S、CH、HO的沸点由高到低顺序为______________。
2 4 2(3)汞的原子序数为80,位于元素周期表第_______________周期第ⅡB族。
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有________。
A.在Ⅰ中硫原子采取sp3杂化
B.在Ⅱ中硫元素的电负性最大
C.在Ⅲ中C—C—C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是
______________。
(6)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可
视为Ge晶体(晶胞如图a所示)中部分锗原子被Hg和Sb取代后形成。
①图b为Ge晶胞中部分锗原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
______________。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为______________;该晶胞中粒子个数比
Hg∶Ge∶Sb = ____________。
③设X的最简式的式量为M,则X晶体的密度为__________g·cm-3(列出算式)。
r倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育