文档内容
人教版(2019) 选择性必修1 第四章 化学反应与能量
第三节 金属的腐蚀与防护
教学设计
教学目标
1、认识金属腐蚀的危害,能利用原电池原理解释电化学腐蚀的原因。
2、能正确书写析氢腐蚀和吸氧腐蚀的电极反应式和总反应式。
3、了解金属腐蚀的防护方法。
教学重难点
重点:吸氧腐蚀、析氢腐蚀的原理
难点:吸氧腐蚀、析氢腐蚀的原理
教学过程
一、导入新课
PPT播放金属腐蚀的图片。金属腐蚀的现象非常普遍,像金属制成的日用品、
生产工具、机器部件、海轮的船壳等,如保养不好,都会腐蚀,从而造成大量金属
的损耗。至于因设备腐蚀损坏而引起停工减产、产品质量下降、污染环境、危害人
体健康,甚至造成严重事故的损失,那就更无法估计了。因此,了解金属腐蚀的原
因,掌握防护的方法,是具有十分重要的意义的。
二、新课讲授
【师】金属腐蚀:金属(或合金)跟周围接触到的气体(或液体)反应而腐蚀损耗的
过程。
【提问】金属腐蚀有哪些种类呢?
【学生】讨论回答。
【师】金属的化学腐蚀:金属跟接触到的物质直接发生化学反应而引起的腐蚀。
例如:铁在高温下与氧气直接化合而被腐蚀,在工业生产中氯气跟铁或与
其他金属化合使金属锈蚀。
特点:反应简单、金属与氧化剂之间的氧化还原反应。
【师】电化学腐蚀 :不纯的金属或合金与电解质溶液接触,会发生原电池反应,比较活泼的金属失电子被氧化的腐蚀。
例如:钢铁在潮湿的空气中生锈就是电化学腐蚀造成的。
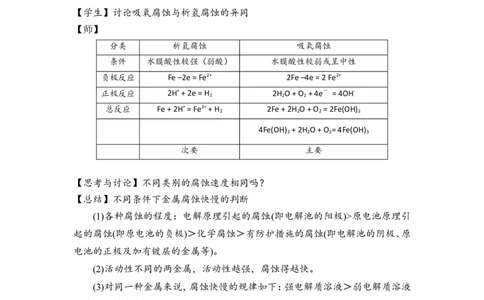
【PPT】展示钢铁的吸氧腐蚀和析氢腐蚀
【学生】讨论吸氧腐蚀与析氢腐蚀的异同
【师】
分类 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强(弱酸) 水膜酸性较弱或呈中性
负极反应 Fe –2e = Fe2+ 2Fe –4e = 2 Fe2+
正极反应 2H+ + 2e = H 2H O + O + 4e- = 4OH-
2 2 2
总反应 Fe + 2H+ = Fe2+ + H 2Fe + 2H O + O = 2Fe(OH)
2 2 2 2
4Fe(OH) + 2H O + O = 4Fe(OH)
2 2 2 3
次要 主要
【思考与讨论】不同类别的腐蚀速度相同吗?
【总结】不同条件下金属腐蚀快慢的判断
(1)各种腐蚀的程度:电解原理引起的腐蚀(即电解池的阳极)>原电池原理引
起的腐蚀(即原电池的负极)>化学腐蚀>有防护措施的腐蚀(即电解池的阴极、原
电池的正极及加有镀层的金属等)。
(2)活动性不同的两金属,活动性越强,腐蚀得越快。
(3)对同一种金属来说,腐蚀快慢的规律如下:强电解质溶液>弱电解质溶液
>非电解质溶液。
【过渡】金属被腐蚀后,在外形、色泽以及机械性能等方面都将发生变化,会使机
器设备、仪器、仪表的精密度和灵敏度降低,影响使用以至报废,甚至发生严重事
故。每年由于钢铁生锈会使我国损失大约100~150亿元。在英国,每90秒钟就有
1吨钢被锈蚀掉。因此防止金属腐蚀有很重要的意义。
【思考与讨论】要想减少或避免电化学腐蚀,我们应该采取什么措施?
【学生】喷漆,涂油
【师】①对金属做必要的精炼,以减少其中能导电的不活泼杂质。②对机器、仪表及时保养,减少金属与腐蚀性气体、电解质溶液、潮湿气
体的接触。
③根据用途不同采取不同的方法使金属与造成发生的介质隔离,如涂油、
喷漆、镀层、表面钝化等。
④选用适宜的金属或非金属制成耐腐蚀的合金,如炼制不锈钢、耐酸钢等
⑤采用电化学防护方法,如在钢铁的船体上焊接上较活泼的金属锌。
板书设计
金属的腐蚀与防护
一、金属的腐蚀
1、 化学腐蚀
2、 电化学腐蚀
二、金属的防护
1、物理防护
2、化学防护