文档内容
课程基本信息
课题 沉淀溶解平衡(第二课时)
书名: 普通高中教科书化学选择性必修1化学反应原理
教科书
出版社:人民教育出版社 出版日期:2020年5月
教学目标
教学目标:
1、通过实验了解沉淀的溶解与转化,能应用化学平衡理论解释沉淀的溶解和转
化。
2、学会通过比较Q、Ksp的大小,从定量的角度分析难溶电解质的溶解和转化。
教学重点:
难溶电解质的沉淀溶解平衡的原理
教学难点:
用沉淀溶解平衡的理论,解释实际情境中沉淀的溶解和转化。
教学过程
时间 教学环节 主要师生活动
在发电、采暖、机械、冶金等很多行业,都需要锅炉供给大
量的热能。锅炉通过加热管道里的水,再利用热水传递热量。
2 使用锅炉,需要定期检查、去除管道内壁的水垢,否则会降
引入
min 低燃料的利用率,造成能源浪费,又会影响锅炉的使用寿命,并
形成安全隐患。
去除水垢的方法和化学原理是什么呢?
水垢主要含有氢氧化镁、碳酸钙、硫酸钙等,除水垢的方法
有“酸洗”,即,用盐酸浸泡。
请运用沉淀溶解平衡的原理解释原因。
【分析】
寻找核心物质:Mg(OH)、CaCO、CaSO、HCl
2 3 4
寻找平衡:
5
任务一
min
【实验】
证明氢氧化镁的沉淀溶解平衡的存在。
向小试管中,加入少量氢氧化镁固体,加入蒸馏水,充分振荡,
溶液仍然浑浊。向浊液中滴加几滴酚酞溶液,变红。少量氢氧化
镁溶解出氢氧根离子,遇酚酞溶液变红。
【分析】
对于Mg(OH) (s) Mg2+(aq) + 2OH-(aq)
2
1如何设计实验证明呢?
【实验】
观看实验视频,将实验现象填写在教科书80页[实验3-3]的
表格里。
【小结】
加水,对Mg(OH) 的沉淀溶解平衡影响不明显。
2
加盐酸,沉淀溶解。
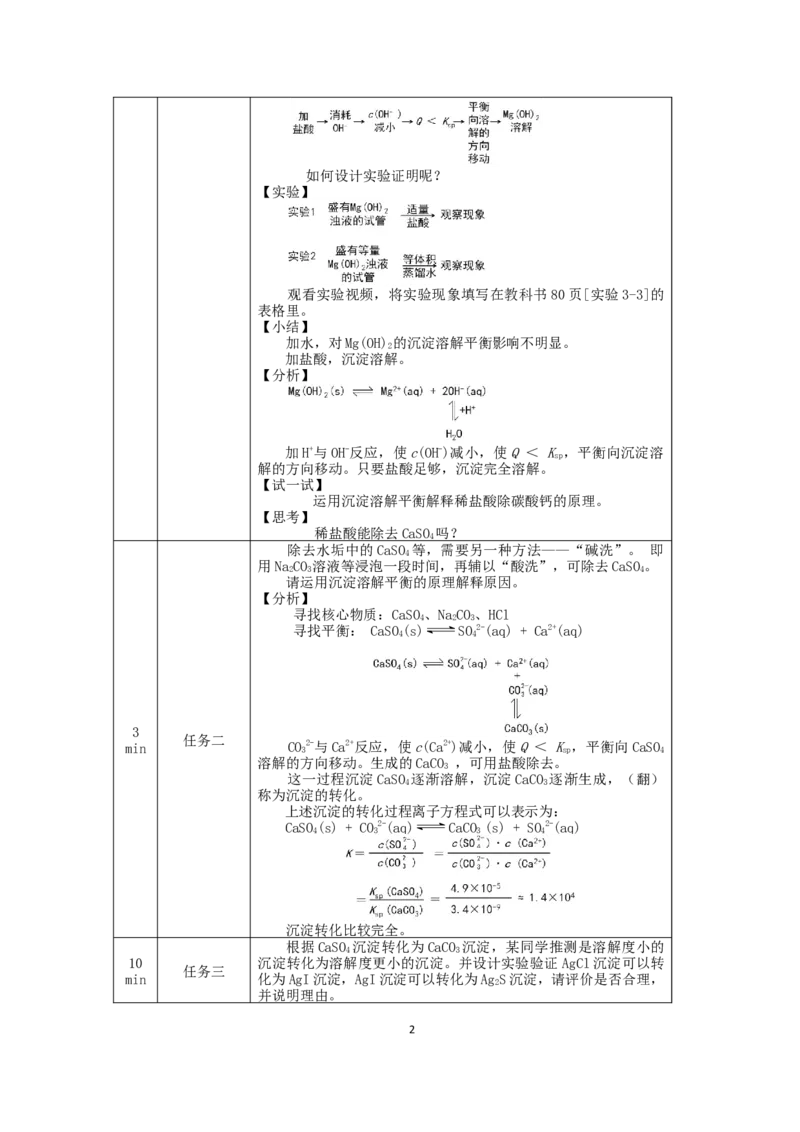
【分析】
加H+与OH-反应,使c(OH-)减小,使Q < K ,平衡向沉淀溶
sp
解的方向移动。只要盐酸足够,沉淀完全溶解。
【试一试】
运用沉淀溶解平衡解释稀盐酸除碳酸钙的原理。
【思考】
稀盐酸能除去CaSO 吗?
4
除去水垢中的CaSO 等,需要另一种方法——“碱洗”。 即
4
用NaCO 溶液等浸泡一段时间,再辅以“酸洗”,可除去CaSO。
2 3 4
请运用沉淀溶解平衡的原理解释原因。
【分析】
寻找核心物质:CaSO、NaCO、HCl
4 2 3
寻找平衡: CaSO(s) SO2-(aq) + Ca2+(aq)
4 4
3
任务二
min CO2-与Ca2+反应,使c(Ca2+)减小,使Q < K ,平衡向CaSO
3 sp 4
溶解的方向移动。生成的CaCO ,可用盐酸除去。
3
这一过程沉淀CaSO 逐渐溶解,沉淀CaCO 逐渐生成,(翻)
4 3
称为沉淀的转化。
上述沉淀的转化过程离子方程式可以表示为:
CaSO(s) + CO2-(aq) CaCO (s) + SO2-(aq)
4 3 3 4
沉淀转化比较完全。
根据CaSO 沉淀转化为CaCO 沉淀,某同学推测是溶解度小的
4 3
10 沉淀转化为溶解度更小的沉淀。并设计实验验证AgCl沉淀可以转
任务三
min 化为AgI沉淀,AgI沉淀可以转化为AgS沉淀,请评价是否合理,
2
并说明理由。
2【分析】
该实验方案设计是合理的。
硝酸银和氯化钠溶液的用量,需保证Ag+不过量。如果银离子
过量。加入KI溶液后,碘离子可以与过量Ag+生成沉淀AgI,无法
证明AgI是由AgCl沉淀通过平衡移动转化成的。同理,加入 NaS
2
溶液后,硫离子可以与过量Ag+生成沉淀AgS,无法证明AgS是由
2 2
AgI沉淀通过平衡移动转化成的。
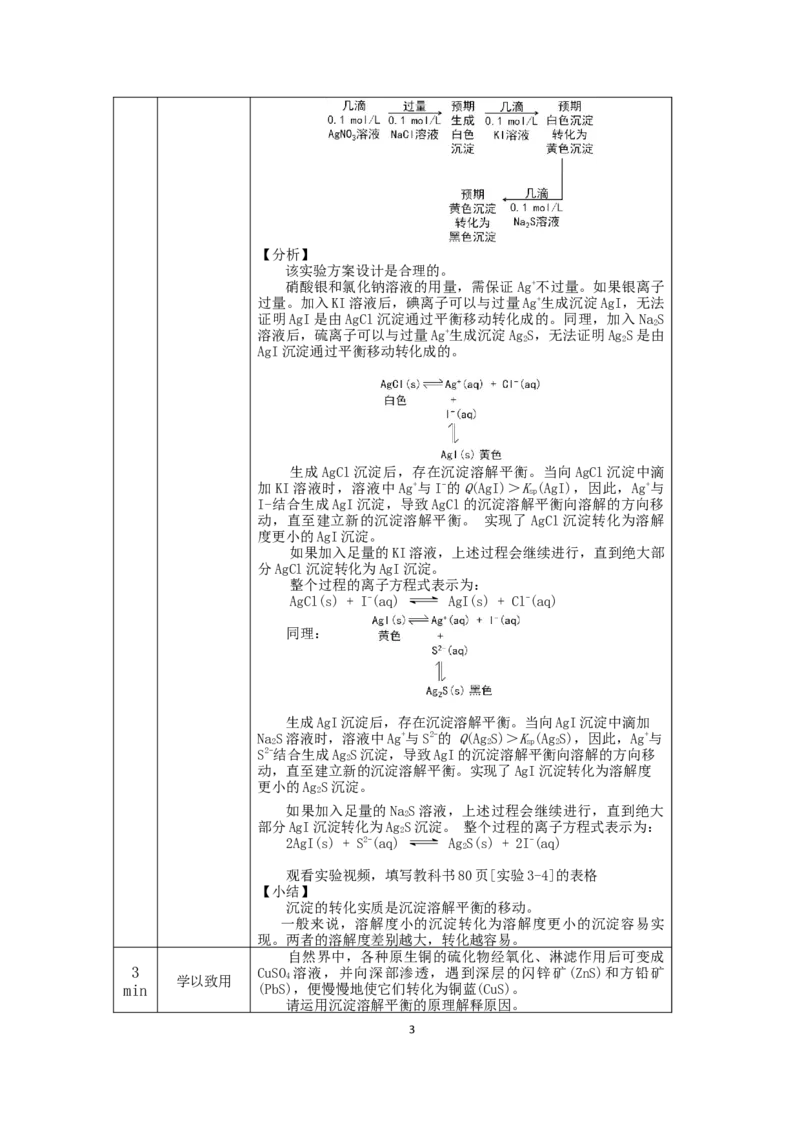
生成AgCl沉淀后,存在沉淀溶解平衡。当向AgCl沉淀中滴
加KI溶液时,溶液中Ag+与I-的Q(AgI)>K(AgI),因此,Ag+与
sp
I-结合生成AgI沉淀,导致AgCl的沉淀溶解平衡向溶解的方向移
动,直至建立新的沉淀溶解平衡。 实现了 AgCl沉淀转化为溶解
度更小的AgI沉淀。
如果加入足量的KI溶液,上述过程会继续进行,直到绝大部
分AgCl沉淀转化为AgI沉淀。
整个过程的离子方程式表示为:
AgCl(s) + I-(aq) AgI(s) + Cl-(aq)
同理:
生成AgI沉淀后,存在沉淀溶解平衡。当向AgI沉淀中滴加
NaS溶液时,溶液中Ag+与S2-的 Q(AgS)>K(AgS),因此,Ag+与
2 2 sp 2
S2-结合生成AgS沉淀,导致AgI的沉淀溶解平衡向溶解的方向移
2
动,直至建立新的沉淀溶解平衡。实现了AgI沉淀转化为溶解度
更小的AgS沉淀。
2
如果加入足量的NaS溶液,上述过程会继续进行,直到绝大
2
部分AgI沉淀转化为AgS沉淀。 整个过程的离子方程式表示为:
2
2AgI(s) + S2-(aq) AgS(s) + 2I-(aq)
2
观看实验视频,填写教科书80页[实验3-4]的表格
【小结】
沉淀的转化实质是沉淀溶解平衡的移动。
一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实
现。两者的溶解度差别越大,转化越容易。
自然界中,各种原生铜的硫化物经氧化、淋滤作用后可变成
3 CuSO 溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿
学以致用 4
min (PbS),便慢慢地使它们转化为铜蓝(CuS)。
请运用沉淀溶解平衡的原理解释原因。
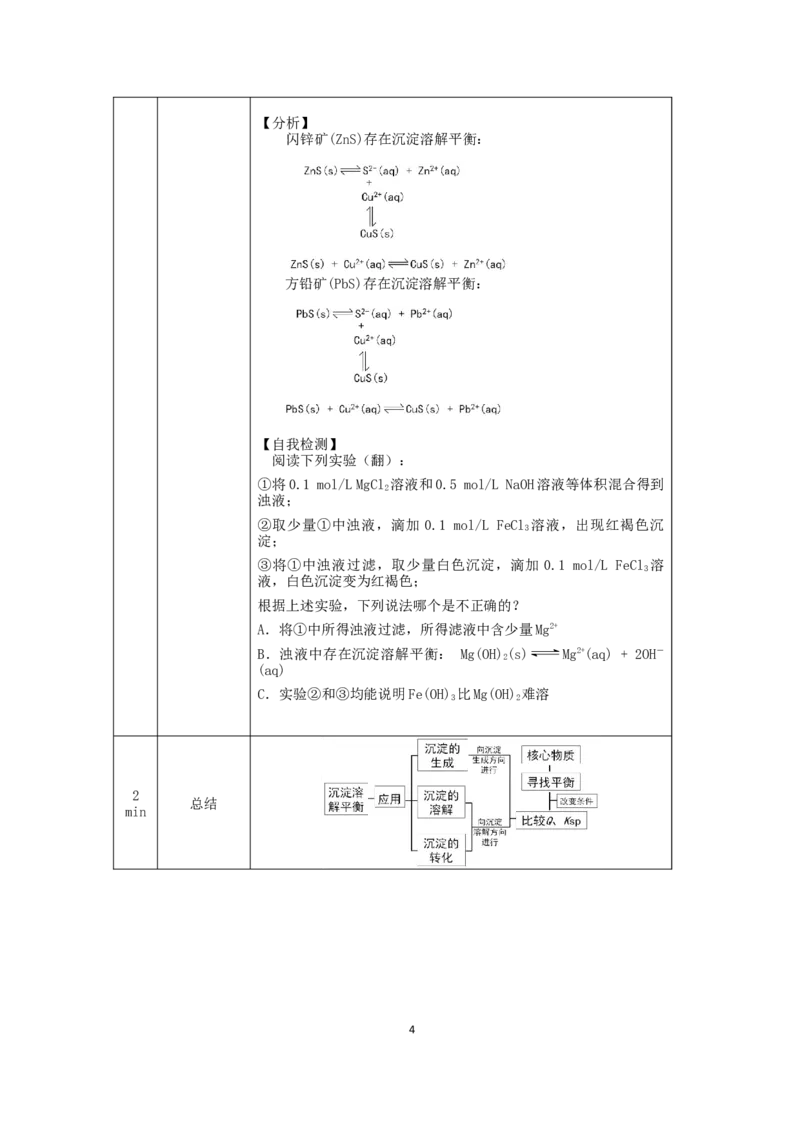
3【分析】
闪锌矿(ZnS)存在沉淀溶解平衡:
方铅矿(PbS)存在沉淀溶解平衡:
【自我检测】
阅读下列实验(翻):
①将0.1 mol/L MgCl 溶液和0.5 mol/L NaOH溶液等体积混合得到
2
浊液;
②取少量①中浊液,滴加 0.1 mol/L FeCl 溶液,出现红褐色沉
3
淀;
③将①中浊液过滤,取少量白色沉淀,滴加 0.1 mol/L FeCl 溶
3
液,白色沉淀变为红褐色;
根据上述实验,下列说法哪个是不正确的?
A.将①中所得浊液过滤,所得滤液中含少量Mg2+
B.浊液中存在沉淀溶解平衡: Mg(OH)(s) Mg2+(aq) + 2OH-
2
(aq)
C.实验②和③均能说明Fe(OH) 比Mg(OH) 难溶
3 2
2
总结
min
4