文档内容
2019-2020 年高一化学高频考题期末组合模拟卷 01
(考试时间:90分钟 试卷满分:100分)
考试内容:必修二 难度:★★★☆☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.我国毛笔的制作技艺属于国家非物质文化遗产,相传古人制作该毛笔的过程为“以枯木为管,
鹿毛为柱,羊毛为被(外衣)”,则下列说法正确的是
A.枯木的主要成分蛋白质
B.鹿毛、羊毛均只含有C、H、O三种元素
C.枯木、鹿毛的主要成分互为同分异构体
D.采用灼烧法可以区分枯木、毛笔的“外衣”
【答案】D
【解析】A.枯木的主要成分是植物纤维,故A错误;
B.鹿毛、羊毛的主要成分是蛋白质,含有C、H、O三种元素,还含有N元素,故B错误;
C.枯木的主要成分是植物纤维,鹿毛的主要成分是蛋白质,它们的分子式不相同,不属于同分
异构体,故C错误;
D.区分蛋白质和化学纤维一般可以使用灼烧法,有烧焦羽毛气味的毛笔的“外衣”羊毛,无此
现象的是枯木,故D正确;
答案选D。
2.下列说法正确的是
A.CO、NO、NO 都是大气污染气体,在空气中都能稳定存在
2
B.明矾在水中生成的Al(OH) 胶体有吸附性,因此常用明矾对水进行消毒
3
C.CO、NO 或SO 都会导致酸雨的形成
2 2 2
D.活性炭、SO 、NaO 都能使品红溶液褪色,原理不同
2 2 2
【答案】D
【解析】A.CO、NO、NO 都是大气污染气体,NO在空气中不能稳定存在,A错误;
2
B.明矾在水中生成的Al(OH) 胶体有吸附性,因此常用明矾对水进行净化,B错误;
3C.NO 或SO 会导致酸雨的形成,CO 不会导致酸雨的形成,C错误;
2 2 2
D.活性炭、SO 、NaO 都能使品红溶液褪色,活性炭是吸附性,SO 与品红化合生成不稳定的
2 2 2 2
无色物质,NaO 是强氧化性漂白,因此原理不同,D正确。
2 2
答案选D。
3.下列关于氮及其化合物的说法,不正确的是
A.硝酸可以与甘油反应生成烈性炸药硝化甘油
B.氯碱工业中可以用氨气检查氯气管道是否泄漏
C.工业上制备硝酸是利用NH 和O 反应生成NO,进一步转化为NO 及HNO
3 2 2 3
D.为提高作物的养分,可以是铵态氮肥与碱性肥料混合使用
【答案】D
【解析】A.甘油在浓硫酸催化下,与浓硝酸反应生成硝酸甘油酯(即硝化甘油)和水,A正确;
B.用氨气检查氯气管道,如果有氯气泄漏,则发生反应3Cl+8NH═6NH Cl+N ,会有白烟产生,
2 3 4 2
白烟为氯化铵固体,B正确;
C.工业上制备硝酸是利用三步反应①4NH +5O 4NO+6H O、②2NO+O ═2NO 、
3 2 2 2 2
③3NO +H O═2HNO +NO,C正确;
2 2 3
D.铵态氮肥能与碱性肥料发生反应,NH ++OH- NH ∙H O NH +H O,氨气易逸出导致平衡向
4 3 2 3 2
右移动,土壤中铵根离子浓度降低,从而降低肥⇌效,所以铵⇌态氮肥不能与碱性肥料混合使用,
D错误。
答案选D。
4.往FeCl 和BaCl 的混合溶液中通入SO ,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产
3 2 2
生,下列说法正确的是
A.该实验表明FeCl 有还原性 B.白色沉淀为BaSO
3 3
C.该实验表明SO 有漂白性 D.反应后溶液酸性增强
2
【答案】D
【解析】A.反应中溶液由由棕黄色变成浅绿色,三价铁变化为二价铁,该实验表明FeCl 具有
3
氧化性,A错误;
B.二氧化硫被氧化为硫酸根,生成的白色沉淀为硫酸钡,B错误;C.二氧化硫的漂白性是指二氧化硫和水反应生成的亚硫酸与有色物质结合为不稳定的无色物质,
此反应中二氧化硫做还原属剂,C错误;
D.反应后生成硫酸酸性增强,D正确;
答案选D。
5.下列化学反应一定是放热反应的是
A.Ba(OH)·8H O晶体与NH Cl晶体混合时
2 2 4
B.金属钠与水反应
C.浓硫酸稀释
D.煅烧石灰石
【答案】B
【解析】A.Ba(OH)·8H O晶体与NH Cl晶体混合属于吸热反应,A不符合题意;
2 2 4
B.金属钠与水反应放出大量的热,可将Na熔化为一个小球,B符合题意;
C.浓硫酸溶于水是物理变化,而非化学变化,故不属于放热反应,C不符合题意;
D.石灰石在高温条件下煅烧发生分解反应,属于吸热反应,D不符合题意;
故选B。
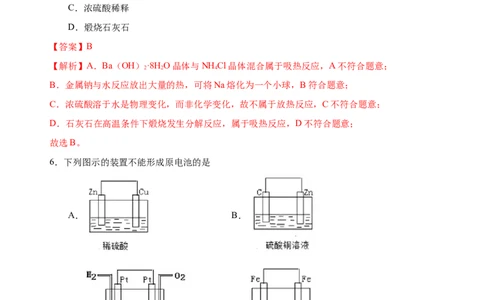
6.下列图示的装置不能形成原电池的是
A. B.
C. D.
【答案】D
【解析】形成原电池的条件为:①自发进行的氧化还原反应,②形成闭合回路,据此解答。
【详解】A.由图可知:锌能与稀硫酸反应且为闭合回路,则A可以构成原电池,A不符合;B.由图可知:锌能与硫酸铜反应且为闭合回路,则B可以构成原电池,B不符合;
C.由图可知:氢气与氧气反应且为闭合回路,则C可以构成原电池,且为燃料电池,C不符合;
D.两侧金属均为铁,直接与稀盐酸发生化学腐蚀,不能形成原电池,D符合;
故选D。
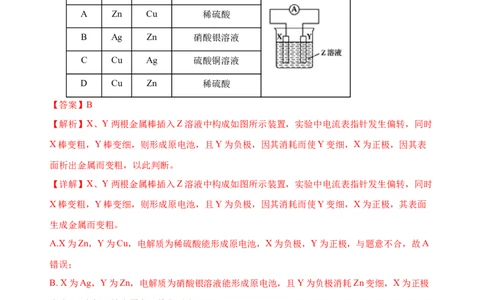
7.X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时X棒
变粗,Y棒变细,则X、Y、Z可能是下列中的
编号 X Y Z
A Zn Cu 稀硫酸
B Ag Zn 硝酸银溶液
C Cu Ag 硫酸铜溶液
D Cu Zn 稀硫酸
【答案】B
【解析】X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时
X棒变粗,Y棒变细,则形成原电池,且Y为负极,因其消耗而使Y变细,X为正极,因其表
面析出金属而变粗,以此判断。
【详解】X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时
X棒变粗,Y棒变细,则形成原电池,且Y为负极,因其消耗而使Y变细,X为正极,其表面
生成金属而变粗。
A.X为Zn,Y为Cu,电解质为稀硫酸能形成原电池,X为负极,Y为正极,与题意不合,故A
错误;
B. X为Ag,Y为Zn,电解质为硝酸银溶液能形成原电池,且Y为负极消耗Zn变细,X为正极
生成Ag变粗,符合题意,故B正确;
C. X为Cu,Y为Ag,电解质为硫酸铜溶液,没有自发的氧化还原反应,不能形成原电池,与题
意不合,故C错误;
D. X为Cu,Y为Zn,电解质为稀硫酸能形成原电池,Y为负极,X为正极生成氢气,没有变粗,
与题意不合,故D错误;故选B。
8.在光照条件下,纳米TiO 能将甲醛催化氧化成二铖化碳和水。经10小时(h)催化氧化后,某
2
密闭空间内甲醛的浓度从2.0×10-7mol/L降到1.0×10-7mol/L,则甲醛在这段时间内的平均反应速率为
A.4.0×10-8mol/(L·h) B.3.0×10-8mol/(L·h)
C.2.0×10-8mol/(L·h) D.1.0×10-8mol/(L·h)
【答案】D
【解析】经 10 小时(h)催化氧化后,某密闭空间内甲醛的浓度从 2.0×10-7mol/L 降到 1.0×10-
7mol/L,甲醛在这段时间内的平均反应速率为 = 1.0×10-
8mol/(L·h),故选D。
9.对于可逆反应 A(g)+3B(s) 2C(g)+2D(g),在不同条件下的化学反应速率如下, 其中
表示的反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1 B.v(B)=1.2 mol·L-1·s-1
C.v(C)=0.1 mol·L-1·s-1 D.v(D)=0.4 mol·L-1·min-1
【答案】C
【解析】A.v(A)=0.5mol/(L•min);
B.B为固体,不能用B表示反应速率;
C.v(A)= v(C)=0.05mol/(L•s)=3mol/(L•min);
D.v(A)= v(D)=0.2mol/(L•min);
根据分析可知,反应速率最快的为C,故选C。
10.下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是
A.10℃20mL3mol/L的盐酸溶液 B.20℃30mL2mol/L的盐酸溶液
C.20℃20mL2mol/L的盐酸溶液 D.20℃10mL4mol/L的盐酸溶液
【答案】D
【解析】锌与盐酸反应的方程式是Zn+2HCl=ZnCl +H↑,所以盐酸的浓度越高,溶液的温度
2 2
越高反应速率越快。选项D中溶液温度和盐酸的浓度均是最高的,因此反应速率最快,答案选D。
11.云南特色小吃“过桥米线”做法如下:先用滚沸的鸡汤一碗,上罩浮油,再辅以切得极薄
的生肉片、乌龟片、火腿片、葱头等,最后把主料米线放入拌食即成。“过桥米线”汤鲜、肉
嫩、料香、米线滑润,吃起来别有一番风味。以下有关“过桥米线”的说法不正确的是
A.上层浮油沸点较高,难以挥发
B.浮油对下层汤水起到很好的“液封”作用,使下层汤水及热量难以外逸
C.去掉上面的一层浮油,将减弱“过桥米线”的保温效果
D.上层浮油高温水解即产生美味的物质
【答案】D
【解析】上层浮油成分是油脂,水解生成甘油和高级脂肪酸,所以选项D是错误的,其余选项
都是正确的,答案选D。
【点睛】该题是基础性试题的考查,试题贴近生活,有助于调到学生的学习兴趣和学习积极性。
试题基础性强,侧重对学生基础知识的巩固和训练,旨在在考查学生灵活运用基础知识解决实
际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。
12.制取一氯乙烷最好采用的方法是
A.乙烷和氯气反应 B.乙烯和氯气反应
C.乙烷和氯化氢反应 D.乙烯和氯化氢反应
【答案】D
【解析】A.乙烷和氯气发生取代反应时会生成多种氯代物,产物不唯一,故A不符合题意;
B.乙烯和氯气发生加成反应生成1,2-二氯乙烷,故B不符合题意;
C.乙烷与氯化氢不反应,故C不符合题意;
D.乙烯和HCl发生加成反应只生成一氯乙烷,故D符合题意;
故答案为D。
13.下列实验能获得成功的是
A.苯和浓溴水用铁做催化剂制溴苯
B.用酸性高锰酸钾溶液除去甲烷中混有的乙烯
C.甲烷与氯气光照制得纯净的一氯甲烷
D.乙烯通入溴的四氯化碳溶液得到1,2—二溴乙烷
【答案】D【解析】A. 苯和液溴发生取代反应生成溴苯而不是溴水;B. 酸性高锰酸钾溶液可将乙烯氧化
为二氧化碳气体杂质;C. 甲烷与氯气光照制得的产物还有二氯甲烷、三氯甲烷、四氯甲烷;D.
乙烯通入溴的四氯化碳溶液可以得到1,2—二溴乙烷。
故选D。
14.在抗击“2019新型冠状病毒”的过程中,大量防护和消毒用品投入使用。下列有关说法正
确的是
A.新型冠状病毒由C、H、O三种元素组成
B.过氧化氢、乙醇、过氧乙酸等消毒液均可以将病毒氧化而达到消毒目的
C.聚丙烯和聚四氟乙烯为生产防护服的主要材料,二者均属于有机高分子材料
D.84消毒液是以NaClO为主要有效成分的消毒液,与医用酒精混合可以提升消毒效果
【答案】C
【解析】A.新型冠状病毒主要成分是蛋白质,由C、H、O、N等元素组成,故A错误;
B.乙醇可以使蛋白质变性,但并不具有氧化性,不能氧化病毒,故B错误;
C.聚丙烯是由丙烯发生加聚反应生成,聚四氟乙烯是由四氟乙烯加聚而成,二者均为有机高分
子材料,故C正确;
D.84消毒液是以NaClO为主要有效成分的消毒液,与医用酒精混合会发生氧化还原反应,降
低消毒效果,故D错误;
故选C。
15.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣
服的汗渍、血迹及人体排放的蛋白质油渍遇到它,皆能水解而除去,下列衣料中不能用加酶洗
衣粉洗涤的是
①棉织品;②毛织品;③晴纶织品;④蚕丝织品;⑤涤纶织品;⑥锦纶织品
A.①②③ B.③④⑤ C.②④ D.③⑤⑥
【答案】C
【解析】根据题意,在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服的汗渍、血
迹及人体排放的蛋白质油渍遇到它,皆能转化而除去。酶是一种生物催化剂,能催化蛋白质等
物质的分解,则含蛋白质的衣料不能用加酶洗衣粉洗涤,据此进行分析解答。
【详解】酶是一种生物催化剂,能催化蛋白质等物质的分解,则含蛋白质的衣料不能用加酶洗
衣粉洗涤。①棉织品是用棉线制成的,不含蛋白质,可以用加酶洗衣粉洗涤;②毛织品、④蚕丝织品分别
是用羊毛、蚕丝制成的,主要成分是蛋白质,不能用加酶洗衣粉洗涤;③腈纶织品、⑤涤纶织
品、⑥锦纶织品均是用合成纤维制成的,不含蛋白质,可以用加酶洗衣粉洗涤。
故②④不能用加酶洗衣粉洗涤。
故选C。
【点睛】本题难度不大,明确含蛋白质的衣料不能用加酶洗衣粉洗涤是正确解答本题的关键。
16.海水提镁的主要流程如下,下列说法正确的是;
①试剂M是盐酸;②流程中的反应全部都是非氧化还原反应;③操作b只是过滤;④用海
水晒盐后的饱和溶液加石灰乳制Mg(OH) ;⑤采用电解法冶炼镁是因为镁很活泼
2
A.①②③④⑤ B.②③ C.④⑤ D.①④⑤
【答案】D
【解析】生石灰溶于水生成氢氧化钙,加入沉淀池沉淀镁离子生成氢氧化镁,过滤后得到氢氧
化镁沉淀,加入试剂M为盐酸,氢氧化镁溶解得到氯化镁溶液,通过浓缩蒸发,冷却结晶,过
滤洗涤得到氯化镁晶体,在氯化氢气流中加热失去结晶水得到固体氯化镁,通电电解生成镁;
【详解】①M是盐酸,用来溶解氢氧化镁沉淀,①正确;
②电解氯化镁生成镁和氯气的反应是氧化还原反应,流程中的反应不全部都是非氧化还原反应,
②错误;
③操作b是浓缩蒸发,冷却结晶,过滤洗涤得到氯化镁晶体的过程,③错误;
④用海水晒盐后的饱和溶液中主要是氯化镁,加石灰乳可以制Mg(OH),④正确;
2
⑤氧化镁熔点高,熔融消耗能量高效益低,电解熔融MgCl 比电解熔融的MgO制金属镁更节约
2
能量,⑤正确,
答案选D。
二、非选择题:包括第17题~第21题5个大题,共52分。
17.(12分)SO 是一种重要的氧化物,可用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也
2
可用作熏蒸剂、防腐剂、消毒剂、还原剂等。(1)SO 性质多变,若将SO 气体通入氢硫酸中,能看到的现象为:__________,该反应中SO
2 2 2
表现出______性;若将SO 气体通入酸性高锰酸钾溶液中,离子反应方程式为_________,该反应中
2
SO 表现出__________性。
2
(2)SO 有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱
2
硫法。石灰-石膏法的吸收原理:① SO +Ca(OH) =CaSO ↓+H O②2CaSO+O +4H O=2CaSO·2H O
2 2 3 2 3 2 2 4 2
碱法的吸收原理:将含SO 的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式
2
__________;
已知:
试剂 Ca(OH) NaOH
2
价格(元/kg) 0.36 2.9
与石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(3)在石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。
上述方法中,实现循环利用的物质是__________,请用化学方程式表示在NaSO 溶液中加入
2 3
CaO后的反应原理__________。
【答案】(1)溶液中生成黄色沉淀 氧化性 2MnO -+5SO+2H O=5SO 2-+2Mn2++4H+
4 2 2 4
还原性
(2) SO +2NaOH=Na SO +H O 成本较高
2 2 3 2
(3)NaOH CaO+H O=Ca(OH) Ca(OH) +Na SO =CaSO ↓+2NaOH
2 2 2 2 3 3
【解析】(1)二氧化硫具有弱氧化性,将SO 气体通入氢硫酸中,发生反应SO +2HS=3S↓+
2 2 2
2HO,看到的现象为溶液中生成黄色沉淀,二氧化硫中S化合价由+4价→0价,化合价降低的
2
反应物作氧化剂,体现氧化性;将SO 气体通入酸性高锰酸钾溶液中,高锰酸钾具有强氧化性,
2
将二氧化硫溶于水后生成的亚硫酸氧化为硫酸,二氧化硫遇到强氧化剂时体现还原性,将MnO -
4
还原为Mn2+,S元素的化合价升高2价,锰元素的化合价降低5价,则高锰酸根系数为2,二氧
化硫系数为5,根据原子守恒,硫酸根系数为5,Mn2+系数为2,根据电荷守恒,右侧补4个氢
原子,最终根据H原子守恒,左侧补2个水,即方程式为:5SO +2MnO-+2H O=5SO 2-+2Mn2+
2 4 2 4
+4H+,二氧化硫中S元素的化合价由+4价→+6价,化合价升高的反应物作还原剂,体现还原性,故答案为溶液中生成黄色沉淀,氧化性,2MnO -+5SO+2H O=5SO 2-+2Mn2++4H+,还原性。
4 2 2 4
(2)二氧化硫作为酸性氧化物,可以和氢氧化钠反应盐和水,参照二氧化碳和氢氧化钠反应的
方程式,写出二氧化硫和氢氧化钠的反应方程式为:2NaOH+SO =Na SO +H O,由于石灰价格
2 2 3 2
低,吸收成本比氢氧化钠低的多,故答案为SO +2NaOH=Na SO +H O,成本较高。
2 2 3 2
(3)从流程图中可以看出,向NaSO 溶液中加入CaO后,生成NaOH,生成的NaOH可以作
2 3
为二氧化硫的吸收剂,故NaOH为循环利用的物质;CaO加入溶液中会先和水反应,即
CaO+H O=Ca(OH) ,生成的Ca(OH) 再和NaSO 溶液反应,根据流程图,反应物之一为
2 2 2 2 3
NaOH,再根据复分解反应原理,另一生成物为CaSO,故反应方程式为:
3
Ca(OH) +Na SO =CaSO ↓+2NaOH,故答案为NaOH,CaO+H O=Ca(OH) 、
2 2 3 3 2 2
Ca(OH) +Na SO =CaSO ↓+2NaOH。
2 2 3 3
18.(7分)请根据化学反应与热能的有关知识,填写下列空白:
(1)某同学做如下实验,以检验反应中的能量变化。
①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是___热反应;(b)
中温度降低,由此可以判断(b)中反应是___热反应。
②根据能量守恒定律,(b)中反应物的总能量应该__其生成物的总能量(填“>”或“<”)。
(2)下列过程中不一定放热的是______ (填字母)。
a.葡萄糖在体内的氧化 b.炸药爆炸 c.燃料燃烧 d.化合反应 e.酸碱中和
(3)已知H 和O 反应放热,且断开1 mol H-H键、1 mol O=O键、1 mol O-H键需吸收的
2 2
能量分别为Q kJ、Q kJ、Q kJ,由此可以推知下列关系正确的是______ (填编号)。
1 2 3
①Q+Q >Q ②2Q+Q <4Q ③Q+Q <2Q ④2Q+Q >2Q
1 2 3 1 2 3 1 2 3 1 2 3
【答案】放 吸 < d ②
【解析】对于吸热反应,反应物的总能量低于生成物的总能量,反应后混合物的温度降低;对
于放热反应,反应物的总能量高于生成物的总能量,反应后混合物的温度升高;放热反应包括
燃烧反应、爆炸反应、酸碱中和反应、活泼金属与酸或水的反应、铝热反应、绝大部分化合反
应等,吸热反应包括绝大部分分解反应、碳与二氧化碳的化合反应、碳与水蒸气制水煤气的反应、八水合氢氧化钡与氯化铵的反应;利用键能可计算反应的热量变化,也可比较反应物与生
成物的能量高低。
【详解】(1)①(a)中温度升高,说明反应物的总能量高于生成物的总能量,反应是放热反应;(b)
中温度降低,说明反应物总能量低于生成物的总能量,反应是吸热反应。答案为:放;吸;
②根据能量守恒定律,(b)中反应需吸收热量,则反应物的总能量应该<其生成物的总能量。答案
为:<;
(2)葡萄糖在体内的氧化、炸药爆炸、燃料燃烧、酸碱中和等都是放热反应,化合反应可能是放
热反应,也可能是吸热反应,所以不一定放热的是d。答案为:d;
(3)用结构式表示的H 和O 反应的化学方程式为2H-H+O=O→2 ,则(2Q+Q )-4Q <0,所
2 2 1 2 3
以2Q+Q <4Q ,②正确。故选:②。
1 2 3
【点睛】C、H、CO、S等的燃烧,是放热的化合反应,而CO 与C生成CO的反应,是吸热的
2 2
化合反应,所以化合反应不一定是放热反应。
19.(10分)分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。
回答下列问题:
(1)下列叙述中,不正确的是___________。
A.B 中铁片是负极,C 中铁片是正极 B.三个烧杯中铁片表面均无气泡产生
C.产生气泡的速率 A 中比B中慢 D.C 溶液中 向Zn片电极移动
(2)装置 B中能量转化的主要形式是________________;
(3)装置 B中正极反应式为__________________;
(4)装置 C负极反应式为________________________;
(5)装置 A 中发生反应的离子方程式________________;
(6)Ba(OH) ·8H O 晶体与 NH C1晶体的反应属于_______反应(填“吸热”或“放热”)若把此
2 2 4
反应设计成原电池,你认为是否可行?_______ (填“是”或“否”)。
【答案】(1)B(2)化学能转化为电能
(3)2H++2e-=H ↑
2
(4)Zn—2e-=Zn2+
(5)2H++Fe=H ↑+Fe2+
2
(6)吸热 否
【解析】形成原电池的条件为:①自发进行的氧化还原反应,②形成闭合回路,故A不是原电
池,B、C为原电池;根据原电池正负极判断方式:一般活泼金属做负极,故B中负极铁发生氧
化反应,C中铁做正极,发生还原反应,据此解答。
【详解】(1)A.根据金属活动性:Zn>Fe>Sn, 一般活泼的金属失电子作负极,因此B中铁片
是负极,C中铁片是正极,故A正确;
B.A烧杯中铁直接反应,表面有气泡,C中铁作正极,烧杯中铁表面有气泡,故B错误;
C.B形成原电池,比A中反应速率快,产生气泡的速率A比B中慢,故C正确;
D.原电池中阴离子向负极移动,B中铁片为负极,因此B溶液中 向铁片电极移动,故D
正确;故答案为:B;
(2装置B形成原电池,变化过程中能量转化的主要形式是:化学能转化为电能;
(3)Sn作正极,正极上氢离子得电子生成氢气,装置B中正极反应式为::2H++2e-=H ↑,故答
2
案为:2H++2e-=H ↑;
2
(4)活泼金属Zn作负极,负极反应式为: Zn—2e-=Zn2+,故答案为:Zn—2e-=Zn2+;
(5)A中时铁直接与硫酸发生置换反应,故答案为:2H++Fe=H ↑+Fe2+;
2
(6)常温下,自发进行的氧化还原反应且为放热反应可设计成原电池,Ba(OH) ·8H O 晶体与
2 2
NH C1晶体的反应为吸热反应,且为非氧化还原反应,不能设计成原电池,故答案为:吸热;
4
否。
20.(15分)乙酸乙酯是无色、具有果香气味的液体。某同学采用12.0mL96%密度为1.05g/mL
的乙酸、23mL95%密度为0.75g/mL的乙醇、12.0mL浓硫酸、饱和NaCO 溶液制备乙酸乙酯,
2 3
其实验装置如图所示(烧杯、部分夹持装置、温度计已略去)。
已知:①氯化钙可与乙醇形成难溶于水的CaCl ·6C HOH
2 2 5
②有关有机物的沸点:
试剂 乙醚 乙醇 乙酸 乙酸乙酯沸点(℃) 34.7 78.5 117.9 77.2
①先向蒸馏烧瓶B中加入试剂__,然后通过仪器A慢慢加入__;
②加热保持油浴温度为135~145℃,至不再有液体流出后,停止加热;
③取带有支管的锥形瓶,将一定量的饱和NaCO 溶液分批、少量、多次地加入馏出液中,
2 3
再将混合物分液,弃去水层,得到有机层。
试回答下列问题:
(1)①蒸馏烧瓶B加入试剂 ,然后通过仪器A慢慢加入 。
(2)写出制备乙酸乙酯的化学方程式 。
(3)仪器A的名称是 ;浓硫酸的作用是 ;仪器C的作用是 。
(4)反应中所用的乙醇是过量的,其目的是 。
(5)③中加入饱和碳酸钠溶液的作用 ,分批、少量、多次地加入饱和碳酸钠的原
因是 。
(6)从③中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入饱和氯化钙溶
液分离出 ,再加入无水硫酸钠,然后进行蒸馏,收集77.2℃的馏分,以得到纯净的乙
酸乙酯9.2g,计算此实验中生成乙酸乙酯的产率为 (写出计算的表达式)。
【答案】(1)乙醇 浓硫酸、乙酸
(2)CHCOOH+CH CHOH CHCOOCH CH+H O
3 3 2 3 2 3 2
(3)分液漏斗 催化剂、吸水剂 冷凝
(4)有利于酯化反应向正方向进行(增大醋酸的利用率)
(5)吸收挥发出来的乙酸和乙醇,降低乙酸乙酯的溶解度便于分层析出 防止反应放热,温
度升高,减少乙酸乙酯的产量(6)乙醇 ×100%
【解析】(1)制备乙酸乙酯时,需先加入乙醇,再加浓硫酸和乙酸,因为硫酸密度较大,若先
加浓硫酸再加乙醇会放出大量的热,若热量不能及时散失,会造成液体飞溅而发生危险,所以
先加乙醇再加浓硫酸有利于散热,避免液体飞溅,最后再加入乙酸;
(2)乙酸和乙醇在浓硫酸的催化下加热可反应生成乙酸乙酯,反应方程式为:
CHCOOH+CH CHOH CHCOOCH CH+H O
3 3 2 3 2 3 2
(3)根据图可知,仪器A是分液漏斗;浓硫酸是反应的催化剂,除此之外,浓硫酸有吸水性,
吸收后平衡向正向移动,有利于乙酸乙酯的生成,故还起到吸水剂的作用;仪器C是冷凝管,
主要作用是冷凝蒸出的气体;
(4)乙醇过量可促进平衡向生成乙酸乙酯的方向移动,有利于乙酸乙酯的生成,提高乙酸的转
化率;
(5)饱和碳酸钠可以吸收乙醇,中和乙酸,降低乙酸乙酯的溶解度,有利于乙酸乙酯的分层;
由于碳酸钠与乙酸反应会放热,温度升高会导致乙酸乙酯挥发,导致产率下降,所以要分批、
少量、多次地加入饱和碳酸钠;
(6)由于CaCl 可与乙醇形成难溶于水的CaCl ·6C HOH,所以加入CaCl 可以除去乙醇;
2 2 2 5 2
由于乙醇过量,生成乙酸乙酯的理论产量按照乙酸计算,乙酸的质量为12mL×1.05g/mL×96%,
物质的量为 ,所以乙酸乙酯的理论产量为
×100%;
【点睛】本题要注意第(6)题,乙醇与乙酸反应,乙醇过量,所以生成的乙酸乙酯的量需要根
据乙酸计算。
21.(8分)如图是海带中提取碘的流程图:回答下列问题。
(1)干海带在_____________________中灼烧(填仪器名称)。
(2)操作I名称为_____________________。
(3)分液漏斗在使用前须清洗干净并_________________,在本实验分离过程中,碘的四
氯化碳应该从分液漏斗的_________________(填“上口倒出”或“下口放出”)。
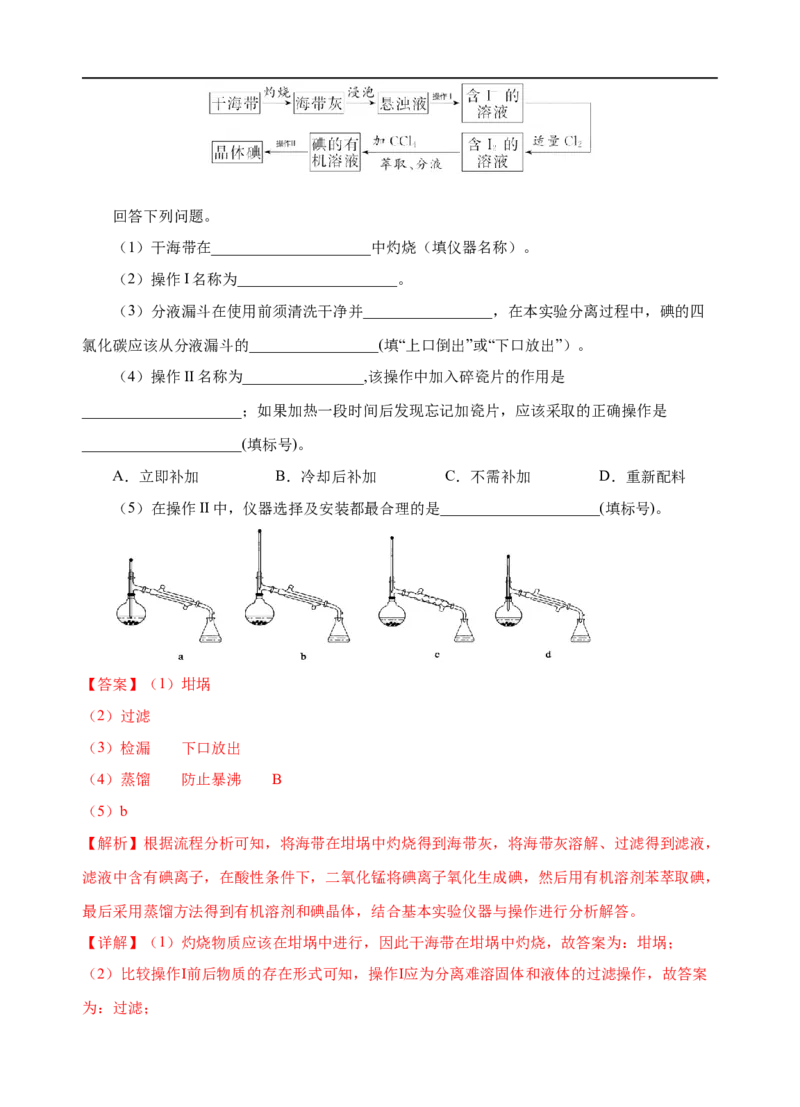
(4)操作II名称为________________,该操作中加入碎瓷片的作用是
_____________________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是
_____________________(填标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(5)在操作II中,仪器选择及安装都最合理的是_____________________(填标号)。
【答案】(1)坩埚
(2)过滤
(3)检漏 下口放出
(4)蒸馏 防止暴沸 B
(5)b
【解析】根据流程分析可知,将海带在坩埚中灼烧得到海带灰,将海带灰溶解、过滤得到滤液,
滤液中含有碘离子,在酸性条件下,二氧化锰将碘离子氧化生成碘,然后用有机溶剂苯萃取碘,
最后采用蒸馏方法得到有机溶剂和碘晶体,结合基本实验仪器与操作进行分析解答。
【详解】(1)灼烧物质应该在坩埚中进行,因此干海带在坩埚中灼烧,故答案为:坩埚;
(2)比较操作Ⅰ前后物质的存在形式可知,操作Ⅰ应为分离难溶固体和液体的过滤操作,故答案
为:过滤;(3)分液漏斗在使用前必须清洗干净并检漏,由于CCl 的密度比水大,所以萃取后碘的四氯化
4
碳溶液在下层,分液时下层液体从下口放出,上层液体从上口倒出,故答案为:检漏;下口放
出;
(4)操作Ⅱ为从碘的有机溶剂中分离出单质碘,则操作Ⅱ应为分离易溶固体和液体的蒸馏操作,
蒸馏时需加入碎瓷片防止暴沸,若加热一段时间后发现忘记加碎瓷片,需停止加热,待冷却后
再补加碎瓷片,故答案为:蒸馏;防止暴沸;B;
(5)蒸馏时,温度计的水银球应位于蒸馏烧瓶的支管口处,冷凝管采用直形冷凝管,便于馏分
流出,故答案为:b。
【点睛】本题通过从海带中提取碘的实验,考查明物质的分离、提纯等知识,重在对所学知识
的灵活运用,掌握物质分离、提纯方法、常见仪器的使用及I-、I 的性质是解题关键,注意对流
2
程的分析理解,明确怎样提取碘。