文档内容
2021-2022 学年高二化学重难点专题突破
模块一 原子结构与性质
综合测试
(75分钟 100分)
一、选择题(本题共15小题,每小题3分,共45分。)
1. 1913年,丹麦科学家玻尔第一次认识到氢原子光谱是氢原子的电子跃迁产生的。玻尔的原子结构理论,
一个很大的成就是( )
A.证明了原子核外电子在圆形轨道上运动
B.提出了原子核是可以进一步细分的
C.解决了氢原子光谱和原子能级之间的关系
D.应用了量子力学理论中的概念和方法
【答案】选D。
【解析】玻尔把量子论用于原子,与卢瑟福核式原子模型结合起来,提出电子在一定轨道上运动的原子结
构模型,成功地解释了氢原子光谱是线状光谱的原因,为后来人们用更多的量子数来标记核外电子的运动
状态来解释复杂的原子光谱提供了可以借鉴的方法。所以D说法正确。
2.下列各项叙述正确的是( )
A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
B.价电子排布式为5s25p1的元素位于第五周期第ⅠA 族,是s区元素
C.所有原子任一电子层的s电子云轮廓图都是球形,但球的半径大小不同
D. Cr原子的核外电子排布式是1s22s22p63s23p63d44s2
24
【答案】选C。
【解析】镁原子由1s22s22p63s2→1s22s22p63p2时,原子吸收能量,由基态转化成激发态,A错误;价电子排
布式为5s25p1的元素,位于第五周期第ⅢA 族,是p区元素,B错误;所有原子任一电子层的s电子云轮
廓图都是球形,电子层越大,球的半径越大,C正确; Cr原子的核外电子排布式是1s22s22p63s23p63d54s1,
24
半充满轨道能量较低,D错误。
3. Al、 P、 S、 Cl是周期表中的短周期主族元素。下列有关说法正确的是( )
13 15 16 17
A.元素Al在周期表中位于第4周期ⅢA族
B.元素P的简单气态氢化物的化学式为PH
4C.第一电离能:I(Al)I(S),故C错误;D.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性
1 1
PAs,所以电负性F>O>As,故D正确。
5.同周期的三种元素X、Y、Z,已知其最高价氧化物对应水化物的酸性强弱为 HXO>H YO >H ZO ,则
4 2 4 3 4
下列判断错误的是( )
A.原子半径:X>Y>Z
B.气态氢化物的稳定性:HX>H Y>ZH
2 3
C.电负性:X>Y>Z
D.非金属性:X>Y>Z
【答案】选A。
【解析】同周期从左到右非金属性逐渐增强,原子半径逐渐减小,所以原子半径:XY>Z,所以气态氢化物的稳定性:HX>H Y>ZH ,故B正
2 3确;非金属性:X>Y>Z,元素的非金属性越强,其电负性越强,则电负性:X>Y>Z,故C正确;最高价
氧化物对应水化物的酸性:HXO>H YO >H ZO,则非金属性:X>Y>Z,故D正确。
4 2 4 3 4
6.在基态多电子原子中,关于核外电子能量的叙述错误的是( )
A.最易失去的电子能量最高
B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
【答案】选C。
【解析】能量越高,越易失去电子,离核越远,故A、B、D正确。p轨道电子能量不一定大于s轨道,例
如2p轨道电子能量低于3s轨道电子能量,C不正确。
7.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为r >r >r >r >r
X Y Z W Q
C.离子Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物酸性比Q的强
【答案】选A。
【解析】由元素在周期表中的位置可推知X、Y、Z、W、Q分别为N、O、Al、S、Cl。元素X(N)的最高
正价+5与元素Z(Al)的最高正价+3之和为8;原子半径的大小顺序为r >r >r >r >r ;Y2-和Z3+的核外电
Z W Q X Y
子数和电子层数均相同;非金属性:W(S)D>E
B.元素A的最外层轨道中无自旋状态相同的电子
C.元素B、C不可能形成化合物
D.与元素B处于同周期且在该周期中第一电离能最小的元素的单质能与HO发生置换反应
2
【答案】选D。
【解析】根据五种元素的电负性和最低负化合价,推知A为C、B为S、C为Cl、D为O、E为F。选项
A,C、D、E的氢化物依次为HCl、HO、HF,氢化物的稳定性顺序:HF>H O>HCl。选项B,碳元素原
2 2
子最外层电子排布式为2s22p2,2p能级上的两个电子分占两个p轨道,且自旋状态相同。选项C,S原子最
外层有6个电子,Cl原子最外层有7个电子,它们之间可通过形成共价键,使两种原子均达到8电子稳定
结构,形成的化合物有SCl 等。选项D,此单质为Na,Na能与HO发生置换反应生成NaOH和H。
2 2 2
12.A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外
K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三
周期中第一电离能最大。下列有关叙述错误的是( )
A.四种元素A、B、C、D分别为O、Ca、Na、Ar
B.元素A、B、C两两组成的化合物可为CaO、CaO、NaO、NaO 等
2 2 2 2
C.元素A、C简单离子的半径大小关系为AN>F比较。
13. (双选)图1、图2表示的是元素的某种性质随原子序数的变化而发生的变化。下列说法正确的是(
)
A.图1可能表示的是元素单质的密度随原子序数变化的规律
B.图1可能表示的是元素原子的电离能随原子序数变化的规律
C.图2可能表示的是元素原子的半径随原子序数变化的规律
D.图2可能表示的是元素的电负性随原子序数变化的规律
【答案】选BD。
【解析】图1中同周期元素的性质呈增大趋势,但第 Ⅱ A、ⅤA族元素出现反常,可推知图1表示第一
电离能的变化。图2中F对应的数值最大,为4.0,可推知图2描述的是电负性与原子序数的关系。
14.(双选)下列说法正确的是( )
A.轨道表示式 能反映钠原子轨道的能级差别和电子的自旋状态
B.金属Cr基态原子的核外电子排布式为1s22s22p63s23p63d44s2
C.基态原子的p能级上半充满的元素一定位于p区
D.X、Y元素同周期且电负性X>Y,则第一电离能:Y<X【答案】选AC。
【解析】根据轨道表示式: 能够清晰地看出原子轨道的能级差别,也可以看出电子的
自旋状态,故A正确;金属Cr基态原子的核外电子排布式为1s22s22p63s23p63d54s1,即3d轨道半满,4s轨
道半满,能量低,稳定,故B错误;基态原子的p能级上半充满的可能为2p3、3p3、4p3等,即最外层一定
是5个电子,该元素为第ⅤA族元素,p区是指周期表中ⅢA族到零族的元素,第ⅤA族元素都属于p区,
故C正确;X、Y元素同周期且电负性X>Y,第一电离能有两种可能:Ⅰ:Y<X,Ⅱ:Y>X,以第二周
期为例,如电负性:N>C,第一电离能:N>C,或电负性:O>N,第一电离能:N>O,即第ⅡA族和
第ⅤA族元素的第一电离能反常,故D错误。
15.现有三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3。则下
列有关比较中正确的是( )
A.第一电离能:③>②>① B.原子半径:③>②>①
C.电负性:③>②>① D.最高正化合价:③=②>①
【答案】选A。
【解析】由三种元素基态原子的电子排布式可知,①是硫元素、②是磷元素、③是氮元素。磷元素原子3p
能级容纳3个电子,为半充满稳定状态,能量较低,第一电离能高于同周期相邻元素,所以第一电离能
SP,故第一电离能N>P>S,即③>②>①,
A正确;同周期主族元素自左而右原子半径逐渐减小,所以原子半径 P>S,同主族元素从上至下原子半径
逐渐增大,所以原子半径P>N,故原子半径P>S>N,即②>①>③,B错误;同周期元素自左而右元素电负
性逐渐增大,所以电负性P②=③,
D错误。
二、非选择题:本题共5小题,共55分。
16.(12分)(1)周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,
b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只
有1个电子,但次外层有18个电子。
请填写下列空白。
①e元素基态原子的核外电子排布式为__________。
② b、c、d 三种元素的第一电离能数值由小到大的顺序为________(填元素符号),其原因是
______________________。
(2)Ni是元素周期表中第 28号元素,第二周期基态原子未成对电子数与 Ni相同且电负性小的元素是
______________;26号元素价层电子排布式为________;L原子核外电子占有9个轨道,而且有一个未成对电子,L是________元素。
(3)硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
①基态硒原子的价层电子排布式为__________。
②锗、砷、硒的第一电离能大小排序为______________。
【解析】 (1)根据已知信息,可以推出a为H,b为N,c为O,d为S,e为Cu。①Cu元素基态原子的核
外电子排布式为1s22s22p63s23p63d104s1。②b、c、d三种元素的第一电离能数值由小到大的顺序为SSe>Ge。
答案:(1)①1s22s22p63s23p63d104s1
②SSe>Ge
17.(10分)有A、B、C、D四种元素,其原子序数依次增大,且质子数均小于18。A元素原子的最外层只
有1个电子,该元素阳离子与N3-核外电子排布相同;B元素原子核外各轨道上均无成单电子;C元素原
子的价电子排布为ns2np1;D-的核外电子构型与Ar相同。
(1)写出A、C、D的元素符号
A________,C________,D________。
(2)写出B元素原子的电子排布式__________,
D元素原子的轨道表示式为________________。
(3)A、B、C、D第一电离能由小到大的顺序为(用元素符号表示,下同)_______________,电负性由小到大
的顺序为________________。
【解析】A形成的阳离子A+与N3-核外电子排布相同,则A是Na。C的价电子排布为ns2np1,是ⅢA族元
素,只能是Al。B为第3周期元素,且原子核外各轨道上均无成单电子,应为Mg。D-的核外电子构型与
Ar相同,D为Cl。
答案:(1)Na Al Cl (2)1s22s22p63s2 (3)Na<Al<Mg<Cl Na<Mg<Al<Cl
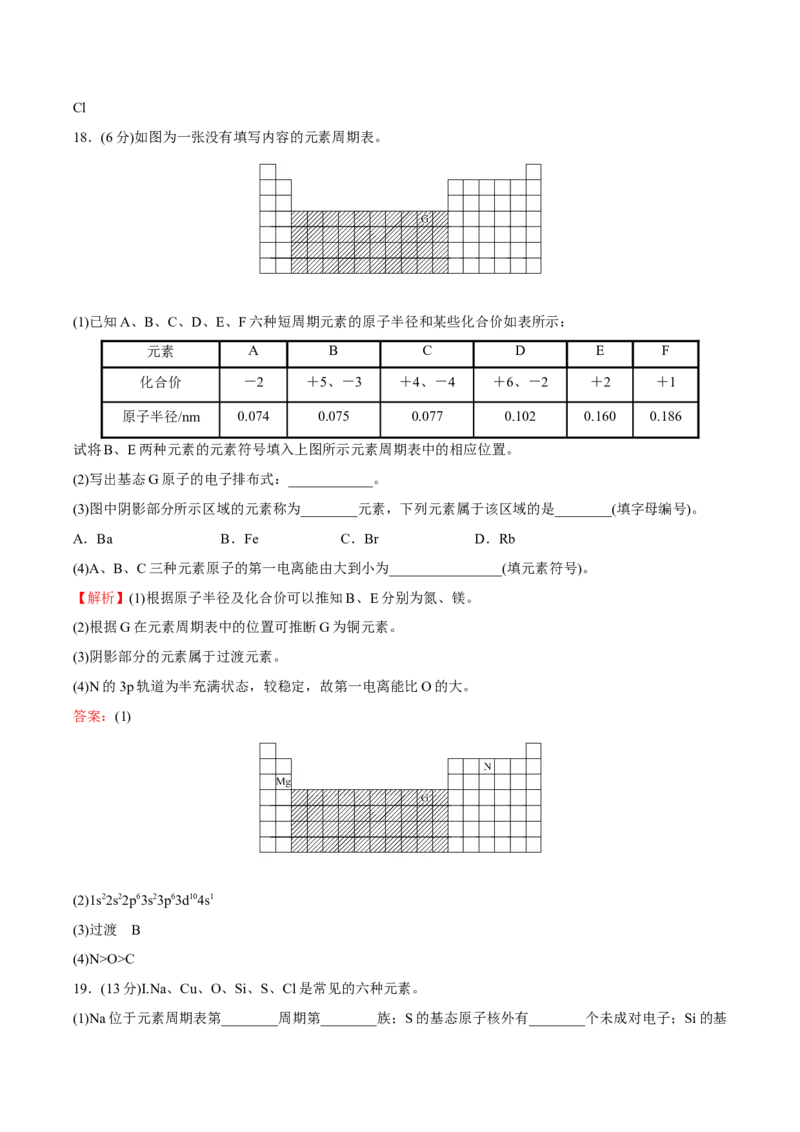
18.(6分)如图为一张没有填写内容的元素周期表。
(1)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如表所示:
元素 A B C D E F
化合价 -2 +5、-3 +4、-4 +6、-2 +2 +1
原子半径/nm 0.074 0.075 0.077 0.102 0.160 0.186
试将B、E两种元素的元素符号填入上图所示元素周期表中的相应位置。
(2)写出基态G原子的电子排布式:____________。
(3)图中阴影部分所示区域的元素称为________元素,下列元素属于该区域的是________(填字母编号)。
A.Ba B.Fe C.Br D.Rb
(4)A、B、C三种元素原子的第一电离能由大到小为________________(填元素符号)。
【解析】(1)根据原子半径及化合价可以推知B、E分别为氮、镁。
(2)根据G在元素周期表中的位置可推断G为铜元素。
(3)阴影部分的元素属于过渡元素。
(4)N的3p轨道为半充满状态,较稳定,故第一电离能比O的大。
答案:(1)
(2)1s22s22p63s23p63d104s1
(3)过渡 B
(4)N>O>C
19.(13分)Ⅰ.Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________。
(2)用“>”或“<”填空:
第一电离能 离子半径 酸性
Si____S O2-____Na+ HSO ____HClO
2 4 4
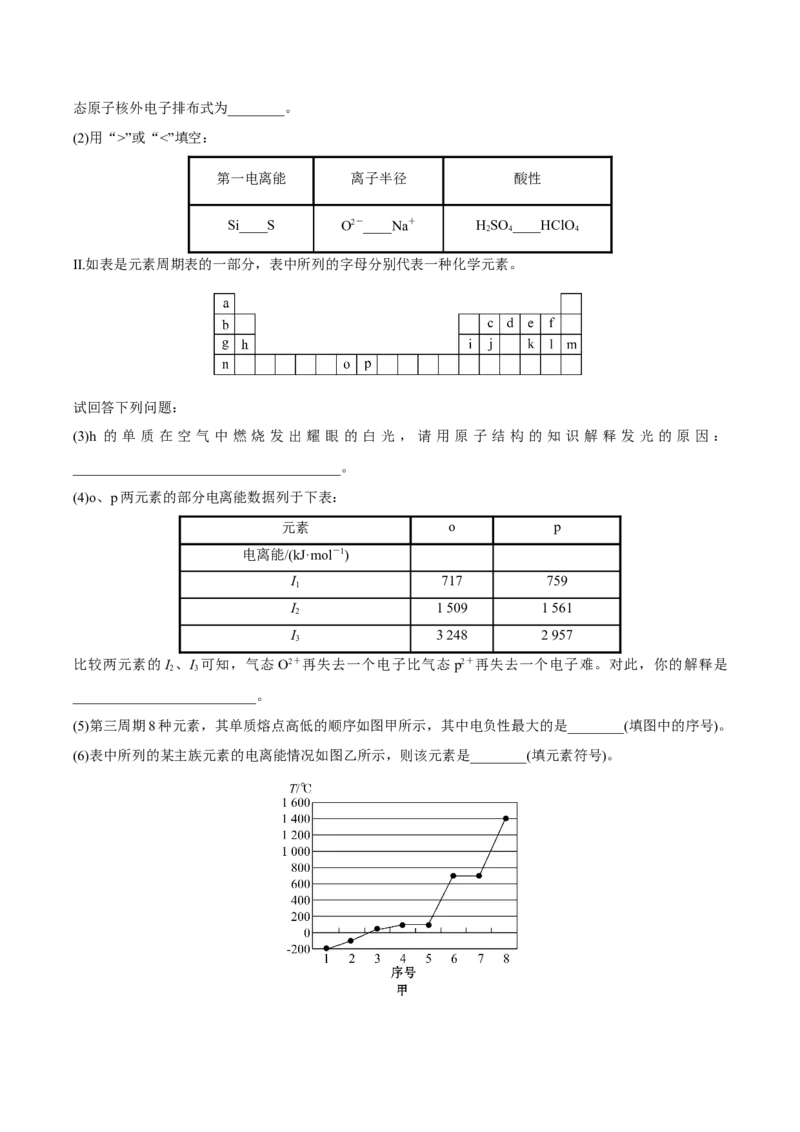
Ⅱ.如表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题:
(3)h 的 单 质 在 空 气 中 燃 烧 发 出 耀 眼 的 白 光 , 请 用 原 子 结 构 的 知 识 解 释 发 光 的 原 因 :
______________________________________。
(4)o、p两元素的部分电离能数据列于下表:
元素 o p
电离能/(kJ·mol-1)
I 717 759
1
I 1 509 1 561
2
I 3 248 2 957
3
比较两元素的I 、I 可知,气态O2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是
2 3
__________________________。
(5)第三周期8种元素,其单质熔点高低的顺序如图甲所示,其中电负性最大的是________(填图中的序号)。
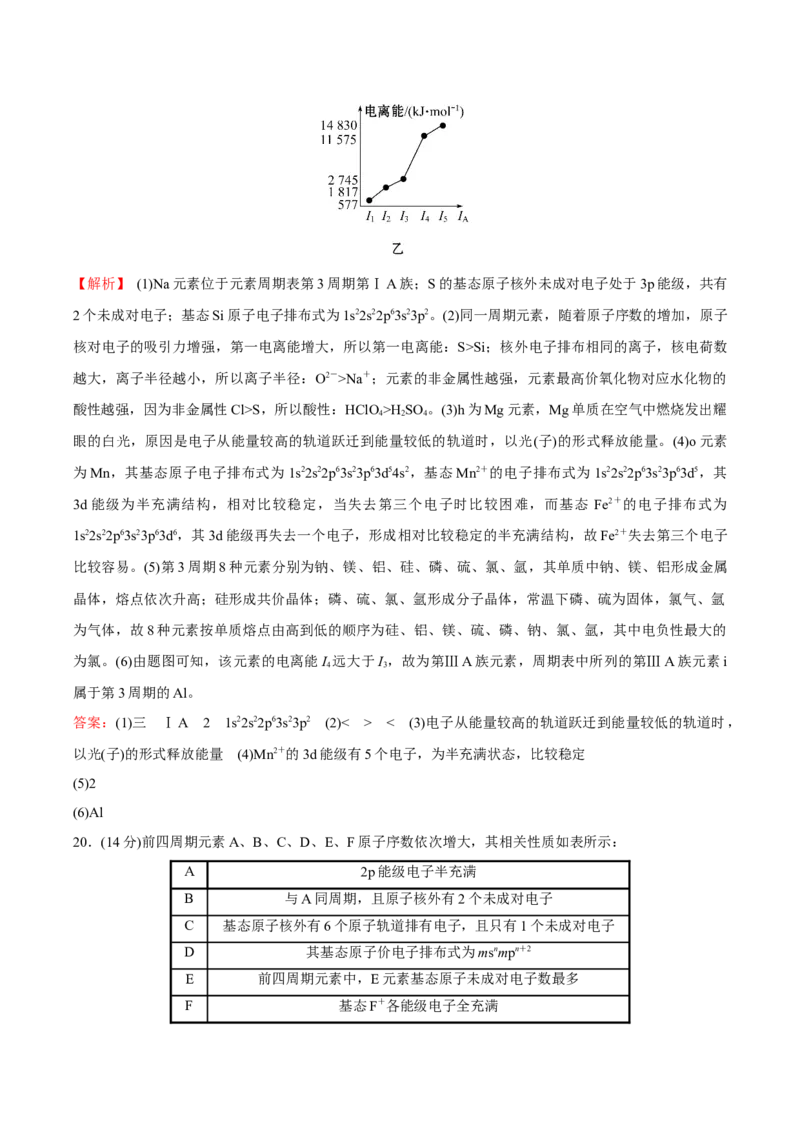
(6)表中所列的某主族元素的电离能情况如图乙所示,则该元素是________(填元素符号)。【解析】 (1)Na元素位于元素周期表第3周期第ⅠA族;S的基态原子核外未成对电子处于3p能级,共有
2个未成对电子;基态Si原子电子排布式为1s22s22p63s23p2。(2)同一周期元素,随着原子序数的增加,原子
核对电子的吸引力增强,第一电离能增大,所以第一电离能:S>Si;核外电子排布相同的离子,核电荷数
越大,离子半径越小,所以离子半径:O2->Na+;元素的非金属性越强,元素最高价氧化物对应水化物的
酸性越强,因为非金属性Cl>S,所以酸性:HClO>H SO 。(3)h为Mg元素,Mg单质在空气中燃烧发出耀
4 2 4
眼的白光,原因是电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量。(4)o元素
为Mn,其基态原子电子排布式为 1s22s22p63s23p63d54s2,基态Mn2+的电子排布式为1s22s22p63s23p63d5,其
3d能级为半充满结构,相对比较稳定,当失去第三个电子时比较困难,而基态 Fe2+的电子排布式为
1s22s22p63s23p63d6,其3d能级再失去一个电子,形成相对比较稳定的半充满结构,故Fe2+失去第三个电子
比较容易。(5)第3周期8种元素分别为钠、镁、铝、硅、磷、硫、氯、氩,其单质中钠、镁、铝形成金属
晶体,熔点依次升高;硅形成共价晶体;磷、硫、氯、氩形成分子晶体,常温下磷、硫为固体,氯气、氩
为气体,故8种元素按单质熔点由高到低的顺序为硅、铝、镁、硫、磷、钠、氯、氩,其中电负性最大的
为氯。(6)由题图可知,该元素的电离能I 远大于I ,故为第ⅢA族元素,周期表中所列的第ⅢA族元素i
4 3
属于第3周期的Al。
答案:(1)三 ⅠA 2 1s22s22p63s23p2 (2)< > < (3)电子从能量较高的轨道跃迁到能量较低的轨道时,
以光(子)的形式释放能量 (4)Mn2+的3d能级有5个电子,为半充满状态,比较稳定
(5)2
(6)Al
20.(14分)前四周期元素A、B、C、D、E、F原子序数依次增大,其相关性质如表所示:
A 2p能级电子半充满
B 与A同周期,且原子核外有2个未成对电子
C 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子
D 其基态原子价电子排布式为msnmpn+2
E 前四周期元素中,E元素基态原子未成对电子数最多
F 基态F+各能级电子全充满请根据以上情况,回答下列问题:
(1)E元素基态原子核外有________种能量不同的电子,电子排布式为________________,F位于元素周期
表第________周期第________族,写出F元素基态原子的价电子排布式________________。
(2)B和C可形成一种同时含有共价键和离子键的化合物,写出此化合物的电子式________。
(3)A、B、C、D四种元素第一电离能由大到小的顺序为________________________________(用元素符号
表示)。B、C、D三种元素的简单离子的半径由大到小的顺序为_______________________(用离子符号表
示)。
(4)写出一个化学方程式证明元素B和D的非金属性强弱___________________。
(5)许多金属盐都可以发生焰色反应,如元素C,其原因是________________。
【解析】2p能级处于半充满状态的元素是氮,A为氮元素,则B为氧元素;C元素核外有11个电子,为
钠元素;由D元素的价电子排布式可知为S;由于半充满状态也是稳定状态,故Cr是前四周期中未成对电
子数最多的元素,E为铬元素;F+各能级都全充满,故为铜元素。(2)钠与氧可形成NaO 和NaO两种化
2 2 2
合物,其中NaO 中既有离子键又有共价键。(3)注意氮原子的2p能级处于半充满状态,结构稳定导致其第
2 2
一电离能比氧大。(4)利用非金属的置换反应证明氧、硫的非金属性强弱关系。(5)焰色反应是由于电子从较
高激发态(高能量)向较低激发态(低能量)或基态跃迁时,多余的能量以光的形式释放出来所产生的。
答案:(1)7 1s22s22p63s23p63d54s1(或[Ar]3d54s1) 四 ⅠB 3d104s1
(2)
(3)N>O>S>Na S2->O2->Na+
(4)2H S+O===2S↓+2HO
2 2 2
(5)激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长(可见光区域)光的形式释放能量倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育