文档内容
2021-2022 学年高二化学重难点专题突破
模块三 晶体结构与性质
综合测试
(75分钟 100分)
一、选择题(本题共15小题,每小题3分,共45分。)
1.关于晶体与非晶体,正确的说法是( )
A.区分晶体与非晶体最可靠的方法是比较硬度
B.凡有规则外形的物体就一定是晶体
C.一种物质不是晶体就是非晶体
D.具有各向异性的固体一定是晶体
【答案】选D。
【解析】区分晶体与非晶体最可靠的方法是X射线衍射法,不能根据硬度来判断晶体与非晶体,故 A错误;
晶体的规则外形是天然形成的,人为制造的规则外形的物体不一定是晶体,如玻璃是非晶体,可以制成各
种规则的形状,故B错误;固体除包含晶体、非晶体外,还有一类介于晶体与非晶体之间,称作准晶体,
故C错误;晶体具有各向异性,因此具有各向异性的固体一定是晶体,故D正确。
2.下列物质性质的变化规律与物质结构间的因果关系,与键能无关的变化规律是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.金刚石的硬度大于硅,其熔、沸点也高于硅
C.NaF、NaCl、NaBr、NaI的熔点依次降低
D.F、Cl、Br 、I 的熔、沸点逐渐升高
2 2 2 2
【答案】选D。
【解析】HF、HCl、HBr、HI热稳定性依次减弱是因为它们的共价键键能逐渐减小,与键能有关;金刚石
的硬度大于硅,熔、沸点高于硅是因为C—C键键能大于Si—Si键键能;NaF、NaCl、NaBr、NaI的熔点
依次降低是它们的离子键键能随离子半径增大逐渐减小;F 、Cl 、Br 、I 为分子晶体,熔、沸点的高低由
2 2 2 2
分子间作用力决定,与键能无关。
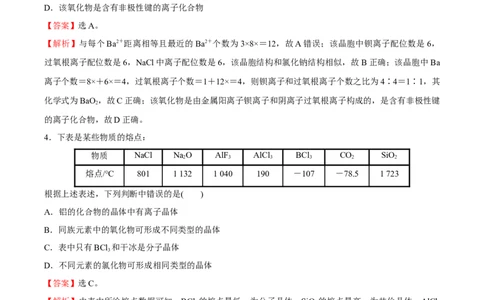
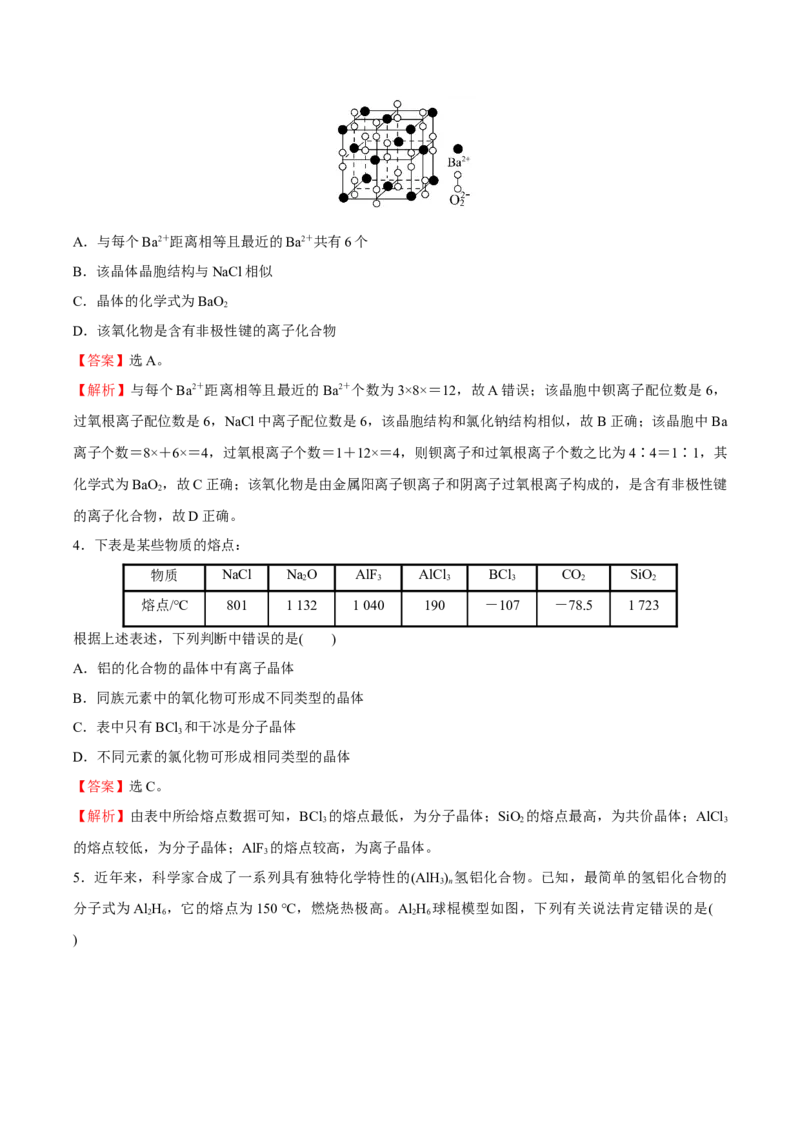
3.钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法错误的是( )A.与每个Ba2+距离相等且最近的Ba2+共有6个
B.该晶体晶胞结构与NaCl相似
C.晶体的化学式为BaO
2
D.该氧化物是含有非极性键的离子化合物
【答案】选A。
【解析】与每个Ba2+距离相等且最近的Ba2+个数为3×8×=12,故A错误;该晶胞中钡离子配位数是6,
过氧根离子配位数是6,NaCl中离子配位数是6,该晶胞结构和氯化钠结构相似,故B正确;该晶胞中Ba
离子个数=8×+6×=4,过氧根离子个数=1+12×=4,则钡离子和过氧根离子个数之比为4∶4=1∶1,其
化学式为BaO,故C正确;该氧化物是由金属阳离子钡离子和阴离子过氧根离子构成的,是含有非极性键
2
的离子化合物,故D正确。
4.下表是某些物质的熔点:
物质 NaCl NaO AlF AlCl BCl CO SiO
2 3 3 3 2 2
熔点/℃ 801 1 132 1 040 190 -107 -78.5 1 723
根据上述表述,下列判断中错误的是( )
A.铝的化合物的晶体中有离子晶体
B.同族元素中的氧化物可形成不同类型的晶体
C.表中只有BCl 和干冰是分子晶体
3
D.不同元素的氯化物可形成相同类型的晶体
【答案】选C。
【解析】由表中所给熔点数据可知,BCl 的熔点最低,为分子晶体;SiO 的熔点最高,为共价晶体;AlCl
3 2 3
的熔点较低,为分子晶体;AlF 的熔点较高,为离子晶体。
3
5.近年来,科学家合成了一系列具有独特化学特性的(AlH ) 氢铝化合物。已知,最简单的氢铝化合物的
3 n
分子式为Al H ,它的熔点为150 ℃,燃烧热极高。Al H 球棍模型如图,下列有关说法肯定错误的是(
2 6 2 6
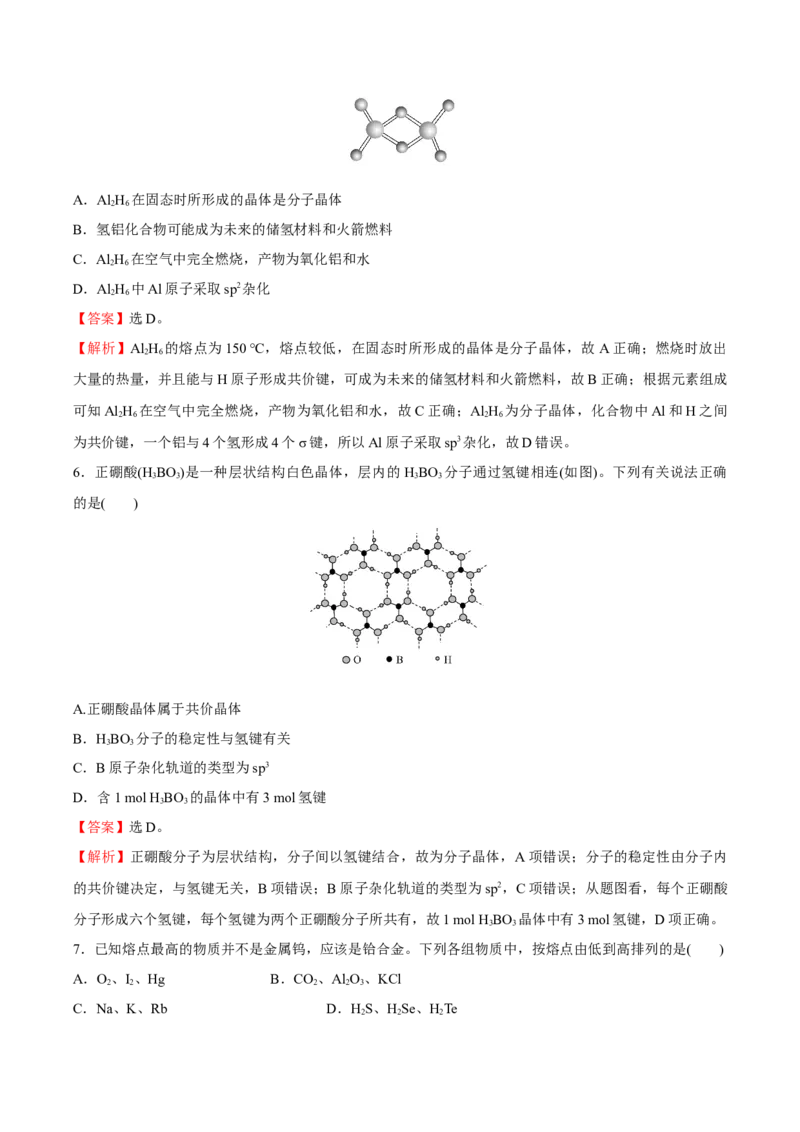
)A.Al H 在固态时所形成的晶体是分子晶体
2 6
B.氢铝化合物可能成为未来的储氢材料和火箭燃料
C.Al H 在空气中完全燃烧,产物为氧化铝和水
2 6
D.Al H 中Al原子采取sp2杂化
2 6
【答案】选D。
【解析】Al H 的熔点为150 ℃,熔点较低,在固态时所形成的晶体是分子晶体,故 A正确;燃烧时放出
2 6
大量的热量,并且能与H原子形成共价键,可成为未来的储氢材料和火箭燃料,故B正确;根据元素组成
可知Al H 在空气中完全燃烧,产物为氧化铝和水,故C正确;Al H 为分子晶体,化合物中Al和H之间
2 6 2 6
为共价键,一个铝与4个氢形成4个σ键,所以Al原子采取sp3杂化,故D错误。
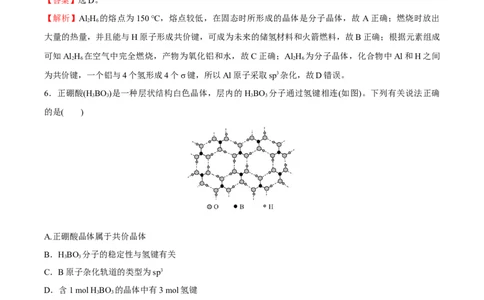
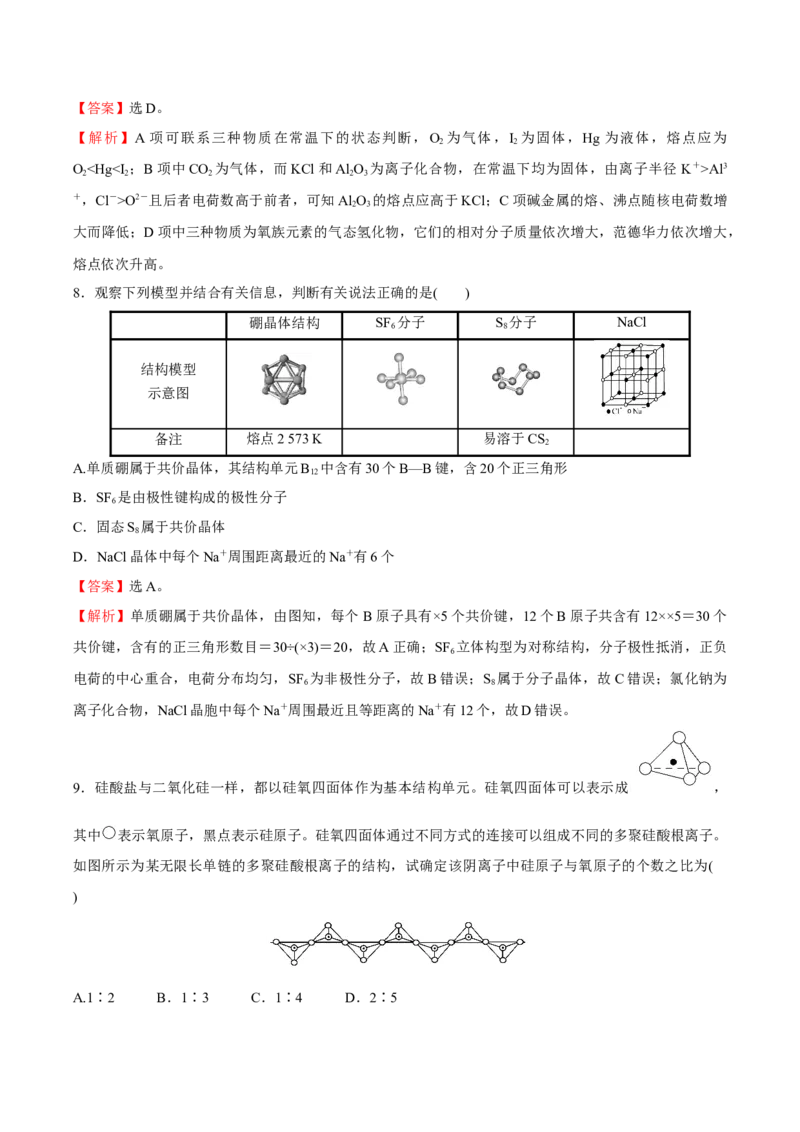
6.正硼酸(H BO)是一种层状结构白色晶体,层内的HBO 分子通过氢键相连(如图)。下列有关说法正确
3 3 3 3
的是( )
A.正硼酸晶体属于共价晶体
B.HBO 分子的稳定性与氢键有关
3 3
C.B原子杂化轨道的类型为sp3
D.含1 mol H BO 的晶体中有3 mol氢键
3 3
【答案】选D。
【解析】正硼酸分子为层状结构,分子间以氢键结合,故为分子晶体,A项错误;分子的稳定性由分子内
的共价键决定,与氢键无关,B项错误;B原子杂化轨道的类型为sp2,C项错误;从题图看,每个正硼酸
分子形成六个氢键,每个氢键为两个正硼酸分子所共有,故1 mol H BO 晶体中有3 mol氢键,D项正确。
3 3
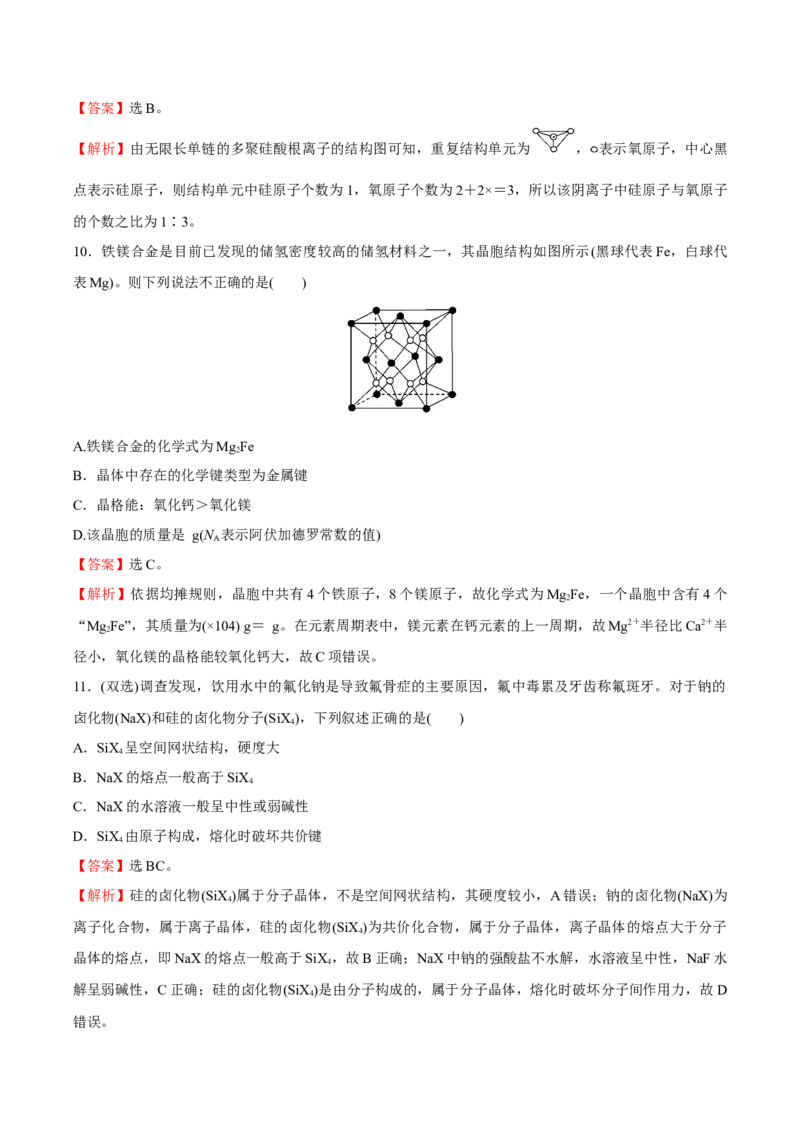
7.已知熔点最高的物质并不是金属钨,应该是铪合金。下列各组物质中,按熔点由低到高排列的是( )
A.O、I、Hg B.CO、Al O、KCl
2 2 2 2 3
C.Na、K、Rb D.HS、HSe、HTe
2 2 2【答案】选D。
【解析】A 项可联系三种物质在常温下的状态判断,O 为气体,I 为固体,Hg 为液体,熔点应为
2 2
OAl3
2 2 2 2 3
+,Cl->O2-且后者电荷数高于前者,可知Al O 的熔点应高于KCl;C项碱金属的熔、沸点随核电荷数增
2 3
大而降低;D项中三种物质为氧族元素的气态氢化物,它们的相对分子质量依次增大,范德华力依次增大,
熔点依次升高。
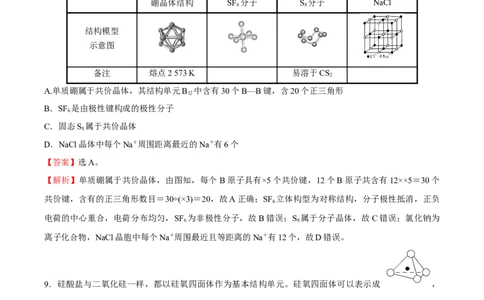
8.观察下列模型并结合有关信息,判断有关说法正确的是( )
硼晶体结构 SF 分子 S 分子 NaCl
6 8
结构模型
示意图
备注 熔点2 573 K 易溶于CS
2
A.单质硼属于共价晶体,其结构单元B 中含有30个B—B键,含20个正三角形
12
B.SF 是由极性键构成的极性分子
6
C.固态S 属于共价晶体
8
D.NaCl晶体中每个Na+周围距离最近的Na+有6个
【答案】选A。
【解析】单质硼属于共价晶体,由图知,每个 B原子具有×5个共价键,12个B原子共含有12××5=30个
共价键,含有的正三角形数目=30÷(×3)=20,故A正确;SF 立体构型为对称结构,分子极性抵消,正负
6
电荷的中心重合,电荷分布均匀,SF 为非极性分子,故B错误;S 属于分子晶体,故C错误;氯化钠为
6 8
离子化合物,NaCl晶胞中每个Na+周围最近且等距离的Na+有12个,故D错误。
9.硅酸盐与二氧化硅一样,都以硅氧四面体作为基本结构单元。硅氧四面体可以表示成 ,
其中 表示氧原子,黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成不同的多聚硅酸根离子。
如图所示为某无限长单链的多聚硅酸根离子的结构,试确定该阴离子中硅原子与氧原子的个数之比为(
)
A.1∶2 B.1∶3 C.1∶4 D.2∶5【答案】选B。
【解析】由无限长单链的多聚硅酸根离子的结构图可知,重复结构单元为 , 表示氧原子,中心黑
点表示硅原子,则结构单元中硅原子个数为1,氧原子个数为2+2×=3,所以该阴离子中硅原子与氧原子
的个数之比为1∶3。
10.铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代
表Mg)。则下列说法不正确的是( )
A.铁镁合金的化学式为MgFe
2
B.晶体中存在的化学键类型为金属键
C.晶格能:氧化钙>氧化镁
D.该晶胞的质量是 g(N 表示阿伏加德罗常数的值)
A
【答案】选C。
【解析】依据均摊规则,晶胞中共有4个铁原子,8个镁原子,故化学式为MgFe,一个晶胞中含有4个
2
“MgFe”,其质量为(×104) g= g。在元素周期表中,镁元素在钙元素的上一周期,故Mg2+半径比Ca2+半
2
径小,氧化镁的晶格能较氧化钙大,故C项错误。
11.(双选)调查发现,饮用水中的氟化钠是导致氟骨症的主要原因,氟中毒累及牙齿称氟斑牙。对于钠的
卤化物(NaX)和硅的卤化物分子(SiX),下列叙述正确的是( )
4
A.SiX 呈空间网状结构,硬度大
4
B.NaX的熔点一般高于SiX
4
C.NaX的水溶液一般呈中性或弱碱性
D.SiX 由原子构成,熔化时破坏共价键
4
【答案】选BC。
【解析】硅的卤化物(SiX)属于分子晶体,不是空间网状结构,其硬度较小,A错误;钠的卤化物(NaX)为
4
离子化合物,属于离子晶体,硅的卤化物(SiX)为共价化合物,属于分子晶体,离子晶体的熔点大于分子
4
晶体的熔点,即NaX的熔点一般高于SiX,故B正确;NaX中钠的强酸盐不水解,水溶液呈中性,NaF水
4
解呈弱碱性,C正确;硅的卤化物(SiX)是由分子构成的,属于分子晶体,熔化时破坏分子间作用力,故D
4
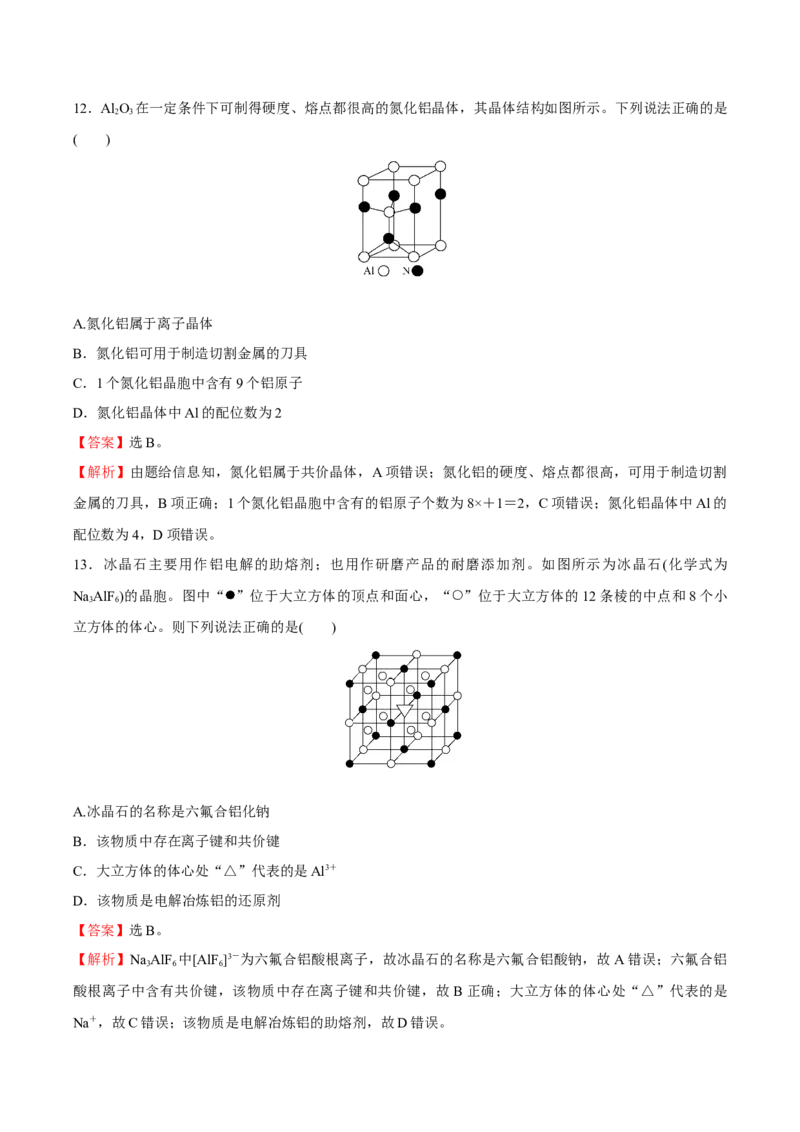
错误。12.Al O 在一定条件下可制得硬度、熔点都很高的氮化铝晶体,其晶体结构如图所示。下列说法正确的是
2 3
( )
A.氮化铝属于离子晶体
B.氮化铝可用于制造切割金属的刀具
C.1个氮化铝晶胞中含有9个铝原子
D.氮化铝晶体中Al的配位数为2
【答案】选B。
【解析】由题给信息知,氮化铝属于共价晶体,A项错误;氮化铝的硬度、熔点都很高,可用于制造切割
金属的刀具,B项正确;1个氮化铝晶胞中含有的铝原子个数为8×+1=2,C项错误;氮化铝晶体中Al的
配位数为4,D项错误。
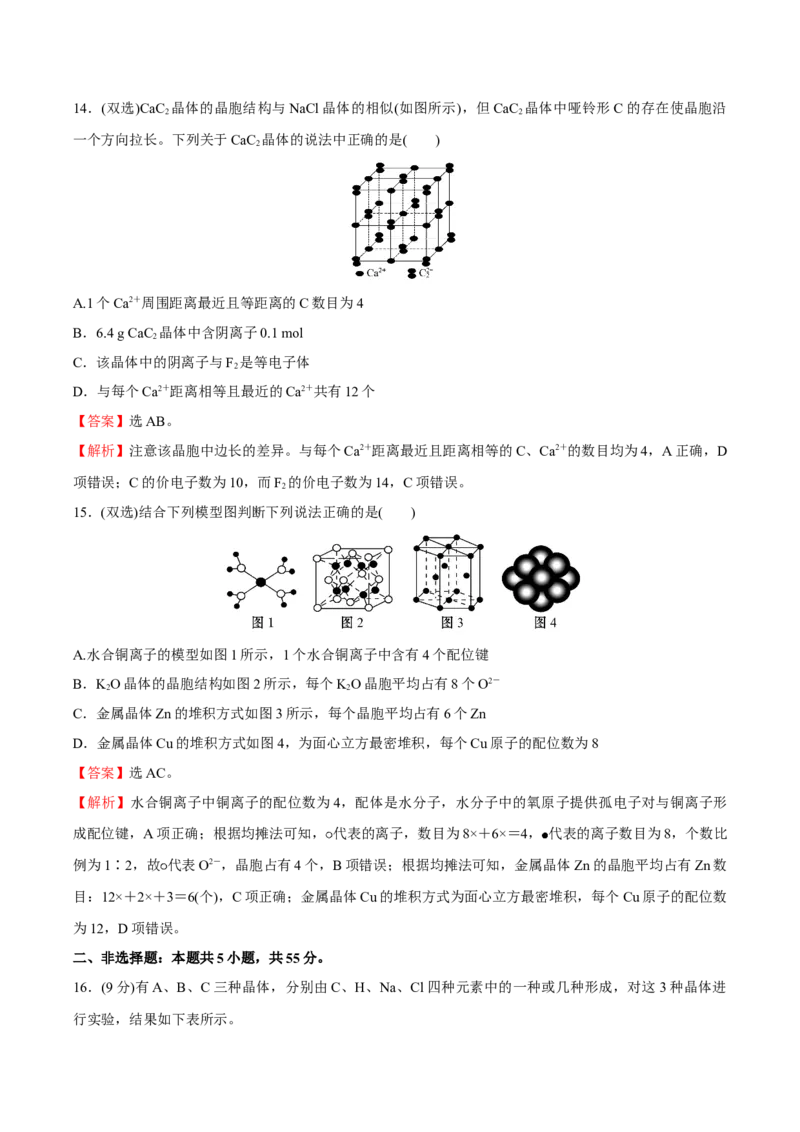
13.冰晶石主要用作铝电解的助熔剂;也用作研磨产品的耐磨添加剂。如图所示为冰晶石(化学式为
NaAlF)的晶胞。图中“ ”位于大立方体的顶点和面心,“ ”位于大立方体的12条棱的中点和8个小
3 6
立方体的体心。则下列说法正确的是( )
A.冰晶石的名称是六氟合铝化钠
B.该物质中存在离子键和共价键
C.大立方体的体心处“△”代表的是Al3+
D.该物质是电解冶炼铝的还原剂
【答案】选B。
【解析】NaAlF 中[AlF ]3-为六氟合铝酸根离子,故冰晶石的名称是六氟合铝酸钠,故 A错误;六氟合铝
3 6 6
酸根离子中含有共价键,该物质中存在离子键和共价键,故 B正确;大立方体的体心处“△”代表的是
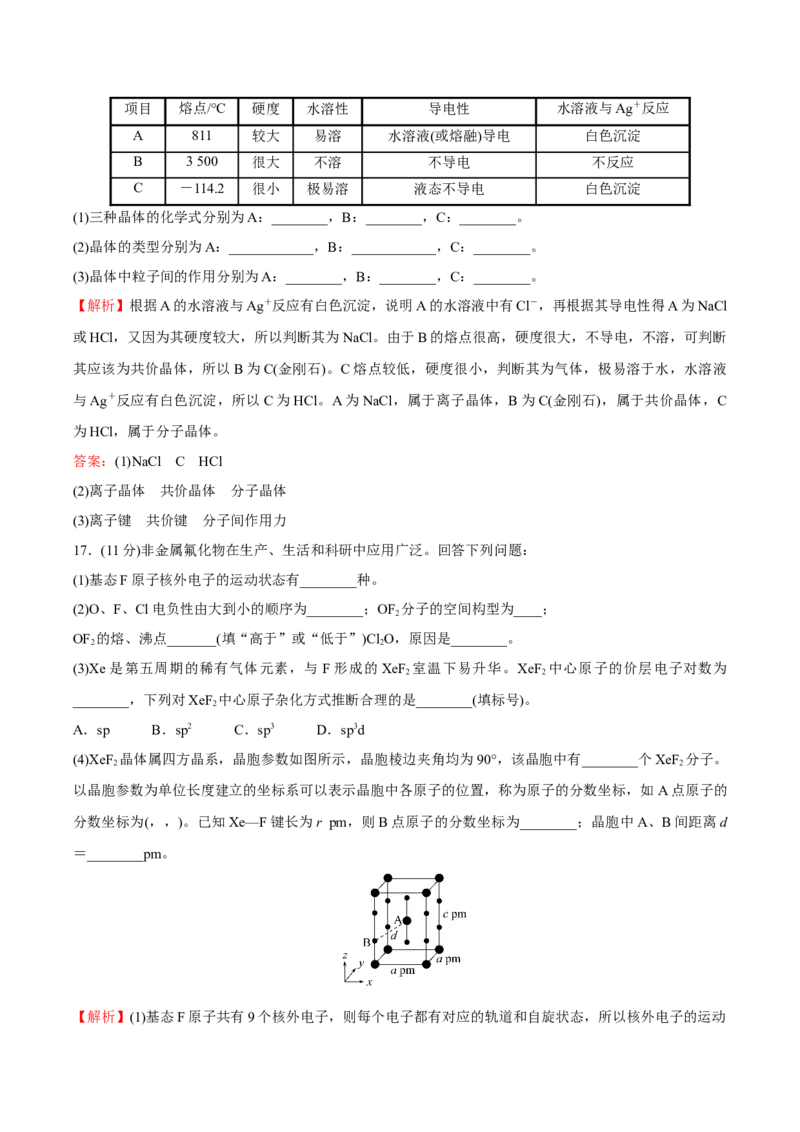
Na+,故C错误;该物质是电解冶炼铝的助熔剂,故D错误。14.(双选)CaC 晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC 晶体中哑铃形C的存在使晶胞沿
2 2
一个方向拉长。下列关于CaC 晶体的说法中正确的是( )
2
A.1个Ca2+周围距离最近且等距离的C数目为4
B.6.4 g CaC 晶体中含阴离子0.1 mol
2
C.该晶体中的阴离子与F 是等电子体
2
D.与每个Ca2+距离相等且最近的Ca2+共有12个
【答案】选AB。
【解析】注意该晶胞中边长的差异。与每个Ca2+距离最近且距离相等的C、Ca2+的数目均为4,A正确,D
项错误;C的价电子数为10,而F 的价电子数为14,C项错误。
2
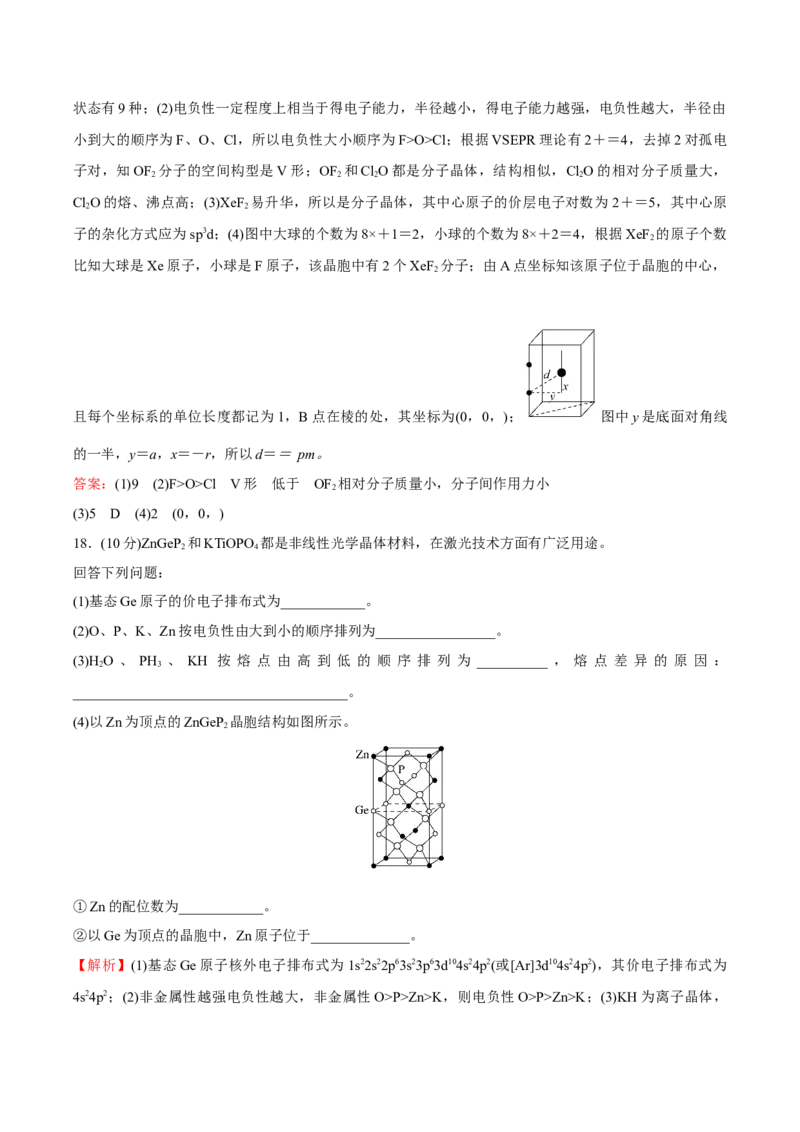
15.(双选)结合下列模型图判断下列说法正确的是( )
A.水合铜离子的模型如图1所示,1个水合铜离子中含有4个配位键
B.KO晶体的晶胞结构如图2所示,每个KO晶胞平均占有8个O2-
2 2
C.金属晶体Zn的堆积方式如图3所示,每个晶胞平均占有6个Zn
D.金属晶体Cu的堆积方式如图4,为面心立方最密堆积,每个Cu原子的配位数为8
【答案】选AC。
【解析】水合铜离子中铜离子的配位数为4,配体是水分子,水分子中的氧原子提供孤电子对与铜离子形
成配位键,A项正确;根据均摊法可知, 代表的离子,数目为8×+6×=4, 代表的离子数目为8,个数比
例为1∶2,故 代表O2-,晶胞占有4个,B项错误;根据均摊法可知,金属晶体Zn的晶胞平均占有Zn数
目:12×+2×+3=6(个),C项正确;金属晶体Cu的堆积方式为面心立方最密堆积,每个Cu原子的配位数
为12,D项错误。
二、非选择题:本题共5小题,共55分。
16.(9分)有A、B、C三种晶体,分别由C、H、Na、Cl四种元素中的一种或几种形成,对这3种晶体进
行实验,结果如下表所示。项目 熔点/℃ 硬度 水溶性 导电性 水溶液与Ag+反应
A 811 较大 易溶 水溶液(或熔融)导电 白色沉淀
B 3 500 很大 不溶 不导电 不反应
C -114.2 很小 极易溶 液态不导电 白色沉淀
(1)三种晶体的化学式分别为A:________,B:________,C:________。
(2)晶体的类型分别为A:____________,B:____________,C:________。
(3)晶体中粒子间的作用分别为A:________,B:________,C:________。
【解析】根据A的水溶液与Ag+反应有白色沉淀,说明A的水溶液中有Cl-,再根据其导电性得A为NaCl
或HCl,又因为其硬度较大,所以判断其为NaCl。由于B的熔点很高,硬度很大,不导电,不溶,可判断
其应该为共价晶体,所以B为C(金刚石)。C熔点较低,硬度很小,判断其为气体,极易溶于水,水溶液
与Ag+反应有白色沉淀,所以C为HCl。A为NaCl,属于离子晶体,B为C(金刚石),属于共价晶体,C
为HCl,属于分子晶体。
答案:(1)NaCl C HCl
(2)离子晶体 共价晶体 分子晶体
(3)离子键 共价键 分子间作用力
17.(11分)非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有________种。
(2)O、F、Cl电负性由大到小的顺序为________;OF 分子的空间构型为____;
2
OF 的熔、沸点_______(填“高于”或“低于”)Cl O,原因是________。
2 2
(3)Xe是第五周期的稀有气体元素,与 F形成的XeF 室温下易升华。XeF 中心原子的价层电子对数为
2 2
________,下列对XeF 中心原子杂化方式推断合理的是________(填标号)。
2
A.sp B.sp2 C.sp3 D.sp3d
(4)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有________个XeF 分子。
2 2
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的
分数坐标为(,,)。已知Xe—F键长为r pm,则B点原子的分数坐标为________;晶胞中A、B间距离d
=________pm。
【解析】(1)基态F原子共有9个核外电子,则每个电子都有对应的轨道和自旋状态,所以核外电子的运动状态有9种;(2)电负性一定程度上相当于得电子能力,半径越小,得电子能力越强,电负性越大,半径由
小到大的顺序为F、O、Cl,所以电负性大小顺序为F>O>Cl;根据VSEPR理论有2+=4,去掉2对孤电
子对,知OF 分子的空间构型是V形;OF 和ClO都是分子晶体,结构相似,ClO的相对分子质量大,
2 2 2 2
ClO的熔、沸点高;(3)XeF 易升华,所以是分子晶体,其中心原子的价层电子对数为 2+=5,其中心原
2 2
子的杂化方式应为sp3d;(4)图中大球的个数为8×+1=2,小球的个数为8×+2=4,根据XeF 的原子个数
2
比知大球是Xe原子,小球是F原子,该晶胞中有2个XeF 分子;由A点坐标知该原子位于晶胞的中心,
2
且每个坐标系的单位长度都记为1,B点在棱的处,其坐标为(0,0,); 图中y是底面对角线
的一半,y=a,x=-r,所以d== pm。
答案:(1)9 (2)F>O>Cl V形 低于 OF 相对分子质量小,分子间作用力小
2
(3)5 D (4)2 (0,0,)
18.(10分)ZnGeP 和KTiOPO 都是非线性光学晶体材料,在激光技术方面有广泛用途。
2 4
回答下列问题:
(1)基态Ge原子的价电子排布式为____________。
(2)O、P、K、Zn按电负性由大到小的顺序排列为_________________。
(3)H O 、 PH 、 KH 按 熔 点 由 高 到 低 的 顺 序 排 列 为 __________ , 熔 点 差 异 的 原 因 :
2 3
_______________________________________。
(4)以Zn为顶点的ZnGeP 晶胞结构如图所示。
2
①Zn的配位数为____________。
②以Ge为顶点的晶胞中,Zn原子位于______________。
【解析】(1)基态Ge原子核外电子排布式为1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2),其价电子排布式为
4s24p2;(2)非金属性越强电负性越大,非金属性O>P>Zn>K,则电负性O>P>Zn>K;(3)KH为离子晶体,HO、PH 均为分子晶体,离子晶体熔点一般高于分子晶体,所以KH的熔点最高,而HO分子间存在氢键,
2 3 2
所以熔点高于PH ,则熔点由高到低的顺序排列为KH>H O>PH ;(4)①以体心的Zn为例,距离其最近且
3 2 3
距离相等的原子有4个,所以配位数为4;②结合晶胞结构示意图可知,以Ge为顶点的晶胞中,Zn原子
位于棱心、面心。
答案:(1)4s24p2 (2)O、P、Zn、K (3)KH、HO、PH KH是离子晶体,HO、PH 都是分子晶体,HO
2 3 2 3 2
分子间存在氢键 (4)①4 ②面心、棱心
19.(12分)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合
物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为________,其沸点比NH 的________(填“高”
3
或“低”),其判断理由是______________________。
(2)Fe成为阳离子时首先失去________轨道电子,Sm的价电子排布式为 4f66s2,Sm3+价电子排布式为
__________________。
(3)比较离子半径:F-________O2-(填“大于”“等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。
图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表
示为________________;通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=
___________________g·cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图 1中原子
1的坐标为(,,),则原子2和3的坐标分别为________、________。
【解析】(1)As与N同族,位于第ⅤA族,其氢化物的结构与氨气相同,则AsH 分子的空间构型为三角锥
3
形;在氨气分子间,存在氢键和范德华力,AsH 分子间只存在范德华力,所以导致沸点AsH 低于NH 。
3 3 3
(2)Fe的核外电子排布式为[Ar]3d64s2,Fe成为阳离子时首先失去最外层两个电子,即4s轨道上的电子。Sm
的价电子排布式为4f66s2,Sm成为阳离子Sm3+时首先失去最外层两个电子,即6s轨道上的电子,再失去4f轨道上的一个电子,所以Sm3+的价电子排布式为4f5。
(3)电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径: F-