文档内容
2019-2020 年高一化学高频考题期末组合模拟卷 01
(考试时间:90分钟 试卷满分:100分)
考试内容:必修二 难度:★★★☆☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.我国毛笔的制作技艺属于国家非物质文化遗产,相传古人制作该毛笔的过程为“以枯木为管,
鹿毛为柱,羊毛为被(外衣)”,则下列说法正确的是
A.枯木的主要成分蛋白质
B.鹿毛、羊毛均只含有C、H、O三种元素
C.枯木、鹿毛的主要成分互为同分异构体
D.采用灼烧法可以区分枯木、毛笔的“外衣”
2.下列说法正确的是
A.CO、NO、NO 都是大气污染气体,在空气中都能稳定存在
2
B.明矾在水中生成的Al(OH) 胶体有吸附性,因此常用明矾对水进行消毒
3
C.CO、NO 或SO 都会导致酸雨的形成
2 2 2
D.活性炭、SO 、NaO 都能使品红溶液褪色,原理不同
2 2 2
3.下列关于氮及其化合物的说法,不正确的是
A.硝酸可以与甘油反应生成烈性炸药硝化甘油
B.氯碱工业中可以用氨气检查氯气管道是否泄漏
C.工业上制备硝酸是利用NH 和O 反应生成NO,进一步转化为NO 及HNO
3 2 2 3
D.为提高作物的养分,可以是铵态氮肥与碱性肥料混合使用
4.往FeCl 和BaCl 的混合溶液中通入SO ,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产
3 2 2
生,下列说法正确的是
A.该实验表明FeCl 有还原性 B.白色沉淀为BaSO
3 3
C.该实验表明SO 有漂白性 D.反应后溶液酸性增强
2
5.下列化学反应一定是放热反应的是
A.Ba(OH)·8H O晶体与NH Cl晶体混合时
2 2 4B.金属钠与水反应
C.浓硫酸稀释
D.煅烧石灰石
6.下列图示的装置不能形成原电池的是
A. B.
C. D.
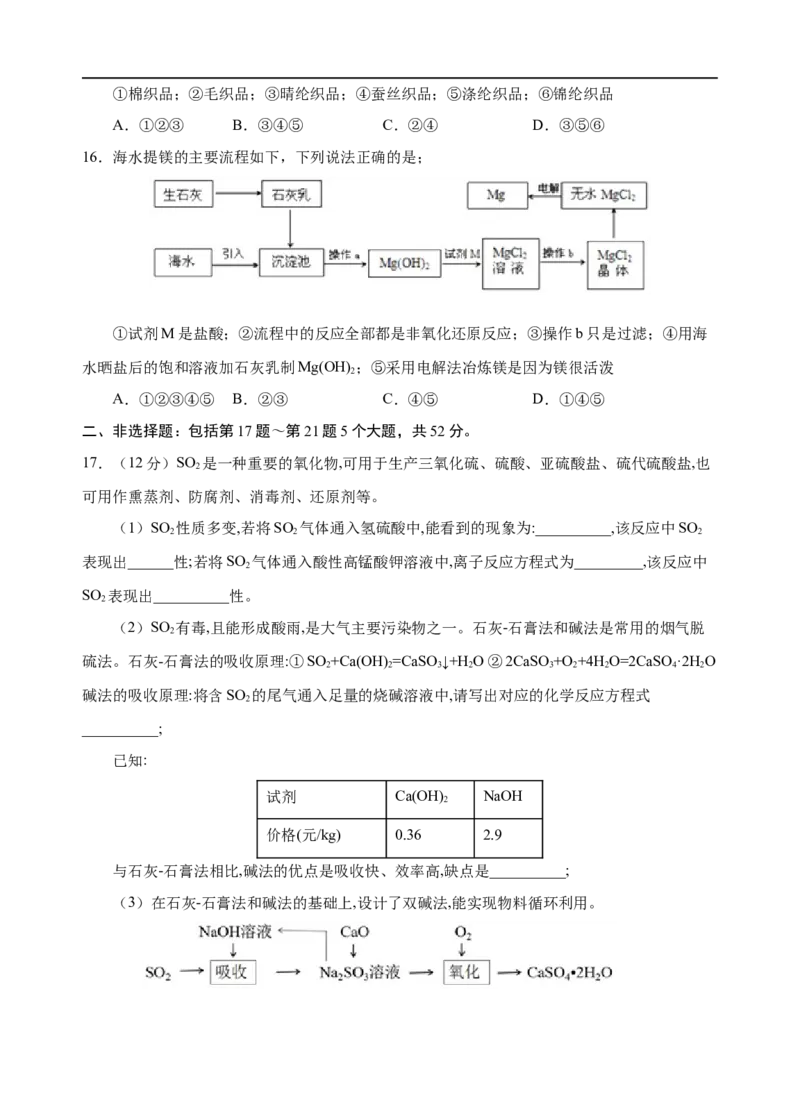
7.X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时X棒
变粗,Y棒变细,则X、Y、Z可能是下列中的
编号 X Y Z
A Zn Cu 稀硫酸
B Ag Zn 硝酸银溶液
C Cu Ag 硫酸铜溶液
D Cu Zn 稀硫酸
8.在光照条件下,纳米TiO 能将甲醛催化氧化成二铖化碳和水。经10小时(h)催化氧化后,某
2
密闭空间内甲醛的浓度从2.0×10-7mol/L降到1.0×10-7mol/L,则甲醛在这段时间内的平均反应速
率为
A.4.0×10-8mol/(L·h) B.3.0×10-8mol/(L·h)
C.2.0×10-8mol/(L·h) D.1.0×10-8mol/(L·h)
9.对于可逆反应 A(g)+3B(s) 2C(g)+2D(g),在不同条件下的化学反应速率如下, 其中
表示的反应速率最快的是A.v(A)=0.5 mol·L-1·min-1 B.v(B)=1.2 mol·L-1·s-1
C.v(C)=0.1 mol·L-1·s-1 D.v(D)=0.4 mol·L-1·min-1
10.下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是
A.10℃20mL3mol/L的盐酸溶液 B.20℃30mL2mol/L的盐酸溶液
C.20℃20mL2mol/L的盐酸溶液 D.20℃10mL4mol/L的盐酸溶液
11.云南特色小吃“过桥米线”做法如下:先用滚沸的鸡汤一碗,上罩浮油,再辅以切得极薄
的生肉片、乌龟片、火腿片、葱头等,最后把主料米线放入拌食即成。“过桥米线”汤鲜、肉
嫩、料香、米线滑润,吃起来别有一番风味。以下有关“过桥米线”的说法不正确的是
A.上层浮油沸点较高,难以挥发
B.浮油对下层汤水起到很好的“液封”作用,使下层汤水及热量难以外逸
C.去掉上面的一层浮油,将减弱“过桥米线”的保温效果
D.上层浮油高温水解即产生美味的物质
12.制取一氯乙烷最好采用的方法是
A.乙烷和氯气反应 B.乙烯和氯气反应
C.乙烷和氯化氢反应 D.乙烯和氯化氢反应
13.下列实验能获得成功的是
A.苯和浓溴水用铁做催化剂制溴苯
B.用酸性高锰酸钾溶液除去甲烷中混有的乙烯
C.甲烷与氯气光照制得纯净的一氯甲烷
D.乙烯通入溴的四氯化碳溶液得到1,2—二溴乙烷
14.在抗击“2019新型冠状病毒”的过程中,大量防护和消毒用品投入使用。下列有关说法正
确的是
A.新型冠状病毒由C、H、O三种元素组成
B.过氧化氢、乙醇、过氧乙酸等消毒液均可以将病毒氧化而达到消毒目的
C.聚丙烯和聚四氟乙烯为生产防护服的主要材料,二者均属于有机高分子材料
D.84消毒液是以NaClO为主要有效成分的消毒液,与医用酒精混合可以提升消毒效果
15.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣
服的汗渍、血迹及人体排放的蛋白质油渍遇到它,皆能水解而除去,下列衣料中不能用加酶洗
衣粉洗涤的是①棉织品;②毛织品;③晴纶织品;④蚕丝织品;⑤涤纶织品;⑥锦纶织品
A.①②③ B.③④⑤ C.②④ D.③⑤⑥
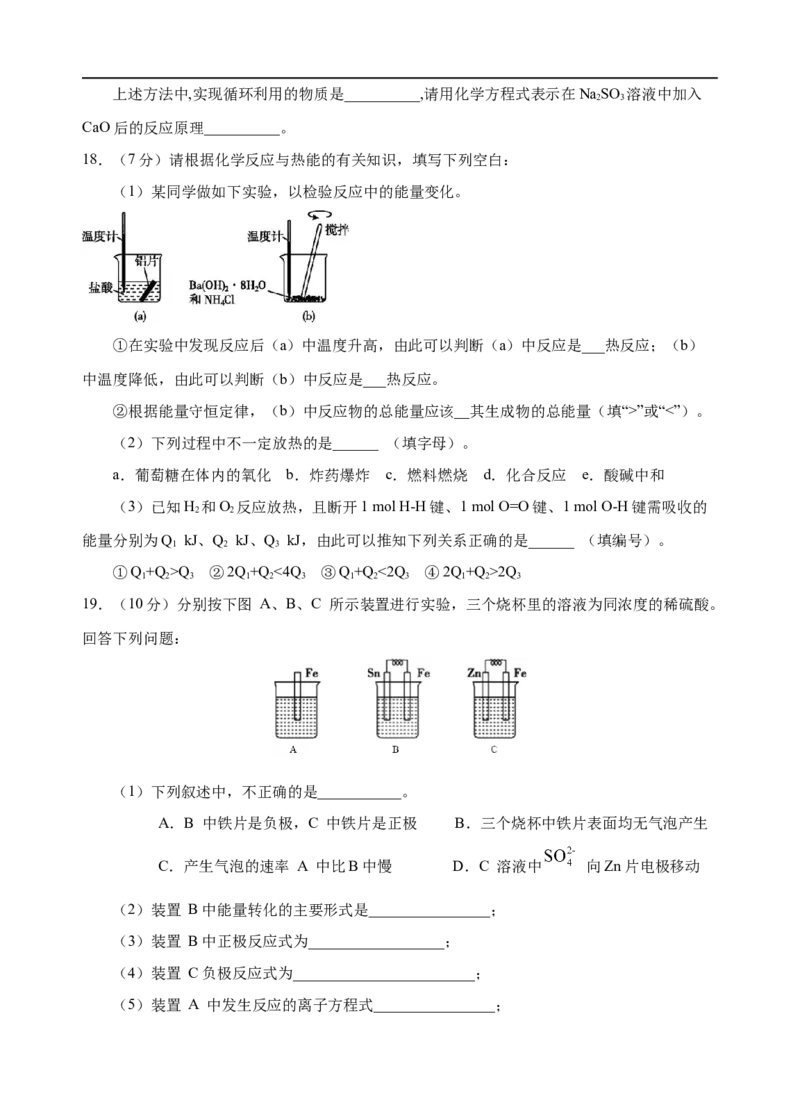
16.海水提镁的主要流程如下,下列说法正确的是;
①试剂M是盐酸;②流程中的反应全部都是非氧化还原反应;③操作b只是过滤;④用海
水晒盐后的饱和溶液加石灰乳制Mg(OH) ;⑤采用电解法冶炼镁是因为镁很活泼
2
A.①②③④⑤ B.②③ C.④⑤ D.①④⑤
二、非选择题:包括第17题~第21题5个大题,共52分。
17.(12分)SO 是一种重要的氧化物,可用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也
2
可用作熏蒸剂、防腐剂、消毒剂、还原剂等。
(1)SO 性质多变,若将SO 气体通入氢硫酸中,能看到的现象为:__________,该反应中SO
2 2 2
表现出______性;若将SO 气体通入酸性高锰酸钾溶液中,离子反应方程式为_________,该反应中
2
SO 表现出__________性。
2
(2)SO 有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱
2
硫法。石灰-石膏法的吸收原理:① SO +Ca(OH) =CaSO ↓+H O②2CaSO+O +4H O=2CaSO·2H O
2 2 3 2 3 2 2 4 2
碱法的吸收原理:将含SO 的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式
2
__________;
已知:
试剂 Ca(OH) NaOH
2
价格(元/kg) 0.36 2.9
与石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(3)在石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。上述方法中,实现循环利用的物质是__________,请用化学方程式表示在NaSO 溶液中加入
2 3
CaO后的反应原理__________。
18.(7分)请根据化学反应与热能的有关知识,填写下列空白:
(1)某同学做如下实验,以检验反应中的能量变化。
①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是___热反应;(b)
中温度降低,由此可以判断(b)中反应是___热反应。
②根据能量守恒定律,(b)中反应物的总能量应该__其生成物的总能量(填“>”或“<”)。
(2)下列过程中不一定放热的是______ (填字母)。
a.葡萄糖在体内的氧化 b.炸药爆炸 c.燃料燃烧 d.化合反应 e.酸碱中和
(3)已知H 和O 反应放热,且断开1 mol H-H键、1 mol O=O键、1 mol O-H键需吸收的
2 2
能量分别为Q kJ、Q kJ、Q kJ,由此可以推知下列关系正确的是______ (填编号)。
1 2 3
①Q+Q >Q ②2Q+Q <4Q ③Q+Q <2Q ④2Q+Q >2Q
1 2 3 1 2 3 1 2 3 1 2 3
19.(10分)分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。
回答下列问题:
(1)下列叙述中,不正确的是___________。
A.B 中铁片是负极,C 中铁片是正极 B.三个烧杯中铁片表面均无气泡产生
C.产生气泡的速率 A 中比B中慢 D.C 溶液中 向Zn片电极移动
(2)装置 B中能量转化的主要形式是________________;
(3)装置 B中正极反应式为__________________;
(4)装置 C负极反应式为________________________;
(5)装置 A 中发生反应的离子方程式________________;(6)Ba(OH) ·8H O 晶体与 NH C1晶体的反应属于_______反应(填“吸热”或“放热”)若把此
2 2 4
反应设计成原电池,你认为是否可行?_______ (填“是”或“否”)。
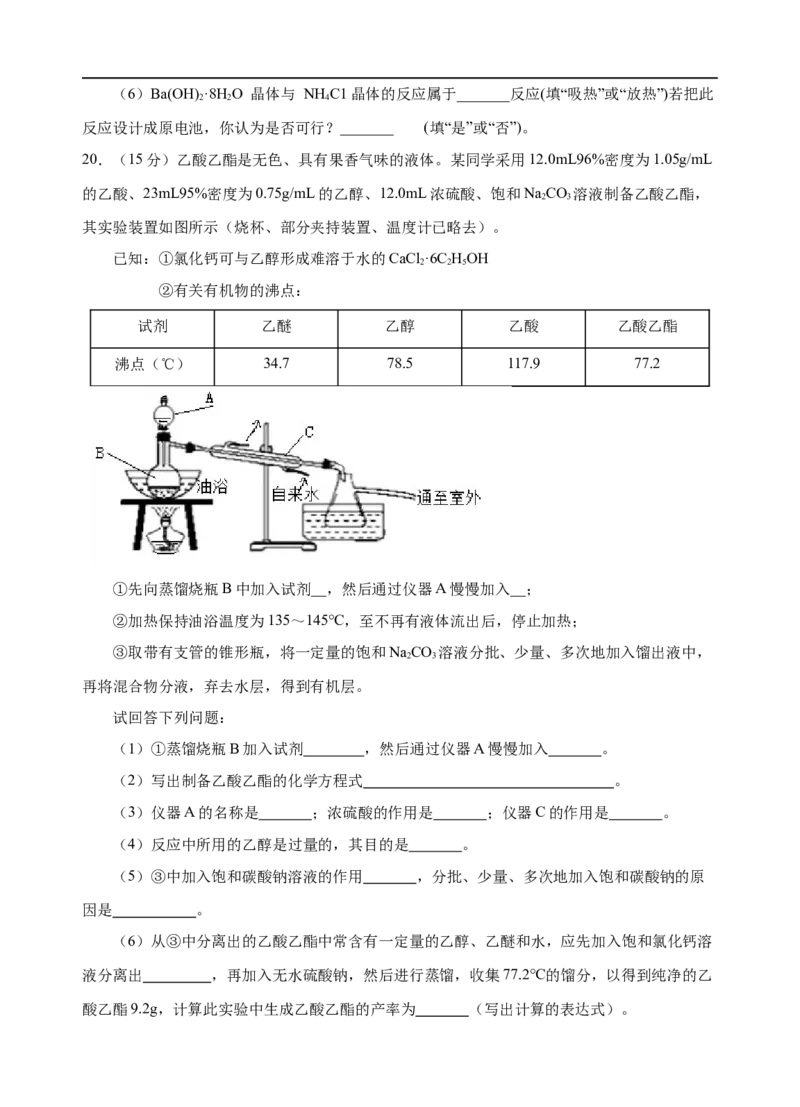
20.(15分)乙酸乙酯是无色、具有果香气味的液体。某同学采用12.0mL96%密度为1.05g/mL
的乙酸、23mL95%密度为0.75g/mL的乙醇、12.0mL浓硫酸、饱和NaCO 溶液制备乙酸乙酯,
2 3
其实验装置如图所示(烧杯、部分夹持装置、温度计已略去)。
已知:①氯化钙可与乙醇形成难溶于水的CaCl ·6C HOH
2 2 5
②有关有机物的沸点:
试剂 乙醚 乙醇 乙酸 乙酸乙酯
沸点(℃) 34.7 78.5 117.9 77.2
①先向蒸馏烧瓶B中加入试剂__,然后通过仪器A慢慢加入__;
②加热保持油浴温度为135~145℃,至不再有液体流出后,停止加热;
③取带有支管的锥形瓶,将一定量的饱和NaCO 溶液分批、少量、多次地加入馏出液中,
2 3
再将混合物分液,弃去水层,得到有机层。
试回答下列问题:
(1)①蒸馏烧瓶B加入试剂 ,然后通过仪器A慢慢加入 。
(2)写出制备乙酸乙酯的化学方程式 。
(3)仪器A的名称是 ;浓硫酸的作用是 ;仪器C的作用是 。
(4)反应中所用的乙醇是过量的,其目的是 。
(5)③中加入饱和碳酸钠溶液的作用 ,分批、少量、多次地加入饱和碳酸钠的原
因是 。
(6)从③中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入饱和氯化钙溶
液分离出 ,再加入无水硫酸钠,然后进行蒸馏,收集77.2℃的馏分,以得到纯净的乙
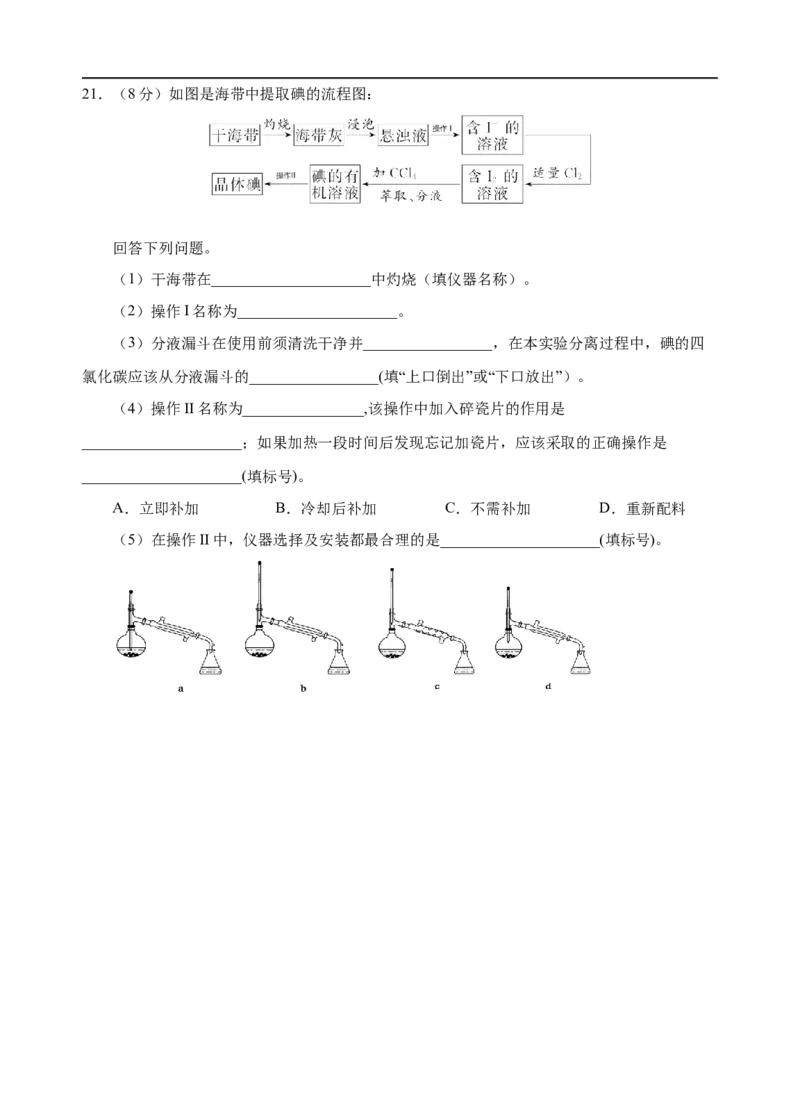
酸乙酯9.2g,计算此实验中生成乙酸乙酯的产率为 (写出计算的表达式)。21.(8分)如图是海带中提取碘的流程图:
回答下列问题。
(1)干海带在_____________________中灼烧(填仪器名称)。
(2)操作I名称为_____________________。
(3)分液漏斗在使用前须清洗干净并_________________,在本实验分离过程中,碘的四
氯化碳应该从分液漏斗的_________________(填“上口倒出”或“下口放出”)。
(4)操作II名称为________________,该操作中加入碎瓷片的作用是
_____________________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是
_____________________(填标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(5)在操作II中,仪器选择及安装都最合理的是_____________________(填标号)。