文档内容
2021-2022 学年高二化学重难点专题突破
模块素养评价(二)
(75分钟 100分)
一、选择题(本题共15小题,每小题3分,共45分。
1.下列表示氮原子结构的化学用语中,对核外电子运动状态描述正确且能据此确定电子的能级的是( )
A. B.
C.1s22s22p3 D.
2.下列各项叙述中正确的是( )
A.电子层序数越大,s原子轨道的形状相同,半径越大
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.镁原子由1s22s22p63s2→1s22s22p63p2时,释放能量,由基态转化成激发态
D.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
3.下列有关说法正确的是( )
A.电负性:N>O>F
B.离子半径由大到小的顺序:H+>Li+>H-
C.键角:BeCl >NCl >CCl
2 3 4
D.晶格能:Al O>MgO>NaCl
2 3
4.下列说法错误的是( )
A.CH 分子球棍模型:
4
B.基态Si原子价电子排布图:
C.第一电离能:N>O>C
D.石墨质软的原因是其层间作用力微弱
5. 以下有关元素性质的说法不正确的是( )
A.具有下列电子排布式的原子中:①1s22s22p63s23p2、②1s22s22p3、③1s22s22p2、④1s22s22p63s23p4,原子
半径最大的是①B.具有下列最外层电子排布式的原子中:①3s23p1、②3s23p2、③3s23p3、④3s23p4,第一电离能最大的是
③
C.①Na、K、Rb、②N、P、As、③O、S、Se、④Na、P、Cl,元素的电负性随原子序数增大而递增的是
④
D.某元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、21
703,当它与氯气反应时可能生成的阳离子是X3+
6.下列关于C、Si及其化合物结构与性质的论述错误的是( )
A.键能C—C>Si—Si 、C—H>Si—H ,因此C H 稳定性大于Si H
2 6 2 6
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C.SiH 中Si的化合价为+4,CH 中C的化合价为-4,因此SiH 还原性小于CH
4 4 4 4
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成p—pπ 键
7.维生素B 可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构简式为以下关于维生素
1
B 的说法正确的是( )
1
A.只含σ键和π键
B.既有共价键又有离子键
C.该物质的熔点可能高于NaCl
D.该物质不易溶于盐酸
8. X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示,该晶体的化学式为(
)
A.NaN B.AlN C.MgN D.Cu N
3 3 2 3
9.葡萄糖的银镜反应实验如下:
步骤1:向试管中加入1 mL 2% AgNO 溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为
3
灰褐色。步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1 mL 10%葡萄糖溶液,振荡,在60~70 ℃水浴中加热,观察到试管内壁形成了
光亮银镜。
下列说法不正确的是( )
A.步骤1中观察到的白色沉淀为AgOH
B.步骤2中沉淀溶解是因为生成了银氨配合物
C.步骤3中产生银镜说明葡萄糖具有还原性
D.如图所示银的晶胞中有14个银原子
10.下面的排序不正确的是( )
A.晶体熔点的高低:对羟基苯甲醛>邻羟基苯甲醛
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点由高到低:Na>Mg>Al
D.晶格能由大到小:NaF>NaCl>NaBr>NaI
11.(双选)某一化合物的分子式为AB ,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的
2
电负性值分别为3.5和4.0,已知AB 分子的键角为103.3°。下列推断不正确的是( )
2
A.AB 分子的空间构型为直线形
2
B.A—B键为极性共价键,AB 分子为非极性分子
2
C.AB 与HO相比,AB 的熔、沸点比HO的低
2 2 2 2
D.AB 分子中无氢原子,分子间不能形成氢键,而HO分子间能形成氢键
2 2
12.B和Al为同族元素,下列说法错误的是( )
A.BF 和AlF 都可以与F-形成配位键
3 3
B.HBO 为三元酸,Al(OH) 呈两性
3 3 3
C.共价键的方向性使晶体B有脆性,原子层的相对滑动使金属Al有延展性
D.B和Al分别与N形成的共价晶体,均具有较高硬度和熔点
13.(双选)短周期主族元素X、Y、Z、W原子序数依次增大,且原子序数Y+Z=X+W,X和W同主族
Z的族序数与周期数相等,四种元素中只有一种金属元素。下列说法正确的是( )A.W有两种常见氧化物
B.原子半径Y C
B.A、B、C第一电离能的大小顺序为C> B > A
C.AD 和ED 两分子的中心原子均为sp3杂化
3 4
D.ED 分子中各原子均达8电子稳定结构
4
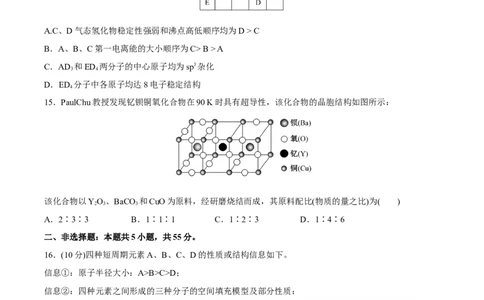
15.PaulChu教授发现钇钡铜氧化合物在90 K时具有超导性,该化合物的晶胞结构如图所示:
该化合物以YO、BaCO 和CuO为原料,经研磨烧结而成,其原料配比(物质的量之比)为( )
2 3 3
A.2∶3∶3 B.1∶1∶1 C.1∶2∶3 D.1∶4∶6
二、非选择题:本题共5小题,共55分。
16.(10分)四种短周期元素A、B、C、D的性质或结构信息如下。
信息①:原子半径大小:A>B>C>D;
信息②:四种元素之间形成的三种分子的空间填充模型及部分性质:
是地球上最常见的物质之一,常
温为液态,是包括人类在内所有 无色,无味且易燃,是 弱酸,有强氧化性,可以用
生命生存的重要资源,也是生物 21世纪的主要能源 于消毒杀菌
体最重要的组成部分
请根据上述信息回答下列问题。(1)甲、乙、丙中含有的共同元素是________(填名称)。
(2)B元素在周期表中的位置为________。
(3)上述元素的原子M层有一个未成对p电子的是________(填元素符号)。
(4)丙的电子式为________,丙与SO 水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为
2
________。
17.(11分)Ⅰ.自从英国化学家巴特列(N.Bartlett)首次合成了第一个稀有气体的化合物XePtF 以来,人们又相
6
继发现了氙的一系列化合物,如XeF 、XeF 等。巴特列为开拓稀有气体化学作出了历史性贡献。
2 4
(1) 请 根 据 XeF 的 结 构 示 意 图 ( 图 1) 判 断 这 个 分 子 是 极 性 分 子 还 是 非 极 性 分 子 ?
4
___________________________。
(2)XeF 晶体是一种无色晶体,图 2 为它的晶胞结构图。XeF 晶体属于哪种类型的晶体?
2 2
_____________________。
Ⅱ.已知有关物质的熔、沸点数据如表:
物质 MgO Al O MgCl AlCl
2 3 2 3
熔点/℃ 2 800 2 072 714 190(2.6×105 Pa)
沸点/℃ 3 600 2 980 1 412 182.7
请参考上述数据填空和回答问题:
(1)工业上常用电解熔融MgCl 的方法生产金属镁,用电解Al O 与冰晶石熔融混合物的方法生产铝。为什
2 2 3
么不用电解MgO的方法生产镁,也不用电解AlCl 的方法生产铝_________________________。
3
(2) 设 计 可 靠 的 实 验 证 明 MgCl 、 AlCl 所 属 的 晶 体 类 型 , 其 实 验 方 法 是
2 3
______________________________________________。
18.(11分)不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,x越大,其原子吸引电子
的能力越强。下面是某些短周期元素的x值:
元素符号 Li Be B C O F Na Al Si P S Clx值 1.0 1.5 2.0 2.5 3.5 4.0 0.9 1.5 1.8 2.1 2.5 3.0
(1)推测x值与原子半径的关系是_________;
根据短周期元素的x值变化特点,体现了元素性质的________变化规律。
(2)分别指出下列两种化合物中氧元素的化合价:HClO________,HFO________。
(3)经验规律告诉我们:成键的两原子相应元素x数值的差值为Δx,当Δx>1.7时,一般为离子键,当Δx<
1.7时,一般为共价键,试推断AlBr 中化学键类型是________。
3
(4)预测元素周期表中,x值最小的元素位于第______周期第________族(放射性元素除外)。
19.(11分)不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要
的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO 以防止腐蚀。
3
(1)基态碳(C)原子的轨道表示式为____________________。
(2)[Cr(H O) Cl]Cl·2HO中Cr的配位数为________。
2 4 2 2
(3)与铜属于同一周期,且未成对价电子数最多的元素基态原子价电子排布式为________。
(4)Fe的一种晶胞结构如甲、乙所示,若按甲中虚线方向切乙得到的A~D图中正确的是________。
(5)据报道,只含镁、镍和碳三种元素的晶体具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关
注。该晶体的晶胞结构如图所示,试写出该晶体的化学式:__________________________。
晶体中每个镁原子周围距离最近的镍原子有______个。
(6)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列问题:
元素代号 I I I I
1 2 3 4
Q 2 080 4 000 6 100 9 400
R 500 4 600 6 900 9 500
S 740 1 500 7 700 10 500
T 580 1 800 2 700 11 600U 420 3 100 4 400 5 900
T元素最可能是________区元素。若T为第2周期元素,F是第3周期元素中原子半径最小的元素,则T、
F形成的化合物的立体构型为________,其中心原子的杂化方式为________。
20.(12分)CdSnAs 是一种高迁移率的新型热电材料,回答下列问题:
2
(1)Sn为ⅣA族元素,单质Sn与干燥Cl 反应生成SnCl 。常温常压下SnCl 为无色液体,SnCl 空间构型为
2 4 4 4
________________________,其固体的晶体类型为__________________________。
(2)NH 、PH 、AsH 的沸点由高到低的顺序为___________________(填化学式,下同),还原性由强到弱的
3 3 3
顺序为______________________,键角由大到小的顺序为__________________________。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
Cd2+配合物的结构如图所示,1 mol该配合物中通过螯合作用形成的配位键有______________mol,该螯合
物中N的杂化方式有____________________种。
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系
CdSnAs 的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
2
坐标
x y z
原子
Cd 0 0 0
Sn 0 0 0.5
As 0.25 0.25 0.125
一个晶胞中有__________个Sn,找出距离Cd(0,0,0)最近的Sn________(用分数坐标表示)。CdSnAs 晶
2
体中与单个Sn键合的As有__________________个。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育