文档内容
2021-2022 学年高二化学重难点专题突破
模块二 分子结构与性质
综合测试
(75分钟 100分)
一、选择题(本题共15小题,每小题3分,共45分。)
1.下列关于离子键、共价键的各种叙述中错误的是( )
A.在离子化合物里,一定存在离子键,可能存在共价键
B.非极性键只存在于双原子的单质分子中
C.在共价化合物分子内,一定不存在离子键
D.由不同元素组成的多原子分子里,可能存在非极性键
【答案】选B。
【解析】含有离子键的化合物为离子化合物,则离子化合物一定存在离子键,也可能存在共价键,如
NaOH为离子化合物,既含有离子键也含有共价键,故A正确;相同非金属元素之间可以形成非极性键,
非极性键可以存在于双原子的单质分子中,如氯气,也可以存在于一些化合物中,如过氧化氢,故 B错误,
D正确;只含有共价键的化合物为共价化合物,含有离子键的化合物为离子化合物,则在共价化合物分子
内,一定不存在离子键,故C正确。
2.下列分子中,属于含极性键的非极性分子的是( )
A.SO B.HO C.BBr D.COCl
2 2 2 3 2
【答案】选C。
【解析】SO 分子中中心原子上的孤电子对数==1,空间构型为角形,属于极性分子;HO 分子中既有非
2 2 2
极性键,又有极性键,是极性分子;COCl 为极性分子。
2
3.人们从未停止对生命起源的研究和探讨,曾经有研究表明生命起源于火山爆发,是因为火山爆发产生
的气体中含有1%的羰基硫(OCS)。已知羰基硫中所有原子均满足8电子稳定结构。下列有关羰基硫的说法
正确的是( )
A.属于非极性分子
B.沸点低于CO
2
C.C原子是sp2杂化
D.三个原子位于同一直线上【答案】选D。
【解析】羰基硫分子可类比学过的CO 分子,其结构式是O==C==S,由于结构不对称,为极性分子,A错;
2
其相对分子质量大于CO 的相对分子质量,沸点应高于CO 的沸点,B错;碳原子形成两个双键,为sp杂
2 2
化,C错。
4.下列关于苯乙炔的说法错误的是( )
A.该分子有8个σ键,5个π键
B.该分子中碳原子有sp和sp2杂化
C.该分子存在非极性键
D.该分子中有8个碳原子在同一平面上
【答案】选A。
【解析】 苯乙炔分子中含14个σ键,碳原子之间形成8个σ键,碳原子与氢原子形
成6个σ键,碳碳三键中含有两个π键,同时苯环中六个碳原子还会形成1个大π键,含3个π键,故A
错误;分子中苯环中碳碳键是介于单双键之间的特殊化学键,碳原子都是sp2杂化,碳碳三键中是sp杂化
该分子中碳原子有sp和sp2杂化,故B正确;同种原子间形成的共价键为非极性键,碳碳键为非极性键,
故C正确;分子中所有碳原子在同一平面上,故D正确。
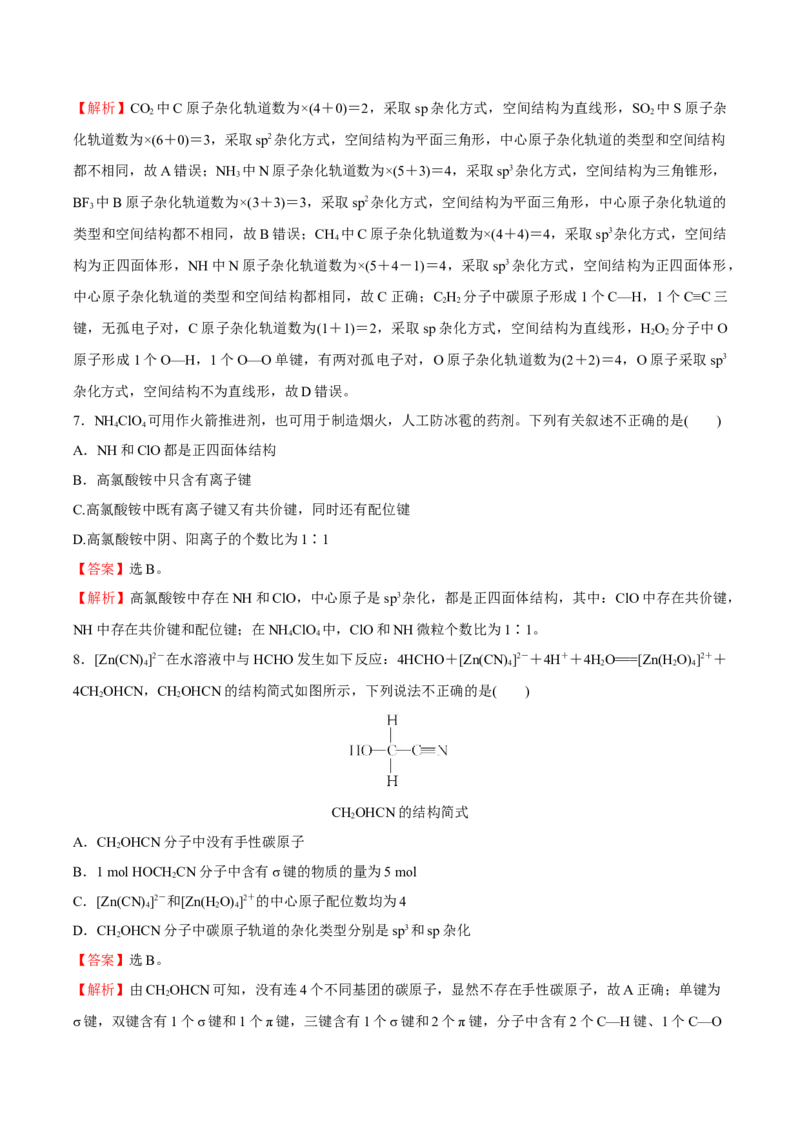
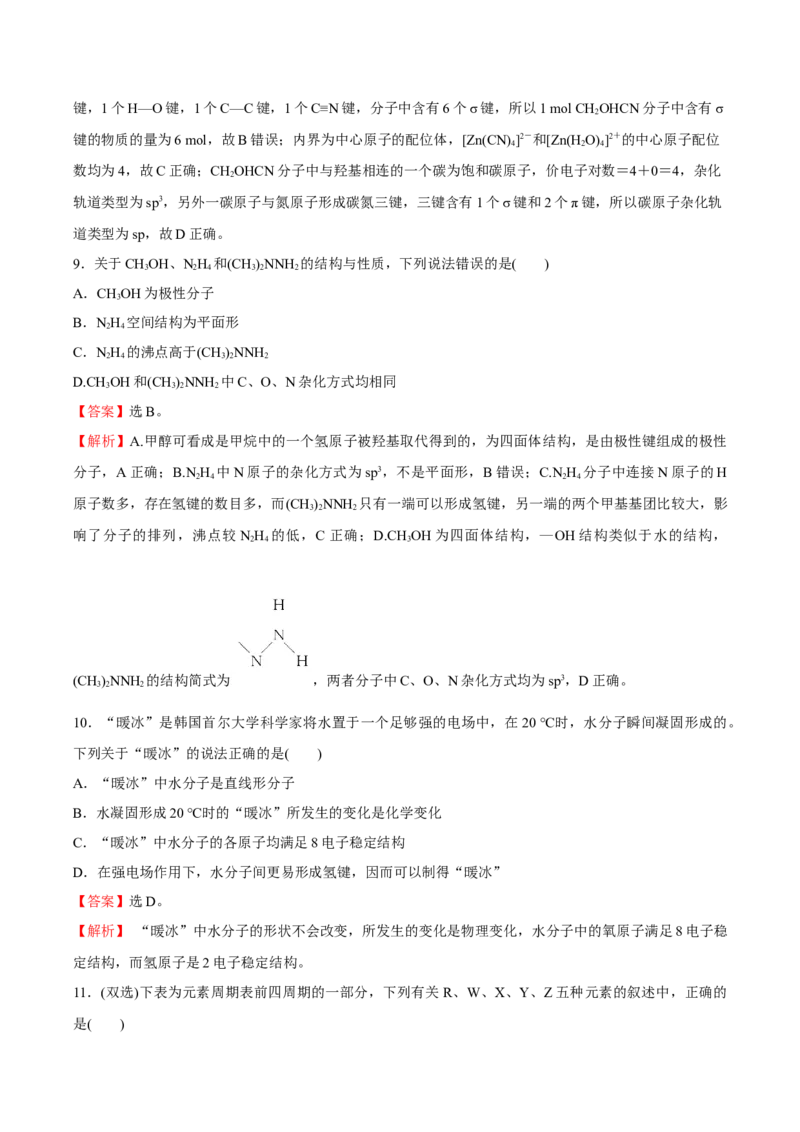
5.卤族元素包括F、Cl、Br等。下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是( )
【答案】选A。
【解析】B项,F无正价;C项,沸点:HF>HBr>HCl;D项,熔点:Br >Cl>F 。
2 2 2
6.下列各组微粒中,中心原子杂化类型和微粒空间结构都相同的是( )
A.CO 与SO B.NH 与BF
2 2 3 3
C.CH 与NH D.C H 与HO
4 2 2 2 2
【答案】选C。【解析】CO 中C原子杂化轨道数为×(4+0)=2,采取sp杂化方式,空间结构为直线形,SO 中S原子杂
2 2
化轨道数为×(6+0)=3,采取sp2杂化方式,空间结构为平面三角形,中心原子杂化轨道的类型和空间结构
都不相同,故A错误;NH 中N原子杂化轨道数为×(5+3)=4,采取sp3杂化方式,空间结构为三角锥形,
3
BF 中B原子杂化轨道数为×(3+3)=3,采取sp2杂化方式,空间结构为平面三角形,中心原子杂化轨道的
3
类型和空间结构都不相同,故B错误;CH 中C原子杂化轨道数为×(4+4)=4,采取sp3杂化方式,空间结
4
构为正四面体形,NH中N原子杂化轨道数为×(5+4-1)=4,采取sp3杂化方式,空间结构为正四面体形,
中心原子杂化轨道的类型和空间结构都相同,故C正确;C H 分子中碳原子形成1个C—H,1个C≡C三
2 2
键,无孤电子对,C原子杂化轨道数为(1+1)=2,采取sp杂化方式,空间结构为直线形,HO 分子中O
2 2
原子形成1个O—H,1个O—O单键,有两对孤电子对,O原子杂化轨道数为(2+2)=4,O原子采取sp3
杂化方式,空间结构不为直线形,故D错误。
7.NH ClO 可用作火箭推进剂,也可用于制造烟火,人工防冰雹的药剂。下列有关叙述不正确的是( )
4 4
A.NH和ClO都是正四面体结构
B.高氯酸铵中只含有离子键
C.高氯酸铵中既有离子键又有共价键,同时还有配位键
D.高氯酸铵中阴、阳离子的个数比为1∶1
【答案】选B。
【解析】高氯酸铵中存在NH和ClO,中心原子是sp3杂化,都是正四面体结构,其中:ClO中存在共价键,
NH中存在共价键和配位键;在NH ClO 中,ClO和NH微粒个数比为1∶1。
4 4
8.[Zn(CN) ]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN) ]2-+4H++4HO===[Zn(H O) ]2++
4 4 2 2 4
4CHOHCN,CHOHCN的结构简式如图所示,下列说法不正确的是( )
2 2
CHOHCN的结构简式
2
A.CHOHCN分子中没有手性碳原子
2
B.1 mol HOCHCN分子中含有σ键的物质的量为5 mol
2
C.[Zn(CN) ]2-和[Zn(HO) ]2+的中心原子配位数均为4
4 2 4
D.CHOHCN分子中碳原子轨道的杂化类型分别是sp3和sp杂化
2
【答案】选B。
【解析】由CHOHCN可知,没有连4个不同基团的碳原子,显然不存在手性碳原子,故A正确;单键为
2
σ键,双键含有1个σ键和1个π键,三键含有1个σ键和2个π键,分子中含有2个C—H键、1个C—O键,1个H—O键,1个C—C键,1个C≡N键,分子中含有6个σ键,所以1 mol CH OHCN分子中含有σ
2
键的物质的量为6 mol,故B错误;内界为中心原子的配位体,[Zn(CN) ]2-和[Zn(HO) ]2+的中心原子配位
4 2 4
数均为4,故C正确;CHOHCN分子中与羟基相连的一个碳为饱和碳原子,价电子对数=4+0=4,杂化
2
轨道类型为sp3,另外一碳原子与氮原子形成碳氮三键,三键含有1个σ键和2个π键,所以碳原子杂化轨
道类型为sp,故D正确。
9.关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错误的是( )
3 2 4 3 2 2
A.CHOH为极性分子
3
B.NH 空间结构为平面形
2 4
C.NH 的沸点高于(CH)NNH
2 4 3 2 2
D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
3 3 2 2
【答案】选B。
【解析】A.甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,为四面体结构,是由极性键组成的极性
分子,A正确;B.N H 中N原子的杂化方式为sp3,不是平面形,B错误;C.N H 分子中连接N原子的H
2 4 2 4
原子数多,存在氢键的数目多,而(CH)NNH 只有一端可以形成氢键,另一端的两个甲基基团比较大,影
3 2 2
响了分子的排列,沸点较 NH 的低,C正确;D.CHOH为四面体结构,—OH结构类似于水的结构,
2 4 3
(CH)NNH 的结构简式为 ,两者分子中C、O、N杂化方式均为sp3,D正确。
3 2 2
10.“暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20 ℃时,水分子瞬间凝固形成的。
下列关于“暖冰”的说法正确的是( )
A.“暖冰”中水分子是直线形分子
B.水凝固形成20 ℃时的“暖冰”所发生的变化是化学变化
C.“暖冰”中水分子的各原子均满足8电子稳定结构
D.在强电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
【答案】选D。
【解析】 “暖冰”中水分子的形状不会改变,所发生的变化是物理变化,水分子中的氧原子满足8电子稳
定结构,而氢原子是2电子稳定结构。
11.(双选)下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的
是( )A.W、R元素单质分子内的化学键都是非极性键
B.X、Z元素都能够形成双原子分子
C.键能:W—HW—H
D.键长:X—HS,键长:P—H>S—
2 2
H,键能:P—HP,键的极性:H—S>P—H,C项正确;键长越长,键能越小,D
项不正确。
12.下列说法错误的是( )
A.O 与SO 的结构相似
3 2
B.硫粉不溶于水,易溶于CS 中
2
C.N≡C—C≡N分子中含有3个σ键和4个π键
D.C 是含有非极性键的极性分子
60
【答案】选D。
【解析】A项,O 与SO 互为等电子体,结构相似;B项,硫为非极性分子,易溶于CS;C项,一个碳氮
3 2 2
三键中包含1个σ键和2个π键,所以该分子中含有3个σ键和4个π键;D项,C 是碳原子之间通过非
60
极性键结合的具有严格对称性的分子,整个分子电荷的分布是均匀的。
13.(双选)下列分子均属于极性分子且中心原子均为sp3杂化的是( )
A.NH 、HO B.SO 、SCl
3 2 2 2
C.PCl 、SO D.CHF 、HO
3 3 3 2 2
【答案】选AD。
【解析】NH 中N原子形成3个σ键,有1个孤电子对,为sp3杂化,分子构型为三角锥形,空间结构不对
3
称为极性分子;HO中O原子形成2个σ键,有2个孤电子对,为sp3杂化,分子构型为角形,空间结构不
2
对称为极性分子,故A正确;SO 中S原子形成2个σ键,孤电子对数=×(6-2×2)=1,价层电子对数为
2
3,为sp2杂化,分子构型为角形,空间结构不对称为极性分子;SCl 中S原子形成2个σ键,孤电子对数
2
=×(6-2×1)=2,价层电子对数为4,为sp3杂化,分子构型为角形,空间结构不对称为极性分子,故 B错误;PCl 中P原子形成3个σ键,孤电子对数=×(5-3×1)=1,价层电子对数为4,为sp3杂化,分子构型
3
为三角锥形,空间结构不对称为极性分子;SO 中S原子形成3个σ键,孤电子对数=×(6-2×3)=0,价电
3
子对数为3,为sp2杂化,分子构型为平面三角形,空间结构对称为非极性分子,故 C错误;CHF 中C原
3
子形成4个σ键,孤电子对数为0,价层电子对数为4,为sp3杂化,分子构型为四面体形,空间结构不对
称为极性分子;HO 为极性分子,两个氧原子都是sp3杂化,故D正确。
2 2
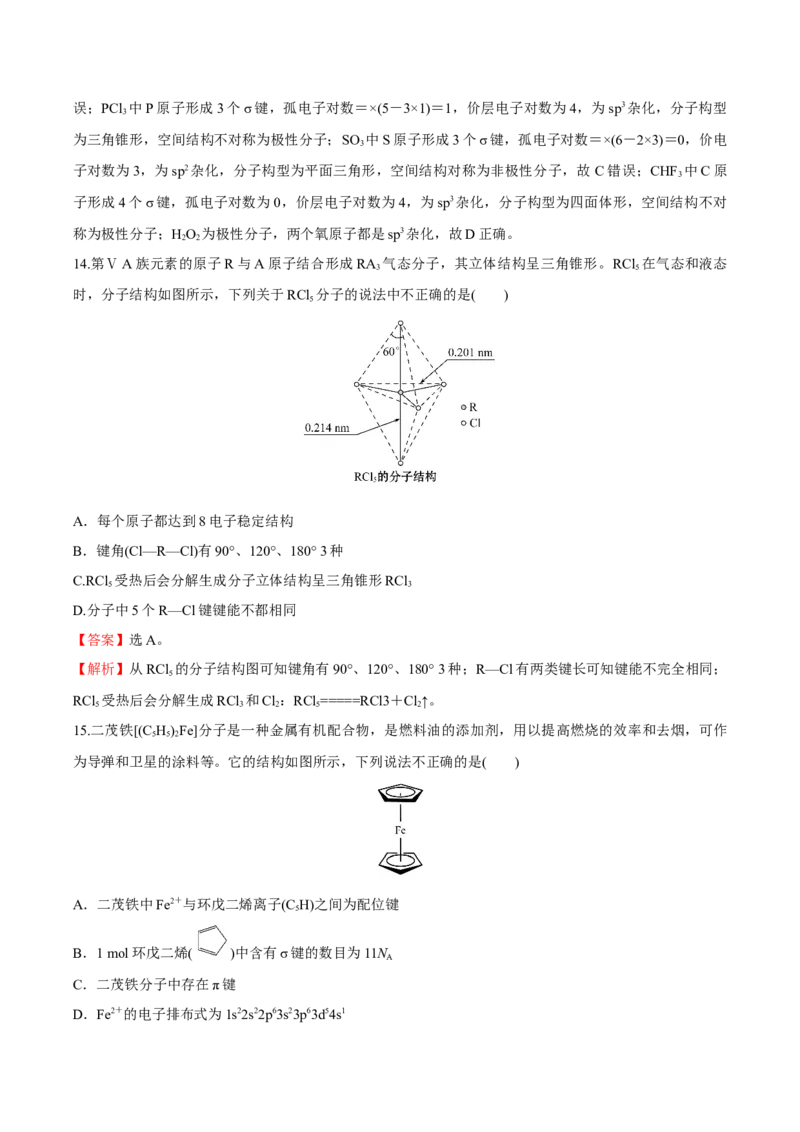
14.第ⅤA族元素的原子R与A原子结合形成RA 气态分子,其立体结构呈三角锥形。RCl 在气态和液态
3 5
时,分子结构如图所示,下列关于RCl 分子的说法中不正确的是( )
5
A.每个原子都达到8电子稳定结构
B.键角(Cl—R—Cl)有90°、120°、180° 3种
C.RCl 受热后会分解生成分子立体结构呈三角锥形RCl
5 3
D.分子中5个R—Cl键键能不都相同
【答案】选A。
【解析】从RCl 的分子结构图可知键角有90°、120°、180° 3种;R—Cl有两类键长可知键能不完全相同;
5
RCl 受热后会分解生成RCl 和Cl:RCl =====RCl3+Cl↑。
5 3 2 5 2
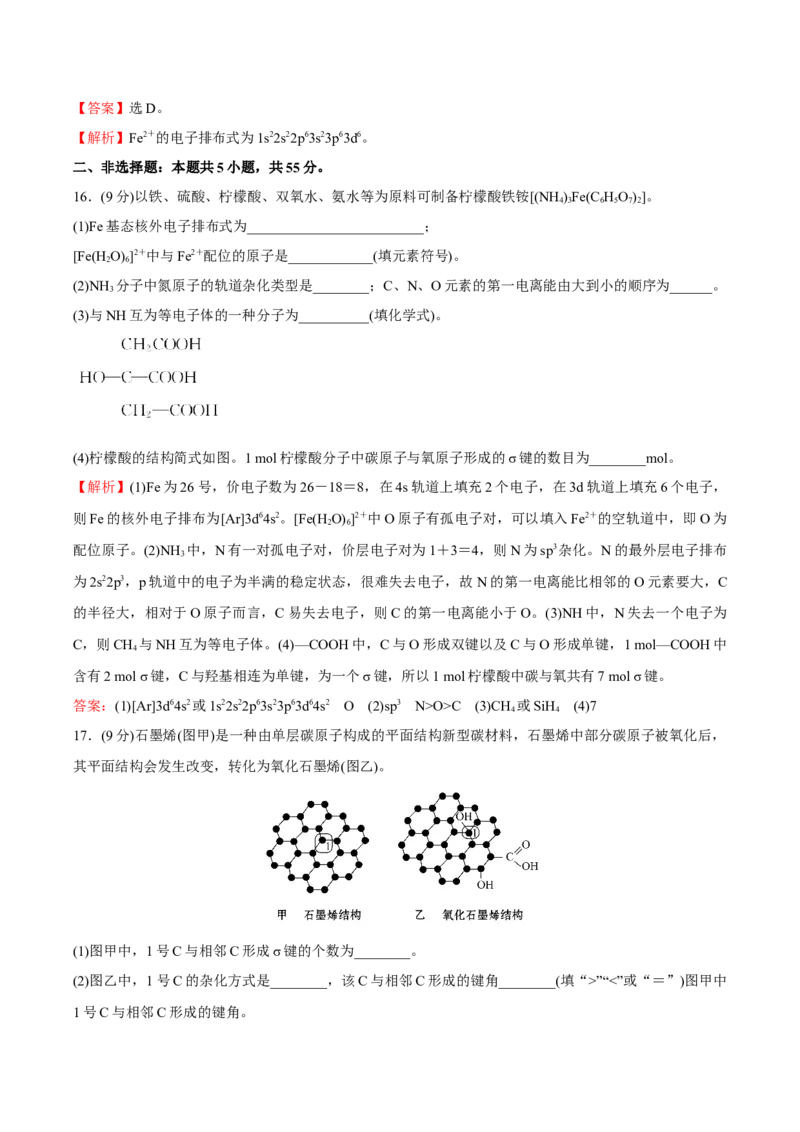
15.二茂铁[(C H)Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作
5 5 2
为导弹和卫星的涂料等。它的结构如图所示,下列说法不正确的是( )
A.二茂铁中Fe2+与环戊二烯离子(C H)之间为配位键
5
B.1 mol环戊二烯( )中含有σ键的数目为11N
A
C.二茂铁分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d54s1【答案】选D。
【解析】Fe2+的电子排布式为1s22s22p63s23p63d6。
二、非选择题:本题共5小题,共55分。
16.(9分)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵[(NH )Fe(C HO)]。
4 3 6 5 7 2
(1)Fe基态核外电子排布式为_________________________;
[Fe(H O) ]2+中与Fe2+配位的原子是____________(填元素符号)。
2 6
(2)NH 分子中氮原子的轨道杂化类型是________;C、N、O元素的第一电离能由大到小的顺序为______。
3
(3)与NH互为等电子体的一种分子为__________(填化学式)。
(4)柠檬酸的结构简式如图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为________mol。
【解析】(1)Fe为26号,价电子数为26-18=8,在4s轨道上填充2个电子,在3d轨道上填充6个电子,
则Fe的核外电子排布为[Ar]3d64s2。[Fe(H O) ]2+中O原子有孤电子对,可以填入Fe2+的空轨道中,即O为
2 6
配位原子。(2)NH 中,N有一对孤电子对,价层电子对为1+3=4,则N为sp3杂化。N的最外层电子排布
3
为2s22p3,p轨道中的电子为半满的稳定状态,很难失去电子,故N的第一电离能比相邻的O元素要大,C
的半径大,相对于O原子而言,C易失去电子,则C的第一电离能小于O。(3)NH中,N失去一个电子为
C,则CH 与NH互为等电子体。(4)—COOH中,C与O形成双键以及C与O形成单键,1 mol—COOH中
4
含有2 mol σ键,C与羟基相连为单键,为一个σ键,所以1 mol柠檬酸中碳与氧共有7 mol σ键。
答案:(1)[Ar]3d64s2或1s22s22p63s23p63d64s2 O (2)sp3 N>O>C (3)CH 或SiH (4)7
4 4
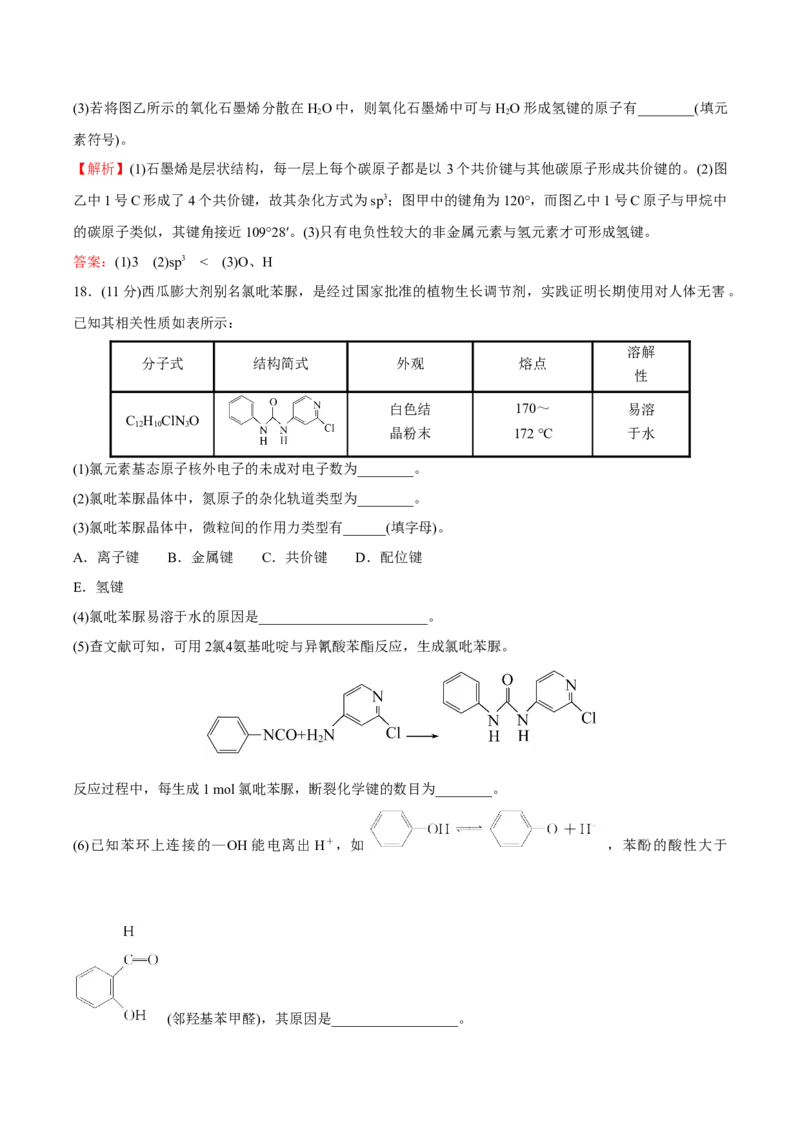
17.(9分)石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,
其平面结构会发生改变,转化为氧化石墨烯(图乙)。
(1)图甲中,1号C与相邻C形成σ键的个数为________。
(2)图乙中,1号C的杂化方式是________,该C与相邻C形成的键角________(填“>”“<”或“=”)图甲中
1号C与相邻C形成的键角。(3)若将图乙所示的氧化石墨烯分散在HO中,则氧化石墨烯中可与HO形成氢键的原子有________(填元
2 2
素符号)。
【解析】(1)石墨烯是层状结构,每一层上每个碳原子都是以3个共价键与其他碳原子形成共价键的。(2)图
乙中1号C形成了4个共价键,故其杂化方式为sp3;图甲中的键角为120°,而图乙中1号C原子与甲烷中
的碳原子类似,其键角接近109°28′。(3)只有电负性较大的非金属元素与氢元素才可形成氢键。
答案:(1)3 (2)sp3 < (3)O、H
18.(11分)西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。
已知其相关性质如表所示:
溶解
分子式 结构简式 外观 熔点
性
白色结 170~ 易溶
C H ClN O
12 10 3
晶粉末 172 ℃ 于水
(1)氯元素基态原子核外电子的未成对电子数为________。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为________。
(3)氯吡苯脲晶体中,微粒间的作用力类型有______(填字母)。
A.离子键 B.金属键 C.共价键 D.配位键
E.氢键
(4)氯吡苯脲易溶于水的原因是________________________。
(5)查文献可知,可用2氯4氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。
反应过程中,每生成1 mol氯吡苯脲,断裂化学键的数目为________。
(6)已知苯环上连接的—OH能电离出H+,如 ,苯酚的酸性大于
(邻羟基苯甲醛),其原因是__________________。【解析】(1)根据构造原理可知,氯元素基态原子的核外电子排布式是1s22s22p63s23p5,所以未成对电子数
为1。(2)根据氯吡苯脲的结构简式可知,有 2个氮原子各形成3个单键,且它们各有1对孤电子对,故属
于sp3杂化。另外1个氮原子形成双键和单键,孤电子对数为1,属于sp2杂化。(3)氯吡苯脲分子为共价化
合物,故微粒间存在共价键。由于氯吡苯脲分子中含亚氨基(—NH—),故微粒间(分子间)能形成氢键。(4)
氯吡苯脲能与水分子形成氢键,所以易溶于水。(5)由于单键都是σ键、而双键是由1个σ键和1个π键构
成的,所以根据反应方程式可知,每生成1 mol氯吡苯脲,断裂N 个N—H σ键和N 个C==N键中的π键。
A A
(6)邻羟基苯甲醛分子中醛基与羟基处于邻位,容易形成分子内氢键,导致羟基上的氢原子难以电离。
答案:(1)1 (2)sp2、sp3 (3)CE (4)氯吡苯脲可以与水分子形成氢键 (5)2N (6)邻羟基苯甲醛会形成分
A
子内氢键,使得羟基上的氢原子难以电离
19.(11分)过渡元素在生活、生产和科技等方面有广泛的用途。
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排
布时,无颜色;为d1~d9排布时,有颜色,如[Co(H O) ]2+显粉红色,据此判断,[Mn(H O) ]2+________(填
2 6 2 6
“有”或“无”)颜色。
(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe (OH) (SO ) m,n<5,m<10}在水体中形
2 n 4 3-]
成絮状物,以吸附重金属离子。下列说法中不正确的是________(填字母)。
A.PFS中铁显+3价
B.铁原子的价电子排布式为3d64s2
C.由FeSO 溶液制PFS需经过氧化、水解和聚合的过程
4
D.PFS中配体只有OH-
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬(Ⅲ)与甲基
丙烯酸根的配合物如下:
①该化合物中存在的化学键类型有____________。
②该化合物中一个Cr的配位数为________。
③甲基丙烯酸分子中C原子的杂化方式为_____________________。
④等电子体是具有相同的价电子数和原子数的分子或离子,与 HO分子互为等电子体的微粒是______(填
2
一种即可)。
⑤与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是________(填元素符号)。
【解析】(1)Mn2+的3d轨道上有5个电子,由题中信息知[Mn(H O) ]2+有颜色。(2)PFS中配体为OH-、
2 6SO。(3)①化合物中的两个Cr(Ⅲ),根据铬的配合物结构可知,该配合物中存在配位键、共价键、离子键。
②2个Cr共有12个配体,则一个Cr的配位数为6。③形成单键时,C原子以sp3形式杂化;形成双键时,
C原子以sp2形式杂化。④利用同族元素互换法,将HO中的O换为S可得HS;利用电子电荷互换法,将
2 2
HO中的O换为N,同时将一个电子转化为一个负电荷,可得 NH。⑤基态铬原子的最外层电子排布式是
2
4s1,3d轨道比4s轨道能量高,当3d轨道全空(K)、半满(Cr)、全满(Cu)时,原子结构稳定。
答案:(1)有 (2)D (3)①配位键、共价键、离子键 ②6 ③sp3和sp2 ④HS(或NH) ⑤K、Cu
2
20.(15分)物质的物理性质与化学键、分子间作用力有密切关系。请回答下列问题:
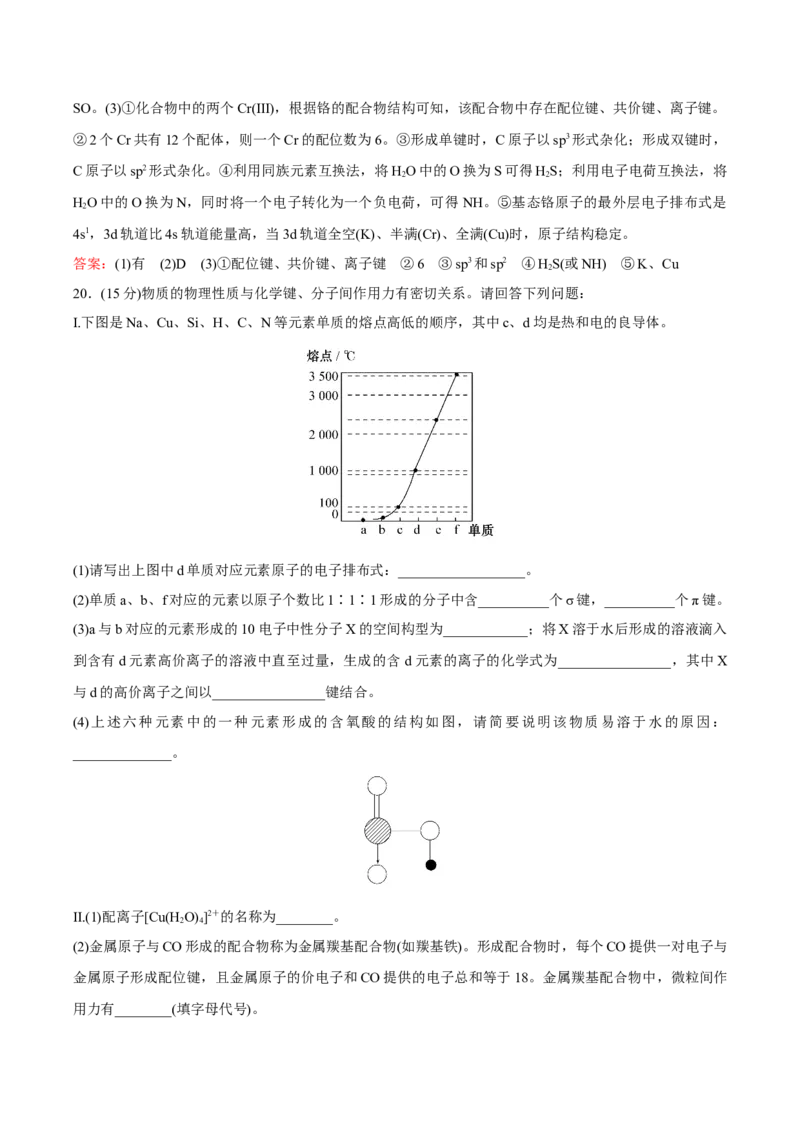
Ⅰ.下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。
(1)请写出上图中d单质对应元素原子的电子排布式:__________________。
(2)单质a、b、f对应的元素以原子个数比1∶1∶1形成的分子中含__________个σ键,__________个π键。
(3)a与b对应的元素形成的10电子中性分子X的空间构型为____________;将X溶于水后形成的溶液滴入
到含有d元素高价离子的溶液中直至过量,生成的含 d元素的离子的化学式为________________,其中X
与d的高价离子之间以________________键结合。
(4)上述六种元素中的一种元素形成的含氧酸的结构如图,请简要说明该物质易溶于水的原因:
______________。
Ⅱ.(1)配离子[Cu(H O) ]2+的名称为________。
2 4
(2)金属原子与CO形成的配合物称为金属羰基配合物(如羰基铁)。形成配合物时,每个CO提供一对电子与
金属原子形成配位键,且金属原子的价电子和CO提供的电子总和等于18。金属羰基配合物中,微粒间作
用力有________(填字母代号)。A.离子键 B.共价键 C.配位键 D.金属键
羰基铁是一种黄色油状液体,熔点-21 ℃、沸点102.8 ℃。由此推测,固体羰基铁更接近于________(填晶
体类型)。若用Fe(CO) 表示羰基铁的化学式,则x=________。
x
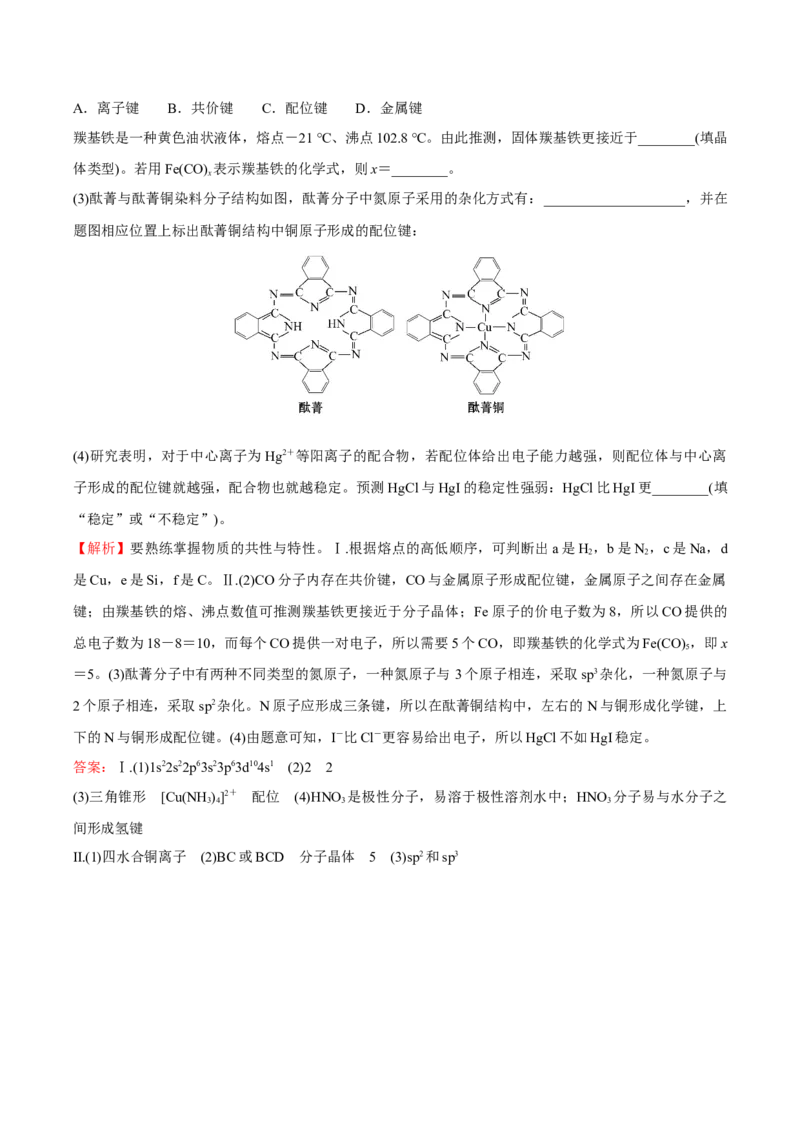
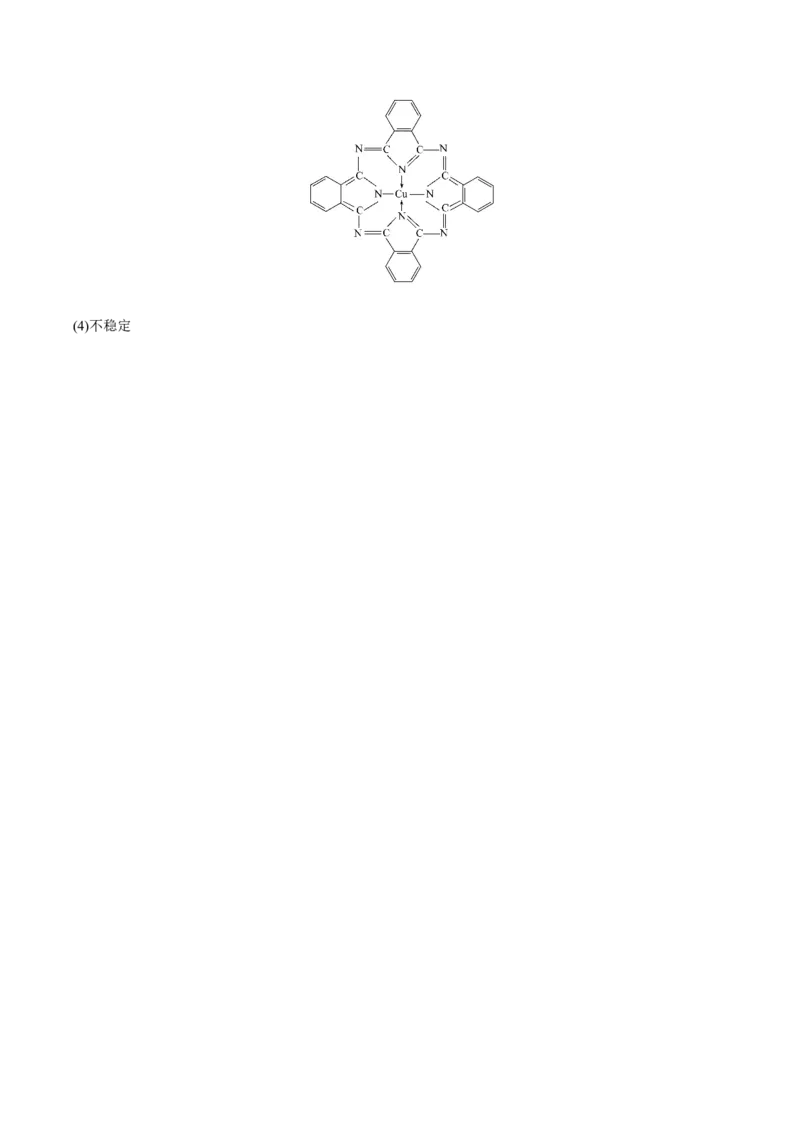
(3)酞菁与酞菁铜染料分子结构如图,酞菁分子中氮原子采用的杂化方式有:____________________,并在
题图相应位置上标出酞菁铜结构中铜原子形成的配位键:
(4)研究表明,对于中心离子为Hg2+等阳离子的配合物,若配位体给出电子能力越强,则配位体与中心离
子形成的配位键就越强,配合物也就越稳定。预测HgCl与HgI的稳定性强弱:HgCl比HgI更________(填
“稳定”或“不稳定”)。
【解析】要熟练掌握物质的共性与特性。Ⅰ.根据熔点的高低顺序,可判断出a是H ,b是N ,c是Na,d
2 2
是Cu,e是Si,f是C。Ⅱ.(2)CO分子内存在共价键,CO与金属原子形成配位键,金属原子之间存在金属
键;由羰基铁的熔、沸点数值可推测羰基铁更接近于分子晶体;Fe原子的价电子数为8,所以CO提供的
总电子数为18-8=10,而每个CO提供一对电子,所以需要5个CO,即羰基铁的化学式为Fe(CO) ,即x
5
=5。(3)酞菁分子中有两种不同类型的氮原子,一种氮原子与 3个原子相连,采取sp3杂化,一种氮原子与
2个原子相连,采取sp2杂化。N原子应形成三条键,所以在酞菁铜结构中,左右的 N与铜形成化学键,上
下的N与铜形成配位键。(4)由题意可知,I-比Cl-更容易给出电子,所以HgCl不如HgI稳定。
答案:Ⅰ.(1)1s22s22p63s23p63d104s1 (2)2 2
(3)三角锥形 [Cu(NH )]2+ 配位 (4)HNO 是极性分子,易溶于极性溶剂水中;HNO 分子易与水分子之
3 4 3 3
间形成氢键
Ⅱ.(1)四水合铜离子 (2)BC或BCD 分子晶体 5 (3)sp2和sp3(4)不稳定倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育