文档内容
2019-2020 年高一化学高频考题期末组合模拟卷 02
(考试时间:90分钟 试卷满分:100分)
考试内容:必修二 难度:★★★☆☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列装置工作时,将化学能转化为电能的是
A B C D
燃气灶 碱性锌锰电池 硅太阳能电池 风力发电机
【答案】B
【解析】A.燃气灶将化学能转化为热能,选项A不选;
B.碱性锌锰电池将化学能转化为电能,选项B可选;
C.硅太阳能电池将太阳能转化为电能,选项C不选;
D.风力发电机将风能转化为电能,选项D不选。故选B。
2.物质类别和核心元素的价态是学习元素及其化合物性质的重要认识视角。如图是某元素的“价类二维
图”,其中单质b是黄色固体,f、h均为正盐,且焰色都是黄色。下列说法不正确的是
A.d能使品红溶液褪色 B.a和c反应可以生成b
C.e的浓溶液可用铝槽车运输 D.h的水溶液呈碱性
【答案】A
【解析】单质b是黄色固体,则b是S元素,故该“价类二维图”是S元素的,f、h均为正盐,且焰色都是黄色,则f为NaSO ,h为NaSO ,故a为HS、b为S、c为SO 、d为SO ,e为HSO ,g为HSO ,
2 4 2 3 2 2 3 2 4 2 3
f为NaSO ,h为NaSO 。
2 4 2 3
A.由分析可知,d为SO ,因为SO 具有漂白性,才会使品红溶液褪色,非SO ,A错误;
3 2 3
B..a为HS、c为SO ,两者反应方程式为:2HS+SO=2S↓+2H O,有S生成即为b,B正确;
2 2 2 2 2
C.e为HSO ,浓硫酸与铝槽常温下发生钝化反应,可用铝槽车运输,C正确;
2 4
D.h为NaSO ,为强碱弱酸盐,亚硫酸根发生水解,SO 2-+HO HSO 2-+OH-,溶液呈碱性,D
2 3 3 2 3
正确;答案选A。
3.下列关于浓HNO 与浓HSO 的叙述正确的是
3 2 4
A.常温下遇铁都发生钝化 B.常温下都能与铜反应产生氢气
C.露置于空气中,溶液质量均不变 D.露置于空气中,溶液浓度均不变
【答案】A
【解析】A.常温下,Fe在浓硝酸、浓硫酸中发生钝化现象,A正确;
B.铜与浓硫酸反应需要加热,铜常温下能溶解于浓硝酸,但均不生成氢气,B错误;
C.露置于空气中,浓硝酸挥发导致溶液质量减小,浓硫酸具有吸水性,溶液质量会增大,C错误;
D.露置于空气中,浓硝酸因为挥发性使得溶质质量减少,浓硫酸因吸水使得溶剂质量增加,溶液浓度均
降低,D错误;答案选A。
4.下列各组物质相互反应时,若改变反应物的用量、条件或浓度,不会引起产物改变的是
A.N 和O B.Na和O C.Cu和HNO 溶液 D.CO 和Ca(OH) 溶液
2 2 2 3 2 2
【答案】A
【解析】A.N 和O 在放电的条件下反应生成NO,只有一种产物,反应物的用量、条件或浓度改变,不
2 2
会引起产物改变,A符合题意;
B.Na和O 反应条件不同,产物不同,常温下生成NaO,点燃生成NaO,B不符合题意;
2 2 2 2
C.Cu和HNO 溶液反应,硝酸的浓度不同,产物不同,Cu和稀HNO 反应生成硝酸铜、一氧化氮和水,
3 3
Cu和浓HNO 反应生成硝酸铜、二氧化氮和水,C不符合题意;
3
D.CO 和Ca(OH) 反应,CO 量不同,产物不同,CO 不足时生成CaCO ,CO 过量时生成Ca(HCO ),
2 2 2 2 3 2 3 2
D不符合题意;答案选A。
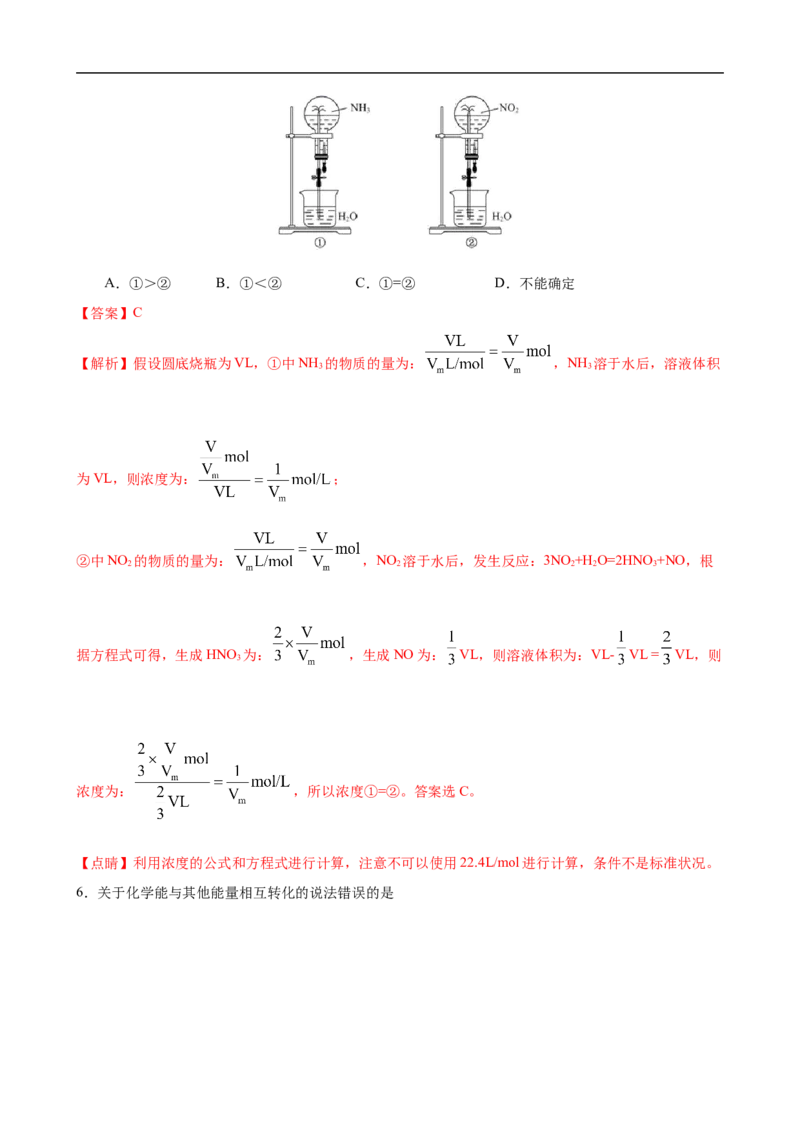
5.如图,同温同压下,两个等体积的干燥圆底烧瓶中分别充满:①NH 、②NO ,进行喷泉实验。经充
3 2
分反应后,瓶内溶质的物质的量浓度为(不考虑瓶内溶液向烧杯中扩散)A.①>② B.①<② C.①=② D.不能确定
【答案】C
【解析】假设圆底烧瓶为VL,①中NH 的物质的量为: ,NH 溶于水后,溶液体积
3 3
为VL,则浓度为: ;
②中NO 的物质的量为: ,NO 溶于水后,发生反应:3NO +H O=2HNO +NO,根
2 2 2 2 3
据方程式可得,生成HNO 为: ,生成NO为: VL,则溶液体积为:VL- VL = VL,则
3
浓度为: ,所以浓度①=②。答案选C。
【点睛】利用浓度的公式和方程式进行计算,注意不可以使用22.4L/mol进行计算,条件不是标准状况。
6.关于化学能与其他能量相互转化的说法错误的是A.图1所示的装置能将化学能转变为电能
B.图2所示的反应为放热反应
C.中和反应中,生成物的总能量比反应物的总能量低
D.化学反应中能量变化的主要原因是化学键的断裂与形成
【答案】A
【解析】A.图1所示的装置没形成闭合回路,不能形成原电池,没有电流通过,所以不能把化学能转变
为电能,故A错误;
B.图2所示的反应,反应物的总能量大于生成物的总能量,所以该反应为放热反应,故B正确;
C.中和反应为放热反应,生成物的总能量比反应物的总能量低,故C正确;
D.化学反应时断键要吸收能量,成键要放出能量,所以化学反应中能量变化的主要原因是化学键的断裂
与生成,故D正确;故选A。
7.下列关于化学反应与能量的说法正确的是
A.中和反应是放热反应 B.H 燃烧时的能量变化如图所示
2
C.化学键断裂放出能量 D.反应物总能量与生成物总能量一定相等
【答案】A
【解析】A.中和反应是放热反应,A正确;
B.氢气燃烧反应是放热反应,而图示物质反应物的能量低于生成物的能量,显示反应是吸热反应,与事
实不符合,B错误;
C.化学键断裂吸收能量,C错误;
D.反应物总能量与生成物总能量一定不相等,因为反应一定会伴随能量变化,因此该说法错误,D错误。
故选A。
8.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
【答案】C
【解析】A.甲是原电池,正极铜片上发生还原反应 2H++2e-=H↑,铜片上有气体产生,乙装置中在锌
2
片上发生反应 Zn+2H+=Zn2++H ↑,铜片上无气体产生,故A错误;
2
B.甲装置是原电池,铜片做正极,乙不是原电池,故B错误;
C.两烧杯中的氢离子发生反应,浓度减少,溶液pH增大,故C正确;
D.原电池反应加快反应速率,故产生气泡的速度甲比乙快,故D错误;
故选C。
【点睛】考查原电池的工作原理、氧化还原反应的实质。原电池的组成条件是活泼性不同的两个电极、
电解质溶液、闭合回路、自发进行的氧化还原反应。装置甲是原电池,锌做负极,铜做正极,气体在铜
片上产生。原电池由于在两个电极上发生氧化反应和还原反应,加快了反应速率。乙不是原电池,乙装
置是锌与稀硫酸直接接触的反应,铜不与稀硫酸反应,气体在锌片上产生。甲和乙相比,相同点:发生
的氧化还原反应原理相同,都消耗H+,反应后溶液pH都增大;不同点:一、气体产生的位置不同,二、
反应速率不同,三、能量转化不同。
9.等质量的两份锌粉a、b,分别加入过量的稀硫酸,同时向a中加入少量的CuSO 溶液,如图表示产生
4
H 的体积(V)与时间(t)的关系,其中正确的是
2
A. B. C. D.
【答案】A
【解析】等质量的两份锌粉a、b,分别加入过量的稀硫酸,向a中加入少量的CuSO 溶液,锌粉与
4
CuSO 发生反应,Zn+Cu2+=Cu+Zn2+,形成铜锌原电池,加快了反应速率,但反应消耗了锌粉,故反应结
4
束后生成的氢气的体积小于b中生成氢气的体积,则选项A的图像符合题意;
故选A。
10.在一个密闭容器中发生反应:2SO (g)+O(g) 2SO (g)。已知反应过程中的某一时间SO 、O 和SO
2 2 3 2 2 3
的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是A.c(O )=0.2mol/L B.c(SO )=0.25mol/L
2 2
C.c(SO )=0.4mol/L D.c(SO )=c(SO )=0.15mol/L
3 2 3
【答案】B
【解析】可逆反应有一定的限度,反应物不能完全转化为生成物,反应过程中的某一时间SO 、O 和SO
2 2 3
的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L,若极限转化,则SO 、O 和SO 的浓度分别为:
2 2 3
0.4mol/L、0.2mol/L和0mol/L或0mol/L、0mol/L和0.4mol/L。
【详解】A.极限转化时c(O )=0.2mol/L,但可逆反应不能完全转化,所以c(O )<0.2mol/L,故A错误;
2 2
B.根据分析可知0<c(SO )<0.4mol∙L-1 ,故B正确;
2
C.极限转化时c(SO )=0.4mol/L,但可逆反应不能完全转化,所以c(SO )<0.4mol/L,故C错误;
3 3
D.根据硫元素守恒,应有c(SO )+c(SO )=0.4mol•L-1,所以不可能出现c(SO )=c(SO )=0.15mol/L,故D
2 3 2 3
错误;故选B。
11.一定温度下,在恒容密闭容器中发生反应:HO(g)+CO(g) CO(g)+H(g)。当HO、CO、CO、H 的
2 2 2 2 2 2
浓度不再变化时,下列说法中,正确的是 ⇌
A.该反应已达化学平衡状态 B.正、逆反应速率相等且等于零
C.HO和CO全部转化为CO 和H D.HO、CO、CO、H 的浓度一定相等
2 2 2 2 2 2
【答案】A
【解析】A.当HO、CO、CO、H 的浓度不再变化时,是化学平衡状态的特征,说明正逆反应速率相等,
2 2 2
反应已达化学平衡状态,故A正确;
B.化学平衡状态是动态平衡,正、逆反应速率相等且大于零,故B错误;
C.可逆反应不可能完全反应,则HO和CO反应不可能全部转化为CO 和H,故C错误;
2 2 2
D.平衡状态时HO、CO、CO、H 的浓度不变,不一定相等,故D错误;
2 2 2
故选A。
12.下列关于常见有机物的说法正确的是
A.用酸性 溶液除去甲烷中的乙烯
B.石油分馏时,得到的产品均为纯净物
C.乙醇、水均能与钠反应,且现象相同
D.在加热条件下,葡萄糖能与含氢氧化钠的氢氧化铜悬浊液发生反应
【答案】D
【解析】A.乙烯与酸性 溶液反应时生成 ,引入新的杂质,A项错误;
B.石油分馏得到的产品均为混合物,B项错误;C.水与钠反应比乙醇与钠反应要剧烈得多,钠是浮在水面上,沉入乙醇底部,C项错误;
D.葡萄糖中含有醛基,在加热条件下,可以被新制氢氧化铜悬浊液氧化,D项正确;
故选D。
13.正确使用化肥和农药可以促进农业生产,下列说法正确的是( )
A.长期使用DDT不会导致残留污染 B.使用可溶性磷肥有利于植物对磷的吸收
C.(NH )SO 和草木灰混合使用肥料更佳 D.有机磷杀虫剂可降解,可以大量使用
4 2 4
【答案】B
【解析】A.DDT难降解,长期使用会残留,A错误;
B.磷肥分水溶性、弱酸溶性、难溶性,使用可溶性磷肥更利于植物吸收,B正确;
C.草木灰呈碱性,铵态氮肥与碱性物质反应能释放氨气,降低肥效,C错误;
D.大量使用有机磷杀虫剂可能导致人中毒,D错误;
答案选B。
14.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是
A.和金属钠反应时键①断裂
B.在铜催化共热下与O 反应时断裂①和③键
2
C.在铜催化共热下与O 反应时断裂①和⑤键
2
D.在空气中完全燃烧时断裂①②③④⑤键
【答案】C
【解析】A.乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;
B.乙醇催化氧化成乙醛时,断裂①和③化学键,B项正确,
C.乙醇催化氧化成乙醛时,断裂①和③化学键,C项错误;
D.乙醇完全燃烧时,化学键①②③④⑤全部断裂,D项正确;
故选C。
15.下列有机反应属于加成反应的是
A.CH=CH +Br CHBrCHBr
2 2 2 2 2
B.CHCHOH+O 2CO+3H O
3 2 2 2 2C. +HNO + H O
3 2
D.CHCHOH+ CHCOOH CHCOOCH CH+H O
3 2 3 3 2 3 2
【答案】A
【解析】A.CH=CH +Br →CHBrCHBr,烯烃含有不饱和双键,与Br 反应生成单键,属于加成反应,
2 2 2 2 2 2
A符合题意;
B.CHCHOH+O 2CO+3H O属于氧化反应,B不符合题意;
3 2 2 2 2
C.苯和浓硝酸、浓硫酸加热发生硝化反应生成硝基苯和水,属于取代反应,C不符合题意;
D.乙酸与乙醇生成乙酸乙酯属于取代反应,也是酯化反应,D不符合题意;
故选A。
【点睛】本题主要考查了加成反应的判断,加成反应的条件是有机物中必须含有不饱和键(如碳碳双键、
碳碳三键等),有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物
的反应是加成反应,结合物质的结构判断。
16.某工厂提取粗盐后的盐卤(主要成分为MgCl )制备金属镁,其工艺流程图如下所示,下列说法错误
2
的是:
A.若在实验室进行操作①,只需要漏斗和烧杯两种玻璃仪器
B.操作①发生的反应为非氧化还原反应
C.操作②是蒸发浓缩结晶
D.在整个制备过程中,未发生置换反应
【答案】A
【解析】A.操作①是过滤,玻璃仪器除了漏斗和烧杯还要用到玻璃棒,A错;
B.操作①发生的反应是复分解反应,复分解反应属于非氧化还原反应,B对;
C.从溶液中得到晶体操作是蒸发浓缩结晶 ,C对;
D.在整个制备过程中,没有发生有单质参加反应和生成的反应,所以未发生置换反应,D对。
故选A。
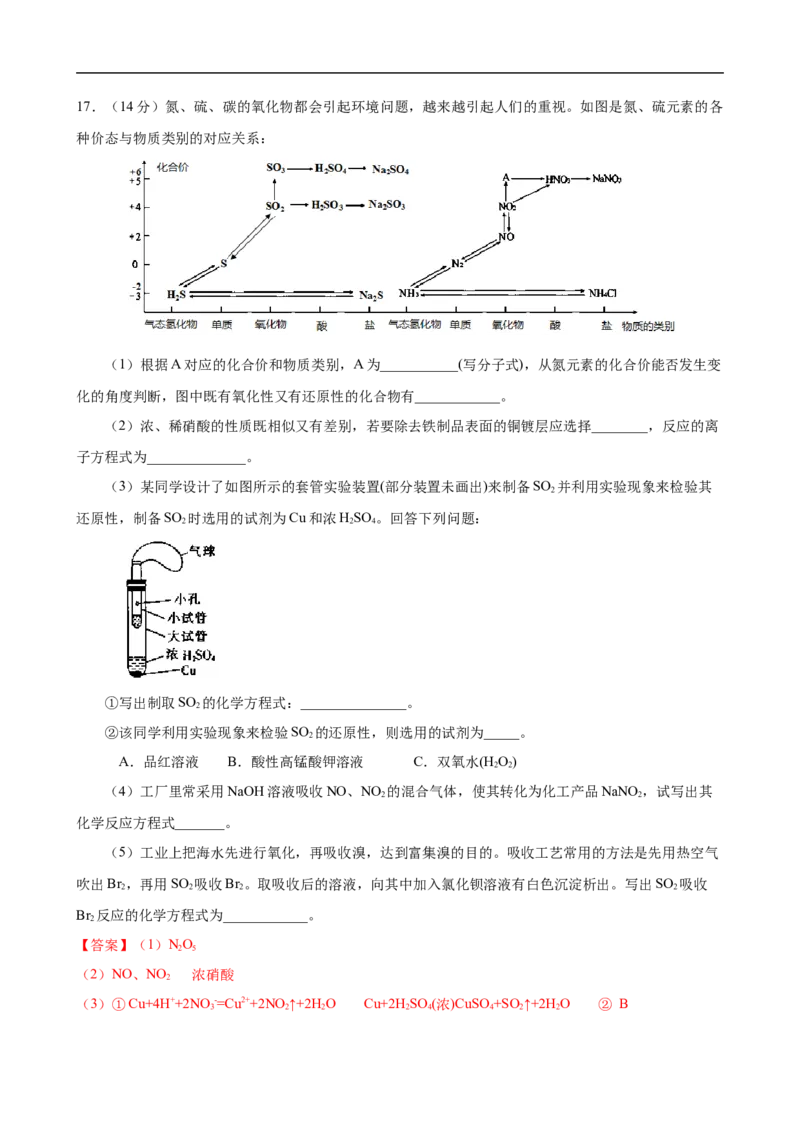
二、非选择题:包括第17题~第21题5个大题,共52分。17.(14分)氮、硫、碳的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各
种价态与物质类别的对应关系:
(1)根据A对应的化合价和物质类别,A为___________(写分子式),从氮元素的化合价能否发生变
化的角度判断,图中既有氧化性又有还原性的化合物有____________。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________,反应的离
子方程式为______________。
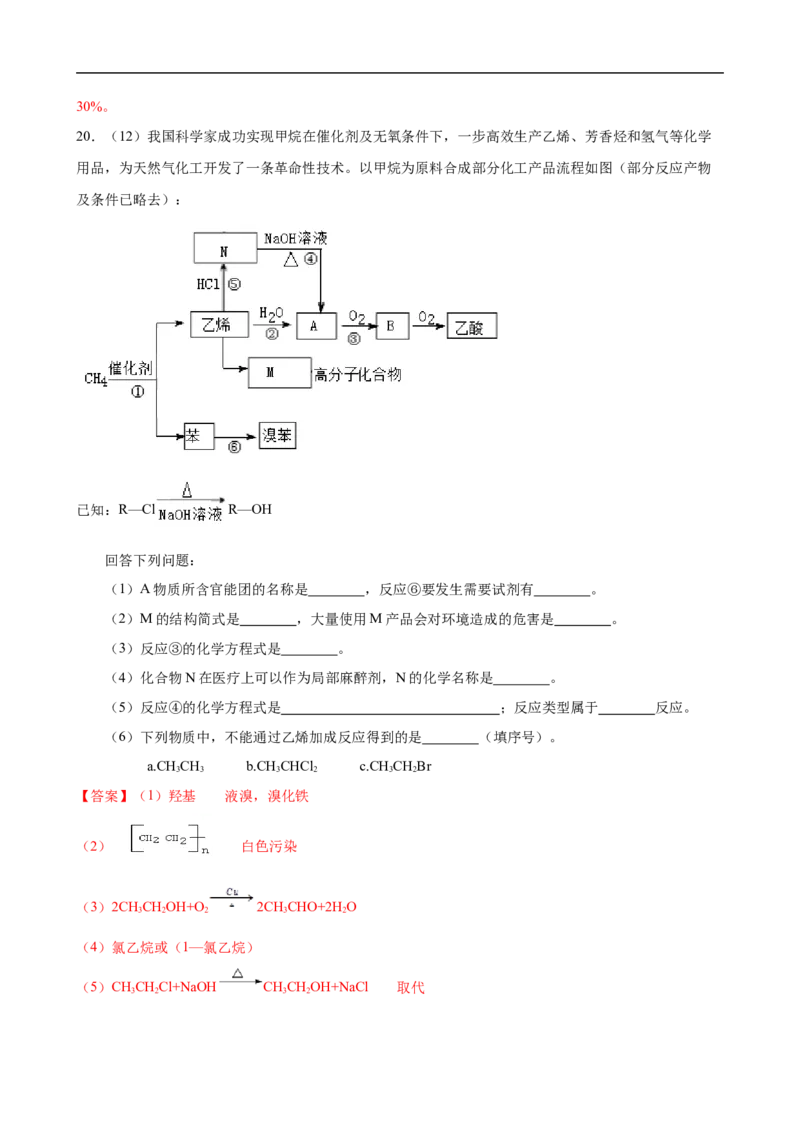
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO 并利用实验现象来检验其
2
还原性,制备SO 时选用的试剂为Cu和浓HSO 。回答下列问题:
2 2 4
①写出制取SO 的化学方程式:_______________。
2
②该同学利用实验现象来检验SO 的还原性,则选用的试剂为_____。
2
A.品红溶液 B.酸性高锰酸钾溶液 C.双氧水(H O)
2 2
(4)工厂里常采用NaOH溶液吸收NO、NO 的混合气体,使其转化为化工产品NaNO ,试写出其
2 2
化学反应方程式_______。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气
吹出Br ,再用SO 吸收Br 。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO 吸收
2 2 2 2
Br 反应的化学方程式为____________。
2
【答案】(1)NO
2 5
(2)NO、NO 浓硝酸
2
(3)①Cu+4H++2NO-=Cu2++2NO↑+2H O Cu+2H SO (浓)CuSO +SO↑+2H O ② B
3 2 2 2 4 4 2 2(4)NO+NO +2NaOH=2NaNO +H O
2 2 2
(5)SO +Br +2H O=HSO +2HBr
2 2 2 2 4
【解析】(1)依据图中化合价与元素化合物之间关系可知A为+5价的氮元素的氧化物,为NO;N原
2 5
子最外层有5个电子,最高为+5价,最低为-3价,NO、NO 中氮元素处于中间价态,化合价既可以升高,
2
又可以降低,所以NO、NO 既有氧化性又有还原性;
2
(2)铜与浓硝酸反应生成硝酸铜、NO 和水,铁与浓硝酸在常温下会发生钝化,所以可用浓硝酸除去铁
2
制品表面的铜镀层,反应的离子方程式:Cu+4H++2NO-=Cu2++2NO↑+2H O;
3 2 2
(3)①在实验室中,一般是用铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,化学方程式:
Cu+2H SO (浓)CuSO +SO↑+2H O;
2 4 4 2 2
②二氧化硫的具有还原性,能够使酸性KMnO 溶液紫色褪色,所以检验SO 的还原性可选酸性高锰酸钾
4 2
溶液,故合理选项是B;
(4)NO、NO 是大气污染物,可用NaOH溶液进行尾气处理,反应的化学方程式为:
2
NO+NO +2NaOH=2NaNO +H O;
2 2 2
(5)二氧化硫与溴水反应生成溴化氢和硫酸,化学方程式:SO +Br +2H O=HSO +2HBr。
2 2 2 2 4
【点睛】本题考查了元素化合物知识,涉及物质氧化性、还原性判断,化学方程式和离子方程式的书写,
明确物质的性质和反应现象是解题关键,掌握元素化合价与物质性质的关系,在氧化还原反应方程式书
写时要符合电子守恒、原子守恒,离子方程式书写要符合电荷守恒和原子守恒。
18.(8分)原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
甲 乙 丙
①下列说法正确的是________。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的 pH 均增大
②在相同时间内, 两烧杯中产生气泡的速度:甲________乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:________________________________。
④当甲中溶液质量增重31.5 g时,电极上转移电子数目为________。
(2)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。通甲烷一极的电极反应方程式为____________________________________________________________。
【答案】(1)BD ② > ③Zn-2e-===Zn2+ ④N
A
(2) CH+10OH—-8e-=CO 2-+7H O
4 3 2
【解析】
(1)①A、甲符合原电池构成条件,所以属于原电池,乙不能构成闭合回路,所以不能构成原电池,选
项A错误;
B、乙不能构成原电池,氢离子在锌片上得电子发生还原反应,所以乙中铜片上没有明显变化,选项B正
确;
C、甲中铜片作正极,正极上氢离子得电子生成氢气,所以铜片质量不变,乙中锌片和氢离子发生置换反
应,所以质量减少,选项C错误;
D、两烧杯中锌和氢离子发生置换反应导致溶液中氢离子浓度减小,则两烧杯中溶液的c(H+)均减小,
选项D正确;
答案选BD;
②甲能构成原电池,乙不能构成原电池,作原电池负极的金属加速被腐蚀,所以在相同时间内,两烧杯
中产生气泡的速度:甲>乙;
③锌的金属性强于铜,锌作为负极,原电池的负极电极反应式为Zn-2e-=Zn2+;
④甲中正极反应为2H++2e-= H ↑,溶液质量增重 31.5g(32.5g-1g)时,消耗0.5molZn,电极上转移电子
2
数目为N ;
A
(2)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是 KOH。通甲烷一极为负极,碱性条
件下甲烷失电子生成碳酸根离子,电极反应方程式为CH+10OH—-8e-=CO 2-+7H O。
4 3 2
19.(11分)某温度下,在一个1L 的密闭容器中,X、Y、Z 三种气态物质的物质的量随时间的变化曲
线如图所示。根据图中数据,填写下列空白:
(1)2min时,Y 的物质的量浓度是____________;
(2)从开始至2min,X 的平均反应速率为_________;
(3)该反应的化学方程式为____________________;(4)1min时,v ____v ,2min时,v ____v (填“>”或“<”或“=”);
(正) (逆) (正) (逆)
(5)在2min时,向容器中通入氩气,增大体系压强,X 的化学反应速率将______;
(6)2min时,x的转化率为________。
【答案】(1)0.9mo1•L-1
(2) 0.15mo1•L-1•min-1
(3) 3X(g)+Y(g) 2Z(g)
(4)> = ⇌
(5)不变
(6)30%
【解析】由图可知,从反应开始到达到平衡,X、Y的物质的量减少,应为反应物,Z的物质的量增加,
应为生成物,从反应开始到第2分钟反应到达平衡状态,X、Y消耗的物质的量分别为0.3 mol、0.1
mol,,Z的生成的物质的量为0.2 mol,物质的量的变化量之比为3: 1: 2,物质的量变化之比等于化学计量
数之比,据此解答。
【详解】(1).由图可知:在2min时Y的物质的量为0.9mol,容器体积为1L,则Y的物质的量的浓度为:
,故答案为:0.9mo1•L-1;
(2).从开始至2min,X的变化的物质的量为1mol -0.7mol=0.3mol,由公式:
;故答案:0.15mo1•L-1•min-1;
(3).由图可知,从反应开始到达到平衡,X、Y的物质的量减少,应为反应物,Z的物质的量增加,应为生
成物,从反应开始到第2分钟反应到达平衡状态,X、Y消耗的物质的量分别为0.3 mol、0.1 mol,,Z的
生成的物质的量为0.2 mol,物质的量的变化量之比为3: 1: 2,物质的量变化之比等于化学计量数之比,
则化学方程式为3X(g)+Y(g) 2Z(g),故答案为:3X(g)+Y(g) 2Z(g);
(4).1min时,平衡正向进行,⇌则正逆反应速率的大小关系为: ⇌v
(正)
>v
(逆)
;2min时反应正好达到平衡,则正
逆反应速率的大小关系为:V =V ,故答案为:>;=;
(正) (逆)
(5).容器体积恒定,通入惰性气体氩气,对反应物浓度没有影响,故X的反应速率不变;故答案为:不变;
(6). 则x的转化率= ,故答案为:30%。
20.(12)我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳香烃和氢气等化学
用品,为天然气化工开发了一条革命性技术。以甲烷为原料合成部分化工产品流程如图(部分反应产物
及条件已略去):
已知:R—Cl R—OH
回答下列问题:
(1)A物质所含官能团的名称是 ,反应⑥要发生需要试剂有 。
(2)M的结构简式是 ,大量使用M产品会对环境造成的危害是 。
(3)反应③的化学方程式是 。
(4)化合物N在医疗上可以作为局部麻醉剂,N的化学名称是 。
(5)反应④的化学方程式是 ;反应类型属于 反应。
(6)下列物质中,不能通过乙烯加成反应得到的是 (填序号)。
a.CH CH b.CH CHCl c.CH CHBr
3 3 3 2 3 2
【答案】(1)羟基 液溴,溴化铁
(2) 白色污染
(3)2CHCHOH+O 2CHCHO+2H O
3 2 2 3 2
(4)氯乙烷或(1—氯乙烷)
(5)CHCHCl+NaOH CHCHOH+NaCl 取代
3 2 3 2(6)b
【解析】由框图可知,CH 在催化剂的作用下生成CH=CH 和 ,乙烯与HO发生加成反应生成A
4 2 2 2
(乙醇),A经氧化反应生成B(乙醛),B再经氧化反应生成乙酸;乙烯与HCl发生加成反应生成N
(CHCHCl),氯乙烷在NaOH的水溶液中加热水解生成A(乙醇);乙烯在一定条件下发生加聚反应
3 2
生成M(聚乙烯); 与Br 在FeBr 的催化下发生取代反应生成 。
2 3
【详解】(1)化合物A是乙醇(CHCHOH),官能团为羟基;根据分析,反应⑥是 与Br 在
3 2 2
FeBr 的催化下发生取代反应生成 ,故需要的试剂是液溴和溴化铁;
3
(2)根据分析,M是聚乙烯( );由于聚乙烯在自然界中很难降解,大量使用聚乙烯产品
会造成白色污染;
(3)根据分析,反应③是乙醇氧化为乙醛的反应,方程式为:2CHCHOH+O 2CHCHO+2H O;
3 2 2 3 2
(4)根据分析,N为氯乙烷或(1—氯乙烷);
(5)根据分析,反应④是氯乙烷的水解反应,方程式为:CHCHCl+NaOH CHCHOH+NaCl;
3 2 3 2
该反应是有机物分子中Cl原子被试剂中羟基所替代的反应,属于取代反应;
(6)a.CHCH 可通过乙烯与氢气加成制得,a不符合题意;
3 3
b.CHCHCl 中两个Cl在同一个C原子上,不能通过加成反应制得,b符合题意;
3 2
c.CHCHBr可通过乙烯与溴化氢加成制得,c不符合题意;
3 2
故选b;
【点睛】本题要注意第(2)题,苯与溴的反应,必须使用液溴,溴的CCl 溶液、溴水都不能反应。
4
21.(7分)以铝土矿(主要成分为 )为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶
解在氢氧化钠溶液中;②向①的所得溶液中通入过量二氧化碳,获得氢氧化铝固体;③使氢氧化铝脱水生成氧化铝;④……
(1)步骤④为冶炼金属铝的过程,应选择的方法是______(填序号)。
A.以C、 或 作还原剂 B.热分解法 C.利用铝热反应原理还原 D.电解法
(2)步骤③所涉及反应的化学方程式为_____________________________________________。
(3)步骤①所涉及反应的离子方程式为_________________________________________________。
(4)步骤②至步骤③的过程中,须经过_____操作。
(5)步骤②所得溶液中含有的大量阴离子是________________(填离子符号)。
【答案】(1)D
(2)
(3)
(4)过滤
(5)
【解析】步骤①中,三氧化铝与氢氧化钠反应生成偏铝酸钠;步骤②中偏铝酸钠与二氧化碳反应生成氢
氧化铝;步骤④采用电解法冶炼金属铝。
【详解】(1)工业上采用电解法冶炼金属铝,故答案选D。
(2)步骤③中氢氧化铝脱水生成氧化铝,化学反应方程式为: 。
(3)步骤①中 与氢氧化钠反应生成偏铝酸钠,离子方程式为: 。
(4)步骤②反应产生氢氧化铝沉淀,故至步骤③的过程中要经过过滤操作。
(5)步骤②中通入过量的二氧化碳,二氧化碳与偏铝酸钠反应生成氢氧化铝和碳酸氢钠,故所得溶液中
含有的大量阴离子为 。