文档内容
2019-2020 年高一化学高频考题期末组合模拟卷 03
(考试时间:90分钟 试卷满分:100分)
考试内容:必修二 难度:★★★☆☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.我国具有独立知识产权的电脑芯片“龙芯一号”的问世,填补了我国计算机制造史上的一项
空白。下列对晶体硅的有关叙述正确的是
A.晶体硅和金刚石的物理性质相似
B.硅在地壳中含量居第二位,可以以游离态存在于自然界中
C.晶体硅是一种良好的半导体材料,但是它提炼工艺复杂,价格昂贵
D.晶体硅具有金属光泽,故它属于金属材料,可以导电
2.化学与生活社会发展息息相关。下列说法错误的是
A. 的乙醇和84消毒液的消毒原理不相同
B.制造N95口罩的聚丙烯树脂属于无机非金属材料
C.玛瑙的主要成分是二氧化硅,陶瓷的主要成分是硅酸盐
D.海轮船体镶嵌锌块是牺牲阳极的阴极保护法,防止船体被腐蚀
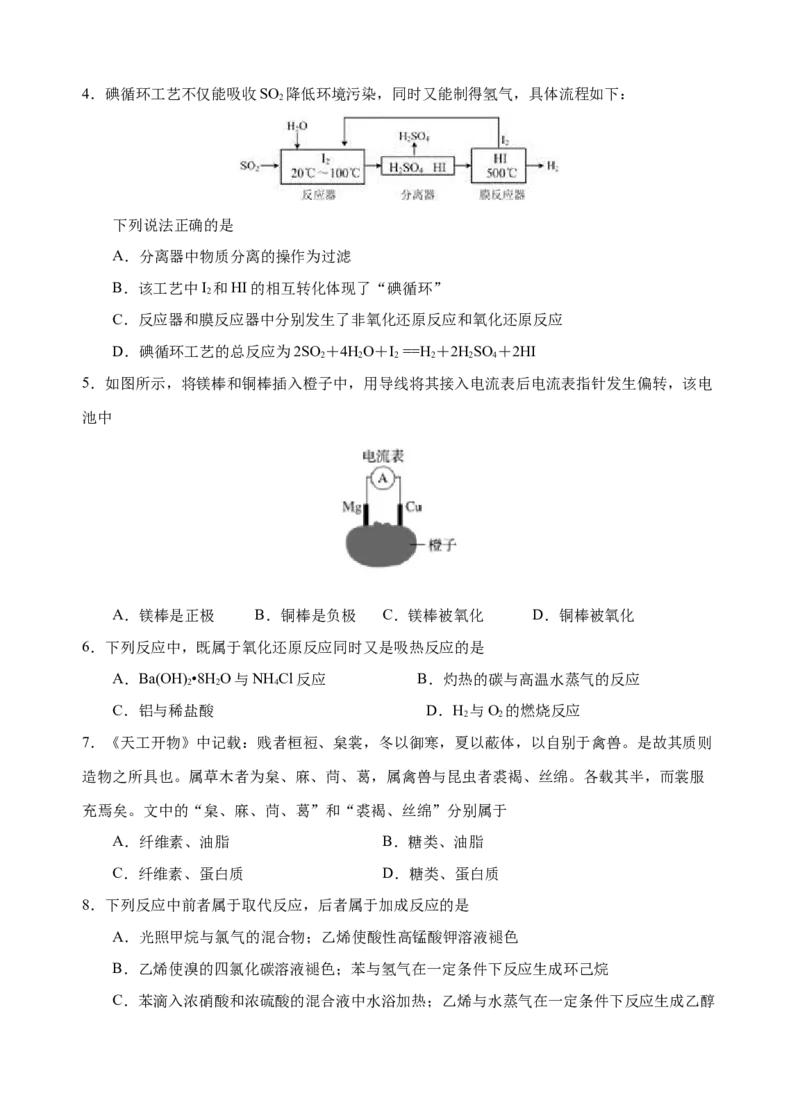
3.实验室模拟氨催化氧化法制硝酸的装置如图所示。下列说法错误的是
A.装置①、②、⑤依次盛装碱石灰、PO、NaOH溶液
2 5
B.装置③中产生红棕色气体
C.装置④中溶液可使紫色石蕊溶液变红,说明有HNO 生成
3
D.通空气的主要作用是鼓出氨气,空气可用N 代替
24.碘循环工艺不仅能吸收SO 降低环境污染,同时又能制得氢气,具体流程如下:
2
下列说法正确的是
A.分离器中物质分离的操作为过滤
B.该工艺中I 和HI的相互转化体现了“碘循环”
2
C.反应器和膜反应器中分别发生了非氧化还原反应和氧化还原反应
D.碘循环工艺的总反应为2SO +4HO+I ==H +2HSO +2HI
2 2 2 2 2 4
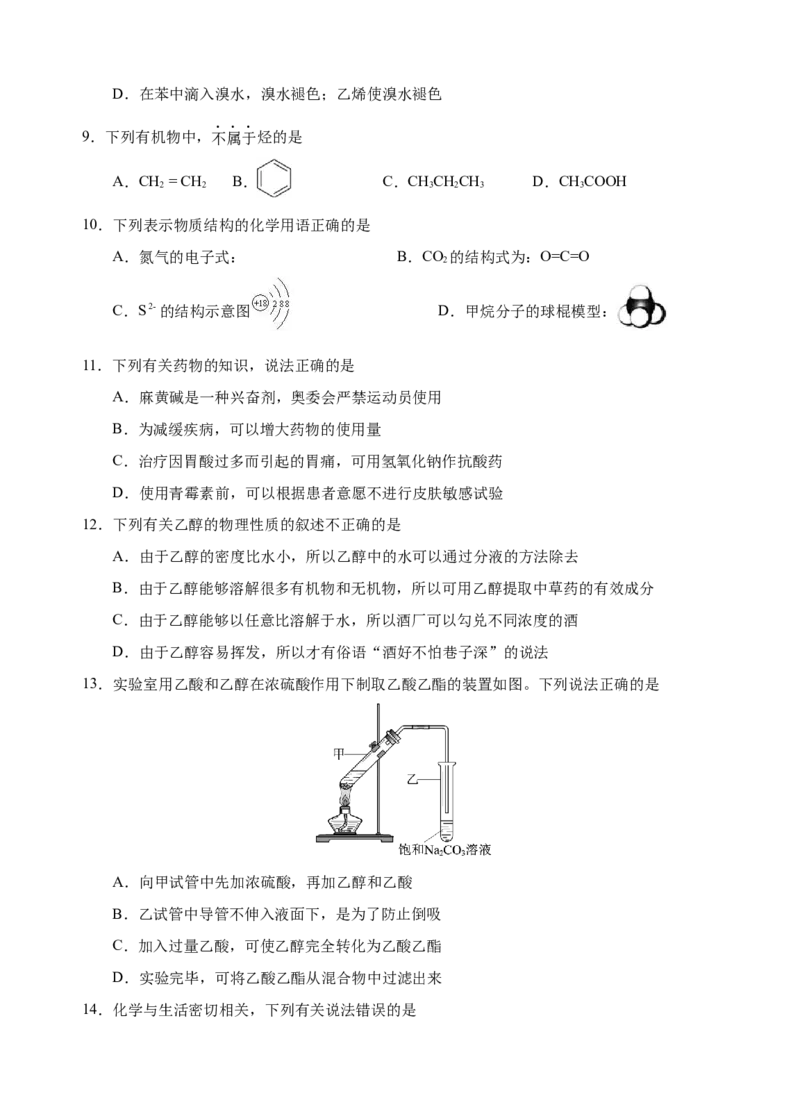
5.如图所示,将镁棒和铜棒插入橙子中,用导线将其接入电流表后电流表指针发生偏转,该电
池中
A.镁棒是正极 B.铜棒是负极 C.镁棒被氧化 D.铜棒被氧化
6.下列反应中,既属于氧化还原反应同时又是吸热反应的是
A.Ba(OH) •8H O与NH Cl反应 B.灼热的碳与高温水蒸气的反应
2 2 4
C.铝与稀盐酸 D.H 与O 的燃烧反应
2 2
7.《天工开物》中记载:贱者桓裋、枲裳,冬以御寒,夏以蔽体,以自别于禽兽。是故其质则
造物之所具也。属草木者为枲、麻、苘、葛,属禽兽与昆虫者裘褐、丝绵。各载其半,而裳服
充焉矣。文中的“枲、麻、苘、葛”和“裘褐、丝绵”分别属于
A.纤维素、油脂 B.糖类、油脂
C.纤维素、蛋白质 D.糖类、蛋白质
8.下列反应中前者属于取代反应,后者属于加成反应的是
A.光照甲烷与氯气的混合物;乙烯使酸性高锰酸钾溶液褪色
B.乙烯使溴的四氯化碳溶液褪色;苯与氢气在一定条件下反应生成环己烷
C.苯滴入浓硝酸和浓硫酸的混合液中水浴加热;乙烯与水蒸气在一定条件下反应生成乙醇D.在苯中滴入溴水,溴水褪色;乙烯使溴水褪色
9.下列有机物中,不属于烃的是
A.CH = CH B. C.CHCHCH D.CHCOOH
2 2 3 2 3 3
10.下列表示物质结构的化学用语正确的是
A.氮气的电子式: B.CO 的结构式为:O=C=O
2
C.S 2- 的结构示意图 D.甲烷分子的球棍模型:
11.下列有关药物的知识,说法正确的是
A.麻黄碱是一种兴奋剂,奥委会严禁运动员使用
B.为减缓疾病,可以增大药物的使用量
C.治疗因胃酸过多而引起的胃痛,可用氢氧化钠作抗酸药
D.使用青霉素前,可以根据患者意愿不进行皮肤敏感试验
12.下列有关乙醇的物理性质的叙述不正确的是
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑不同浓度的酒
D.由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法
13.实验室用乙酸和乙醇在浓硫酸作用下制取乙酸乙酯的装置如图。下列说法正确的是
A.向甲试管中先加浓硫酸,再加乙醇和乙酸
B.乙试管中导管不伸入液面下,是为了防止倒吸
C.加入过量乙酸,可使乙醇完全转化为乙酸乙酯
D.实验完毕,可将乙酸乙酯从混合物中过滤出来
14.化学与生活密切相关,下列有关说法错误的是A.用灼烧的方法可以区分蚕丝和人造纤维
B.食用油反复加热会产生稠环芳香烃等有害物质
C.加热能杀死流感病毒是因为蛋白质受热变性
D.医用消毒酒精中乙醇的浓度(体积分数)为95%
15.下列物质中,互为同分异构体的是
A.蔗糖和麦芽糖 B.淀粉和葡萄糖
C.淀粉和纤维素 D.果糖和蔗糖
16.下列关于化石燃料的加工说法正确的是
A.煤的气化和液化是物理变化,是高效、清洁地利用煤的重要途径
B.石油分馏是化学变化,可得到汽油、煤油、柴油等
C.石蜡油高温分解的产物中含有烷烃和烯烃
D.石油催化裂化主要得到乙烯
二、非选择题:包括第17题~第21题5个大题,共52分。
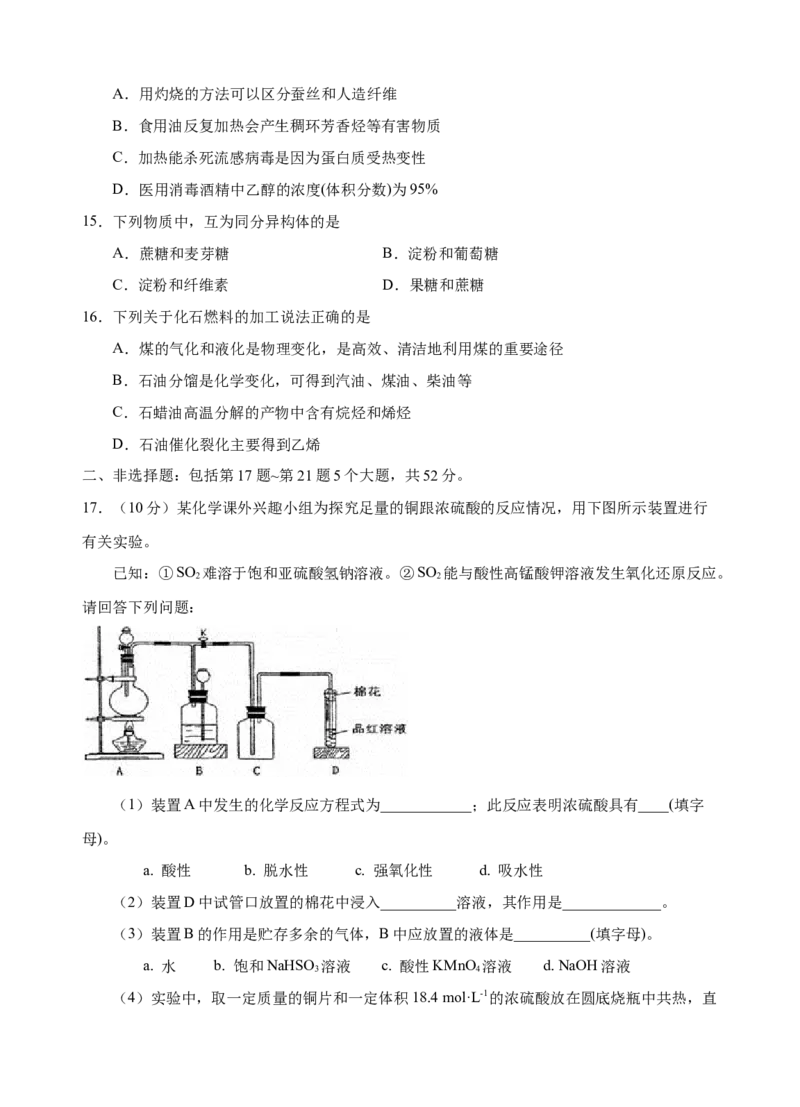
17.(10分)某化学课外兴趣小组为探究足量的铜跟浓硫酸的反应情况,用下图所示装置进行
有关实验。
已知:①SO 难溶于饱和亚硫酸氢钠溶液。②SO 能与酸性高锰酸钾溶液发生氧化还原反应。
2 2
请回答下列问题:
(1)装置A中发生的化学反应方程式为____________;此反应表明浓硫酸具有____(填字
母)。
a. 酸性 b. 脱水性 c. 强氧化性 d. 吸水性
(2)装置D中试管口放置的棉花中浸入__________溶液,其作用是_____________。
(3)装置B的作用是贮存多余的气体,B中应放置的液体是__________(填字母)。
a. 水 b. 饱和NaHSO 溶液 c. 酸性KMnO 溶液 d. NaOH溶液
3 4
(4)实验中,取一定质量的铜片和一定体积18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫
酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是____________。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________(填字母)。
a. 银粉 b. 铁粉 c. BaCl 溶液 d. NaHCO 溶液
2 3
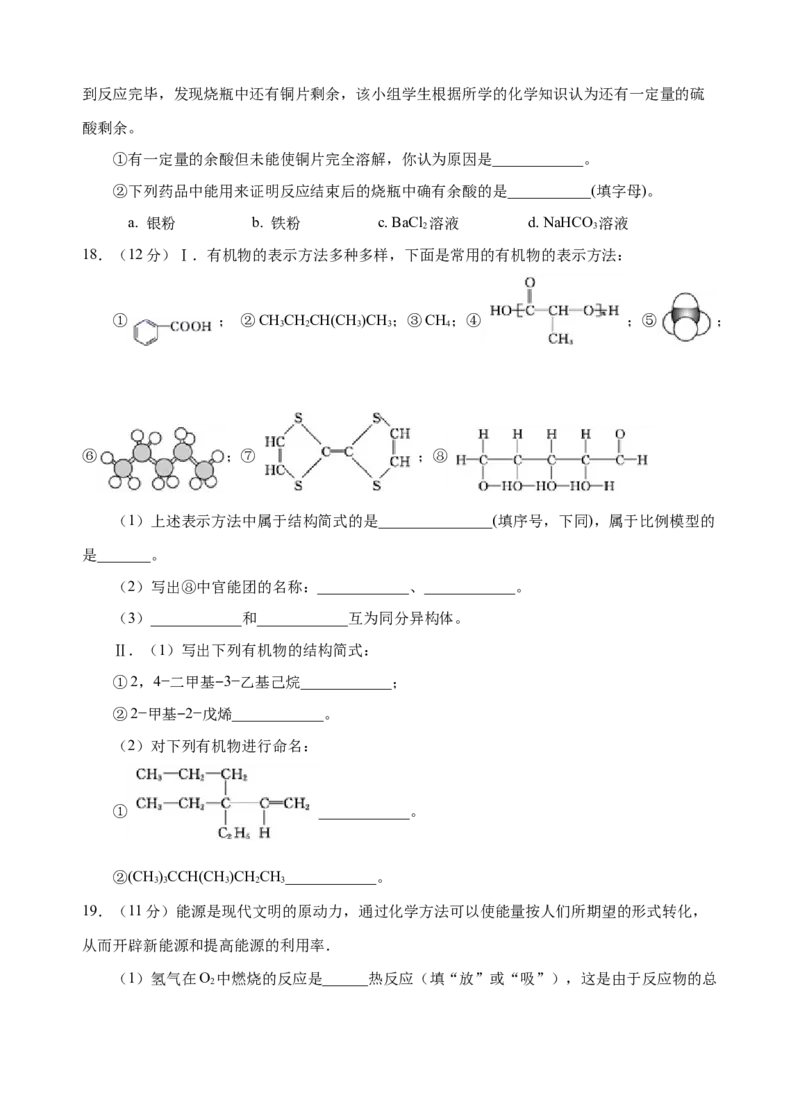
18.(12分)Ⅰ.有机物的表示方法多种多样,下面是常用的有机物的表示方法:
① ; ②CHCHCH(CH )CH;③CH;④ ;⑤ ;
3 2 3 3 4
⑥ ;⑦ ;⑧
(1)上述表示方法中属于结构简式的是_______________(填序号,下同),属于比例模型的
是_______。
(2)写出⑧中官能团的名称:____________、____________。
(3)____________和____________互为同分异构体。
Ⅱ.(1)写出下列有机物的结构简式:
①2,4−二甲基−3−乙基己烷____________;
②2−甲基−2−戊烯____________。
(2)对下列有机物进行命名:
① ____________。
②(CH)CCH(CH )CHCH____________。
3 3 3 2 3
19.(11分)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,
从而开辟新能源和提高能源的利用率.
(1)氢气在O 中燃烧的反应是______热反应(填“放”或“吸”),这是由于反应物的总
2能量______生成物的总能量(填“大于”、“小于”或“等于”,下同);
(2)从化学反应的本质角度来看,氢气的燃烧是由于断裂反应物中的化学键吸收的总能量
______形成产物的化学键放出的总能量。已知破坏1mol H-H键、1mol O=O键、1mol H-O键时
分别需要吸收a kJ、b kJ、c kJ的能量。则2mol H(g)和1mol O(g)转化为2mol HO(g)
2 2 2
时放出的热量为____________________kJ。
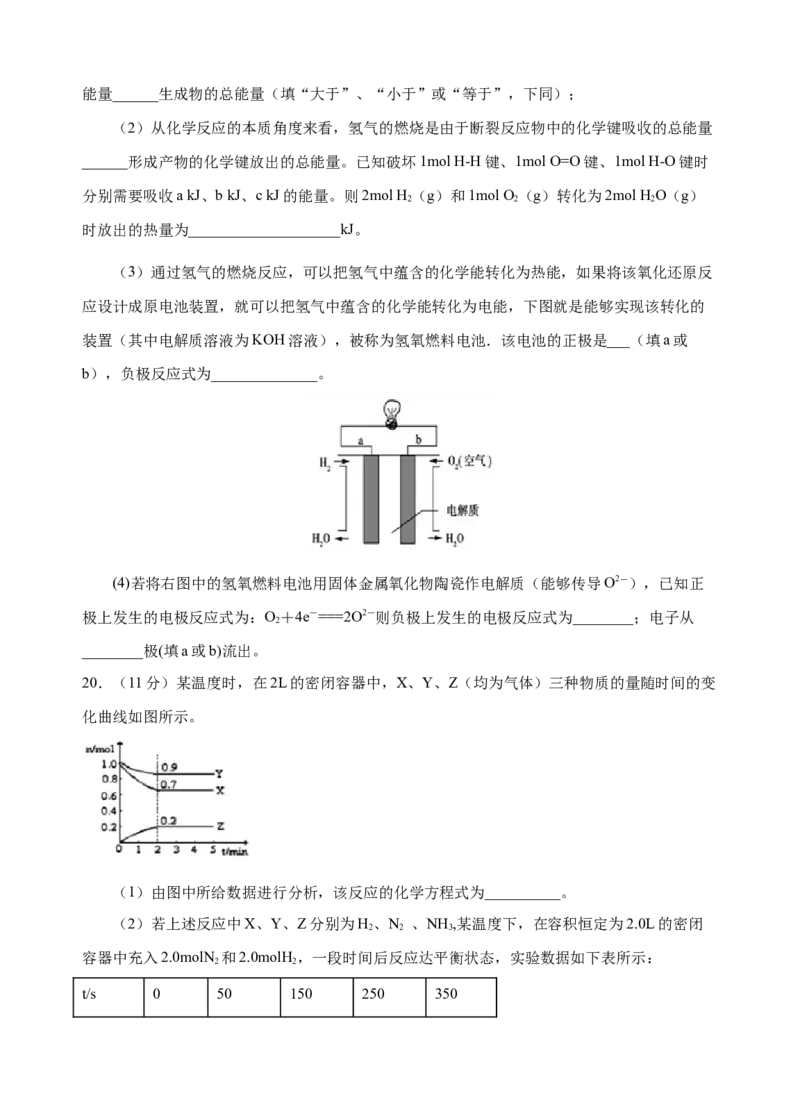
(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反
应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的
装置(其中电解质溶液为KOH溶液),被称为氢氧燃料电池.该电池的正极是___(填a或
b),负极反应式为______________。
(4)若将右图中的氢氧燃料电池用固体金属氧化物陶瓷作电解质(能够传导O2-),已知正
极上发生的电极反应式为:O+4e-===2O2-则负极上发生的电极反应式为________;电子从
2
________极(填a或b)流出。
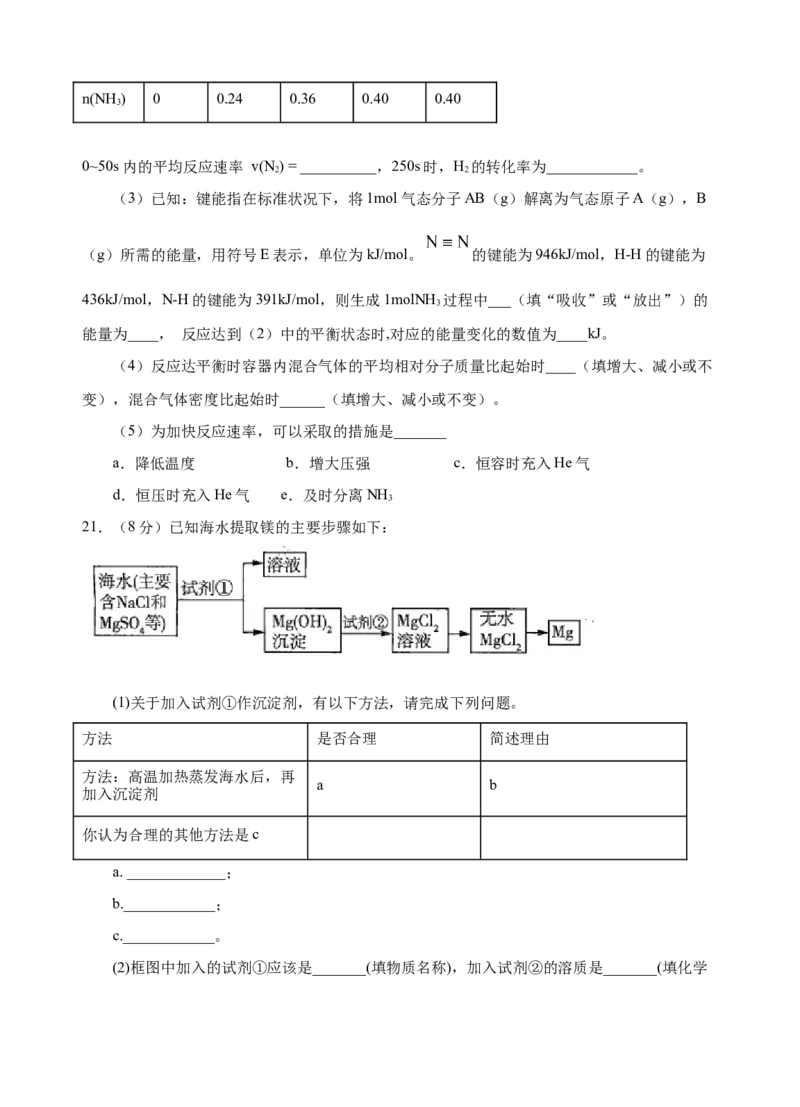
20.(11分)某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变
化曲线如图所示。
(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H、N 、NH ,某温度下,在容积恒定为2.0L的密闭
2 2 3
容器中充入2.0molN 和2.0molH,一段时间后反应达平衡状态,实验数据如下表所示:
2 2
t/s 0 50 150 250 350n(NH ) 0 0.24 0.36 0.40 0.40
3
0~50s内的平均反应速率 v(N ) = __________,250s时,H 的转化率为____________。
2 2
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B
(g)所需的能量,用符号E表示,单位为kJ/mol。 的键能为946kJ/mol,H-H的键能为
436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH 过程中___(填“吸收”或“放出”)的
3
能量为____, 反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)反应达平衡时容器内混合气体的平均相对分子质量比起始时____(填增大、减小或不
变),混合气体密度比起始时______(填增大、减小或不变)。
(5)为加快反应速率,可以采取的措施是_______
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH
3
21.(8分)已知海水提取镁的主要步骤如下:
(1)关于加入试剂①作沉淀剂,有以下方法,请完成下列问题。
方法 是否合理 简述理由
方法:高温加热蒸发海水后,再
a b
加入沉淀剂
你认为合理的其他方法是c
a. _____________;
b.____________;
c.____________。
(2)框图中加入的试剂①应该是_______(填物质名称),加入试剂②的溶质是_______(填化学式)。工业上由无水 制取镁的化学方程式为___________。