文档内容
2019-2020 年高一化学高频考题期末组合模拟卷 04
(考试时间:90分钟 试卷满分:100分)
考试内容:必修二 难度:★★★☆☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
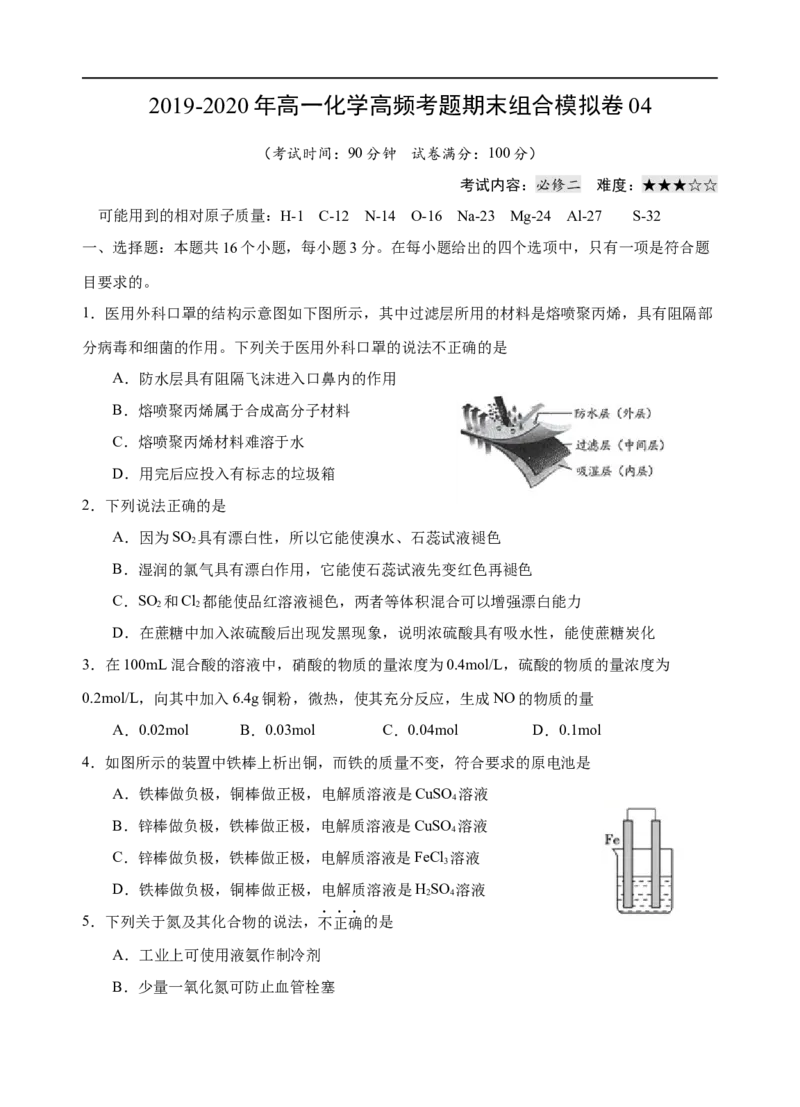
1.医用外科口罩的结构示意图如下图所示,其中过滤层所用的材料是熔喷聚丙烯,具有阻隔部
分病毒和细菌的作用。下列关于医用外科口罩的说法不正确的是
A.防水层具有阻隔飞沫进入口鼻内的作用
B.熔喷聚丙烯属于合成高分子材料
C.熔喷聚丙烯材料难溶于水
D.用完后应投入有标志的垃圾箱
2.下列说法正确的是
A.因为SO 具有漂白性,所以它能使溴水、石蕊试液褪色
2
B.湿润的氯气具有漂白作用,它能使石蕊试液先变红色再褪色
C.SO 和Cl 都能使品红溶液褪色,两者等体积混合可以增强漂白能力
2 2
D.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性,能使蔗糖炭化
3.在100mL混合酸的溶液中,硝酸的物质的量浓度为0.4mol/L,硫酸的物质的量浓度为
0.2mol/L,向其中加入6.4g铜粉,微热,使其充分反应,生成NO的物质的量
A.0.02mol B.0.03mol C.0.04mol D.0.1mol
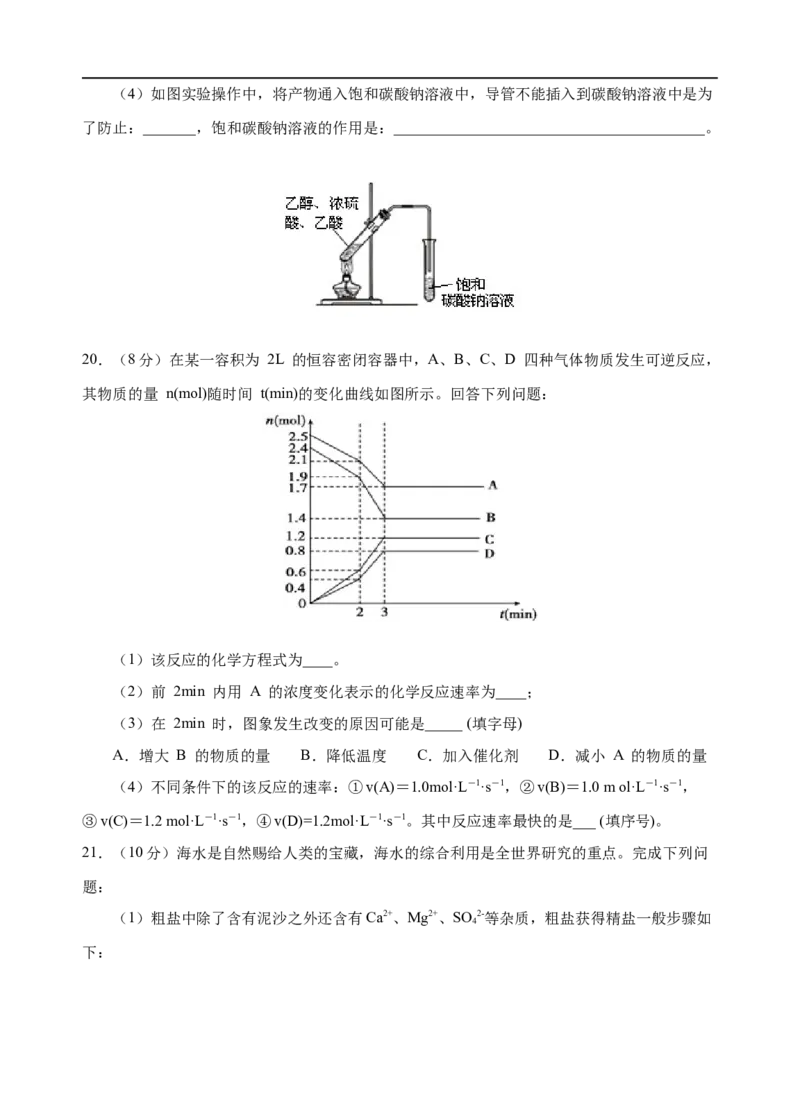
4.如图所示的装置中铁棒上析出铜,而铁的质量不变,符合要求的原电池是
A.铁棒做负极,铜棒做正极,电解质溶液是CuSO 溶液
4
B.锌棒做负极,铁棒做正极,电解质溶液是CuSO 溶液
4
C.锌棒做负极,铁棒做正极,电解质溶液是FeCl 溶液
3
D.铁棒做负极,铜棒做正极,电解质溶液是HSO 溶液
2 4
5.下列关于氮及其化合物的说法,不正确的是
A.工业上可使用液氨作制冷剂
B.少量一氧化氮可防止血管栓塞C.铵态氮肥宜与草木灰(主要成分为KCO)混合使用
2 3
D.硝酸可用于制造TNT、硝化甘油和硝化纤维
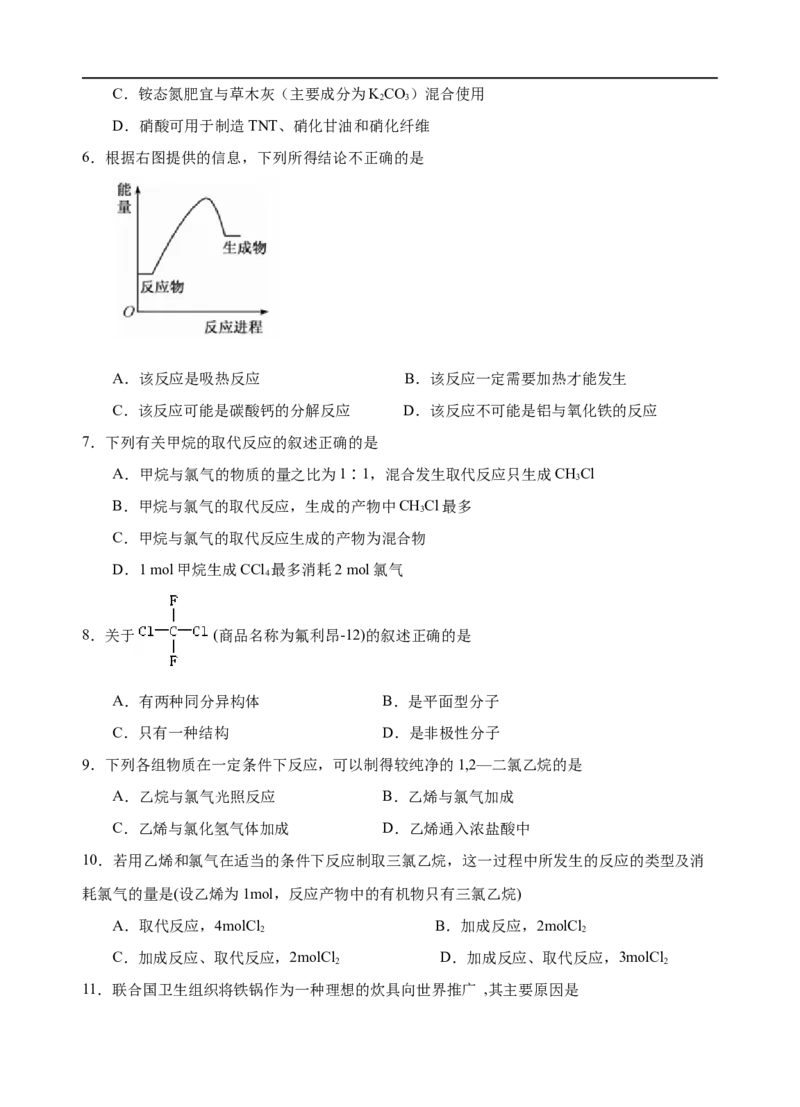
6.根据右图提供的信息,下列所得结论不正确的是
A.该反应是吸热反应 B.该反应一定需要加热才能发生
C.该反应可能是碳酸钙的分解反应 D.该反应不可能是铝与氧化铁的反应
7.下列有关甲烷的取代反应的叙述正确的是
A.甲烷与氯气的物质的量之比为1∶1,混合发生取代反应只生成CHCl
3
B.甲烷与氯气的取代反应,生成的产物中CHCl最多
3
C.甲烷与氯气的取代反应生成的产物为混合物
D.1 mol甲烷生成CCl 最多消耗2 mol氯气
4
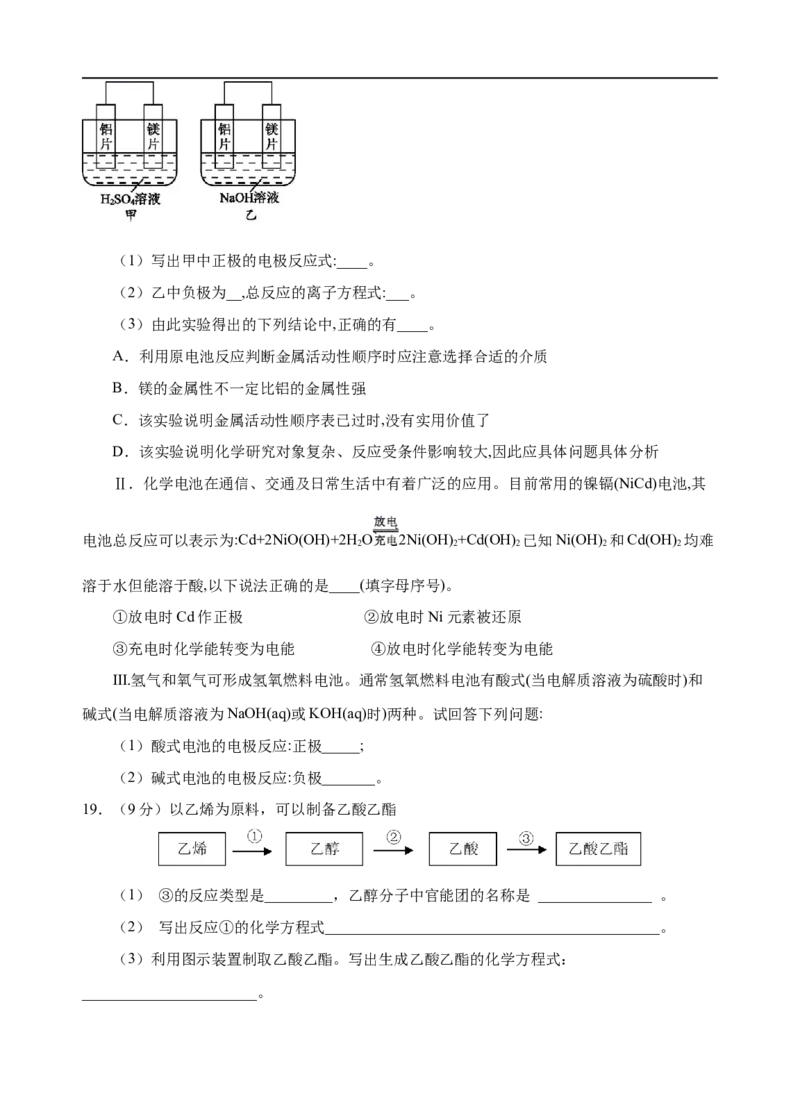
8.关于 (商品名称为氟利昂-12)的叙述正确的是
A.有两种同分异构体 B.是平面型分子
C.只有一种结构 D.是非极性分子
9.下列各组物质在一定条件下反应,可以制得较纯净的1,2—二氯乙烷的是
A.乙烷与氯气光照反应 B.乙烯与氯气加成
C.乙烯与氯化氢气体加成 D.乙烯通入浓盐酸中
10.若用乙烯和氯气在适当的条件下反应制取三氯乙烷,这一过程中所发生的反应的类型及消
耗氯气的量是(设乙烯为1mol,反应产物中的有机物只有三氯乙烷)
A.取代反应,4molCl B.加成反应,2molCl
2 2
C.加成反应、取代反应,2molCl D.加成反应、取代反应,3molCl
2 2
11.联合国卫生组织将铁锅作为一种理想的炊具向世界推广 ,其主要原因是A.吸热慢 、散热也慢 、宜于食物保温
B.烹饪出的食物中含有对人体有益的元素
C.生产过程简单 、不易生锈 、价格便宜
D.生铁中含有碳元素 、能产生对人体有益的有机物
12.将1.0体积乙烷和乙烯的混合气体在氧气中充分燃烧,生成2.0体积的CO 和2.4体积的水
2
蒸气,则混合物中乙烷和乙烯的体积比为(气体体积在同温同压下测定)
A.3∶1 B.1∶3 C.3∶2 D.2∶3
13.A、B、C三种醇分别与足量的金属钠完全反应,在相同条件下产生相同的体积 ,消耗
这三种醇的物质的量之比为3:6:2,则A、B、C三种醇分子中所含羟基的个数之比为
A.3:2:1 B.2:6:3 C.3:1:2 D.2:1:3
14.下列有关能源和能量转换的叙述正确的是
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
B.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
C.普通锌锰干电池不含环境污染物,用完后可以随意扔掉,使用方便
D.燃料电池是利用燃料燃烧,将化学能转化为热能,然后再转化为电能的化学电源
15.下列关于煤和石油综合利用的叙述中,正确的是
A.煤的气化是对其进行加热直接变为气体
B.煤的干馏和石油的分馏都是化学变化
C.石油产品裂解能生产乙烯
D.石油分馏的各馏分均是纯净物
16.从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
A.灼烧过程中使用的玻璃仪器有酒精灯、烧杯、玻璃棒
B.氧化过程中发生反应的离子方程式为C.检验碘单质时,可选用淀粉,若淀粉变蓝说明海带中一定含有碘单质
D.分液时,先打开活塞放出下层液体,再关闭活塞,从上口倒出上层液体
二、非选择题:包括第17题~第21题5个大题,共52分。
17.(12分)氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综
合处理含NH +废水和工业废气(主要含NO、CO、CO、SO 、N)的流程如图:
4 2 2 2
已知:NO+NO +2NaOH=2NaNO +H O 2NO +2NaOH=NaNO +NaNO +H O
2 2 2 2 3 2 2
(1)固体1的主要成分有Ca(OH) 、__________(填化学式)。
2
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为
__________g。
(3)用NaNO 溶液处理含NH +废水反应的离子方程式为__________。
2 4
(4)验证废水中NH +已基本除净的方法是___________(写出操作、现象与结论)。
4
(5)气体1转化为气体2时空气不能过量的原因是__________。
(6)捕获剂捕获的气体主要是__________(填化学式)。
(7)流程中生成的NaNO 因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO
2 2
能发生如下反应:2NaNO +4HI=2NO↑+I +2NaI+2H O;I 可以使淀粉变蓝。根据上述反应,选择
2 2 2 2
生活中常见的物质和有关试剂进行实验,以鉴别NaNO 和NaCl。需选用的物质是
2
__________(填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤
18.(13分)Ⅰ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片
和铝片作电极,但甲同学将电极放入6 mol·L-1的HSO 溶液中,乙同学将电极放入6 mol·L-1的
2 4
NaOH溶液中,如图所示。(1)写出甲中正极的电极反应式:____。
(2)乙中负极为__,总反应的离子方程式:___。
(3)由此实验得出的下列结论中,正确的有____。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
Ⅱ.化学电池在通信、交通及日常生活中有着广泛的应用。目前常用的镍镉(NiCd)电池,其
电池总反应可以表示为:Cd+2NiO(OH)+2H O 2Ni(OH) +Cd(OH) 已知Ni(OH) 和Cd(OH) 均难
2 2 2 2 2
溶于水但能溶于酸,以下说法正确的是____(填字母序号)。
①放电时Cd作正极 ②放电时Ni元素被还原
③充电时化学能转变为电能 ④放电时化学能转变为电能
Ⅲ.氢气和氧气可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和
碱式(当电解质溶液为NaOH(aq)或KOH(aq)时)两种。试回答下列问题:
(1)酸式电池的电极反应:正极_____;
(2)碱式电池的电极反应:负极_______。
19.(9分)以乙烯为原料,可以制备乙酸乙酯
(1) ③的反应类型是_________,乙醇分子中官能团的名称是 _______________ 。
(2) 写出反应①的化学方程式____________________________________________。
(3)利用图示装置制取乙酸乙酯。写出生成乙酸乙酯的化学方程式:
_______________________。(4)如图实验操作中,将产物通入饱和碳酸钠溶液中,导管不能插入到碳酸钠溶液中是为
了防止:_______,饱和碳酸钠溶液的作用是:_________________________________________。
20.(8分)在某一容积为 2L 的恒容密闭容器中,A、B、C、D 四种气体物质发生可逆反应,
其物质的量 n(mol)随时间 t(min)的变化曲线如图所示。回答下列问题:
(1)该反应的化学方程式为____。
(2)前 2min 内用 A 的浓度变化表示的化学反应速率为____;
(3)在 2min 时,图象发生改变的原因可能是_____ (填字母)
A.增大 B 的物质的量 B.降低温度 C.加入催化剂 D.减小 A 的物质的量
(4)不同条件下的该反应的速率:①v(A)=1.0mol·L-1·s-1,②v(B)=1.0 m ol·L-1·s-1,
③v(C)=1.2 mol·L-1·s-1,④v(D)=1.2mol·L-1·s-1。其中反应速率最快的是___ (填序号)。
21.(10分)海水是自然赐给人类的宝藏,海水的综合利用是全世界研究的重点。完成下列问
题:
(1)粗盐中除了含有泥沙之外还含有Ca2+、Mg2+、SO 2-等杂质,粗盐获得精盐一般步骤如
4
下:加入的试剂①、②分别是:_________、_________。
(2)某学生在实验室中模拟海水提取溴的步骤为:
取25 L除去悬浮杂质后的海水,浓缩至2L,向其中通入足量氯气。
① 氧化步骤中生成Br 的离子方程式为_______________________________。
2
② 将吹出的Br (g)用纯碱溶液全部吸收,发生反应:3Br +3Na CO=5NaBr+NaBrO +3CO ↑
2 2 2 3 3 2
,产生的CO 通入足量澄清石灰水中,得到1g白色沉淀。计算海水中溴的浓度为_______g/L。
2
③实验室中若用CCl 提取少量的溴:向溴水中加入CCl 振荡、静置……得溴的四氯化碳溶
4 4
液,该分离提纯溴的方法叫________;用到的主要仪器为_____________。
(3)实验证明金属制品在海水中更容易生锈,铜锈的化学式为: _____________。