文档内容
2019-2020 年高一化学高频考题期末组合模拟卷 05
(考试时间:90分钟 试卷满分:100分)
考试内容:必修二 难度:★★★☆☆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.“笔、墨、纸、砚”在中国传统文化中被称为“文房四宝”,下列说法中错误的是
A B C D
用灼烧法可鉴别羊毫与 墨的主要成分是 纸的主要成分属于 用石材制作砚台的过
尼龙毫的真伪 碳单质 合成材料 程是物理变化
2.据我国古代第一部药物学专著《神农本草经》记载:“石硫黄(即硫磺)能化金银钢铁,奇
物”。硫与某些金属单质化合所得的产物可能是
A.AlS B.AgS C.CuS D.FeS
3.下列关于浓硫酸的性质叙述正确的是
A.加热时与铜反应只体现酸性 B.干燥氢气体现脱水性
C.使白纸变黑体现吸水性 D.加热时与碳反应体现强氧化性
4.下列关于铵盐的叙述:①铵盐中氮元素化合价都是-3价;②铵盐都是晶体,都易溶于水;③
铵盐与碱共热放出氨气;④铵盐都不能与酸反应;⑤铵盐都易分解。其中正确的是
A.①②③ B.②③④ C.③④⑤ D.②③⑤
5.下列说法中正确的是
A.物质发生化学反应时不一定伴随着能量变化
B.伴随能量变化的过程都是化学变化
C.在一个确定的化学反应中,反应物的总能量与生成物的总能量一定不同
D.在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量6.有一稀硫酸和稀硝酸的混合酸,其中HSO 和HNO 的物质的量浓度分别是4mol·L-1和
2 4 3
2mol·L-1,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气
体的体积为(假设反应中HNO 的还原产物全部为NO)
3
A.224mL B.448mL C.672mL D.896mL
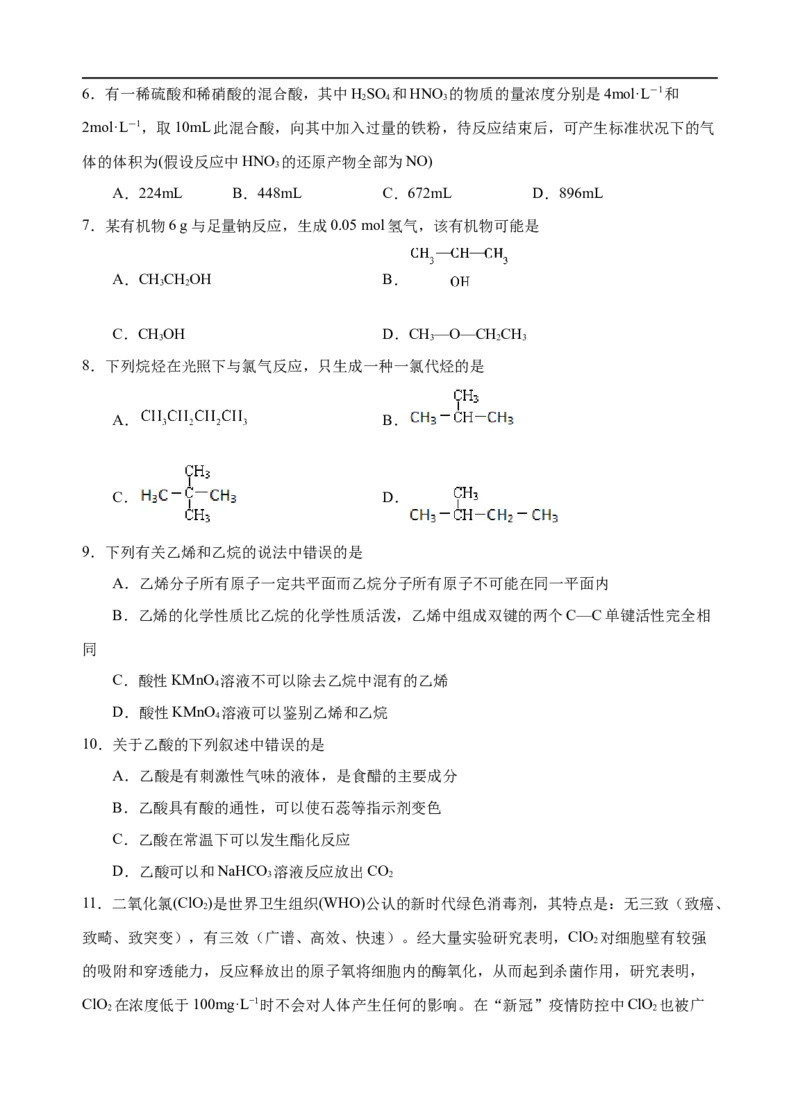
7.某有机物6 g与足量钠反应,生成0.05 mol氢气,该有机物可能是
A.CHCHOH B.
3 2
C.CHOH D.CH—O—CH CH
3 3 2 3
8.下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是
A. B.
C. D.
9.下列有关乙烯和乙烷的说法中错误的是
A.乙烯分子所有原子一定共平面而乙烷分子所有原子不可能在同一平面内
B.乙烯的化学性质比乙烷的化学性质活泼,乙烯中组成双键的两个C—C单键活性完全相
同
C.酸性KMnO 溶液不可以除去乙烷中混有的乙烯
4
D.酸性KMnO 溶液可以鉴别乙烯和乙烷
4
10.关于乙酸的下列叙述中错误的是
A.乙酸是有刺激性气味的液体,是食醋的主要成分
B.乙酸具有酸的通性,可以使石蕊等指示剂变色
C.乙酸在常温下可以发生酯化反应
D.乙酸可以和NaHCO 溶液反应放出CO
3 2
11.二氧化氯(ClO )是世界卫生组织(WHO)公认的新时代绿色消毒剂,其特点是:无三致(致癌、
2
致畸、致突变),有三效(广谱、高效、快速)。经大量实验研究表明,ClO 对细胞壁有较强
2
的吸附和穿透能力,反应释放出的原子氧将细胞内的酶氧化,从而起到杀菌作用,研究表明,
ClO 在浓度低于100mg·L−1时不会对人体产生任何的影响。在“新冠”疫情防控中ClO 也被广
2 2泛的用于公共场所的消杀。下列关于ClO 的说法正确的是
2
A.ClO 能用于消毒是因为它是氯的最高价氧化物
2
B.在进行消毒作业时使用的ClO 溶液浓度越大越好
2
C.ClO 杀菌力强,是一种比“84”性能更优越的消毒剂
2
D.ClO 可与NaOH在一条件下发生反应,产物只有NaClO 和HO
2 3 2
12.交警对驾驶员进行呼气酒精检测的原理是酒精能将橙色的KCr O 酸性溶液迅速还原成蓝绿
2 2 7
色的Cr3+。下列对乙醇的描述与此测定原理有关的是:
①乙醇沸点低;②乙醇密度比水小;③乙醇有还原性;④乙醇的组成中含氧元素
A.①③ B.②③ C.②④ D.①④
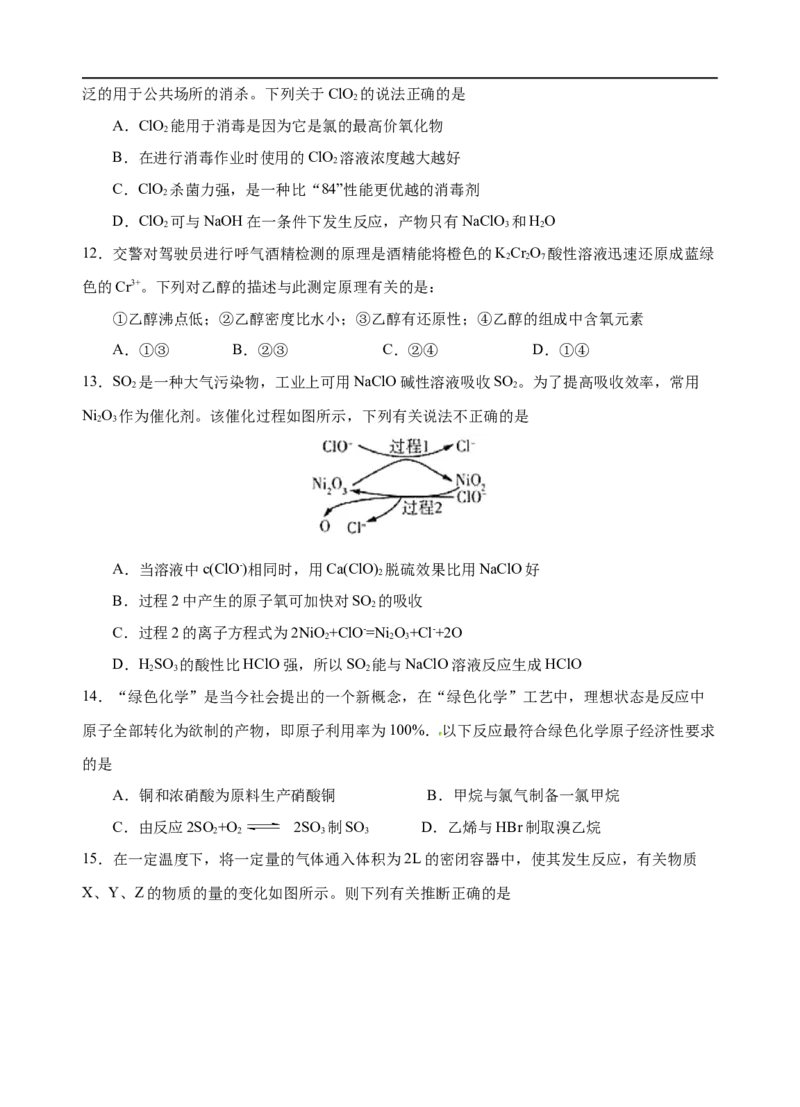
13.SO 是一种大气污染物,工业上可用NaClO碱性溶液吸收SO 。为了提高吸收效率,常用
2 2
Ni O 作为催化剂。该催化过程如图所示,下列有关说法不正确的是
2 3
A.当溶液中c(ClO-)相同时,用Ca(ClO) 脱硫效果比用NaClO好
2
B.过程2中产生的原子氧可加快对SO 的吸收
2
C.过程2的离子方程式为2NiO+ClO-=NiO+Cl-+2O
2 2 3
D.HSO 的酸性比HClO强,所以SO 能与NaClO溶液反应生成HClO
2 3 2
14.“绿色化学”是当今社会提出的一个新概念,在“绿色化学”工艺中,理想状态是反应中
原子全部转化为欲制的产物,即原子利用率为100%.以下反应最符合绿色化学原子经济性要求
的是
A.铜和浓硝酸为原料生产硝酸铜 B.甲烷与氯气制备一氯甲烷
C.由反应2SO +O 2SO 制SO D.乙烯与HBr制取溴乙烷
2 2 3 3
15.在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,有关物质
X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是A.t时,X、Y、Z的质量不再改变
B.该反应的化学方程式为:3Z=3X+2Y
C.t时,Z的浓度为1.2mol/L
D.t时,反应停止,反应速率为0
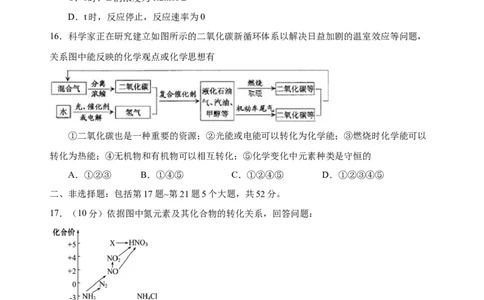
16.科学家正在研究建立如图所示的二氧化碳新循环体系以解决日益加剧的温室效应等问题,
关系图中能反映的化学观点或化学思想有
①二氧化碳也是一种重要的资源;②光能或电能可以转化为化学能;③燃烧时化学能可以
转化为热能;④无机物和有机物可以相互转化;⑤化学变化中元素种类是守恒的
A.①②③ B.①④⑤ C.①②④⑤ D.①②③④⑤
二、非选择题:包括第17题~第21题5个大题,共52分。
17.(10分)依据图中氮元素及其化合物的转化关系,回答问题:
(1)上图中 X 的化学式为______,从化合价上看,X 具有_______性(填“氧化”或“还
原”);
(2)写出 NO 与水反应的化学方程式____________;
2
(3)写出稀硝酸与铜反应的离子方程式____________;
(4)实验室常用 NH Cl与 Ca(OH) 制取氨气,写出反应的化学方程式_________;
4 2(5)下列试剂不能用于干燥 NH 的是________ (填字母);
3
A.浓硫酸 B.碱石灰 C.NaOH 固体
(6)氨气是重要的化工原料,写出其催化氧化的化学方程式__________。
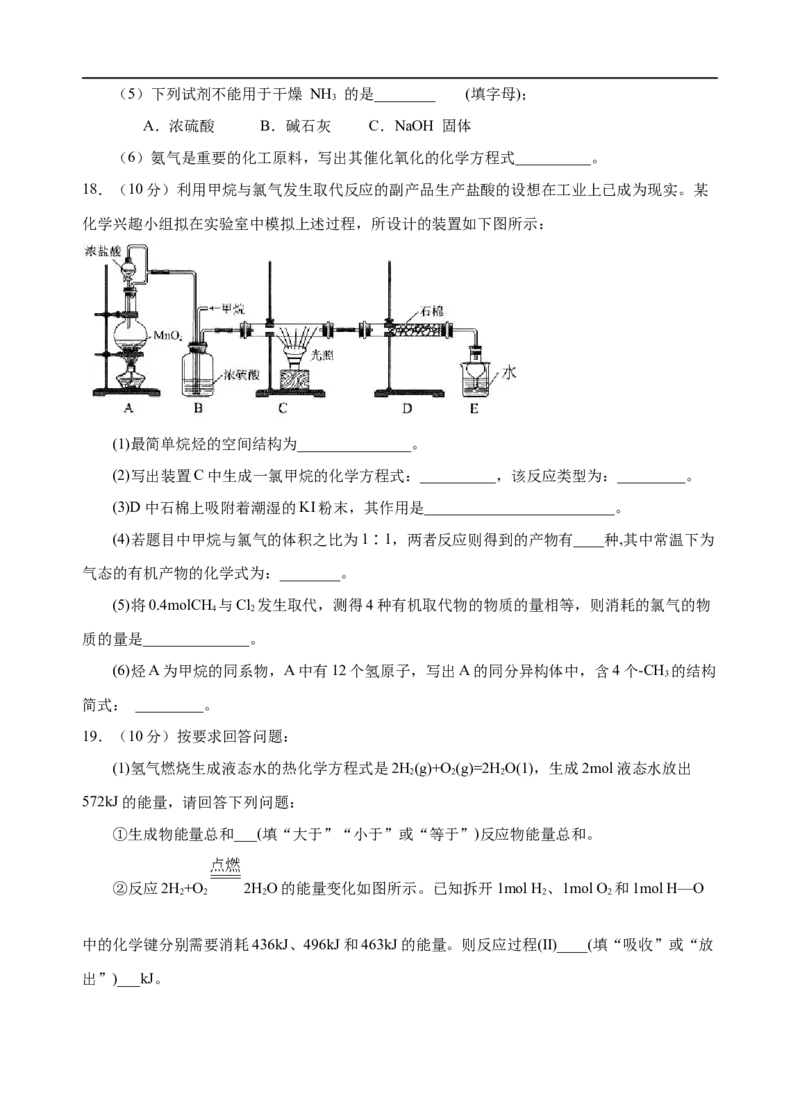
18.(10分)利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某
化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
(1)最简单烷烃的空间结构为_______________。
(2)写出装置C中生成一氯甲烷的化学方程式:__________,该反应类型为:_________。
(3)D中石棉上吸附着潮湿的KI粉末,其作用是_________________________。
(4)若题目中甲烷与氯气的体积之比为1∶1,两者反应则得到的产物有____种,其中常温下为
气态的有机产物的化学式为:________。
(5)将0.4molCH 与Cl 发生取代,测得4种有机取代物的物质的量相等,则消耗的氯气的物
4 2
质的量是______________。
(6)烃A为甲烷的同系物,A中有12个氢原子,写出A的同分异构体中,含4个-CH 的结构
3
简式: _________。
19.(10分)按要求回答问题:
(1)氢气燃烧生成液态水的热化学方程式是2H(g)+O(g)=2HO(1),生成2mol液态水放出
2 2 2
572kJ的能量,请回答下列问题:
①生成物能量总和___(填“大于”“小于”或“等于”)反应物能量总和。
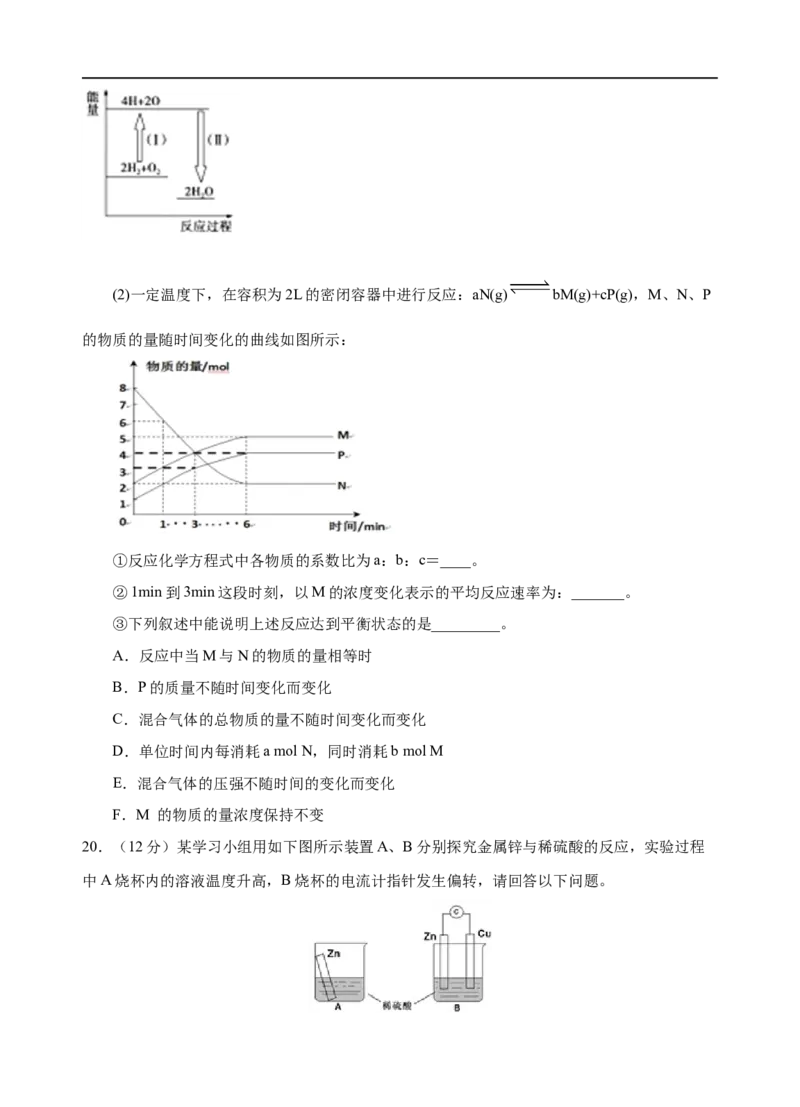
②反应2H+O 2HO的能量变化如图所示。已知拆开1mol H、1mol O 和1mol H—O
2 2 2 2 2
中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)____(填“吸收”或“放
出”)___kJ。(2)一定温度下,在容积为2L的密闭容器中进行反应:aN(g) bM(g)+cP(g),M、N、P
的物质的量随时间变化的曲线如图所示:
①反应化学方程式中各物质的系数比为a:b:c=____。
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:_______。
③下列叙述中能说明上述反应达到平衡状态的是_________。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗a mol N,同时消耗b mol M
E.混合气体的压强不随时间的变化而变化
F.M 的物质的量浓度保持不变
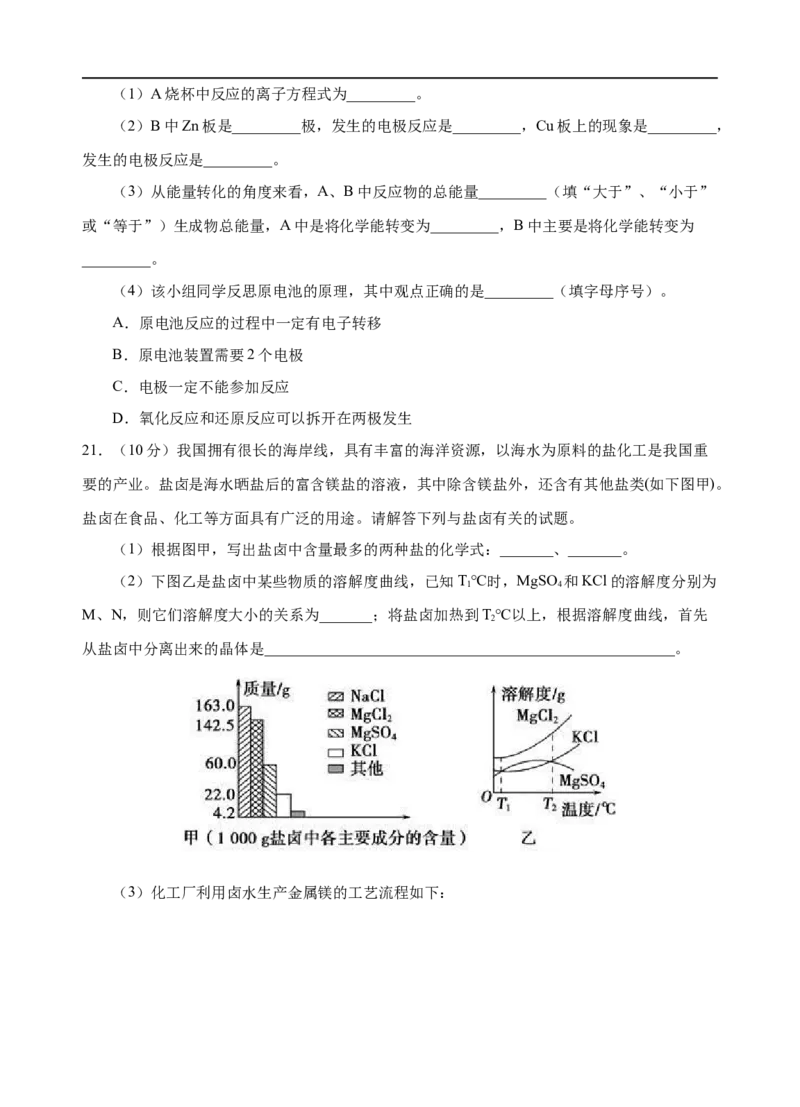
20.(12分)某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程
中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。(1)A烧杯中反应的离子方程式为_________。
(2)B中Zn板是_________极,发生的电极反应是_________,Cu板上的现象是_________,
发生的电极反应是_________。
(3)从能量转化的角度来看,A、B中反应物的总能量_________(填“大于”、“小于”
或“等于”)生成物总能量,A中是将化学能转变为_________,B中主要是将化学能转变为
_________。
(4)该小组同学反思原电池的原理,其中观点正确的是_________(填字母序号)。
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
21.(10分)我国拥有很长的海岸线,具有丰富的海洋资源,以海水为原料的盐化工是我国重
要的产业。盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如下图甲)。
盐卤在食品、化工等方面具有广泛的用途。请解答下列与盐卤有关的试题。
(1)根据图甲,写出盐卤中含量最多的两种盐的化学式:_______、_______。
(2)下图乙是盐卤中某些物质的溶解度曲线,已知T℃时,MgSO 和KCl的溶解度分别为
1 4
M、N,则它们溶解度大小的关系为_______;将盐卤加热到T℃以上,根据溶解度曲线,首先
2
从盐卤中分离出来的晶体是______________________________________________________。
(3)化工厂利用卤水生产金属镁的工艺流程如下:“操作①”的目的是将氢氧化镁沉淀分离出来,操作①的名称是_______。氢氧化镁与试剂
B反应的化学方程式为______________________________。
操作②的名称是_______。该方法的优点为___________________________。
(4)用电解法制备金属镁,两位同学分别设计了下面的两种方法。
甲:电解氯化镁溶液。
乙:电解熔融的氯化镁。
其中同学_______(填“甲”或“乙”)能够成功地制备金属镁,假设生产过程中镁元素没有
损失,则100 g卤水可制备镁_______g。