文档内容
《氮及其化合物》第三课时教学设计
课题 《 氮 及 其 化 合 单元 5 学科 化学 年级 高一
物》第三课时
本节教学内容是人教版高中化学必修第二册第五章《化工生产中的重要非金属元素》
第二节《氮及其化合物》的第三课时。本节内容是典型的元素化合物知识,这一课时的教学
内容主要是硝酸及其化学性质。教材通过浓硝酸的的颜色变化以及硝酸和铜的反应,让我
们认识硝酸的化学性质。硝酸是无机酸中一种十分重要的酸,在工业生产中有重要的应用。
通过硝酸和铜的反应实验,重点掌握硝酸的强氧化性;而通过硝酸的工业制法,也要认识到
硝酸在现代工业中的重要作用。通过硝酸和铜反应实验,进行观察思考,探究认识硝酸的性
质、用途。同时也要在在学习过程中,了解人类活动对自然界氮循环和环境的影响。
Vwijb4Hj2
教材 另外,在硝酸的生产制造过程中,产生了大气污染物。我们要严格遵循新课程标准“关
分析 注人类面临的与化学相关的问题,培养学生的社会责任感、参与意识和决策能力”的要求,
加强环境教育,关注环境问题,要对我们的社会负责,也要对我们的环境负责。在介绍硝酸
的性质与应用时,不止看到化学对我们带来的好处,也要关注化学对我们带来的负面效果。
而解决环境问题,最终的还要从化学学科入手,找到解决的根本方法。我们一定要培养学生
科学的学习态度和方法,为解决我们的环境问题,尽自己的一份力量。
本节安排了“硝酸”,“思考与讨论”,“酸雨及防治”“阅读课本的研究与实
践--------测定雨水的pH”这四部分内容。学生通过学习这部分知识,掌握硝酸的化学性质
以及硝酸的工业制法、酸雨形成以及防治。
宏观辨识与微观探析:通过硝酸和铜的反应实验,了解硝酸的化学性质,同时要了解硝酸的
工业制取原理;对于硝酸,要掌握硝酸的强氧化性,由于浓度的不同,导致生成物不同。
证据推理与模型认知:通过硝酸的工业生产原理,认识到工业生成就在我们身边,要学会理
教学目 论知识和生产的结合,通过理论和生产的结合激发学生学习化学的兴趣。。
标与核 科学探究与创新意识:从现象和结构出发,设计探究方案,探究硝酸和铜实验的原理,在探
心素养 究中互利合作,培养团队精神。
科学精神与社会责任:激发学生透过现象探究本质的兴趣,尊重科学,认真学习科学的学习
方法;通过参与探究过程,培养自身严谨的科学态度和辩证分析能力。同时,我们也要注重
化学知识在现实生活中的应用,注重理论联系实际。
重点 氨和铵盐的化学性质。
难点
教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 玻尔巧藏诺贝尔金质奖章-------玻尔是丹麦的物理学家,
曾获得诺贝尔奖。二战中,玻尔被迫离开祖国,他决定将诺贝
尔金质奖章溶解在一种溶液里,装于玻璃瓶中。后来,纳粹分
子窜进玻尔的住宅,那瓶溶有奖章的溶液就在眼皮底下,他
们却一无所知。战争结束后,玻尔又从溶液中还原提取出金,
并重新铸成奖章。新铸成的奖章---它凝聚着玻尔对祖国无限
的热爱和无穷的智慧。
这种溶液是什么????
讲授新课 第一节 氮及其化合物
一、硝酸
(1)硝酸的物理性质
①纯硝酸是无色、易挥发、有刺激性气味的液体;②能以任意比溶于水;
③密度比水大,(1.5027g/cm3);
④沸点低:83℃;
⑤常用浓硝酸的浓度为69%,98%的浓硝酸叫
作“发烟硝酸”。
(2) 不稳定性
4HNO == 4NO ↑+O ↑+2H O
3 2 2 2
问题一 久置的浓硝酸为何呈黄色?
硝酸分解生成的NO 溶于硝酸中
2
问题二 如何保存硝酸?
盛放在棕色试剂瓶里,并贮放在黑暗且温度低的地方
!!!!硝酸具有强氧化性,对皮肤、衣物等有腐蚀作
用,使用时应注意安全
(3) 硝酸具有强的氧化性,几乎可以使所有金属(金、
铂 除外)氧化而生成硝酸盐。当HNO 与金属反应时,HNO
3 3
被还原的程度(即氮元素化合价降低的程度)取决于硝酸的
浓度和金属单质还原性的强弱。对于同一金属单质而言,
HNO 的浓度越小,HNO 被还原的程度越大,氮元素的化合
3 3
价降低越多。
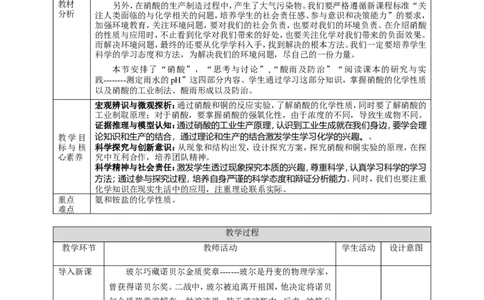
(4)【实验5-8】如图5-14所示,在橡胶塞侧面挖一个凹槽,并嵌入下端
卷成螺旋状的铜丝,向两支试管中分别加入2mL浓硝酸和稀
硝酸,用橡胶塞塞住试管口,使铜丝与硝酸接触,观察并比较
实验现象,向上拉铜丝,停止反应。
①Cu与浓硝酸的反应
实验现象:浓硝酸与铜能剧烈反应,放出红棕色的气体,
铜不断溶解,溶液变成绿色。
反应产物:二氧化氮、硝酸铜和水
化学方程式:Cu+4HNO(浓) =Cu(NO )+2NO↑+2H O
3 3 2 2 2
②Cu与稀硝酸的反应
实验现象:铜与稀硝酸反应较缓慢,溶液变成蓝色,生成
无色的气体,遇空气变为红棕色
反应产物:硝酸铜、一氧化氮、水
化 学 方 程 式 :3Cu+8HNO ( 稀 ) = 3Cu(NO )+
3 3 2
2NO↑+4H O
2
思考:
①在上述的两个反应中硝酸都表现出哪些性质。
氧化性和酸性
②上述两反应中,若有1molCu消耗,则被还
原的硝酸的物质的量分别是多少?
2mol和2/3mol
③写出上述两反应的离子反应方程式
Cu+4H++2NO- =Cu2++2NO↑+2H O
3 2 2
3Cu+8H++2NO-= 3Cu2++ 2NO↑+4H O
3 2
(5)硝酸的化学性质
① 常温下,浓硝酸使铁、铝等金属钝化(加热时也会发
生反应)
②硝酸与金属反应不放出氢气。
③氧化性:浓硝酸>稀硝酸(均比浓硫酸强)
④一般反应规律为:金属 + HNO(浓) → 硝酸盐+ NO ↑+ HO
3 2 2
金属 + HNO(稀) → 硝酸盐+ NO↑+ HO
3 2
较活泼的金属:(如Mg、Zn等) + HNO(极稀) →
3
硝酸盐 + HO + NO↑(或NH 或铵盐等)
2 2 3
⑤变价金属与硝酸反应时
3Fe(过量)+8HNO(稀)=3Fe(NO )+2NO↑+4HO
3 3 2 2
Fe(不足)+4HNO(稀)=Fe(NO )+NO↑+2HO
3 3 3 2
⑥浓HNO 与浓盐酸按体积比1∶3配制而成的混合液
3
叫王水。王水溶解金属的能力更强,能溶解金属Pt、Au。记忆
方法 :“三言(盐)一笑(硝)”
⑦NO -的检验:晶体或浓溶液与浓硫酸、Cu共热时,若
3
产生红棕色气体则含有NO - ;若为稀溶液则先浓缩后再检
3
验。
(6)与非金属的反应
将一块红热的木炭投入浓硝酸中
现象:剧烈反应,产生红棕色气体
△
C+4HNO (浓))======CCOO↑+4NO↑+2H O
3 2 2 2
硝酸:是一元酸、强酸、氧化性酸、低沸点酸、不稳定性
酸、易溶性酸。
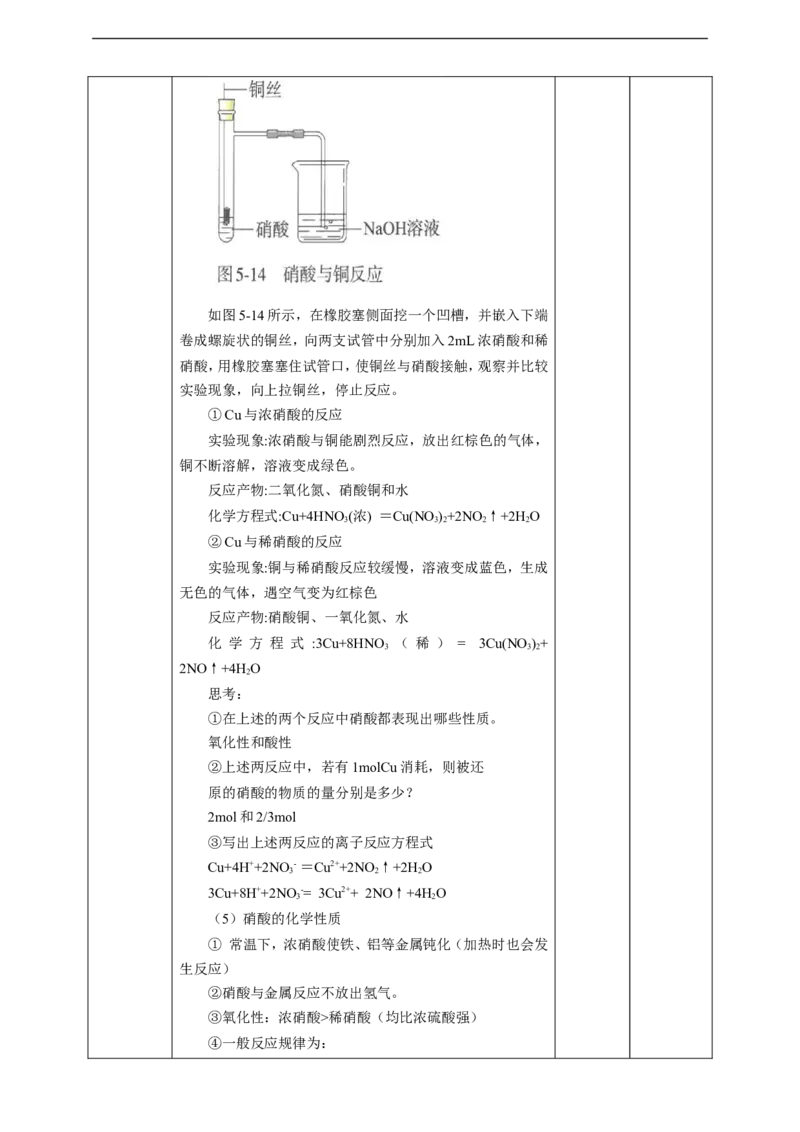
二、思考与讨论
硝酸是重要的化工原料,用于制话费、农药、炸药、燃料
等。工业上制硝酸的原理是将氨经过一系列反应得到硝酸,
如下图所示:
(1)写出每一步反应的化学方程式。
(2)情分析上述反应中的物质;类别和氮元素化合价的
变化情况,以及每一步反应中含氮物质发生的是氧化反应还
是还原反应。
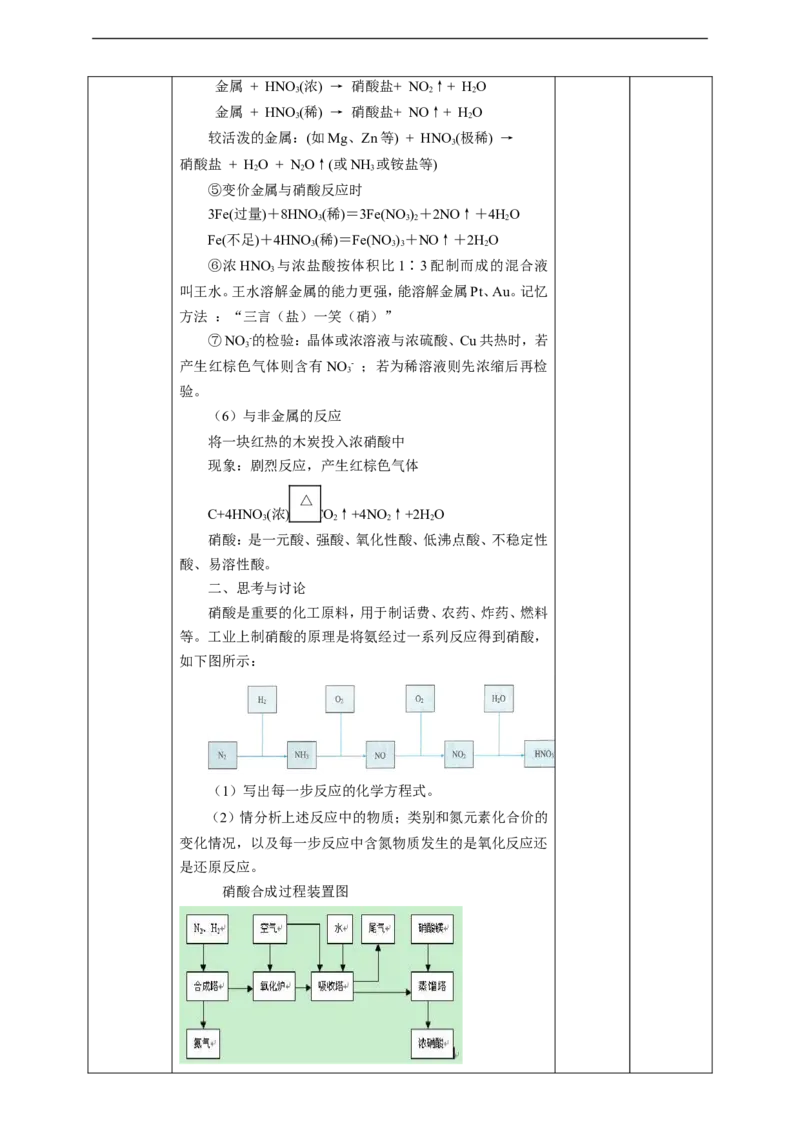
硝酸合成过程装置图1. 硝酸的工业制法-氨的催化氧化法
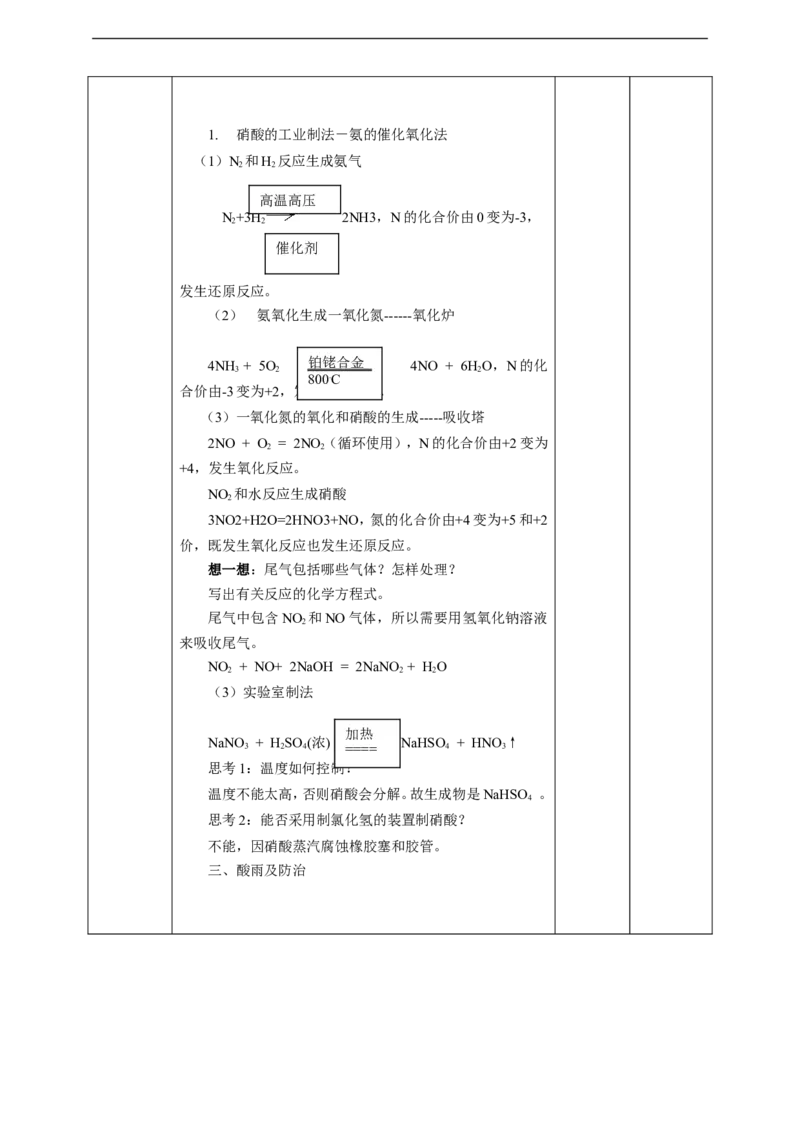
(1)N 和H 反应生成氨气
2 2
高温高压
N++33HH 2NH3,N的化合价由0变为-3,
2 2
催化剂
发生还原反应。
(2) 氨氧化生成一氧化氮------氧化炉
4NH + 5O 铂 铑 合 金 4NO + 6HO,N的化
3 2 2
800.C
合价由-3变为+2,,发发生生氧氧化化反反应应。。
(3)一氧化氮的氧化和硝酸的生成-----吸收塔
2NO + O = 2NO(循环使用),N的化合价由+2变为
2 2
+4,发生氧化反应。
NO 和水反应生成硝酸
2
3NO2+H2O=2HNO3+NO,氮的化合价由+4变为+5和+2
价,既发生氧化反应也发生还原反应。
想一想:尾气包括哪些气体?怎样处理?
写出有关反应的化学方程式。
尾气中包含NO 和NO气体,所以需要用氢氧化钠溶液
2
来吸收尾气。
NO + NO+ 2NaOH = 2NaNO + HO
2 2 2
(3)实验室制法
加热
NaNO + HSO (浓) NaHSO + HNO↑
3 2 4 ==== 4 3
思考1::温温度度如如何何控控制制??
温度不能太高,否则硝酸会分解。故生成物是NaHSO 。
4
思考2:能否采用制氯化氢的装置制硝酸?
不能,因硝酸蒸汽腐蚀橡胶塞和胶管。
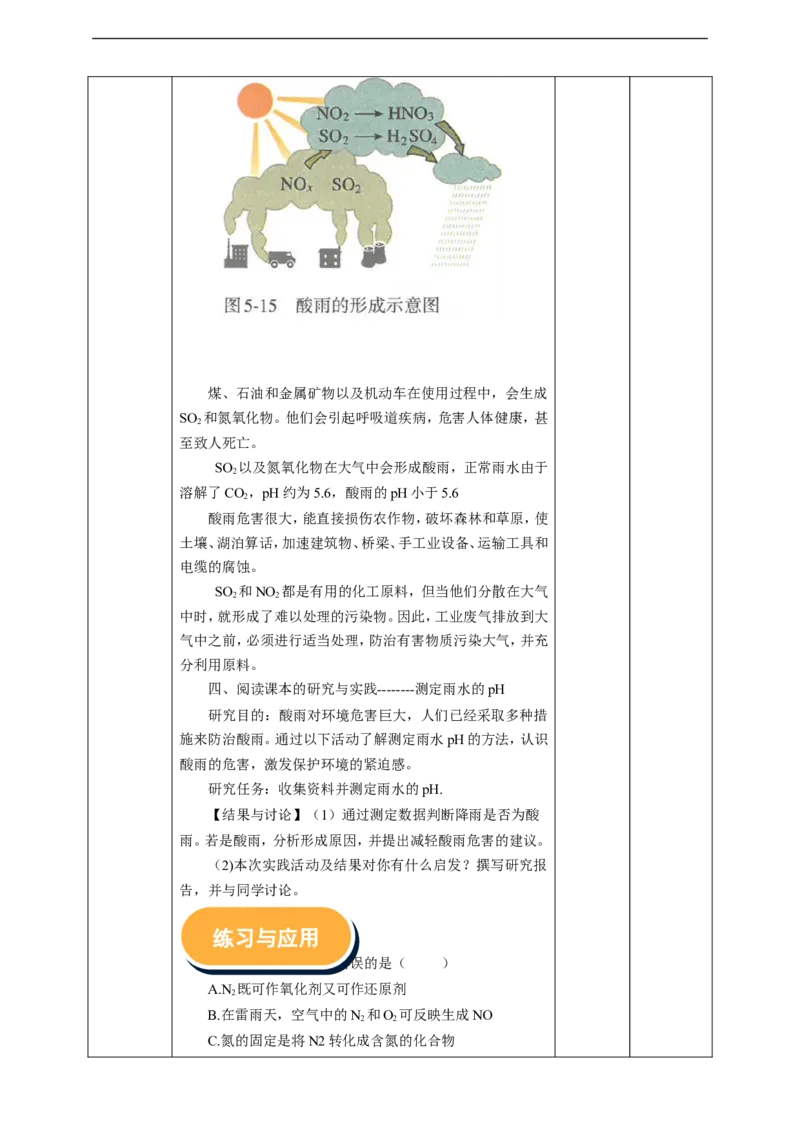
三、酸雨及防治煤、石油和金属矿物以及机动车在使用过程中,会生成
SO 和氮氧化物。他们会引起呼吸道疾病,危害人体健康,甚
2
至致人死亡。
SO 以及氮氧化物在大气中会形成酸雨,正常雨水由于
2
溶解了CO,pH约为5.6,酸雨的pH小于5.6
2
酸雨危害很大,能直接损伤农作物,破坏森林和草原,使
土壤、湖泊算话,加速建筑物、桥梁、手工业设备、运输工具和
电缆的腐蚀。
SO 和NO 都是有用的化工原料,但当他们分散在大气
2 2
中时,就形成了难以处理的污染物。因此,工业废气排放到大
气中之前,必须进行适当处理,防治有害物质污染大气,并充
分利用原料。
四、阅读课本的研究与实践--------测定雨水的pH
研究目的:酸雨对环境危害巨大,人们已经采取多种措
施来防治酸雨。通过以下活动了解测定雨水pH的方法,认识
酸雨的危害,激发保护环境的紧迫感。
研究任务:收集资料并测定雨水的pH.
【结果与讨论】(1)通过测定数据判断降雨是否为酸
雨。若是酸雨,分析形成原因,并提出减轻酸雨危害的建议。
(2)本次实践活动及结果对你有什么启发?撰写研究报
告,并与同学讨论。
练习与应用
练习与应用
1.下列关于N 的叙述错误的是( )
2
A.N 既可作氧化剂又可作还原剂
2
B.在雷雨天,空气中的N 和O 可反映生成NO
2 2
C.氮的固定是将N2转化成含氮的化合物D.1molN 可与3molH 完全反应生成2molNH
2 2 3
答案为:D
解析:N 和H 生成氨气的反应时可逆反应,不
2 2
能完全转化
2. 在NO 与水的反应中()
2
A.氮元素的化合价不发生变化
B.NO 只是氧化剂
2
C.NO 只是还原剂
2
D.NO 既是氧化剂,有事还原剂
2
答案为:D
解析:3NO +H O=2HNO +NO,反应中NO 的化合价
2 2 3 2
由+4价变为+5和+2价既是氧化剂又是还原剂。
3.只用一种试剂可将NH Cl、(NH )SO 、NaCl、NaSO 四
4 4 2 4 2 4
种溶液区别开来的是( )
A. NaOH溶液 B. AgNO 溶液
3
C. BaCl 溶液 D. Ba(OH) 溶液
2 2
答案为:D
解析:A.氯化铵、硫酸铵均与NaOH反应生成氨气,氯化
钠、硫酸钠均与NaOH不反应,不能鉴别;
B.均与硝酸银反应生成白色沉淀,不能鉴别;
C.硫酸铵、硫酸钠均与氯化钡反应生成白色沉淀,氯化
铵、氯化钠均与氯化钡不反应,不能鉴别;
D.氯化铵、硫酸铵、氯化钠、硫酸钠四种溶液分别与Ba
(OH)溶液反应的现象为:刺激性气体、白色沉淀和刺激性
2
气体、无现象、白色沉淀,现象不同,可鉴别;
4.根据图5-11“氨溶于水的喷泉实验装置”,下列叙述不
正确的是( )
A.该实验说明氨气极易溶于水
B.烧瓶充满氯气,交投滴管和烧瓶中充满浓碱也可能形
成喷泉
C.红色喷泉说明氨水有碱性
D.烧杯中换成其他液体无法形成喷泉
答案为:D
解析:喷泉反应的原理是可以快速溶解或者反应形成压
强差,所以换成其他液体也可以。
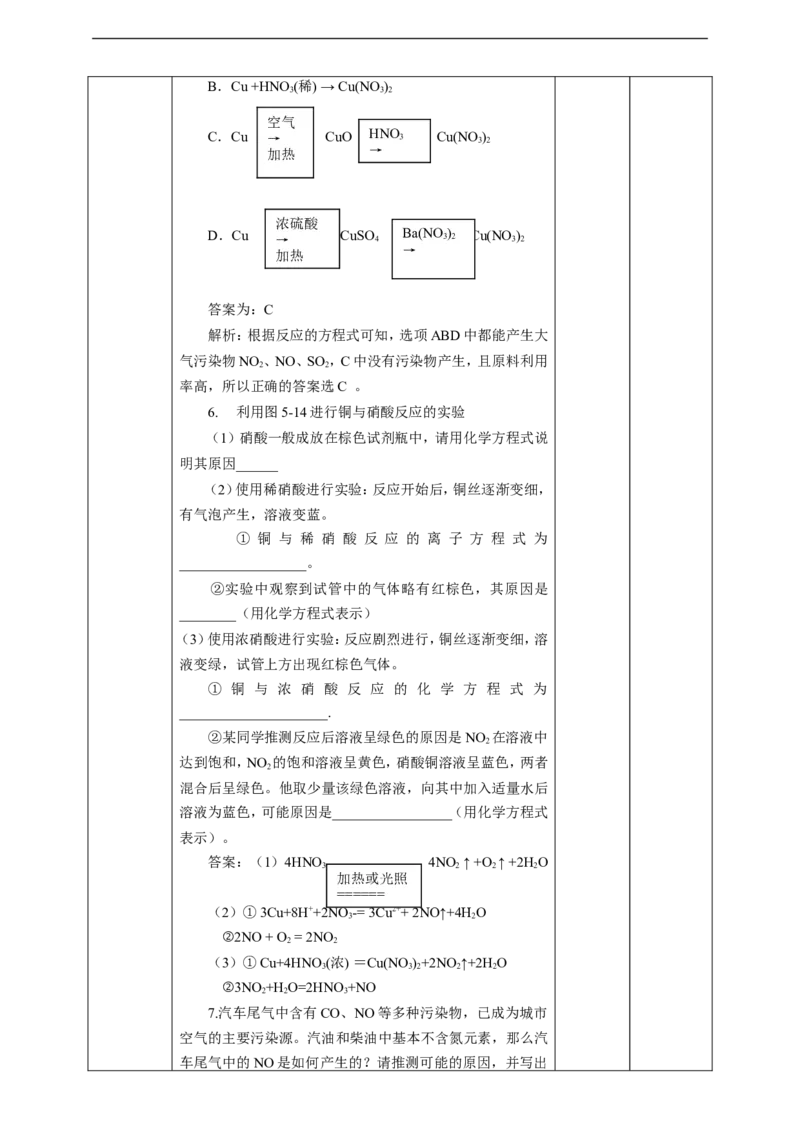
5.工业上用废铜屑作原料制备硝酸铜,下列四种方法中,
适宜采用的是哪一种,请从节约原料和污染保护的角度说明
原因。
A.Cu + HNO (浓) → Cu(NO )
3 3 2B.Cu +HNO(稀) → Cu(NO )
3 3 2
空气
C.Cu → CuO H NO 3 Cu(NO 3 ) 2
加热 →
浓硫酸
D.Cu → CuSO 4 B a (NO 3 ) 2 Cu(NO 3 ) 2
→
加热
答案为:C
解析:根据反应的方程式可知,选项ABD中都能产生大
气污染物NO 、NO、SO ,C中没有污染物产生,且原料利用
2 2
率高,所以正确的答案选C 。
6. 利用图5-14进行铜与硝酸反应的实验
(1)硝酸一般成放在棕色试剂瓶中,请用化学方程式说
明其原因______
(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,
有气泡产生,溶液变蓝。
① 铜 与 稀 硝 酸 反 应 的 离 子 方 程 式 为
__________________。
②实验中观察到试管中的气体略有红棕色,其原因是
________(用化学方程式表示)
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶
液变绿,试管上方出现红棕色气体。
① 铜 与 浓 硝 酸 反 应 的 化 学 方 程 式 为
_____________________.
②某同学推测反应后溶液呈绿色的原因是NO 在溶液中
2
达到饱和,NO 的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者
2
混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后
溶液为蓝色,可能原因是_________________(用化学方程式
表示)。
答案:(1)4HNO 4NO ↑ +O ↑ +2H O
3 2 2 2
加热或光照
======
(2)①3Cu+8H+++22NNOO-= 3Cu2+++ 22NNOO↑↑++44HH O
3 2
②2NO + O = 2NO
2 2
(3)①Cu+4HNO (浓) =Cu(NO )+2NO↑+2H O
3 3 2 2 2
②3NO +H O=2HNO +NO
2 2 3
7.汽车尾气中含有CO、NO等多种污染物,已成为城市
空气的主要污染源。汽油和柴油中基本不含氮元素,那么汽
车尾气中的NO是如何产生的?请推测可能的原因,并写出有关反应的化学方程式。
放电
解答:N
2
+O
2
= = = 2NO;
8.根据图5-9简简简单单单描描描述述述氮氮氮在在在自自自然然然界界界的的的循循循环环环过过过 程程程,,,并并并思思思
考和讨论一下问题。
(1)氮在自然界中主要以哪些形式存在?
(2)人体蛋白质中的氮是从哪里来的?
(3)自然界中有哪些固定氮的途径?
(4)人类的哪些活动参与了氮的循环
解答:
(1)氮以化合态的形式存在于多种无机物和有机物中。
(2)从食物中来。
(3)生物固氮,高能固氮,工业固氮。
(4)工业固氮,人的排遗。
课堂小结 一、硝酸的化学性质
①硝酸的不稳定性
②浓硝酸和铜的反应
③稀硝酸和铜的反应
二、硝酸的工业制法
硝酸工业制法的的流程。
板书 一、硝酸的化学性质
二、硝酸的工业制法
三、酸雨及防治
四、阅读课本的研究与实践--------测定雨水的pH