文档内容
高二化学上学期期中测试卷 01
(考试时间:90分钟 满分100分)
考试范围:新教材人教版选择性必修1第一、二、三章
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 S 32 Cl 35.5
K 39 Ca 40 Fe 56 Cu 64 Ge 73 Ag 108 Ba 137
选择题部分
一、选择题(本大题共20小题,每小题2分,共40分。每个小题列出的四个备选项中只有一个是符合
题目要求的,不选、多选、错选均不得分)
1.反应进行的方向是化学反应原理的三个重要组成部分之一、下列说法中正确的是( )
A. , 的反应一定可以自发进行
B.根据反应的自发性可以预测该反应发生的快慢
C.可逆反应正向进行时,正反应具有自发性, 一定小于零
D.常温下,反应C(s)+ CO (g) 2CO(g)不能自发进行,该反应的ΔH>0
2
2.硫酸是当今世界上最重要的化工产品之一,广泛应用于工业各个方面。硫酸的生产工艺几经改进,
目前工业上主要采用接触法制备硫酸。接触室中发生如下反应:2SO + O 2SO 。该反应也是放
2 2 3
热反应,下列说法不正确的是( )
A.形成SO 中的硫氧键放出能量 B.断开SO 中的硫氧键放出能量
3 2
C.反应物的总能量大于生成物的总能量 D.放热反应的逆反应一定是吸热反应
3.在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl氧化为Cl:4HCl(g)+O (g)=2HO(g)
2 2 2 2 2 2
+2Cl(g) ΔH<0,下列有关说法不正确的是( )
2
A.降低温度,可提高Cl 产率
2
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
4.化学反应中的能量变化,通常主要表现为热量的变化。下列相关表述正确的是( )
A.一定条件下,将0.5molH(g)和0.5molI(g)置于密闭容器中充分反应生成 放热 ,其热化学方
2 2
程式为:I(g )+H (g) 2HI(g) H=-2akJ•mol-1
2 2
△B.在101kPa时,2 g H 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学方程式
2
表示为:
C.S(g)+ O (g)=SO(g) ΔH S(g)+ O (g)=SO(g) ΔH ΔH>ΔH
2 2 1 2 2 2 1 2
D.HCl和NaOH反应的中和热 ,则0.5molHSO 和足量Ba(OH) 反应的
2 4 2
5.常温下,下列说法正确的是( )
A. 的HA溶液与 的ROH溶液任意比混合:c(R+)+c(H+)=c(A-)+c(OH-)
B.pH相等的NH Cl、HCl和(NH )SO 三种溶液: c(HCl)<c(NH Cl)<c[(NH )SO ]
4 4 2 4 4 4 2 4
C.中和等体积等pH的盐酸和醋酸,消耗氢氧化钠的物质的量相等
D.分别向等体积等pH的氢氧化钾和醋酸钾溶液中加入等体积的水,pH变化大的是醋酸伽
6.下列说法正确的是( )
A.某酸和某碱等体积混合,充分反应后,溶液呈酸性,可以推测BOH为弱碱
B.pH=1的盐酸和pH=11的氨水等体积混合后,恰好完全反应,则所用盐酸和氨水的物质的量浓度相
等
C.pH=7的NaCl溶液和pH=7的CHCOONH 溶液,水的电离程度相同
3 4
D.同物质的量浓度的盐酸与醋酸分别中和同体积同浓度的NaOH溶液,消耗醋酸的体积多
7.某反应的反应机理可以分成如下两步,下列说法正确的是( )
第一步反应 第二步反应
反应机理
NO +CO=NO+CO (快反
2NO =NO+NO (慢反应) 3 2 2
2 3 应)
A.第一步反应的活化能高于第二步反应的活化能
B.该反应的总反应方程式为NO+CO =NO+CO
2 2
C.该反应的速率主要由第二步反应决定
D.加入合适的催化剂既可以加快反应速率,又可以提高NO 的转化率
2
8.我国科技工作者研究利用 (氢型 分子筛)为载体,以CO 和氢气为原料合
2
成绿色燃料甲醚。一定条件下发生反应:2CO(g)+6H(g) CHOCH (g)+3HO(g)
2 2 3 3 2
H=-123.8kJ·mol-1。下列叙述正确的是( )
1
△ A.恒容时,升高温度,CO 2 的平衡转化率增大
B.恒容恒温时,及时分离出甲醚,平衡右移,反应速率增大C.恒容恒温时,增大c(CO),反应物转化率均增大
2
D. 是该反应的催化剂,可加快反应速率
9.常温下,下列有关说法不正确的是( )
A.pH=13的氨水、NaOH溶液中,c(NH +)=c(Na+)
4
B.某氨水的pH=x,某盐酸的pH=14-x,两者等体积混合后,pH>7
C.等pH的盐酸和氯化铵两种溶液,导电能力相同
D.向0.1 mol•L-1的HS溶液中加入一定量的NaOH溶液,当溶液中存在:c(Na+)=c(S2-)+c(HS-)+c(H S)
2 2
时,溶液的主要溶质为NaHS
10.已知常温下CHCOOH和NH ·H O的电离平衡常数分别为K、K 。若在常温下向0.1 mol·L-1的醋
3 3 2 a b
酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是( )
A.加入氨水的过程中,溶液的导电性一直不断增强
B.CHCOONH 在水溶液中的水解平衡常数K =
3 4 h
C.若K≈K ,当加入等体积的氨水时,溶液基本呈中性
a b
D.该等式在滴加过程中始终成立c(CHCOO-)+c(CHCOOH)=c(NH)+c(NH ·H O)
3 3 3 2
11.室温下,向 溶液中逐滴加入 溶液,溶液 与所加
溶液体积(V)的关系如下表所示:
A B C D E F
V/mL 5 10 15 20 40
pH 4 4.5 7 7.8
下列说法不正确的是( )
A.F点时,离子浓度大小关系:c(Na+)>c(OH―)>c(X-)>c(H+)
B.E点的n(Na+)与 点的n(HX) + n(X-)的值相等
C.由B点可得:
D.随着NaOH滴入,溶液中c(Na+)+ c(HX)+ c(X-)的值逐渐减小
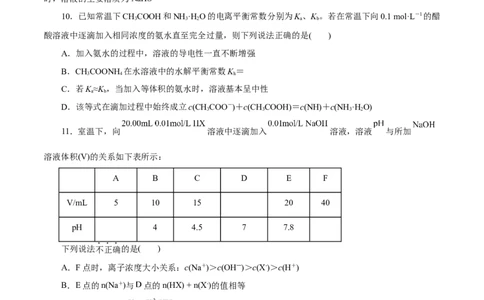
12.研究表明,在一定条件下,气态HCN(a)与HNC(b)两种分子的互变反应过程能量变化如图所示。
下列说法正确的是( )A.HNC比HCN更稳定
B.HCN转化为HNC,反应条件一定要加热
C.HNC(g) HCN(g) ΔH=-59.3 kJ·mol-1
D.加入催化剂,可以减小反应的热效应
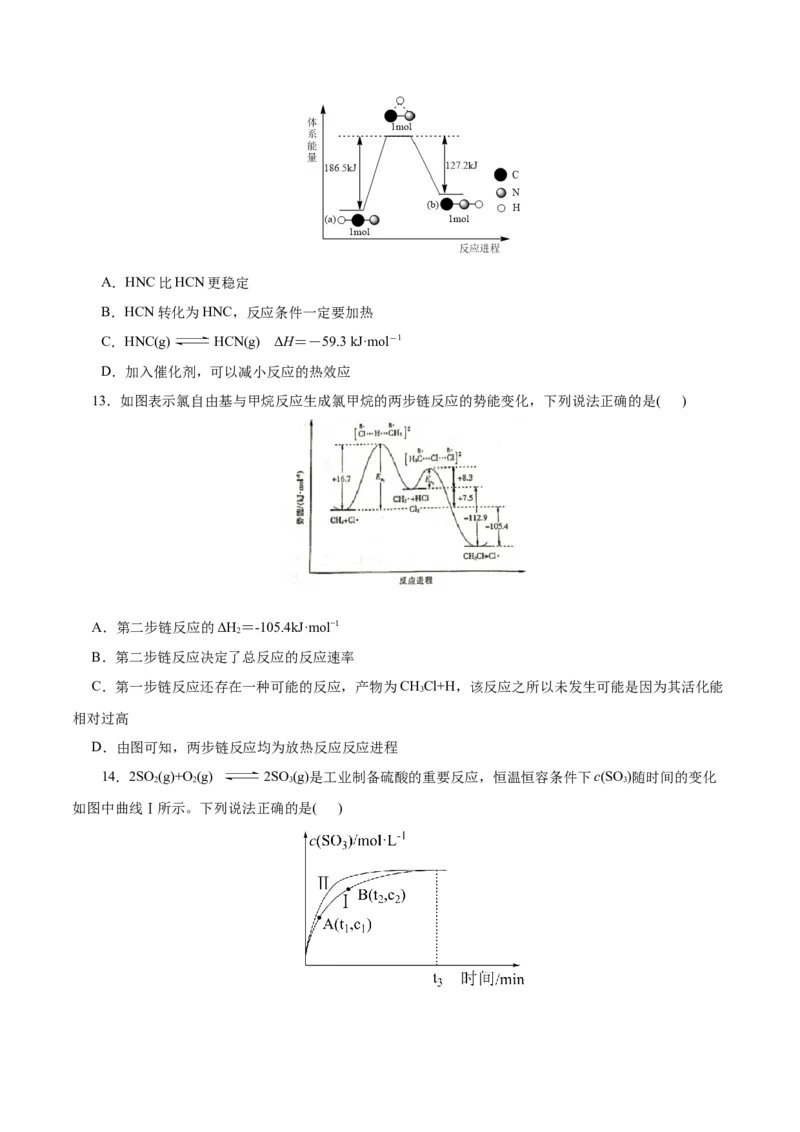
13.如图表示氯自由基与甲烷反应生成氯甲烷的两步链反应的势能变化,下列说法正确的是( )
A.第二步链反应的ΔH=-105.4kJ·mol−1
2
B.第二步链反应决定了总反应的反应速率
C.第一步链反应还存在一种可能的反应,产物为CHCl+H,该反应之所以未发生可能是因为其活化能
3
相对过高
D.由图可知,两步链反应均为放热反应反应进程
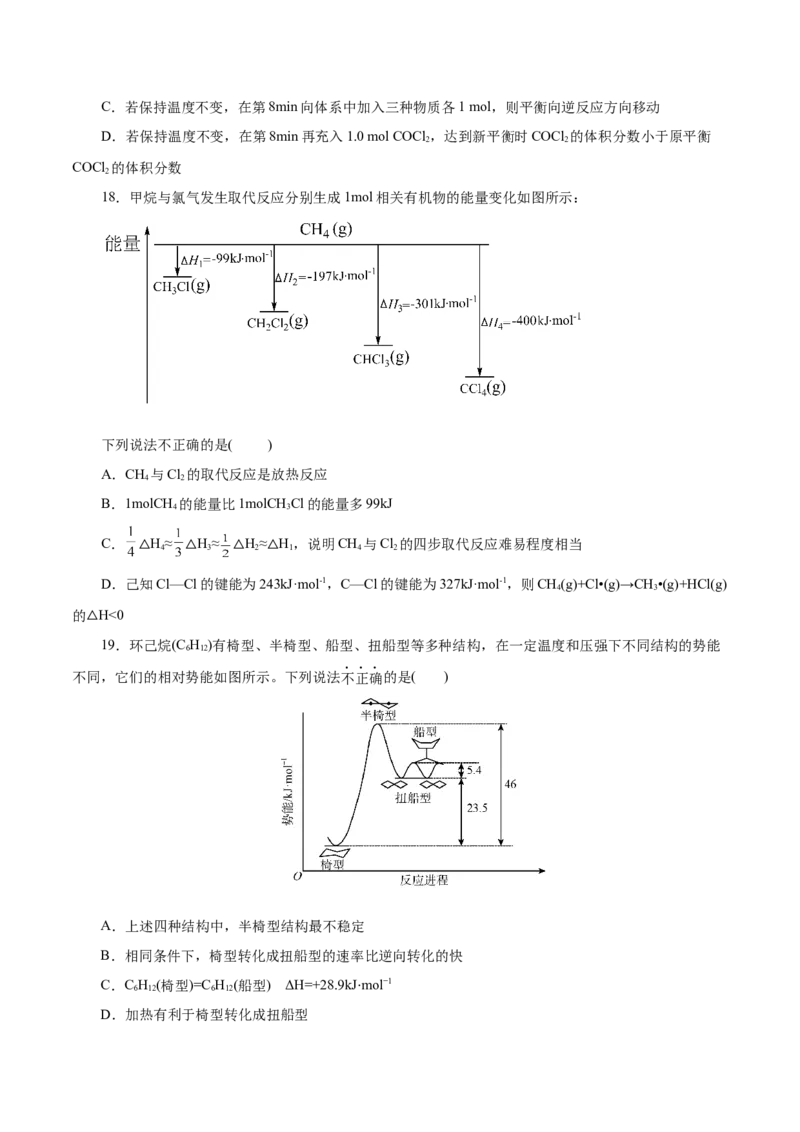
14.2SO (g)+O(g) 2SO (g)是工业制备硫酸的重要反应,恒温恒容条件下c(SO )随时间的变化
2 2 3 3
如图中曲线Ⅰ所示。下列说法正确的是( )A.t~tmin,v(SO ) = mol·L-1·min-1
1 2 3 正
B.曲线Ⅱ对应的条件改变可能是增大了压强
C.工业上采用高温高压的反应条件以提高SO 的转化率
2
D.相同条件下,t 时再充入与起始投料等量的反应物,达到平衡后,SO 转化率增大
3 2
15.已知NaHCO 溶液与盐酸,反应生成CO 吸热,NaCO 溶液与盐酸反应生成CO 放热。关于下列
3 2 2 3 2
△H的判断正确的是( )
CO2-(aq)+H+(aq)= HCO -(aq) ΔH
3 3 1
HCO -(aq)+H+(aq)= HCO(aq) ΔH
3 2 3 2
HCO(aq) CO(g)+HO(l) ΔH
2 3 2 2 3
CO(g)+HO(l)+CO 2-(aq)=2 HCO -(aq) ΔH
2 2 3 3 4
A.ΔH<0,ΔH>0 B.ΔH+ΔH >0
1 2 2 3
C.ΔH+ΔH +ΔH >0 D.ΔH<ΔH
1 2 3 1 4
16.相同温度和压强下,有如下热化学方程式,下列叙述正确的是( )
N(g)+4H(g) +Cl(g) 2NH Cl(s) ΔH
2 2 2 4 1
NH (g)+ H+(g) NH +(g) ΔH
3 4 2
H(g)+Cl(g) 2H+(g)+ Cl-(g) ΔH =3066kJ·mol−1
2 2 2
N(g)+3H(g) 2NH (g) ΔH
2 2 3 4
NH (g)+HCl(g) NH Cl(s) ΔH <0
3 4 5
A.ΔH<ΔH B.ΔH<0,ΔH>0
1 4 1 2
C.H-Cl键键能为1533 kJ·mol−1 D.ΔH=2ΔH+ΔH+ΔH+2ΔH
1 2 3 4 5
17.一定条件下,在1.0L的密闭容器中进行反应:Cl (g)+ CO(g) COCl (g)。
2 2
反应过程中的有关数据见表:
0 2 6 8
2.4 1.6 0.6
2 0.2
0
下列说法正确的是( )
A.2 时,用CO表示的化学反应速率为0.75 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(COCl )=1.5mol/L,则反应的ΔH<0
2C.若保持温度不变,在第8min向体系中加入三种物质各1 mol,则平衡向逆反应方向移动
D.若保持温度不变,在第8min再充入1.0 mol COCl ,达到新平衡时COCl 的体积分数小于原平衡
2 2
COCl 的体积分数
2
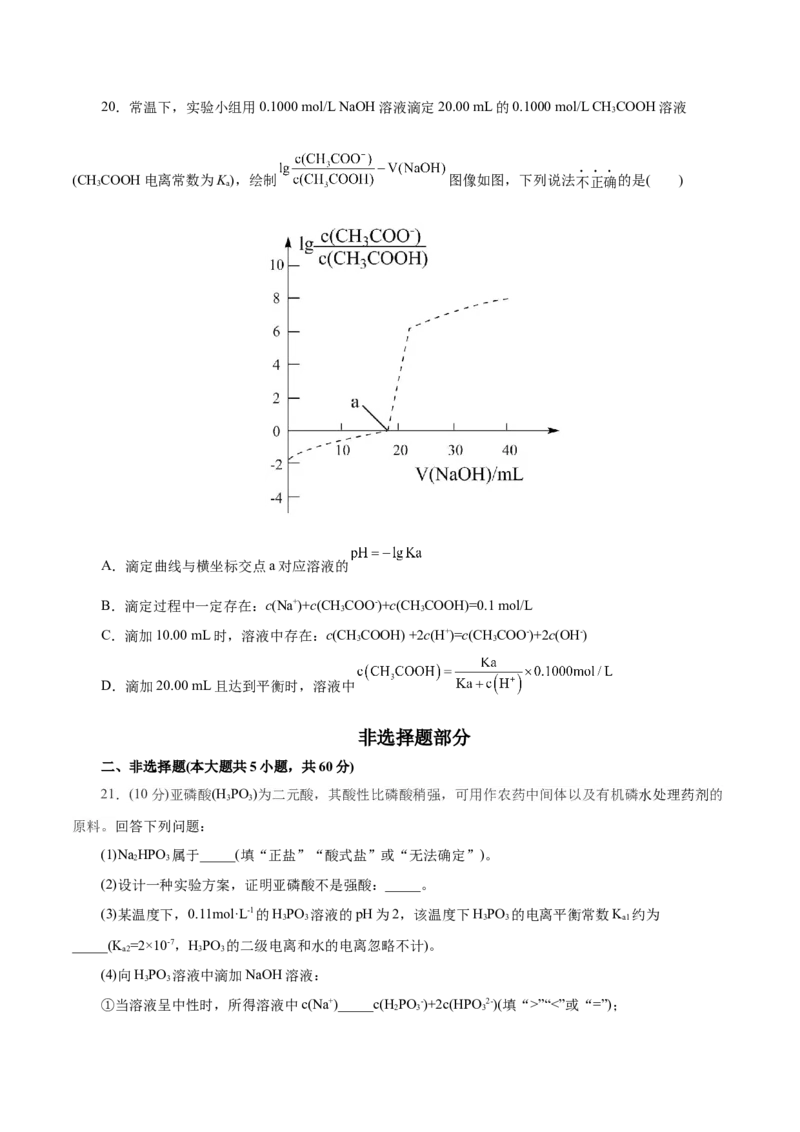
18.甲烷与氯气发生取代反应分别生成1mol相关有机物的能量变化如图所示:
下列说法不正确的是( )
A.CH 与Cl 的取代反应是放热反应
4 2
B.1molCH 的能量比1molCH Cl的能量多99kJ
4 3
C. H≈ H≈ H≈ H,说明CH 与Cl 的四步取代反应难易程度相当
4 3 2 1 4 2
△ △ △ △
D.己知Cl—Cl的键能为243kJ·mol-1,C—Cl的键能为327kJ·mol-1,则CH(g)+Cl•(g)→CH •(g)+HCl(g)
4 3
的 H<0
△19.环己烷(C
6
H
12
)有椅型、半椅型、船型、扭船型等多种结构,在一定温度和压强下不同结构的势能
不同,它们的相对势能如图所示。下列说法不正确的是( )
A.上述四种结构中,半椅型结构最不稳定
B.相同条件下,椅型转化成扭船型的速率比逆向转化的快
C.C H (椅型)=C H (船型) ΔH=+28.9kJmol−1
6 12 6 12
D.加热有利于椅型转化成扭船型 ⋅20.常温下,实验小组用0.1000 mol/L NaOH溶液滴定20.00 mL的0.1000 mol/L CH COOH溶液
3
(CHCOOH电离常数为K),绘制 图像如图,下列说法不正确的是( )
3 a
A.滴定曲线与横坐标交点a对应溶液的
B.滴定过程中一定存在:c(Na+)+c(CHCOO-)+c(CHCOOH)=0.1 mol/L
3 3
C.滴加10.00 mL时,溶液中存在:c(CHCOOH) +2c(H+)=c(CHCOO-)+2c(OH-)
3 3
D.滴加20.00 mL且达到平衡时,溶液中
非选择题部分
二、非选择题(本大题共5小题,共60分)
21.(10分)亚磷酸(H PO )为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的
3 3
原料。回答下列问题:
(1)Na HPO 属于_____(填“正盐”“酸式盐”或“无法确定”)。
2 3
(2)设计一种实验方案,证明亚磷酸不是强酸:_____。
(3)某温度下,0.11mol·L-1的HPO 溶液的pH为2,该温度下HPO 的电离平衡常数K 约为
3 3 3 3 a1
_____(K =2×10-7,HPO 的二级电离和水的电离忽略不计)。
a2 3 3
(4)向HPO 溶液中滴加NaOH溶液:
3 3
①当溶液呈中性时,所得溶液中c(Na+)_____c(HPO -)+2c(HPO 2-)(填“>”“<”或“=”);
2 3 3②若用甲基橙做指示剂,用NaOH溶液滴定,达到滴定终点时,所得溶液中c(Na+)____c(HPO -)
2 3
+2c(HPO2-)(填“>”“<”或“=”)。
3
22.(11分)乙二酸(HOOC—COOH)俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。回
答下列问题:
(1)在恒温、恒容密闭容器中发生反应:HC O(s) HO(g)+CO(g)+CO (g),下列描述能说明反应
2 2 4 2 2
已经达到平衡状态的是____________(填标号)。
A.压强不再变化 B.CO(g)的体积分数保持不变
2
C.混合气体密度不再变化 D.混合气体平均摩尔质量保持不变
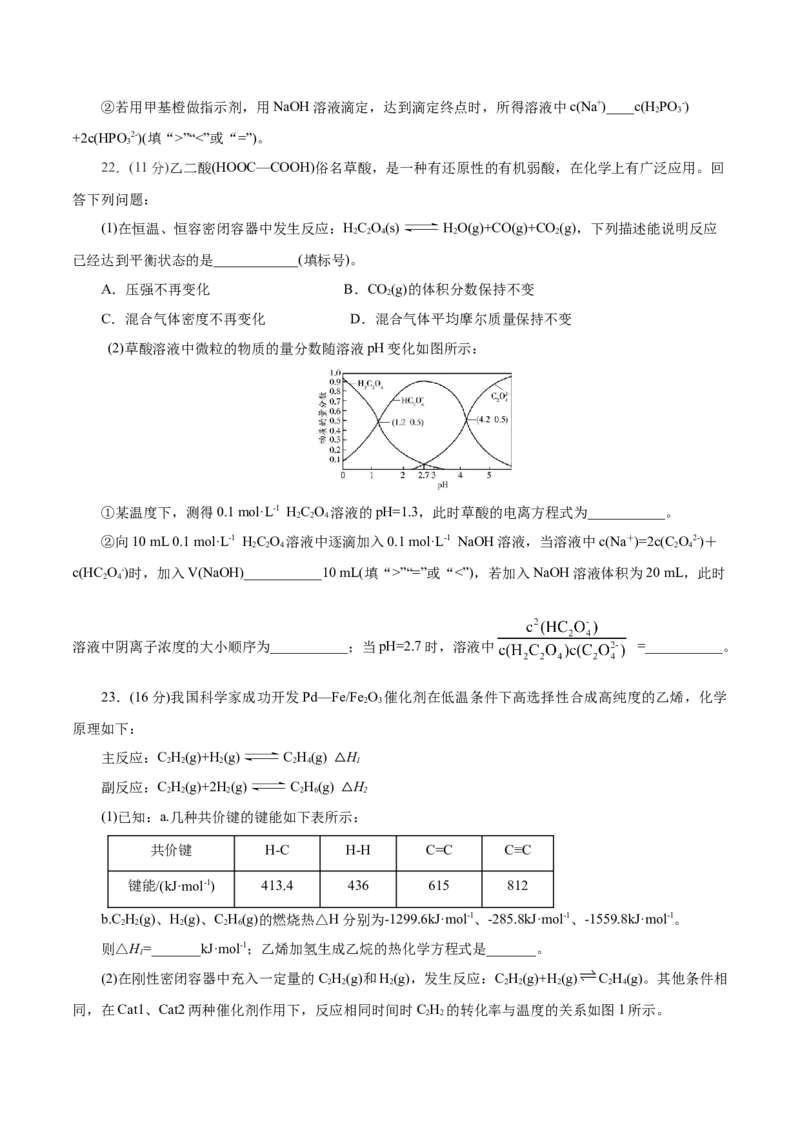
(2)草酸溶液中微粒的物质的量分数随溶液pH变化如图所示:
①某温度下,测得0.1 mol·L-1 HC O 溶液的pH=1.3,此时草酸的电离方程式为___________。
2 2 4
②向10 mL 0.1 mol·L-1 HC O 溶液中逐滴加入0.1 mol·L-1 NaOH溶液,当溶液中c(Na+)=2c(C O2-)+
2 2 4 2 4
c(HC O-)时,加入V(NaOH)___________10 mL(填“>”“=”或“<”),若加入NaOH溶液体积为20 mL,此时
2 4
溶液中阴离子浓度的大小顺序为___________;当pH=2.7时,溶液中 =___________。
23.(16分)我国科学家成功开发Pd—Fe/Fe O 催化剂在低温条件下高选择性合成高纯度的乙烯,化学
2 3
原理如下:
主反应:C H(g)+H(g) C H(g) H
2 2 2 2 4 1
副反应:C
2
H
2
(g)+2H
2
(g) C
2
H
6
(g)△ H
2
(1)已知:a.几种共价键的键能如下表所示△:
共价键 H-C H-H C=C C≡C
键能/(kJ·mol-1) 413.4 436 615 812
b.C H(g)、H(g)、C H(g)的燃烧热△H分别为-1299.6kJ·mol-1、-285.8kJ·mol-1、-1559.8kJ·mol-1。
2 2 2 2 6
则△H=_______kJ·mol-1;乙烯加氢生成乙烷的热化学方程式是_______。
1
(2)在刚性密闭容器中充入一定量的C H(g)和H(g),发生反应:C H(g)+H(g) C H(g)。其他条件相
2 2 2 2 2 2 2 4
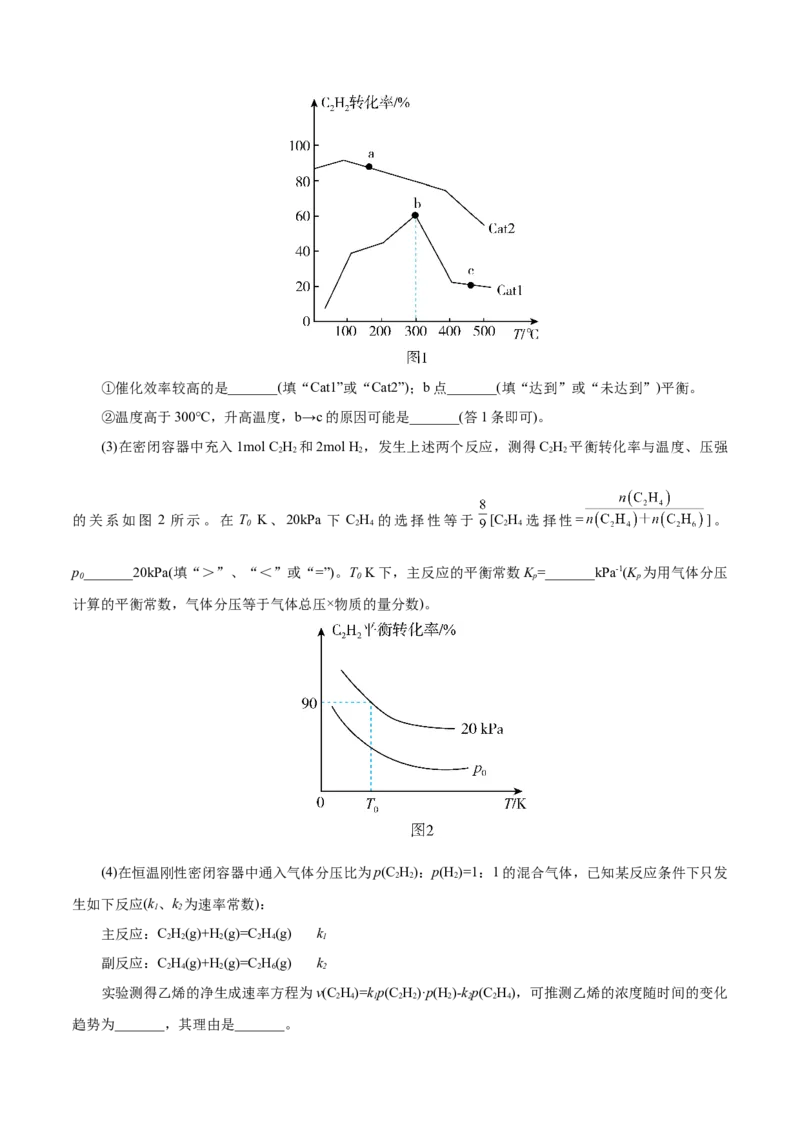
同,在Cat1、Cat2两种催化剂作用下,反应相同时间时C H 的转化率与温度的关系如图1所示。
2 2①催化效率较高的是_______(填“Cat1”或“Cat2”);b点_______(填“达到”或“未达到”)平衡。
②温度高于300℃,升高温度,b→c的原因可能是_______(答1条即可)。
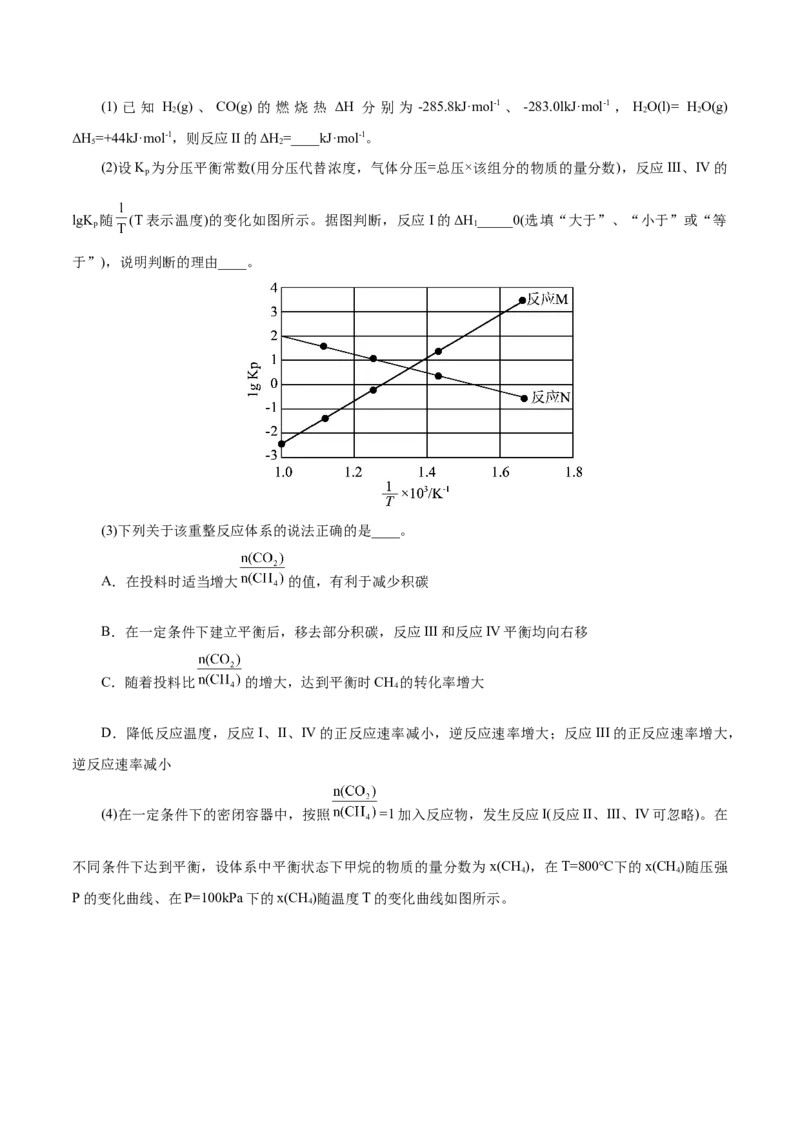
(3)在密闭容器中充入1mol C H 和2mol H ,发生上述两个反应,测得C H 平衡转化率与温度、压强
2 2 2 2 2
的关系如图 2 所示。在 T K、20kPa 下 C H 的选择性等于 [C H 选择性= ]。
0 2 4 2 4
p_______20kPa(填“>”、“<”或“=”)。T K下,主反应的平衡常数K =_______kPa-1(K 为用气体分压
0 0 p p
计算的平衡常数,气体分压等于气体总压×物质的量分数)。
(4)在恒温刚性密闭容器中通入气体分压比为p(C H):p(H )=1:1的混合气体,已知某反应条件下只发
2 2 2
生如下反应(k、k 为速率常数):
1 2
主反应:C H(g)+H(g)=C H(g) k
2 2 2 2 4 1
副反应:C H(g)+H(g)=C H(g) k
2 4 2 2 6 2
实验测得乙烯的净生成速率方程为v(C H)=kp(C H)·p(H )-kp(C H),可推测乙烯的浓度随时间的变化
2 4 1 2 2 2 2 2 4
趋势为_______,其理由是_______。24.(11分)硫酸是化学工业当中最基本也是最重要的化工原料之一,硫酸的产量是衡量一个国家化工
水平的标志。请回答:
(1)工业上大规模制备浓硫酸一般采用硫铁矿或硫磺粉为原料。
①298K,101kPa下,下列反应
S(g)+O(g) SO (g) ΔH=-296.83kJ·mol−1
2 2
S(g)+3/2O (g) SO (g) ΔH=-395.70kJ·mol−1
2 3
则反应SO (g)+1/2O (g) SO (g)能自发进行的条件是_______。
2 2 3
②两种方法在制备工艺上各有其优缺点,下列选项正确的是(可多选)_______。
A.在制备SO 阶段,硫铁矿法产生较多的矿渣,且生成的气体净化处理比硫磺粉法复杂得多
2
B.两种方法产生的气体都不需要干燥
C.在SO 转化为SO 阶段,控制温度在500℃左右的主要原因是为了提高反应速率和平衡转化率
2 3
D.将原料粉碎后送入沸腾炉中,可以提高原料的利用率
(2)对于反应2SO (g)+O(g) 2SO (g)
2 2 3
①某温度下,假设进入接触室内SO 的物质的量恒定。当SO 和O 的物质的量比为1∶1,反应达到平
2 2 2
衡时压强减少1/5;保持温度不变欲使 的平衡转化率提高到90%,则O 和SO 的物质的量比为应为
2 2
_______(计算结果保留1位小数)。
②VO 催化氧化SO 的反应过程可分为三步,请写出步骤Ⅱ的化学方程式:
2 5 2
步骤Ⅰ:VO+ SO = VO+SO
2 5 2 2 4 3
步骤Ⅱ:_______。
步骤Ⅲ:2VOSO=V O+SO+SO
4 2 5 2 3
(3) SO 能溶于液态SO 中,并存在如下两个平衡(未配平)
3 2
SO +SO SO 2-+SO2+
2 3 4
SO +SO SO2-+SO2+
2 3 2 7
当稀释SO 时,c(SO 2-)/ c(S O2-)的值_______(增大、减小或不变),理由是_______。
3 4 2 7
25.(12分)我国力争2060年前实现碳中和。CH 与CO 催化重整是实现碳中和的热点研究课题。该催
4 2
化重整反应体系主要涉及以下反应:
反应I:主反应CH(g)+CO (g) 2CO(g)+2H(g) ΔH K
4 2 2 1 p1
反应II:副反应CO(g)+H(g) CO(g)+HO(g) ΔH K
2 2 2 2 p2
反应III:积碳反应2CO(g) CO(g)+C(s) ΔH K
2 3 p3
反应IV:积碳反应CH(g) C(s)+2H(g) ΔH K
4 2 4 p4(1) 已 知 H(g) 、 CO(g) 的 燃 烧 热 ΔH 分 别 为 -285.8kJ·mol-1 、 -283.0lkJ·mol-1 , HO(l)= H O(g)
2 2 2
ΔH=+44kJ·mol-1,则反应II的ΔH=____kJ·mol-1。
5 2
(2)设K 为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应III、IV的
p
lgK 随 (T表示温度)的变化如图所示。据图判断,反应 I的ΔH_____0(选填“大于”、“小于”或“等
p 1
于”),说明判断的理由____。
(3)下列关于该重整反应体系的说法正确的是____。
A.在投料时适当增大 的值,有利于减少积碳
B.在一定条件下建立平衡后,移去部分积碳,反应III和反应IV平衡均向右移
C.随着投料比 的增大,达到平衡时CH 的转化率增大
4
D.降低反应温度,反应I、II、IV的正反应速率减小,逆反应速率增大;反应III的正反应速率增大,
逆反应速率减小
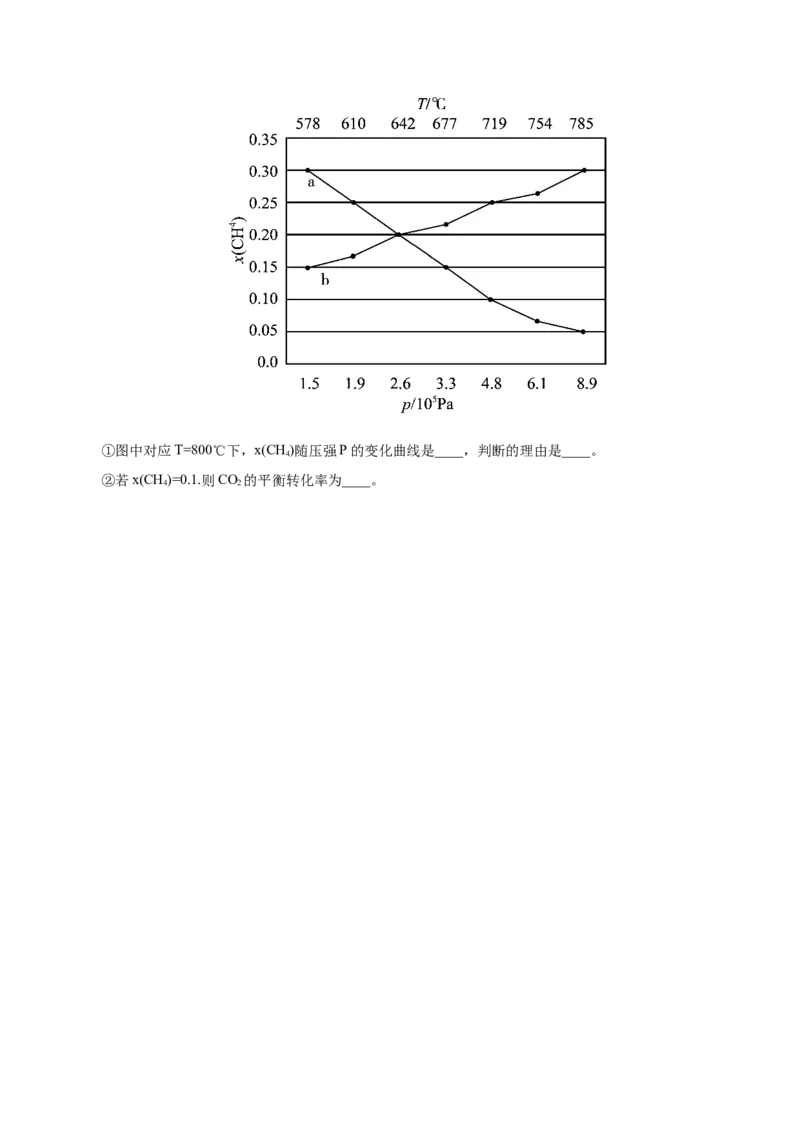
(4)在一定条件下的密闭容器中,按照 =1加入反应物,发生反应I(反应II、III、IV可忽略)。在
不同条件下达到平衡,设体系中平衡状态下甲烷的物质的量分数为 x(CH),在T=800℃下的x(CH)随压强
4 4
P的变化曲线、在P=100kPa下的x(CH)随温度T的变化曲线如图所示。
4①图中对应T=800℃下,x(CH)随压强P的变化曲线是____,判断的理由是____。
4
②若x(CH)=0.1.则CO 的平衡转化率为____。
4 2