文档内容
高二化学上学期期中测试卷 03
(考试时间:90分钟 满分100分)
考试范围:新教材人教版选择性必修1第一、二、三章
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 S 32 Cl 35.5
K 39 Ca 40 Fe 56 Cu 64 Ag 108 Ba 137
选择题部分
一、选择题(本大题共20小题,每小题2分,共40分。每个小题列出的四个备选项中只有一个是符合
题目要求的,不选、多选、错选均不得分)
1.25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热 ΔH为-57.3 kJ·mol-1,辛烷的标准
燃烧热ΔH为-5 518 kJ·mol-1。下列热化学方程式书写正确的是( )
A.2H+(aq)+SO2- (aq)+2Na+(aq)+2OH-(aq)=Na SO (aq)+2H O(l) ΔH=-57.3 kJ·mol-1
4 2 4 2
B.KOH(aq)+ HSO (aq)= KSO (aq)+H O(l) ΔH=-57.3 kJ·mol-1
2 4 2 4 2
C.C H (l)+ O(g)=8CO (g)+9HO(g) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
D.2C H (l)+25O (g)=16CO (g)+18HO(l) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
【答案】B
【解析】A项,所列热化学方程式中有两个错误,一是中和热是指反应生成1 mol H O(l)时的反应热,
2
二是当有BaSO 沉淀生成时,反应的热效应会有所变化,生成1 mol H O(l)时产生的热量不再是57.3 kJ,A
4 2
错误;B 项,中和热是指反应生成1 mol H O(l)时的反应热,B正确;C 项,燃烧热是指1 mol可燃物完全
2
燃烧生成稳定的物质时所产生的热量,这时产物中的水应为液态水,C错误;D项,当2 mol液态辛烷完
全燃烧时,产生的热量为11036 kJ,D错误;故选B。
2.在一容积不变,绝热的密闭容器中发生可逆反应:2X(s) Y(g)+Z(g),以下不能说明该反应达
到化学平衡状态的是( )
A.混合气体的密度不再变化 B.反应容器中Y的质量分数不变
C.该反应的化学平衡常数不变 D.容器中混合气体的平均相对分子量不变
【答案】D
【解析】A项,由2X(s) Y(g)+Z(g)可知,反应前后气体的质量是变量,容器的体积不变,反应
过程中混合气体的密度是变量,当混合气体的密度不再变化时,各气体的质量不再改变,反应达到平衡状
态,所以混合气体的密度不再变化,能判断反应达到平衡状态,故A不符合题意;B项,当反应容器中Y
的质量分数不变时,体积不变,说明Y的浓度不再改变,反应达到平衡,所以反应容器中Y的质量分数不变,能说明该反应达到化学平衡状态,故B不符合题意;C项,由2X(s) Y(g)+Z(g)反应是在绝热的
密闭容器中进行可知,温度是变量,而平衡常数只是温度的函数,当反应的化学平衡常数不变时,说明温
度不再改变,反应达到平衡状态,所以该反应的化学平衡常数不变,能说明该反应达到化学平衡状态,故
C不符合题意;D项,由2X(s) Y(g)+Z(g)可知,反应前反应物是固体,反应后产物是气体,且产生
的气体比例不会改变,总是1:1,则混合气体的平均相对分子量M= 是定值,所以当容器内气体的
平均相对分子量不变时,不能判断反应达到平衡状态,故D符合题意;故选D。
3.两种盐的稀溶液:amol·L-1NaX溶液和bmol·L-1NaY溶液。下列说法不正确的是( )
A.若a=b,且pH(NaX)>pH(NaY),则酸性HXb,且c(X-)=c(Y-),则溶液中c(HX)>c(HY)
C.若a=b,且c(X-)=c(Y-)+c(HY),则HX为强酸
D.若两溶液等体积混合后c(X-)+c(HX)=c(Y-)+c(HY)=0.1mol·L-1,则a=b=0.1mol·L-1
【答案】D
【解析】A项,两种溶液浓度相同,pH(NaX)>pH(NaY),说明NaX的碱性更强,对应的X-的水解程
度更强,因此酸性HXb并且c(X-)=c(Y-),根据物料守恒a=c(X-)+c(HX),b=c(Y-)
+c(HY),所以溶液中(HX)>c(HY),故B正确;C项,a=b且c(X-)=c(Y-)+c(HY),因此可以看出X-没有水解,
因此HX为强酸,故C正确;D项,两种溶液混合以前,根据物料守恒a=c(X-)+c(HX),b=c(Y-)+c(HY),若
等体积混合,则混合后的体积是混合前的两倍,此时c(X-)+c(HX)= ,c(Y-)+c(HY)= ,又因为c(X-)
+c(HX)=c(Y-)+c(HY)=0.1mol/L,则a=b=0.2,故D错误;故选D。
4.下列说法正确的是( )
A.室温下,pH=3的醋酸溶液稀释100倍后,溶液中所有离子的浓度均降低
B.室温下,相同pH的CHCOOH与NH Cl溶液导电能力相同
3 4
C.室温下,同浓度的NaOH溶液分别与等体积、相同pH的盐酸和醋酸溶液反应至溶液呈中性,盐酸
消耗的NaOH溶液体积少
D.常温下,pH=3的醋酸溶液中加入少量醋酸钠固体溶液的pH增大,醋酸的电离度增大
【答案】C
【解析】A项,醋酸为弱酸,稀释醋酸溶液时促进醋酸电离,醋酸根离子和氢离子浓度都减小,温度
不变,水的离子积常数不变,导致氢氧根离子浓度增大,A错误;B项,CHCOOH为弱电解质,在水溶
3
液中只发生部分电离,使溶液呈酸性,NH Cl为强电解质,在水中发生水解反应使溶液呈酸性,则相同pH
4的CHCOOH与NH Cl溶液比较,NH Cl离子浓度多,即导电能力不同,B错误;C项,醋酸为弱酸,相
3 4 4
同pH的盐酸和醋酸,其溶质的浓度比较:盐酸小于醋酸,所以与同浓度的NaOH溶液等体积混合反应至
中性,盐酸消耗的NaOH溶液体积少,C正确;D项,醋酸存在电离平衡:CHCOOH CHCOO-
3 3
+H+,则加入少量醋酸钠固体,使醋酸根离子浓度增大,电离平衡向逆向移动,醋酸的电离度减小,氢离
子浓度减小,pH增大,D错误;故选D。
5.N 可以与O 化合生成NO,是自然界固氮的重要方式之一、下图所示是以1mol N 和1mol O,作
2 2 2 2
为反应物的相应能量变化。判断下列说法不正确的是( )
A.上图所示的反应中转移电子的物质的量为4 mol
B.完全断开1mol NO中的化学键需吸收1264kJ能量
C.该反应中产物所具有的总能量高于反应物所具有的总能量
D.NO分解的热化学方程式为2NO(g)=N (g) +O (g) H=-180kJ·mol-1
2 2
【答案】B △
【解析】A项,1mol氮气和1mol氧气反应生成2mol NO,反应中转移电子的物质的量为4 mol,故A
正确;B项,根据图示,完全断开2mol NO中的化学键需吸收1264kJ能量,故B错误;C项,根据图示,
该反应断键吸收的能量是946+498=1444kJ,成键放出的能量是1264kJ,总反应吸热,所以产物所具有的总
能量高于反应物所具有的总能量,故C正确;D项,根据图示,N(g) +O (g)= 2NO(g)
2 2
H=946kJ·mol-1+498 kJ·mol-1-1264kJ·mol-1= +180kJ·mol-1,所以NO分解的热化学方程式为2NO(g)=N (g)
2
△+O (g) H= -180kJ·mol-1,故D正确;故选B。
2
6.氨△是化肥生产工业的重要原料。传统的Haber—Bosch法目前仍是合成氨的主要方式,反应原理为
N(g)+3H(g) 2NH (g),其生产条件需要高温高压。近来电催化氮气合成氨因节能、环境友好等优势,
2 2 3
受到广泛关注,下列有关Haber-Bosch法合成氨反应的说法正确的是( )
A.该反应的ΔH>0、ΔS<0
B.将氨气及时液化分离可加快化学反应速率
C.当2v(H ) =3v(NH ) 时,反应达到平衡状态
2 正 3 逆
D.提高体系的压强可增大反应的化学平衡常数
【答案】C
【解析】A项,由N(g)+3H(g) 2NH (g)反应可知,该反应是一个化合反应,为放热反应,ΔH<
2 2 3
0,该反应是一个气体体积减小的反应,ΔS<0,故A错误;B项,将氨气及时液化分离,减小生成物浓度,平衡正向移动,反应速率减小,故B错误;C项,速率之比等于方程式系数比,当2v(H ) =3v(NH ) 时,
2 正 3 逆
表示正逆反应速率相等,反应达到平衡状态,故C正确;D项,由N(g)+3H(g) 2NH (g)反应可知,
2 2 3
提高体系的压强,平衡正向移动,但化学平衡常数只是温度的函数,温度不变,化学平衡常数不变,故D
错误;故选C。
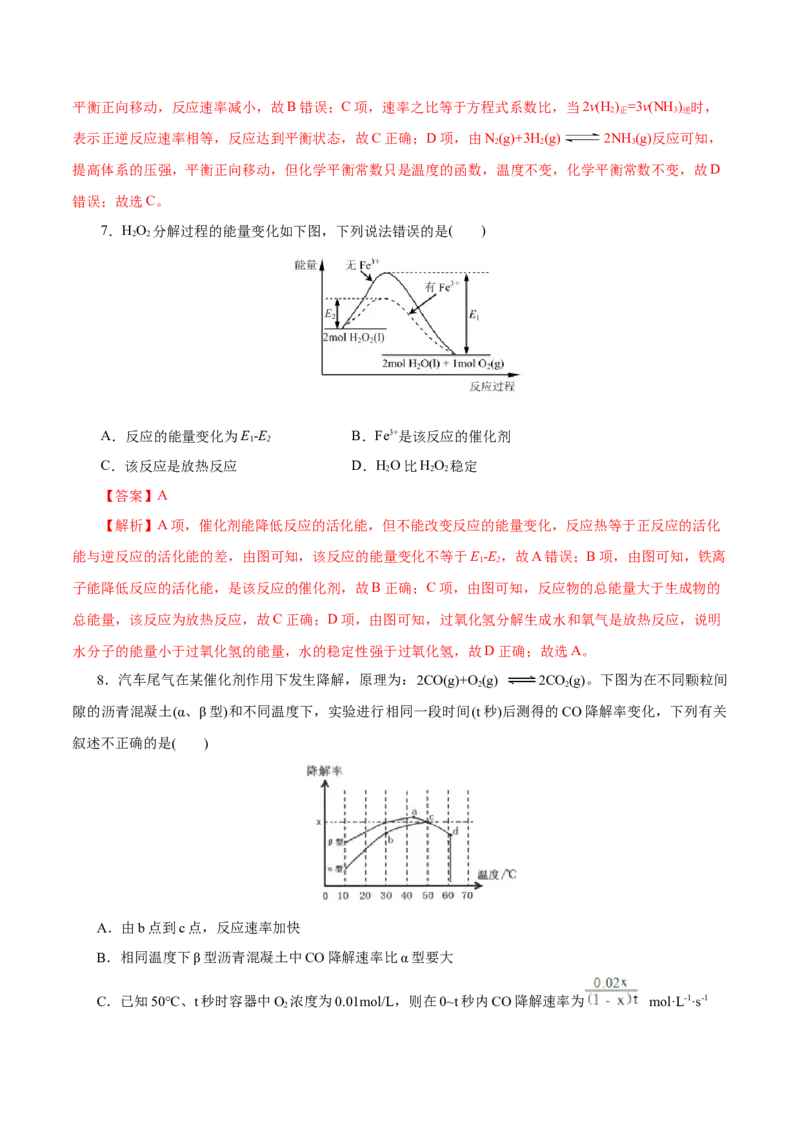
7.HO 分解过程的能量变化如下图,下列说法错误的是( )
2 2
A.反应的能量变化为E-E B.Fe3+是该反应的催化剂
1 2
C.该反应是放热反应 D.HO比HO 稳定
2 2 2
【答案】A
【解析】A项,催化剂能降低反应的活化能,但不能改变反应的能量变化,反应热等于正反应的活化
能与逆反应的活化能的差,由图可知,该反应的能量变化不等于E-E,故A错误;B项,由图可知,铁离
1 2
子能降低反应的活化能,是该反应的催化剂,故B正确;C项,由图可知,反应物的总能量大于生成物的
总能量,该反应为放热反应,故C正确;D项,由图可知,过氧化氢分解生成水和氧气是放热反应,说明
水分子的能量小于过氧化氢的能量,水的稳定性强于过氧化氢,故D正确;故选A。
8.汽车尾气在某催化剂作用下发生降解,原理为:2CO(g)+O(g) 2CO(g)。下图为在不同颗粒间
2 2
隙的沥青混凝土(α、β型)和不同温度下,实验进行相同一段时间(t秒)后测得的CO降解率变化,下列有关
叙述不正确的是( )
A.由b点到c点,反应速率加快
B.相同温度下β型沥青混凝土中CO降解速率比α型要大
C.已知50℃、t秒时容器中O 浓度为0.01mol/L,则在0~t秒内CO降解速率为 mol·L-1·s-1
2D.c点后降解率出现突变的原因可能是温度升高后催化剂失效
【答案】C
【解析】 A项,由b点到c点,随温度的升高降解率增大,A正确;B项,根据图示,相同温度下β
型沥青混凝土反应速率快,B正确;C项,若开始时,CO和O 按2:1进行反应,则根据三段法计算得出
2
v(CO)= mol·L-1·s-1,但实际上降解反应并不一定按2:1进行,C错误;D项,在适宜的温度下
催化剂的效果最好,D正确。
9.已知某温度下 CHCOOH 和 NH ·H O 的电离常数相等,现向 10 mL 浓度为 0.1 mol·L-1的
3 3 2
CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B.c(NH)/c(NH ·H O)先增大再减小
3 2
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
【答案】D
【解析】开始滴加氨水时,水的电离程度增大,二者恰好完全反应时,水的电离程度最大,再继续滴
加氨水时,水的电离程度减小,A项错误;向醋酸中滴加氨水,溶液的酸性减弱,碱性增强,c(OH-)增大,
由 NH ·H O NH+OH-可知 K=,则=,故减小,B 项错误;根据原子守恒知 n(CHCOO-)与
3 2 3
n(CHCOOH)之和不变,但滴加氨水过程中,溶液体积不断增大,故 c(CHCOO-)与c(CHCOOH)之和减小,
3 3 3
C项错误;由CHCOOH和NH ·H O的电离常数相等可知当二者恰好完全反应时,溶液呈中性,结合电荷
3 3 2
守恒知c(CHCOO-)+c(OH-)=c(NH)+c(H+),则c(CHCOO-)=c(NH),D项正确。
3 3
10.下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O(g)═CO (g);ΔH C(s)+ O(g)═CO(g);ΔH
2 2 1 2 2
②S(s)+O (g)═SO (g);ΔH S(g)+O (g)═SO (g);ΔH
2 2 3 2 2 4
③H(g)+ O(g)═H O(l);ΔH 2H (g)+O(g)═2H O(l);ΔH
2 2 2 5 2 2 2 6
④CaCO (s)═CaO(s)+CO (g);ΔH CaO(s)+H O(l)═Ca(OH) (s);ΔH
3 2 7 2 2 8
A.① B.④ C.②③④ D.①②③
【答案】C
【解析】①②③为放热反应,物质发生化学反应时,生成液态水比生成气态水放出的热量多,反应越
完全,放出的热量越多;④中前者为吸热反应,后者为放热反应,吸热反应△H>0,放热反应△H<0。①两个反应都为放热反应,△H<0,前者完全反应,放出的热量多,则△H<△H,故①错误;②都为放热
1 2
反应,其△H<0,前者S为固态,则前者放出的热量少,则△H>△H,故②正确;③都是放热反应,前
3 4
者反应物系数较小,则前者放出热量较少,则△H>△H,故③正确;④前者为吸热反应,△H>0,后
5 6 7
者为放热反应,△H<0,则△H>△H,故④正确;根据分析可知,反应的△H前者大于后者的是②③④;
8 7 8
故选C。
11.相同温度和压强下,关于反应的 ,下列判断正确的是( )
CoCl ·6H O(s)=CoCl ·2H O(s)+4H O(l) ∆H
2 2 2 2 2 1
CoCl ·2H O(s)=CoCl ·H O(s)+H O(l) ∆H
2 2 2 2 2 2
CoCl ·H O(s)=CoCl (s)+HO(l) ∆H
2 2 2 2 3
CoCl ·6H O(s)=CoCl (s)+6HO(l) ∆H
2 2 2 2 4
A.∆H>0,∆H<0 B.∆H<∆H+∆H
1 2 1 2 3
C.∆H-∆H=∆H+∆H D.∆H<∆H
4 1 2 3 2 3
【答案】C
【解析】题给四个反应都是吸热反应,反应的∆H都大于0,将题干4个反应依次编号为①、②、③、
④,结合盖斯定律作答。A项,CoCl ·6H O(s)=CoCl ·2H O(s)+4H O(l) 和CoCl ·2H O(s)=CoCl ·H O(s)
2 2 2 2 2 2 2 2 2
+H O(l)都是吸热反应,故∆H>0,∆H>0,A错误;B项,根据盖斯定律,将②+③得
2 1 2
CoCl ·2H O(s)=CoCl (s)+2HO(l) ∆H=∆H+∆H(标为⑤),该反应为吸热反应,该反应失去2mol结晶水,
2 2 2 2 2 3
反应①失去4mol结晶水,失去水的物质的量是⑤的两倍,故反应①吸收的热量更多,则∆H>∆H+∆H,B
1 2 3
错误;C项,根据盖斯定律,将①+②+③=④,则∆H+∆H+∆H=∆H,则∆H-∆H=∆H+∆H,C正确;D项,
1 2 3 4 4 1 2 3
反应②、③都失去1mol结晶水,由题意无法判断∆H、∆H 的大小,D错误;故选C。
2 3
12.一定条件下进行反应:COCl (g) Cl(g)+CO(g)。向2.0L恒容密闭容器中充入
2 2
1.0molCOCl (g),经过一段时间后达到平衡。反应过程中测得的有关数据见表:
2
t/s 0 2 4 6 8
n(Cl )/mol 0 0.30 0.39 0.40 0.40
2
下列说法正确的是( )
A.保持其他条件不变,升高温度,平衡时c(Cl )=0.22mol·L-1,则反应的△H<0
2
B.若在2L恒容绝热(与外界没有热量变换)密闭容器进行该反应,化学平衡常数不变
C.保持其他条件不变,起始向容器中充入1.20molCOCl 、0.60molCl 和0.60molCO,反应达到平衡前
2 2
的速率:v(正)0,A错误;B项,正反应为吸热反应,恒容绝热密
闭容器进行该反应,随反应进行温度降低,而平衡常数只受温度影响,故平衡常数一定发生变化,B错误;
C项,平衡时c(Cl )=0.2mol·L-1,列三段式:
2
该温度下平衡常数 ,若起始向容器中充入1.2mol COCl 、0.60mol Cl 和
2 2
0.60molCO,此时 >0.13,则反应向逆反应方向移动,反应达到平衡前v正(A2-)>c(Na+)>(HA-)
D.向0.1mol·L-1KHA中滴加NaOH溶液至pH=7:c(Na+)+c(H A)=c(A2-)
2
【答案】D
【解析】A项,KHA的水解常数Kh= 1mol/L,(HA-)<1mol/L,可知
a2 2
c(K+)>(HA-)>c(Na+)>( A2-),故C错误;D项,由电荷守恒得:c(H+)+c(K+)+ c(Na+)=c(HA- )+2c(A2-)
+c(OH―),由物料守恒得:c(K+)=c(HA- )+c(A2-)+c(H A),又pH=7,c(H+)=c(OH―),则c(Na+)
2
+c(H A)=c(A2-),故D正确;故选C。
2
15.根据下列能量变化示意图,说法不正确的是( )
A.破坏相同质量的NO (g)和NO(g)中的化学键,后者所需的能量较高
2 2 4
B.NH(l)+NO(g)=3/2N (g) +2 HO(l) ∆H;则∆H>∆H
2 4 2 2 2 4
C.2HO(g) 2H(g)+ O (g) ∆H<-∆H
2 2 2 6 5
D.∆H=∆H+∆H+∆H+∆H
5 1 2 3 4
【答案】B【解析】A项,∆H<0,即1molNO (g)转化为1/2molNO(g)的反应为放热反应,所以破坏1molNO (g)
3 2 2 4 2
分子中的化学键所吸收的能量比形成1/2mol N O(g)分子中的化学键所放出的热量少,所以破坏相同质量
2 4
的NO (g)和NO(g)中的化学键,后者所需的能量较高,故A不符合要求;B项,NH(l)+NO(g)=3/2N (g)
2 2 4 2 4 2 2
+2 H O(l) ∆H,∆H=∆H+∆H,因为∆H<0,故∆H>∆H,故B符合要求; C项,∆H 为生成2mol液态水的
2 4 3 3 4 5
反应热,则有2mol的液态水分解吸收热量为∆H=-∆H,而C中是2mol的气态水分解,则吸收的热量减少
6 5
即∆H 的值减小,所以∆H<-∆H,故C不符合要求。D项,由盖斯定律可知∆H=∆H+∆H+∆H+∆H,故D
6 6 5 5 1 2 3 4
不符合要求;故选B。
16.在标准状态下,将指定单质生成1mol物质的反应焓称为该化合物的生成焓,符号为 。由题
图所给的数据可得,下列说法正确的是( )
A.生成MgF 时放出热量最多,故化合时反应速率最快
2
B.MgCl (s) +I (s)=MgI (s)+Cl (g) ΔH=277kJ·mol−1
2 2 2 2
C.由图可知,断开1 mol Cl (g)中的化学键所吸收的能量大于断开1 mol Br (l)中的化学键所吸收的能
2 2
量
D.MgI 的热稳定性比MgBr 高
2 2
【答案】B
【解析】A项,由题干图示信息可知,生成MgF 时放出热量最多,但反应速率快慢与反应需要的活
2
化能有关,而与焓变的大小没有必然的关系,故化合时反应速率不一定最快,A错误;B项,由题干图示
信息可知,反应I:Mg(s)+Cl (g)=MgCl (s) ΔH =-641kJ·mol−1,反应II:Mg(s)+I (s)=MgI (s) ΔH
2 2 1 2 2 2
=-364kJ·mol−1,则目标反应MgCl (s) +I (s)=MgI (s)+Cl (g) 可由II-I,根据盖斯定律可知:ΔH=ΔH-ΔH
2 2 2 2 2 1
=(-364kJ·mol−1)- (-641kJ·mol−1)=277kJ·mol−1,B正确;C项,根据反应热等于反应物总的键能减去生成物
的总的键能,由于生成物的总的键量各不相同,故根据图示信息无法比较断开1 mol Cl (g)中的化学键所吸
2
收的能量与断开1 mol Br (l)中的化学键所吸收的能量的相对大小,C错误;D项,由题干图示可知,相同
2
物质的量的MgI 具有的总能量高于MgBr 的,能量越高越不稳定,故MgI 的热稳定性比MgBr 低,D错
2 2 2 2误;故选B。
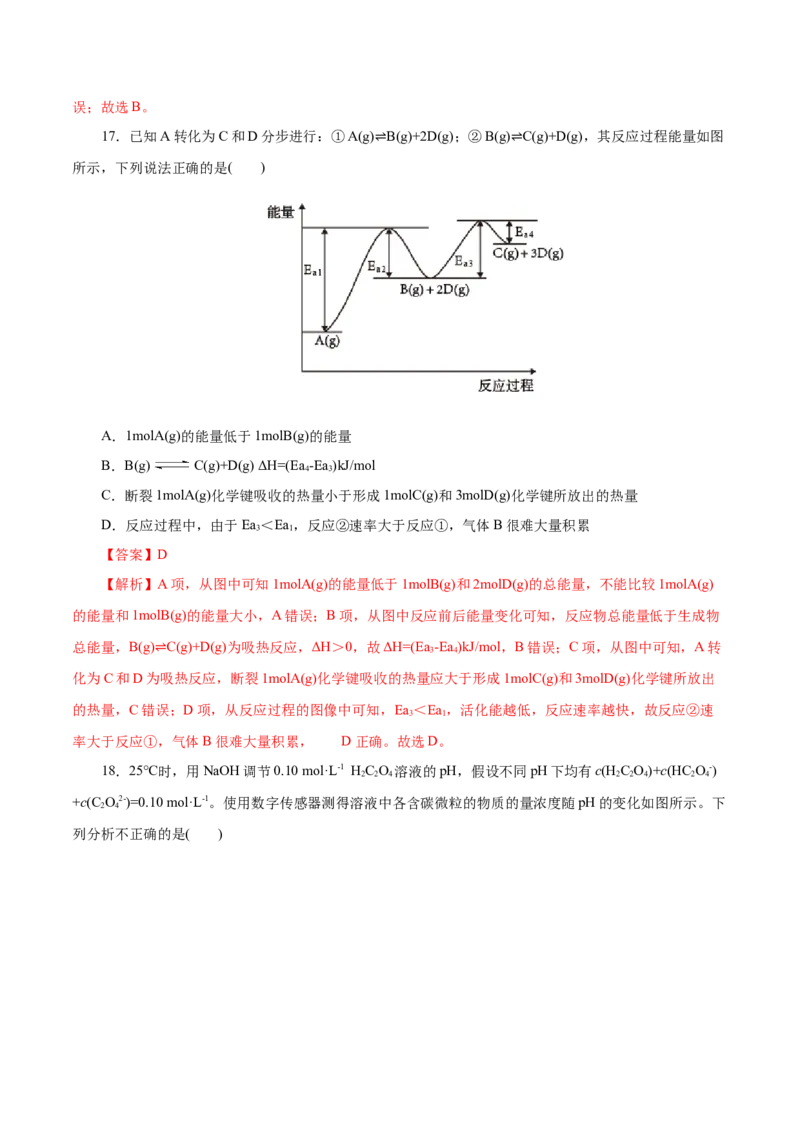
17.已知A转化为C和D分步进行:①A(g) B(g)+2D(g);②B(g) C(g)+D(g),其反应过程能量如图
所示,下列说法正确的是( ) ⇌ ⇌
A.1molA(g)的能量低于1molB(g)的能量
B.B(g) C(g)+D(g) ΔH=(Ea -Ea )kJ/mol
4 3
C.断裂1molA(g)化学键吸收的热量小于形成1molC(g)和3molD(g)化学键所放出的热量
D.反应过程中,由于Ea<Ea,反应②速率大于反应①,气体B很难大量积累
3 1
【答案】D
【解析】A项,从图中可知1molA(g)的能量低于1molB(g)和2molD(g)的总能量,不能比较1molA(g)
的能量和1molB(g)的能量大小,A错误;B项,从图中反应前后能量变化可知,反应物总能量低于生成物
总能量,B(g) C(g)+D(g)为吸热反应,ΔH>0,故ΔH=(Ea -Ea )kJ/mol,B错误;C项,从图中可知,A转
3 4
化为C和D为⇌吸热反应,断裂1molA(g)化学键吸收的热量应大于形成1molC(g)和3molD(g)化学键所放出
的热量,C错误;D项,从反应过程的图像中可知,Ea<Ea,活化能越低,反应速率越快,故反应②速
3 1
率大于反应①,气体B很难大量积累, D正确。故选D。
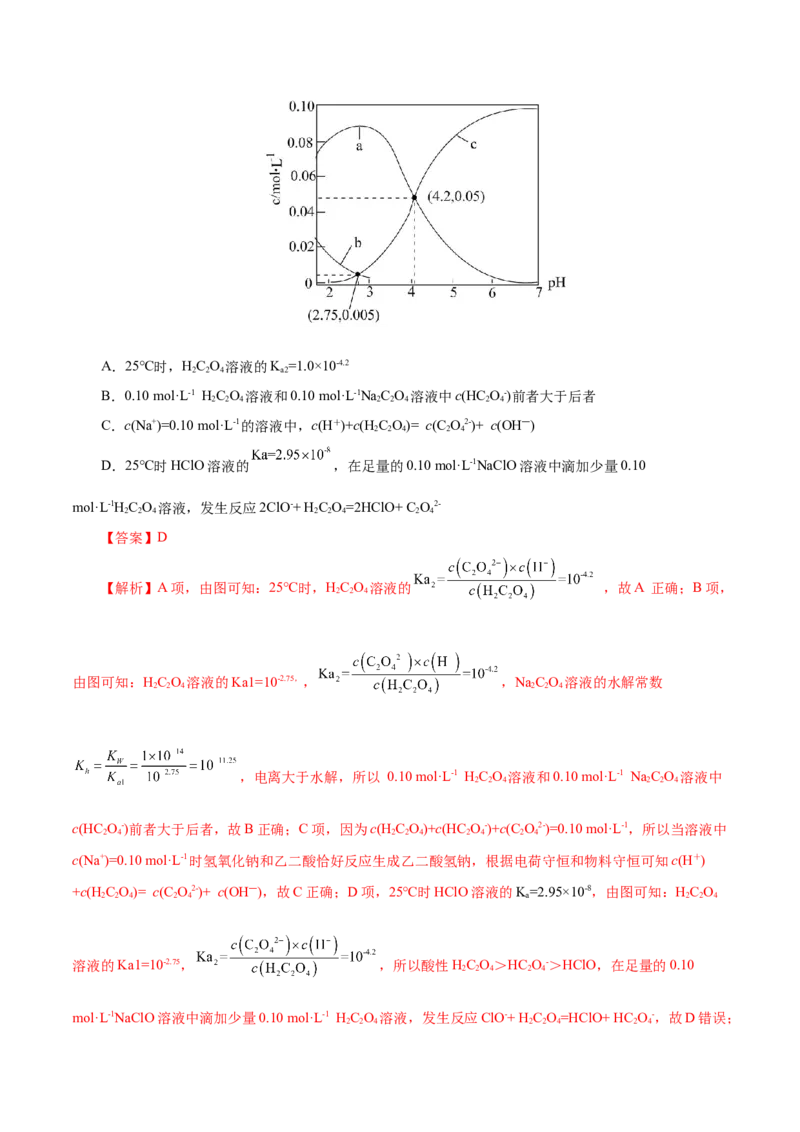
18.25℃时,用NaOH调节0.10 mol·L-1 HC O 溶液的pH,假设不同pH下均有c(H C O)+c(HC O-)
2 2 4 2 2 4 2 4
+c(C O2-)=0.10 mol·L-1。使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化如图所示。下
2 4
列分析不正确的是( )A.25℃时,HC O 溶液的K =1.0×10-4.2
2 2 4 a2
B.0.10 mol·L-1 HC O 溶液和0.10 mol·L-1NaC O 溶液中c(HC O-)前者大于后者
2 2 4 2 2 4 2 4
C.c(Na+)=0.10 mol·L-1的溶液中,c(H+)+c(H C O)= c(C O2-)+ c(OH―)
2 2 4 2 4
D.25℃时HClO溶液的 ,在足量的0.10 mol·L-1NaClO溶液中滴加少量0.10
mol·L-1HC O 溶液,发生反应2ClO-+ H C O=2HClO+ C O2-
2 2 4 2 2 4 2 4
【答案】D
【解析】A项,由图可知:25℃时,HC O 溶液的 ,故A 正确;B项,
2 2 4
由图可知:HC O 溶液的Ka1=10-2.75,, ,NaC O 溶液的水解常数
2 2 4 2 2 4
,电离大于水解,所以 0.10 mol·L-1 HC O 溶液和0.10 mol·L-1 Na C O 溶液中
2 2 4 2 2 4
c(HC O-)前者大于后者,故B正确;C项,因为c(H C O)+c(HC O-)+c(C O2-)=0.10 mol·L-1,所以当溶液中
2 4 2 2 4 2 4 2 4
c(Na+)=0.10 mol·L-1时氢氧化钠和乙二酸恰好反应生成乙二酸氢钠,根据电荷守恒和物料守恒可知c(H+)
+c(H C O)= c(C O2-)+ c(OH―),故C正确;D项,25℃时HClO溶液的K=2.95×10-8,由图可知:HC O
2 2 4 2 4 a 2 2 4
溶液的Ka1=10-2.75, ,所以酸性HC O>HC O->HClO,在足量的0.10
2 2 4 2 4
mol·L-1NaClO溶液中滴加少量0.10 mol·L-1 HC O 溶液,发生反应ClO-+ H C O=HClO+ HC O-,故D错误;
2 2 4 2 2 4 2 4故选D。
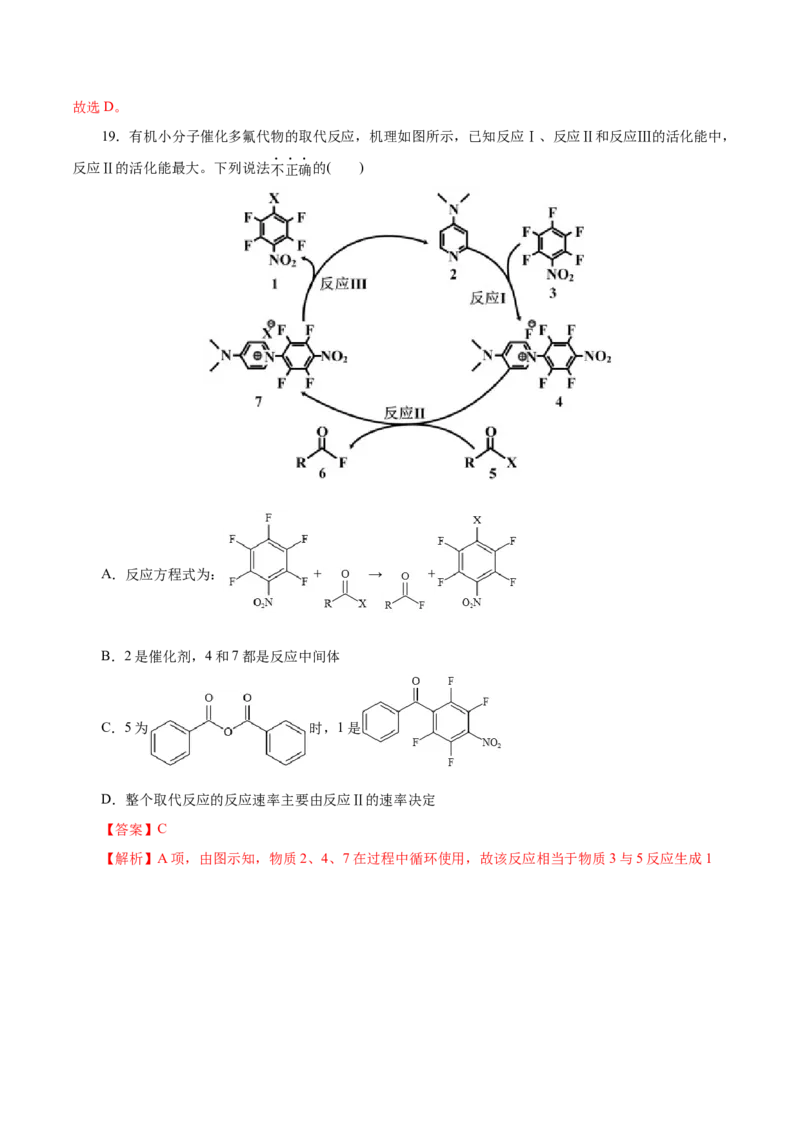
19.有机小分子催化多氟代物的取代反应,机理如图所示,已知反应Ⅰ、反应Ⅱ和反应Ⅲ的活化能中,
反应Ⅱ的活化能最大。下列说法不正确的( )
A.反应方程式为: + → +
B.2是催化剂,4和7都是反应中间体
C.5为 时,1是
D.整个取代反应的反应速率主要由反应Ⅱ的速率决定
【答案】C
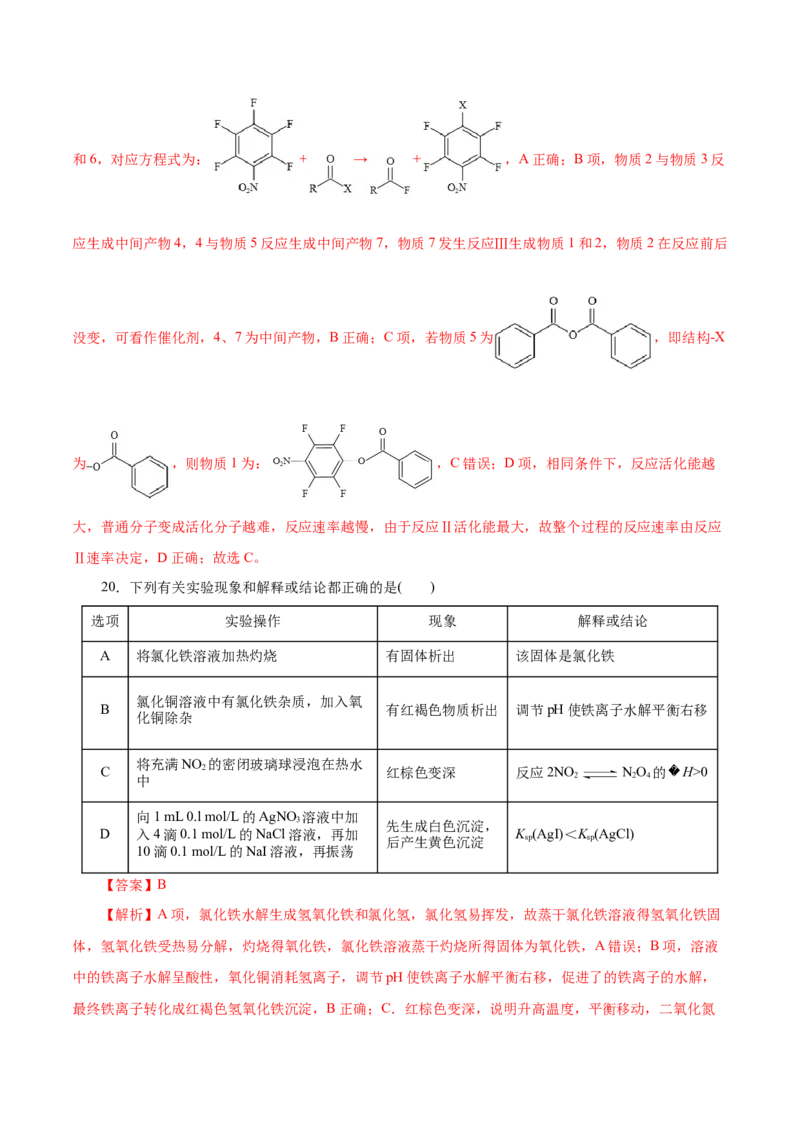
【解析】A项,由图示知,物质2、4、7在过程中循环使用,故该反应相当于物质3与5反应生成1和6,对应方程式为: + → + ,A正确;B项,物质2与物质3反
应生成中间产物4,4与物质5反应生成中间产物7,物质7发生反应Ⅲ生成物质1和2,物质2在反应前后
没变,可看作催化剂,4、7为中间产物,B正确;C项,若物质5为 ,即结构-X
为 ,则物质1为: ,C错误;D项,相同条件下,反应活化能越
大,普通分子变成活化分子越难,反应速率越慢,由于反应Ⅱ活化能最大,故整个过程的反应速率由反应
Ⅱ速率决定,D正确;故选C。
20.下列有关实验现象和解释或结论都正确的是( )
选项 实验操作 现象 解释或结论
A 将氯化铁溶液加热灼烧 有固体析出 该固体是氯化铁
氯化铜溶液中有氯化铁杂质,加入氧
B 有红褐色物质析出 调节pH使铁离子水解平衡右移
化铜除杂
将充满NO 的密闭玻璃球浸泡在热水
C 2 红棕色变深 反应2NO NO 的 H>0
中 2 2 4
向1 mL 0.l mol/L的AgNO 溶液中加
3 先生成白色沉淀,
D 入4滴0.1 mol/L的NaCl溶液,再加 K (AgI)<K (AgCl)
后产生黄色沉淀 sp sp
10滴0.1 mol/L的NaI溶液,再振荡
【答案】B
【解析】A项,氯化铁水解生成氢氧化铁和氯化氢,氯化氢易挥发,故蒸干氯化铁溶液得氢氧化铁固
体,氢氧化铁受热易分解,灼烧得氧化铁,氯化铁溶液蒸干灼烧所得固体为氧化铁,A错误;B项,溶液
中的铁离子水解呈酸性,氧化铜消耗氢离子,调节pH使铁离子水解平衡右移,促进了的铁离子的水解,
最终铁离子转化成红褐色氢氧化铁沉淀,B正确;C.红棕色变深,说明升高温度,平衡移动,二氧化氮的浓度增大,则说明反应2NO NO 的△H<0,C错误;D项,1 mL溶液约有20滴,向1 mL 0.l
2 2 4
mol/L的AgNO 溶液中加入4滴0.1 mol/L的NaCl溶液,再加10滴0.1 mol/L的NaI溶液,AgNO 是过量的,
3 3
不能确定是AgCl转化为AgI,所以不能比较K ,故D错误;故选B。
sp
非选择题部分
二、非选择题(本大题共5小题,共60分)
21.(12分)已知K、K、K 、K、K 分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离
a b w h sp
子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据:K
w
=1.0×10-14,K(CHCOOH)=1.8×10-5,K(HSCN)=0.13,K(HF)=4.0×10-4,K [Mg(OH) ]=1.8×10-11
a 3 a a sp 2
(1)有关上述常数的说法正确的是__________。
A.它们都能反映一定条件下对应变化进行的程度
B.所有弱电解质的电离常数和难溶电解质的K 都随温度的升高而增大
sp
C.常温下,CHCOOH在水中的K 大于在饱和CHCOONa溶液中的K
3 a 3 a
D.一定温度下,在CHCOONa溶液中,K =K·K
3 w a h
(2)25℃时,1.0 mol·L-1 HF溶液的pH约等于__________(已知lg2≈0.3)。将浓度相等的HF与NaF溶液
等体积混合,判断溶液呈_______(填“酸”、“碱”或“中”)性,并结合有关数据解释原因:
_____________。
(3)已知CHCOONH 溶液为中性,又知CHCOOH溶液加到NaCO 溶液中有气体放出,现有25℃时
3 4 3 2 3
等浓度的四种溶液:A.NH Cl,B.NH SCN,C.CHCOONH,D.NH HCO 。回答下列问题:
4 4 3 4 4 3
①试推断NH HCO 溶液的pH__________7(填“>”、“<”或“=”);
4 3
②将四种溶液按NH +浓度由大到小的顺序排列是:__________(填序号)。
4
③NH SCN溶液中所有离子浓度由大到小的顺序为_________。
4
【答案】 (1)AD (2分)
(2)1.7 (1 分) 酸(1 分) HF 和 NaF 的浓度相等,K(HF)=4.0×10-4,NaF 溶液中 K =
a h
K /K=2.5×10-9,所以HF电离程度大于NaF的水解程度,溶液显酸性(2分)
w a
(3) ①>(2分) ②A>B>C>D (2分) ③c(SCN-)> c(NH +)> c(H+)> c(OH-) (2分)
4
【解析】(1)A项,平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比,所以它们都能反映一定
条件下对应变化进行的程度,A正确;B项,难溶电解质Ca(OH) 的K 随温度的升高而减小,B错误;C
2 sp
项,电离平衡常数只与温度有关,温度相同电离平衡常数相同,C 错误;D 项,一定温度下,在
CHCOONa溶液中, = = ,所以K =K K ,
3 W a h
⋅D 正确;故选 AD;(2)25℃时,1.0 mol·L-1 HF 溶液中,K(HF)= = =4.0×10-4,
a
c(H+)=2.0×10-2,pH≈7,HF和NaF的浓度相等,K(HF)=4.0×10-4,NaF溶液中K =K /K=2.5×10-9,所以
a h w a
HF电离程度大于NaF的水解程度,溶液呈酸性; HF和NaF的浓度相等,K(HF)=4.0×10-4,NaF溶液中
a
K =K /K=0.25×10-10,所以HF电离程度大于NaF的水解程度,溶液显酸性;(3)①已知CHCOONH 溶液
h w a 3 4
为中性,说明CHCOO-和NH +水解程度相同,又知CHCOOH溶液加到NaCO 溶液中有气体放出,说明
3 4 3 2 3
酸性:CHCOOH>H CO ,越弱越水解,可知HCO -水解程度大于NH +水解程度,所以NH HCO 溶液显碱
3 2 3 3 4 4 3
性,pH>7;②根据电离平衡常数可知,酸性:HSCN> CH COOH>H CO ,越弱越水解,所以四种溶液按
3 2 3
NH +浓度由大到小的顺序:A>B>C>D;③酸性:HSCN> CH COOH ,CHCOO-和NH +水解程度相同,
4 3 3 4
所以NH +水解程度大于 SCN-水解程度,NH SCN溶液显酸性,其所有离子浓度由大到小的顺序为:
4 4
c(SCN-)> c(NH +)> c(H+)> c(OH-)。
4
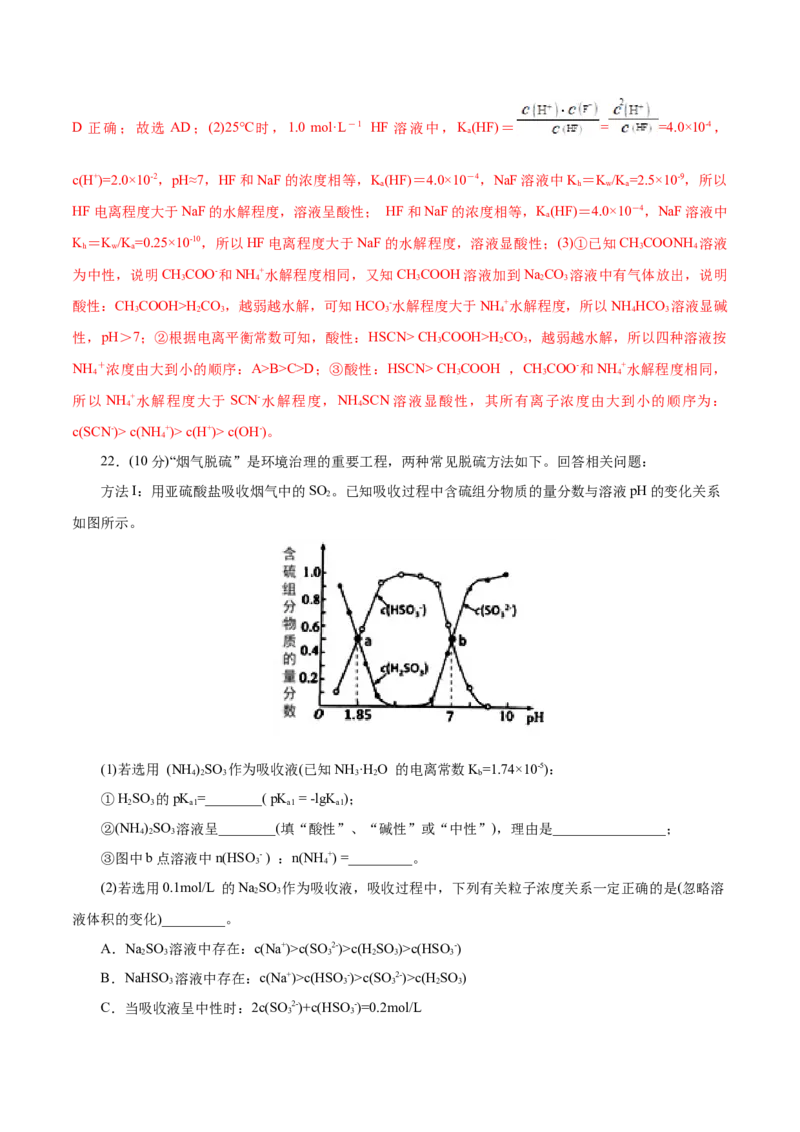
22.(10分)“烟气脱硫”是环境治理的重要工程,两种常见脱硫方法如下。回答相关问题:
方法I:用亚硫酸盐吸收烟气中的SO 。已知吸收过程中含硫组分物质的量分数与溶液pH的变化关系
2
如图所示。
(1)若选用 (NH )SO 作为吸收液(已知NH ·H O 的电离常数K=1.74×10-5):
4 2 3 3 2 b
①HSO 的pK =________( pK = -lgK );
2 3 a1 a1 a1
②(NH )SO 溶液呈________(填“酸性”、“碱性”或“中性”),理由是________________;
4 2 3
③图中b点溶液中n(HSO - ) :n(NH +) =_________。
3 4
(2)若选用0.1mol/L 的NaSO 作为吸收液,吸收过程中,下列有关粒子浓度关系一定正确的是(忽略溶
2 3
液体积的变化)_________。
A.NaSO 溶液中存在:c(Na+)>c(SO2-)>c(H SO )>c(HSO -)
2 3 3 2 3 3
B.NaHSO 溶液中存在:c(Na+)>c(HSO -)>c(SO2-)>c(H SO )
3 3 3 2 3
C.当吸收液呈中性时:2c(SO 2-)+c(HSO -)=0.2mol/L
3 3D.当吸收液呈酸性时:c(Na+)=c(SO2-)+c(HSO -)+c(H SO )
3 3 2 3
方法II:用含铬废水吸收烟气中的SO 。吸收原理如图所示:
2
(3)“吸收”中反应的离子方程式为____________________
(4)欲使废水中的铬元素完全转化为Cr(OH) 沉淀,应调节pH的范围为____。(常温下
3
K [Cr(OH) ]=1.0×10-32)
sp 3
【答案】(1) ①1.85(1分) ②碱性(1分)
(3)SO 2-的水解程度大于NH +的水解程度(1分) ③1:3 (2分)
3 4
(2)BC(2分) (3) 3SO +Cr O2-+2H+ =2Cr3++3SO2-+H O(1分) (4)≥5(2分)
2 2 7 4 2
【解析】(1)①K = ,根据图像可知当pH=1.85时,n(HSO - ) =n(H SO ),也即c(HSO -
a1 3 2 3 3
) =c(HSO ),所以K =10-1.85,则pK =1.85;②NH ·H O 的电离常数K=1.74×10-5,则铵根的水解平衡常数
2 3 a1 a1 3 2 b
为 ,亚硫酸根的水解平衡常数 根据图像可知当
pH=7时,n(HSO -)=n(SO2-),即c(HSO -)=c(SO2-),所以亚硫酸根的水解平衡常数为1×10-7,大于铵根的水
3 3 3 3
解平衡常数,所以亚硫酸根的水解程度大,溶液显碱性;③b点溶液呈中性,即c(H+)=c(OH-),同时溶液
中存在电荷守恒2c(SO 2-)+c(HSO -)+ c(OH-)= c(NH +)+ c(H+),则有2c(SO 2-)+c(HSO -)= c(NH +),根据图像
3 3 4 3 3 4
可知该点c(HSO -)=c(SO2-),所以有3c(HSO -)= c(NH +),所以n(HSO - ) : n(NH +) =1:3;(2)A项,根据
3 3 3 4 3 4
分析可知,在吸收二氧化硫之前,HSO 是水解产生的,且为更为微弱的第二步水解产生,所以此时
2 3
c(HSO -)>c(H SO ),故A错误;B项,NaHSO 溶液中存在硫酸氢根的电离和水解,根据图像可知硫酸氢钠
3 2 3 3
水溶液显酸性即电离大于水解,所以c(SO 2-)>c(H SO ),溶液中存在c(Na+)>c(HSO -)>c(SO2-)>c(H SO ),
3 2 3 3 3 2 3
故 B 正确;C 项,吸收至中性时存在电荷守恒 2c(SO 2-)+c(HSO -)+ c(OH-)= c(Na+)+ c(H+),且此时
3 3
c(H+)=c(OH-),所以有2c(SO 2-)+c(HSO -)=c(Na+)=0.2mol/L,故C正确;D项,当吸收溶液呈酸性时,溶液
3 3
中有电荷守恒:2c(SO 2-)+c(HSO -)+ c(OH-)= c(Na+)+ c(H+),溶液显酸性则 c(H+)c(Na+),根据图像可知当溶液呈酸性时c(HSO )> c(SO 2-)是,所以c(SO 2-)+c(HSO -)+c(H SO )>
3 2 3 3 3 3 2 3
c(Na+),故D错误;故选BC;(3)根据产物可知该过程中Cr O2-被还原成Cr3+,二氧化硫做还原剂被氧化
2 7
成硫酸根,根据电子守恒和元素守恒可得方程式为:3SO +Cr O2-+2H+ =2Cr3++3SO2-+H O;(4)设铬元素
2 2 7 4 2完全转化为Cr(OH) 沉淀时溶液中的c(OH-)=amol/L,K [Cr(OH) ]=c(Cr3+)·c3(OH-)=1×10-5×a3=1.0×10-32,解
3 sp 3
得a=1.0×10-9 amol/L,此时pH值为5,所以欲使废水中的铬元素完全转化为Cr(OH) 沉淀,应调节pH的
3
范围为≥5。
23.(12分)甲醇、乙烯都是重要的有机化工原料,工业上可利用 CO 和 H 在催化剂作用下合成,
2 2
发生的主要反应有:
i.2CO(g)+6H(g) C H(g)+4HO(g ) ∆H=-127.89kJ/mol
2 2 2 4 2
ii.CO(g)+H(g) HO(g)+CO(g) ∆H=+41.2kJ/mol
2 2 2
iii.CO(g)+3H(g) CHOH(g)+H O(g) ∆H=-49.5kJ/mol
2 2 3 2
(1)上述反应iii中的活化能E(正)______ E(逆)(填“>”或“<”),该反应应选择__________高效催化
a a
剂(填“高温”或“低温”)。
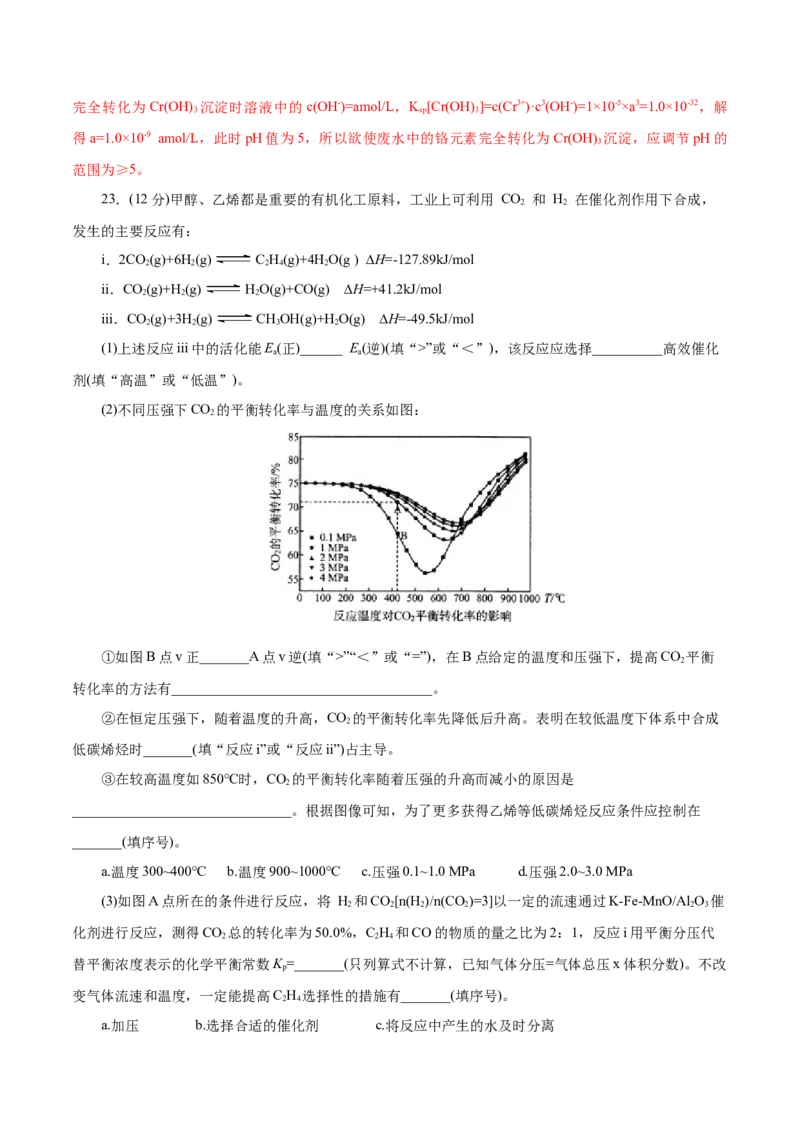
(2)不同压强下CO 的平衡转化率与温度的关系如图:
2
①如图B点v正_______A点v逆(填“>”“<”或“=”),在B点给定的温度和压强下,提高CO 平衡
2
转化率的方法有_____________________________________。
②在恒定压强下,随着温度的升高,CO 的平衡转化率先降低后升高。表明在较低温度下体系中合成
2
低碳烯烃时_______(填“反应i”或“反应ii”)占主导。
③在较高温度如850℃时,CO 的平衡转化率随着压强的升高而减小的原因是
2
_______________________________。根据图像可知,为了更多获得乙烯等低碳烯烃反应条件应控制在
_______(填序号)。
a.温度300~400℃ b.温度900~1000℃ c.压强0.1~1.0 MPa d.压强2.0~3.0 MPa
(3)如图A点所在的条件进行反应,将 H 和CO[n(H )/n(CO)=3]以一定的流速通过K-Fe-MnO/Al O 催
2 2 2 2 2 3
化剂进行反应,测得CO 总的转化率为50.0%,C H 和CO的物质的量之比为2:1,反应i用平衡分压代
2 2 4
替平衡浓度表示的化学平衡常数K =_______(只列算式不计算,已知气体分压=气体总压x体积分数)。不改
p
变气体流速和温度,一定能提高C H 选择性的措施有_______(填序号)。
2 4
a.加压 b.选择合适的催化剂 c.将反应中产生的水及时分离【答案】(1)<(1分) 低温(1分)
(2①<(1分) 增大氢碳比、将生成物及时分离(1分) ②反应i (1分)
③850℃时,反应ii占主导,加压使反应i平衡正移,HO的含量增加,从而引起反应ii向左移动,
2
CO 的平衡转化率随着压力的升高而降低(2分) ad(2分)
2
(3) (MPa)-3(2分) abc(2分)
【解析】(1)ΔH= E(正)-E(逆),CO(g)+3H(g) CHOH(g)+HO(g) ΔH= -58kJ•mol -1,故上述反
a a 2 2 3 2
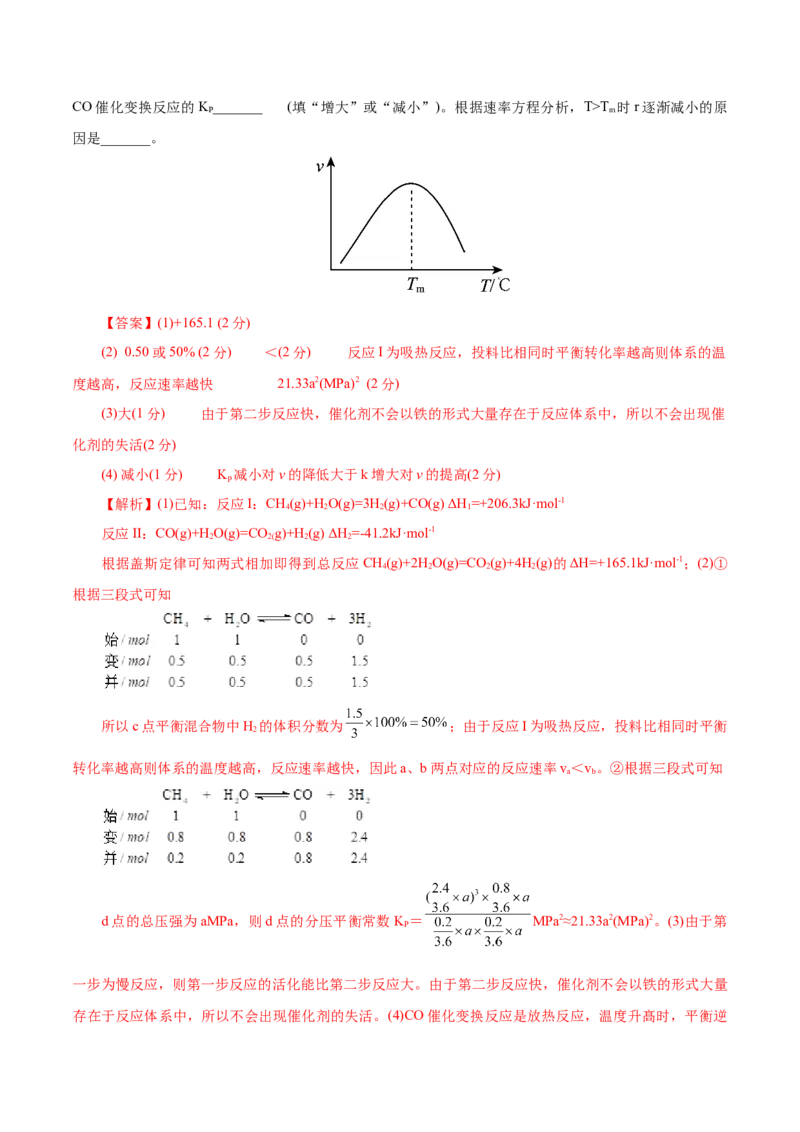
应中的活化能E(正)T 时r逐渐减小的原
P m
因是_______。
【答案】(1)+165.1 (2分)
(2) 0.50或50% (2分) <(2分) 反应I为吸热反应,投料比相同时平衡转化率越高则体系的温
度越高,反应速率越快 21.33a2(MPa)2 (2分)
(3)大(1分) 由于第二步反应快,催化剂不会以铁的形式大量存在于反应体系中,所以不会出现催
化剂的失活(2分)
(4) 减小(1分) K 减小对v的降低大于k增大对v的提高(2分)
p
【解析】(1)已知:反应I:CH(g)+HO(g)=3H (g)+CO(g) ΔH =+206.3kJ·mol-1
4 2 2 1
反应II:CO(g)+HO(g)=CO g)+H (g) ΔH =-41.2kJ·mol-1
2 2( 2 2
根据盖斯定律可知两式相加即得到总反应CH(g)+2HO(g)=CO(g)+4H(g)的ΔH=+165.1kJ·mol-1;(2)①
4 2 2 2
根据三段式可知
所以c点平衡混合物中H 的体积分数为 ;由于反应I为吸热反应,投料比相同时平衡
2
转化率越高则体系的温度越高,反应速率越快,因此a、b两点对应的反应速率v<v。②根据三段式可知
a b
d点的总压强为aMPa,则d点的分压平衡常数K = MPa2≈21.33a2(MPa)2。(3)由于第
P
一步为慢反应,则第一步反应的活化能比第二步反应大。由于第二步反应快,催化剂不会以铁的形式大量
存在于反应体系中,所以不会出现催化剂的失活。(4)CO催化变换反应是放热反应,温度升髙时,平衡逆向进行,所以CO催化变换反应的K 减小。根据速率方程可知当T>T 时K 减小对v的降低大于k增大对v
P m p
的提高,所以r逐渐减小。
25.(12分)我国力争在2030年前实现碳达峰,降低碳排放的一个重要措施是 CO 的综合利用,如工业
2
利用CO 合成CHOH,再合成CHOCH 。
2 3 3 3
I. CO(g)+3H(g) CHOH(g)+H O(g) (主反应)
2 2 3 2
II. CO (g)+H(g) CO(g)+HO(g) (副反应)
2 2 2
请回答:
(1)工业原料气配比中需加入一定量的 ,原因是_______。
(2)在温度为T,恒压P的条件下,充入 的CO 和3 mol H 此时体积为2升,发生I、Ⅱ反应达平衡
2 2
时CO的物质的量为 ,HO的物质的量分数为 ,求:(保留2位小数)
2
①CO 的转化率_______。
2
②反应I的平衡常数K为_______。
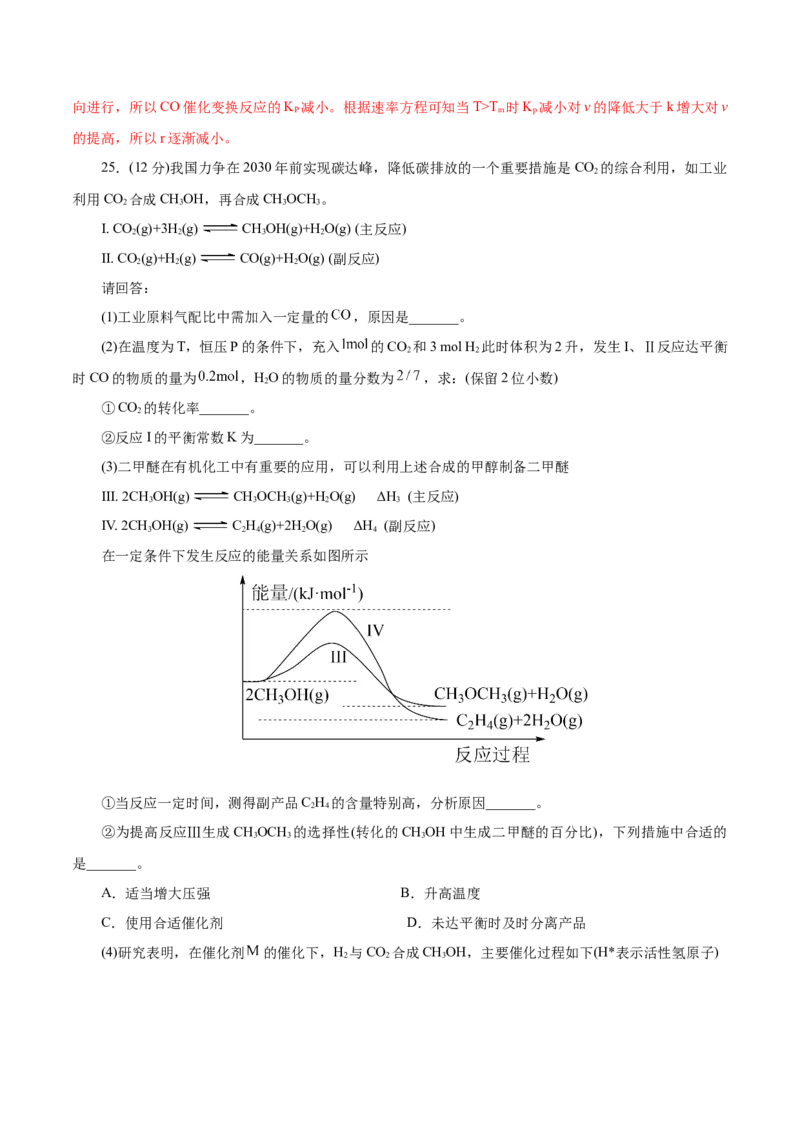
(3)二甲醚在有机化工中有重要的应用,可以利用上述合成的甲醇制备二甲醚
III. 2CH OH(g) CHOCH (g)+HO(g) ΔH (主反应)
3 3 3 2 3
IV. 2CH OH(g) C H(g)+2HO(g) ΔH (副反应)
3 2 4 2 4
在一定条件下发生反应的能量关系如图所示
①当反应一定时间,测得副产品C H 的含量特别高,分析原因_______。
2 4
②为提高反应Ⅲ生成CHOCH 的选择性(转化的CHOH中生成二甲醚的百分比),下列措施中合适的
3 3 3
是_______。
A.适当增大压强 B.升高温度
C.使用合适催化剂 D.未达平衡时及时分离产品
(4)研究表明,在催化剂 的催化下,H 与CO 合成CHOH,主要催化过程如下(H*表示活性氢原子)
2 2 3则A、B结构是_______、_______。
【答案】(1)抑制副反应的发生;与HO反应使反应Ⅰ正向移动,提高CO 的转化率(2分)
2 2
(2) 80%(2分) 4.70或18.82/P2(2分)
(3)对于副反应ΔH <0,且ΔS>0,该反应只向正反应进行,温度越高,时间越长,都会生成更多的
4
C H(2分) CD(2分)
2 4
(4) (2分)
【解析】(1)加入CO,可使反应Ⅱ左移、增大二氧化碳和氢气浓度、有利于反应Ⅰ,则工业原料气配
比中需加入一定量的CO,原因是抑制副反应的发生;与HO反应使反应Ⅰ正向移动,提高CO 的转化率。
2 2
(2) ①已知:发生I、Ⅱ反应达平衡时CO的物质的量为0.2 mol,则:
,
则平衡时,n(CO)=0.2mol,n(CO)=(1-x- 0.2) mol,n(H )=(3-3x- 0.2) mol,n(CHOH)= x mol,
2 2 3
n(H O)=( x+0.2) mol,n(总)=(4-2x) mol,已知HO的物质的量分数为2/7,则 ,得x=0.6,
2 2
则平衡时,n(CO)=0.2mol,n(CO)= 0.2 mol,n(H )=1mol,n(CHOH)= 0.6 mol,n(H O)=0.8mol,n(总)=2.8
2 2 3 2
mol,故:CO 的转化率为 。②在温度为T,恒压P的条件下体积之比为物质的
2
量之比,反应初始时充入1 mol的CO 和3 mol H 此时体积为2升,则 ,平衡时2.8mol气体
2 2总体积 V 应为 1.4L,反应 I 的平衡常数 K 为 。或:
。(3)①由图知,反应Ⅲ、Ⅳ均为放热反应,反
应Ⅲ活化能较小、反应Ⅳ活化能较大,升高温度有利于反应Ⅳ。则当反应一定时间,测得副产品 C H 的含
2 4
量特别高的原因为:对于副反应ΔH<0,且ΔS>0,该反应只向正反应进行,温度越高,时间越长,都会
4
生成更多的C H。②为提高反应Ⅲ生成CHOCH 的选择性(转化的CHOH中生成二甲醚的百分比),则:A
2 4 3 3 3
项,适当增大压强,不影响反应Ⅲ,A错误;B项,由图可知主反应为放热反应,升高温度平衡左移,B
错误;C项,催化剂具有选择性,使用合适催化剂有利于提高生成CHOCH 的选择性,C正确;D项,未
3 3
达平衡时及时分离产品,有利于平衡右移、提高生成CHOCH 的选择性,D正确;故选CD。(4)由图知,
3 3
反应过程中,C原子上碳氧双键中先断一根碳氧键变成碳氧单键、在 C上引入2个H, A、B生成时有C-
O键断裂、C上引入1个H生成A、O原子上引入另一个H生成另一物质B,A和B中断裂M-O继续引入
H同时生成M,则A为 、B结构是 。