文档内容
高二化学上学期期中测试卷 02
(考试时间:90分钟 满分100分)
考试范围:新教材人教版选择性必修1第一、二、三章
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 S 32 Cl 35.5
K 39 Ca 40 Fe 56 Cu 64 Ag 108 Ba 137
选择题部分
一、选择题(本大题共20小题,每小题2分,共40分。每个小题列出的四个备选项中只有一个是符合
题目要求的,不选、多选、错选均不得分)
1.下列说法正确的是( )
A.从HO(g)→H O (l)→H O (s),熵依次增加
2 2 2
B.可逆反应都有一定的限度,限度越大反应物的转化率一定越高
C.可逆反应,若总键能:反应物>生成物,则升高温度不利于提高反应物的转化率
D.对于气体反应,其他条件不变,增大压强反应速率加快,与活化分子的百分含量无关
2.关于反应2SO (g)+ O(g) 2SO (g)的下列描述正确的是( )
2 2 3
A.使用催化剂,SO 的平衡转化率增大
2
B.其它条件不变,增大SO 浓度,平衡常数 增大
3
C.当v (SO )=v (O )时,反应达到平衡状态
正 2 逆 2
D.该反应在一定条件下自发进行的原因是ΔH<0
3.下列关于能量变化的说法正确的是( )
A.“冰,水为之,而寒于水“说明相同质量的水和冰相比较,冰的能量高
B.已知,C(s,石墨)=C(s,金刚石) H>0,则金刚石比石墨稳定
C.灼热的碳与CO
2
反应既是吸热反应△,又是氧化还原反应
D.放热反应都不需要加热,吸热反应都需要加热才能发生
4.在一容积不变,绝热的密闭容器中发生可逆反应:2X(s) Y(g)+Z(g),以下不能说明该反应达
到化学平衡状态的是( )
A.混合气体的密度不再变化 B.反应容器中Y的质量分数不变
C.该反应的化学平衡常数不变 D.容器中混合气体的平均相对分子量不变
5.下列说法不正确的是( )
A.将纯水加热,K 增大,pH不变,仍为中性
W
B.常温下,向 的CHCOOH溶液中加入少量CHCOONH 晶体,溶液的pH增大,说明
3 3 4CHCOOH溶液存在电离平衡
3
C.常温下,酸式盐NaHA的 ,则HA一定是弱酸
2
D.常温下,等pH的盐酸和醋酸溶液加水稀释10倍后,c(Cl-)0
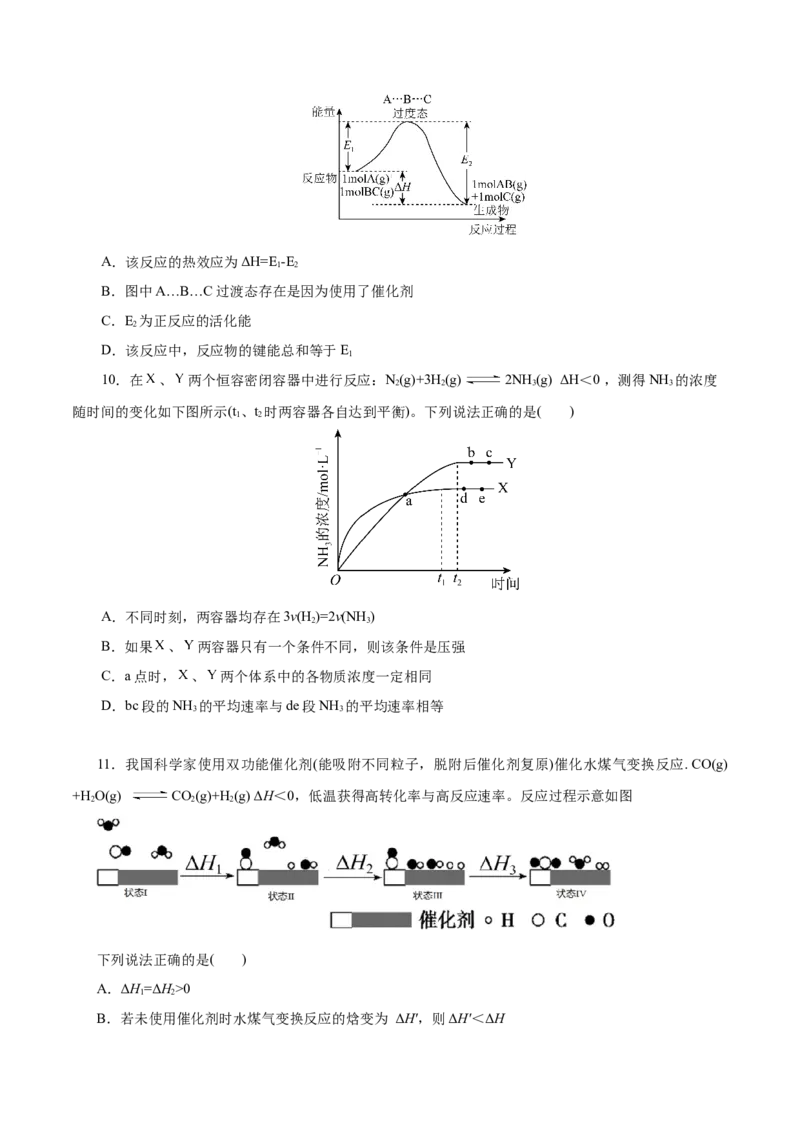
1 2
B.若未使用催化剂时水煤气变换反应的焓变为 ΔH',则ΔH'<ΔHC.图示显示.状态Ⅰ的HO 分子在变换过程中均参与了反应
2
D.ΔH=ΔH+ΔH+ΔH
1 2 3
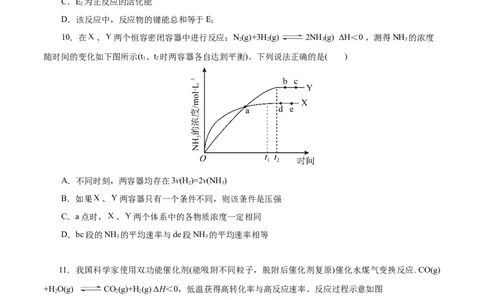
12.在2L密闭恒容容器内,500℃时反应:2NO (g)+CO(g) 2NO (g)体系中,n(NO)随时间的
2 2 2
变化如表:
时间(s) 0 1 2 3 4
0.020 0.010 0.008 0.007
/(mol) 0.007
下列说法正确的是(K表示平衡常数) ( )
A.2s内消耗氧气的平均速率为3.0×10-3mol·L-1·s-1
B.反应达到平衡时,
C.当容器内气体的密度或气体颜色不再发生变化时,该反应达到平衡状态
D.若 ,第4s后升温至达到新平衡过程中逆反应速率先增大后减小
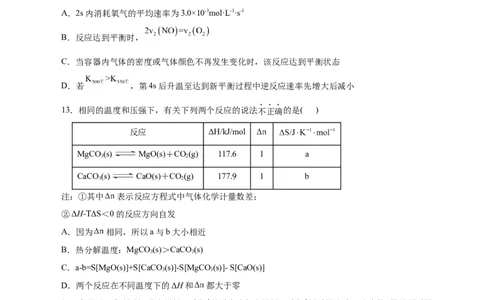
13.相同的温度和压强下,有关下列两个反应的说法不正确的是( )
反应 ΔH/kJ/mol
MgCO(s) MgO(s)+CO(g) 117.6 1 a
3 2
CaCO (s) CaO(s)+CO(g) 177.9 1 b
3 2
注:①其中 表示反应方程式中气体化学计量数差;
②ΔH-TΔS<0的反应方向自发
A.因为 相同,所以a与b大小相近
B.热分解温度:MgCO(s)>CaCO (s)
3 3
C.a-b=S[MgO(s)]+S[CaCO (s)]-S[MgCO(s)]- S[CaO(s)]
3 3
D.两个反应在不同温度下的ΔH和 都大于零
14.室温下,向20.00 mL 0.1000 mol·L−1盐酸中滴加0.1000 mol·L−1 NaOH溶液,溶液的pH随NaOH
溶液体积的变化如图,已知lg3=0.5。下列说法不正确的是( )A.用移液管量取20.00 mL 0.1000 mol·L−1盐酸时,移液管水洗后需用待取液润洗
B.V(NaOH)=10.00 mL 时,pH约为1.5
C.选择甲基红指示反应终点,误差比甲基橙的大
D.都使用酚酞做指示剂,若将NaOH换成同浓度的氨水,所消耗氨水的体积较NaOH多
15.可溶性钡盐有毒,医院中常用硫酸钡这种钡盐(俗称钡餐)作为内服造影剂。医院抢救钡离子中毒
患者时除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:Ksp(BaCO )=5.1×10-9;Ksp(BaSO )=
3 4
1.1×10-10。下列推断正确的是( )
A.BaCO 的溶度积常数表达式为 Ksp(BaCO )= n(Ba2+)·n(CO 2-)
3 3 3
B.可用2%~5%的NaSO 溶液给钡离子中毒患者洗胃
2 4
C.若误服含c(Ba2+)=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO )>Ksp(BaSO )
3 4
16.已知:
反应Ⅰ. CHCHCHCH(g) CH=CH-CH=CH (g)+2H(g) ΔH=-236.6 kJ·mol-1
3 2 2 3 2 2
反应Ⅱ. CHCHCHCH(g) CH-C≡C-CH(g)+ 2H(g) ΔH=-272. 7kJ·mol-1
3 2 2 3 3 3 2
根据上述数据,下列推理不正确的是( )
A.无法比较反应Ⅰ和反应Ⅱ的反应速率的快慢
B.可比较等物质的量的1,3-丁二烯和2-丁炔总键能大小
C.可计算1,3-丁二烯和2-丁炔相互转化的热效应
D.可判断一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
17.已知NaHCO 溶液与盐酸,反应生成CO 吸热,NaCO 溶液与盐酸反应生成CO 放热。关于下列
3 2 2 3 2
△H的判断正确的是( )
CO2-(aq)+H+(aq)= HCO -(aq) ΔH
3 3 1
HCO -(aq)+H+(aq)= HCO(aq) ΔH
3 2 3 2
HCO(aq) CO(g)+HO(l) ΔH
2 3 2 2 3
CO(g)+HO(l)+CO 2-(aq)=2 HCO -(aq) ΔH
2 2 3 3 4A.ΔH<0,ΔH>0 B.ΔH+ΔH >0
1 2 2 3
C.ΔH+ΔH +ΔH >0 D.ΔH<ΔH
1 2 3 1 4
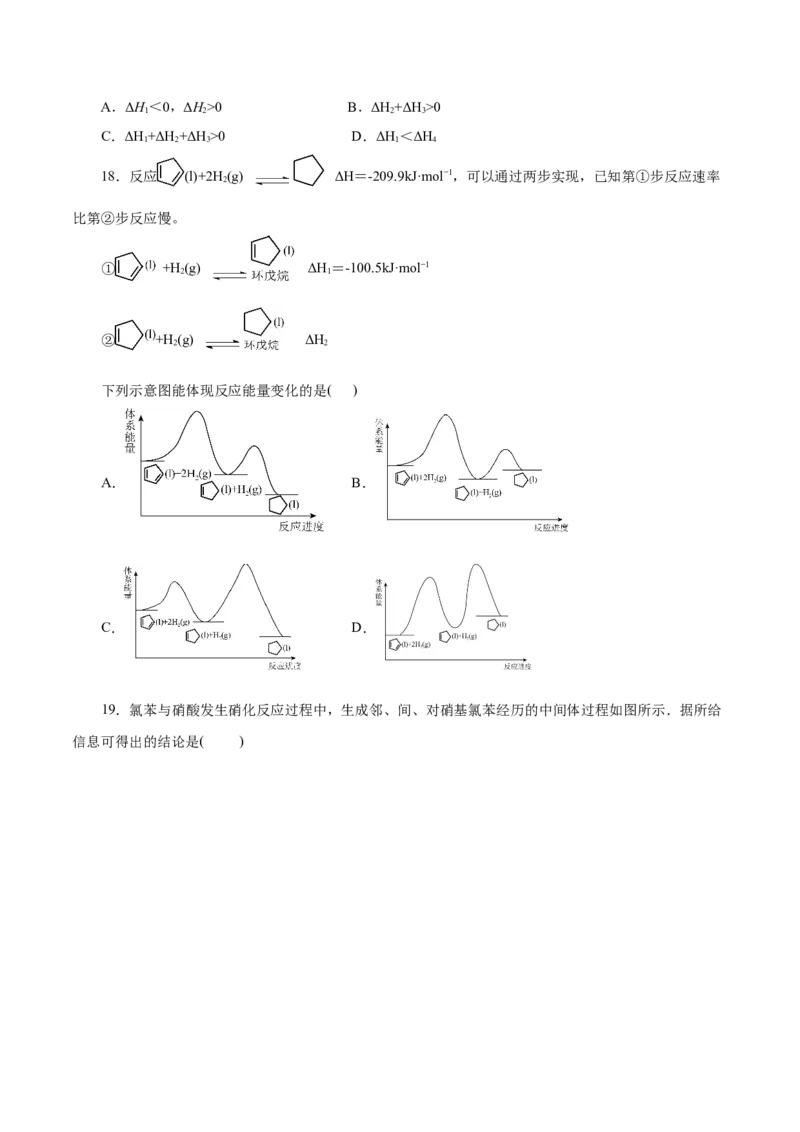
18.反应 (l)+2H (g) ΔH=-209.9kJ·mol−1,可以通过两步实现,已知第①步反应速率
2
比第②步反应慢。
① +H (g) ΔH=-100.5kJ·mol−1
2 1
② +H (g) ΔH
2 2
下列示意图能体现反应能量变化的是( )
A. B.
C. D.
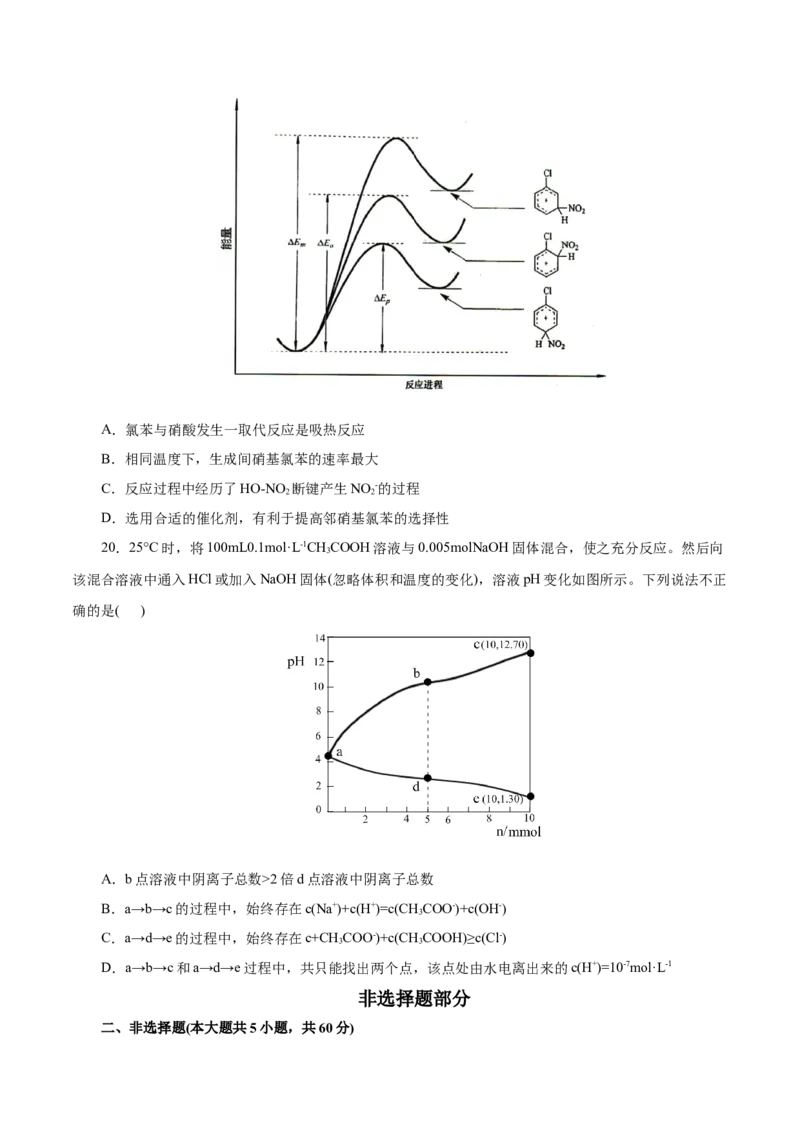
19.氯苯与硝酸发生硝化反应过程中,生成邻、间、对硝基氯苯经历的中间体过程如图所示.据所给
信息可得出的结论是( )A.氯苯与硝酸发生一取代反应是吸热反应
B.相同温度下,生成间硝基氯苯的速率最大
C.反应过程中经历了HO-NO 断键产生NO -的过程
2 2
D.选用合适的催化剂,有利于提高邻硝基氯苯的选择性
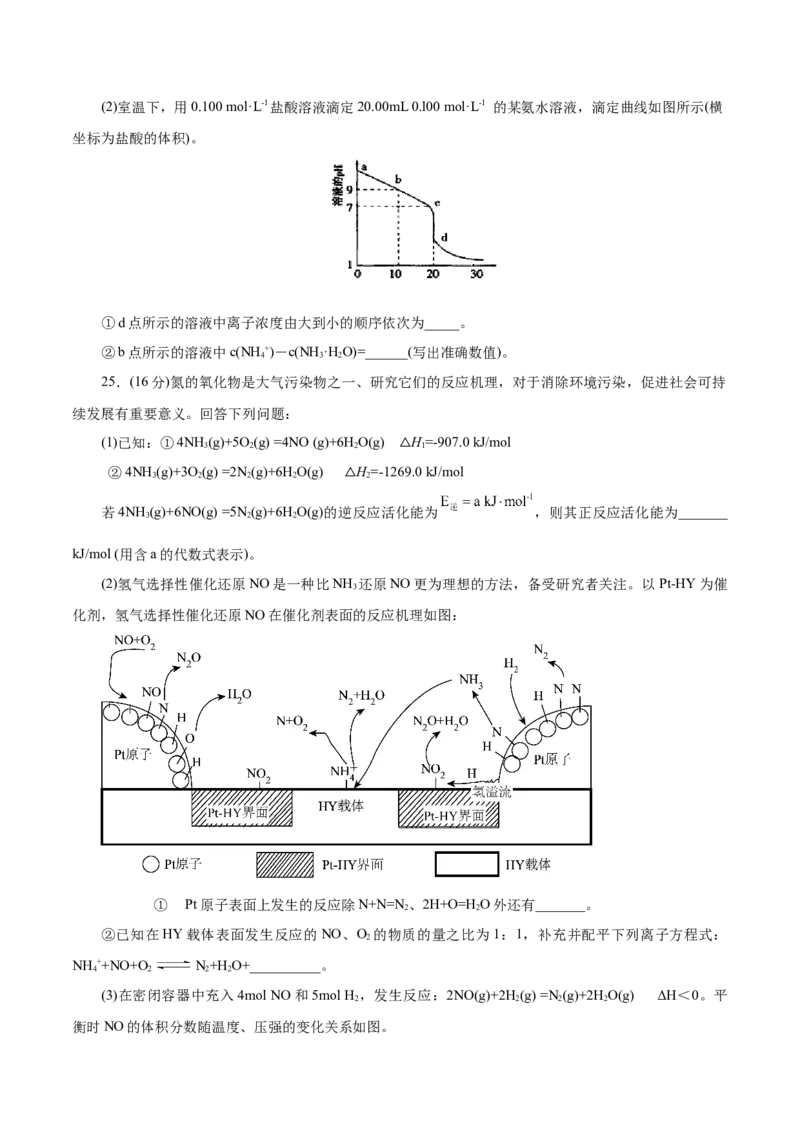
20.25°C时,将100mL0.1mol·L-1CHCOOH溶液与0.005molNaOH固体混合,使之充分反应。然后向
3
该混合溶液中通入HCl或加入NaOH固体(忽略体积和温度的变化),溶液pH变化如图所示。下列说法不正
确的是( )
A.b点溶液中阴离子总数>2倍d点溶液中阴离子总数
B.a→b→c的过程中,始终存在c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3
C.a→d→e的过程中,始终存在c+CH COO-)+c(CH COOH)≥c(Cl-)
3 3
D.a→b→c和a→d→e过程中,共只能找出两个点,该点处由水电离出来的c(H+)=10-7mol·L-1
非选择题部分
二、非选择题(本大题共5小题,共60分)21.(10分)碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回
答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6 kJ·mol-1, 则M与N较稳定的
是_________。
(2)已知CHOH(l)的燃烧热为726.5 kJ·mol-1,CHOH(l) +1/2 O (g)===CO(g)+2HO(g) ΔH=-a
3 3 2 2 2
kJ·mol-1,则a________726.5(填“>”、“<”或“=”)。
(3)使Cl 和HO(g)通过灼热的炭层,生成HCl和CO ,当有1 mol Cl 参与反应时放出145 kJ热量,写
2 2 2 2
出该反应的热化学方程式:___________________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所
得物质可作耐高温材料,4Al(s)+3TiO(s)+3C(s)===2Al O(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过
2 2 3
程中,每转移1 mol电子放出的热量为 __________ 。
(5)已知拆开1 mol H-H键、1 mol N-H键、1 mol N≡N 键分别需要的能量是a kJ、b kJ、c kJ,则N
2
与H 反应生成NH 的热化学方程式为 _______________________ 。
2 3
(6)通过以下反应可获得新型能源二甲醚(CHOCH )。
3 3
①C(s)+HO(g)===CO(g)+H(g) ΔH=a kJ·mol-1
2 2 1
②CO(g)+HO(g)===CO (g)+H(g) ΔH=b kJ·mol-1
2 2 2 2
③CO(g)+3H(g)===CHOH(g)+HO(g) ΔH=c kJ·mol-1
2 2 3 2 3
④2CHOH(g)===CH OCH (g)+HO(g) ΔH=d kJ·mol-1
3 3 3 2 4
则反应2CO(g)+4H(g)===CHOCH (g)+HO(g)的ΔH=___________(用含a,b,c,d的式子表示)。
2 3 3 2
22.(12分)高炉炼铁过程中发生的主要反应为Fe O(s)+CO(g) Fe(s)+CO (g),已知该反应在不
2 3 2
同温度下的平衡常数如表所示:
温度/℃ 1000 1150 1300
平衡常数 4.0 3.7 3.5
请回答下列问题:
(1)该反应的平衡常数表达式K=___________,ΔH___________(填“>”“<”或“=”)0。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe O 各5.0mol;CO、CO 各1.0mol,反应经
2 3 2
过10min后达到平衡则CO的平衡转化率=___________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是___________。A.减少Fe的量 B.移出部分CO C.增加Fe O 的量
2 2 3
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
(4)1000℃时平衡时再向容器中充入2molCO ,则达到新平衡时CO 的浓度___________。
2 2
(5)对于反应2SO (g)+O(g) 2SO (g)ΔH<0,则该反应在___________自发反应;对于反应
2 2 3
SiO(s)+Na CO(s) NaSiO(s)+CO(g)ΔH>0,则该反应在___________自发反应。
2 2 3 2 3 2
23.(10分)2022年风湿领域的重疾之一——痛风领域的新进展。人体内尿酸(HUr)含量偏高,关节滑液
中产生尿酸钠晶体(NaUr)会引发痛风,有关平衡如下:
① HUr(尿酸,aq) Ur-(尿酸根,aq)+H+(aq) 37℃时,Ka =4.0×10-6)
②NaUr(s) Ur-(aq)+Na+(aq)
(1)37℃时,某病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3mol/L,其中尿酸分子的浓度为
5.0×10-4mol/L,该病人尿液的c(H+)为_________。
(2)关节炎发作大都在脚趾和手指的关节处,这说明温度降低时,反应②的K ______(填“增大”、“减
sp
小”或“不变”),生成尿酸钠晶体的反应是_______(填“放热”或“吸热”)反应。
(3) 某课题组配制“模拟关节滑液”进行研究。已知:37℃时,模拟关节滑液pH =7.4,c(Ur-) =
4.6×10−4 mol∙L−1
①37℃时,1.0L水中可溶解8.0×10-3mol尿酸钠,此温度下尿酸钠的K 为________。
sp
②37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______c(Ur−) (填
“>”、“<”或“=”)。
③37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶
体析出,请写出判断过程_____________________________________。
24.(12分)电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 CHCOOH HCN HCO
3 2 3
Ka1=5.0×l0-7
电离常数(25℃) Ka = 1.8×10-5 Ka=4.3×l0-10
Ka2=5.6×l0-11
①0.1 mol·L-1 NaCN溶液和0.1 mol·L-1 NaHCO 溶液中,c(CN-)______c(HCO -)(填“>”、“<”或“=”)。
3 3
②常温下,物质的量浓度相同的三种溶液:A.CHCOONa B.NaCN C.NaCO,其pH由大到小
3 2 3
的顺序是________(填编号)。
③将少量CO 通入NaCN溶液,反应的离子方程式是__________。
2
④室温下,-定浓度的CHCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______,溶液
3
中c(CHCOO-)/c(CH COOH) =________。
3 3(2)室温下,用0.100 mol·L-1盐酸溶液滴定20.00mL 0.l00 mol·L-1 的某氨水溶液,滴定曲线如图所示(横
坐标为盐酸的体积)。
①d点所示的溶液中离子浓度由大到小的顺序依次为_____。
②b点所示的溶液中c(NH +)-c(NH ·H O)=______(写出准确数值)。
4 3 2
25.(16分)氮的氧化物是大气污染物之一、研究它们的反应机理,对于消除环境污染,促进社会可持
续发展有重要意义。回答下列问题:
(1)已知:①4NH (g)+5O(g) =4NO (g)+6H O(g) H=-907.0 kJ/mol
3 2 2 1
②4NH
3
(g)+3O
2
(g) =2N
2
(g)+6H
2
O(g) H
2
=-126△9.0 kJ/mol
△
若4NH (g)+6NO(g) =5N (g)+6HO(g)的逆反应活化能为 ,则其正反应活化能为_______
3 2 2
kJ/mol (用含a的代数式表示)。
(2)氢气选择性催化还原NO是一种比NH 还原NO更为理想的方法,备受研究者关注。以Pt-HY为催
3
化剂,氢气选择性催化还原NO在催化剂表面的反应机理如图:
① Pt原子表面上发生的反应除N+N=N、2H+O=HO外还有_______。
2 2
②已知在HY载体表面发生反应的NO、O 的物质的量之比为1:1,补充并配平下列离子方程式:
2
NH ++NO+O N+H O+__________。
4 2 2 2
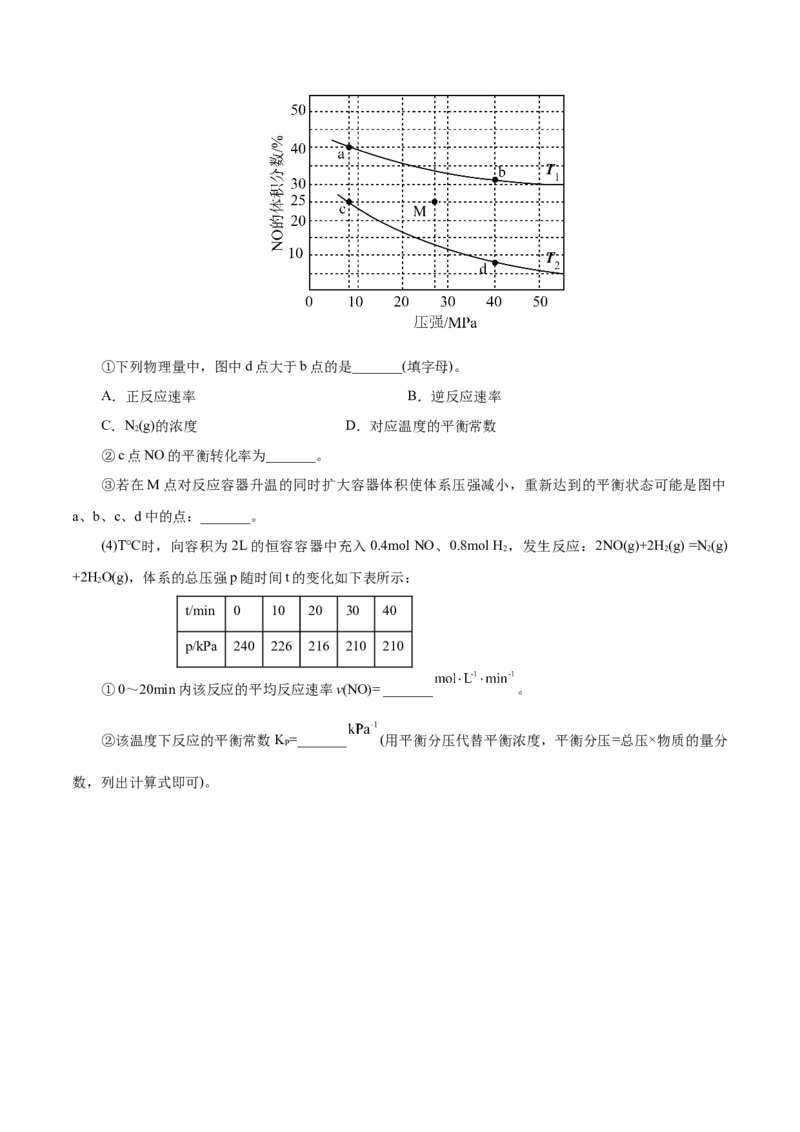
(3)在密闭容器中充入4mol NO和5mol H ,发生反应:2NO(g)+2H (g) =N (g)+2HO(g) ΔH<0。平
2 2 2 2
衡时NO的体积分数随温度、压强的变化关系如图。①下列物理量中,图中d点大于b点的是_______(填字母)。
A.正反应速率 B.逆反应速率
C.N(g)的浓度 D.对应温度的平衡常数
2
②c点NO的平衡转化率为_______。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中
a、b、c、d中的点:_______。
(4)T℃时,向容积为2L的恒容容器中充入0.4mol NO、0.8mol H ,发生反应:2NO(g)+2H (g) =N (g)
2 2 2
+2H O(g),体系的总压强p随时间t的变化如下表所示:
2
t/min 0 10 20 30 40
p/kPa 240 226 216 210 210
①0~20min内该反应的平均反应速率v(NO)= _______ 。
②该温度下反应的平衡常数K =_______ (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分
P
数,列出计算式即可)。