文档内容
人教版(2019) 选择性必修1 第四章 化学反应与能量
第二节 课时2 电解原理的应用
教学设计
教学目标
1、掌握电解饱和食盐水的原理。
2、了解电解原理在电镀、金属精炼、电冶金等方面的应用。
3、掌握电解的有关计算。
教学重难点
重点:电解饱和食盐水的原理;电解的有关计算
难点:电解原理的应用
教学过程
一、导入新课
上节课我们学习了电解的原理,电解是通过电流引起化学反应的过程,即将
电能转变成了化学能。电解的原理在工业上有哪些应用呢?这节课就向同学们介
绍几个电解原理在工业上应用的事例.
二、新课讲授
【师】电解饱和食盐水以制备烧碱、氢气和氯气,电解饱和食盐水的工业生产叫氯
碱工业。
实验原理:阳极(放电顺序:Cl―>OH―):2Cl―-2e— == Cl ↑ (氧化反应)
2
阴极(放电顺序:H+>Na+):2H++2e—==H ↑(还原反应)
2
总反应:2NaCl+2H O 2NaOH +H↑+ Cl↑
2 2 2
【注意】在学习电解食盐水的化学原理时,学生往往不容易理解碱为什么在阴极
区生成。这点可以从H+在阴极上大量被还原,从而引起水的电离平衡被破
坏,来分析在阴极区积累大量OH―的理由。
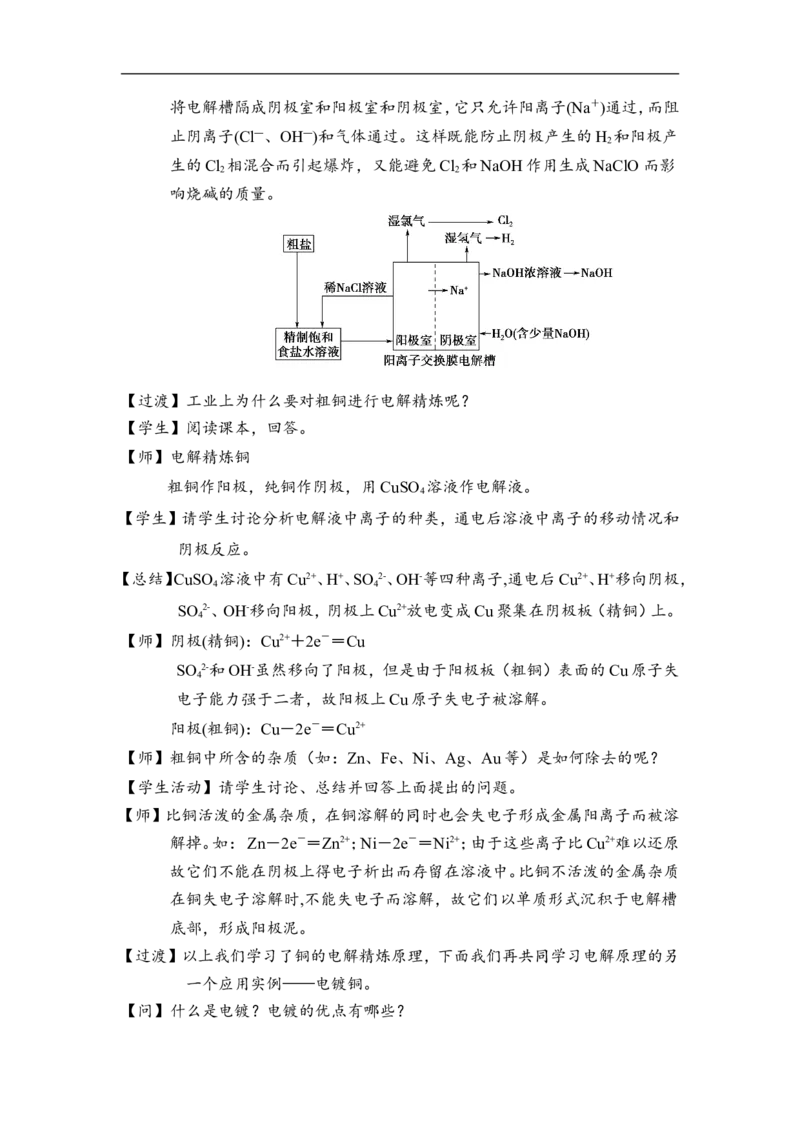
【师】工业制备方法——离子交换膜法
由阳极、阴极、离子交换膜、电解槽框和导电铜棒等组成,每台电解槽由
若干个单元槽串联或并联组成。将电解槽隔成阴极室和阳极室和阴极室,它只允许阳离子(Na+)通过,而阻
止阴离子(Cl―、OH―)和气体通过。这样既能防止阴极产生的H 和阳极产
2
生的Cl 相混合而引起爆炸,又能避免Cl 和NaOH作用生成NaClO 而影
2 2
响烧碱的质量。
【过渡】工业上为什么要对粗铜进行电解精炼呢?
【学生】阅读课本,回答。
【师】电解精炼铜
粗铜作阳极,纯铜作阴极,用CuSO 溶液作电解液。
4
【学生】请学生讨论分析电解液中离子的种类,通电后溶液中离子的移动情况和
阴极反应。
【总结】CuSO 溶液中有Cu2+、H+、SO 2-、OH-等四种离子,通电后Cu2+、H+移向阴极,
4 4
SO 2-、OH-移向阳极,阴极上Cu2+放电变成Cu聚集在阴极板(精铜)上。
4
【师】阴极(精铜):Cu2++2e-=Cu
SO 2-和OH-虽然移向了阳极,但是由于阳极板(粗铜)表面的Cu原子失
4
电子能力强于二者,故阳极上Cu原子失电子被溶解。
阳极(粗铜):Cu-2e-=Cu2+
【师】粗铜中所含的杂质(如:Zn、Fe、Ni、Ag、Au等)是如何除去的呢?
【学生活动】请学生讨论、总结并回答上面提出的问题。
【师】比铜活泼的金属杂质,在铜溶解的同时也会失电子形成金属阳离子而被溶
解掉。如: Zn-2e-=Zn2+;Ni-2e-=Ni2+;由于这些离子比Cu2+难以还原
故它们不能在阴极上得电子析出而存留在溶液中。比铜不活泼的金属杂质
在铜失电子溶解时,不能失电子而溶解,故它们以单质形式沉积于电解槽
底部,形成阳极泥。
【过渡】以上我们学习了铜的电解精炼原理,下面我们再共同学习电解原理的另
一个应用实例——电镀铜。
【问】什么是电镀?电镀的优点有哪些?【学生活动】指导学生查找阅读教材中相关内容,请学生代表回答。
【师】电镀时,把待镀金属制品作为阴极;把镀层金属作为阳极;用含有镀层金属
离子的电解质配成电镀液。通低压直流电,阳极金属在溶液中成为阳离子
移向阴极,在阴极获得电子被还原成金属,在待镀件表面上覆盖上一层均
匀光洁而致密的镀层。
【师】这里还需要我们注意的是,电镀生产过程中产生的废水、废气、废渣中含有
多种对环境有害的物质,处理后应符合国家规定的排放标准,对其中的有
用成分要回收利用。
【过渡】Na、Mg、Al等活泼金属都可用电解它们的熔融盐或氧化物制得。这种方
法是利用电解法来冶炼活泼金属,我们将其称之为电冶金。
【师】电冶金
(1)本质:利用电解使矿石中的金属离子获得电子,从它们的化合物中还原
出来
(2)适用范围:制取活泼金属单质,如电解NaCl、MgCl 、Al O 制取Na、Mg、
2 2 3
Al
板书设计
电解原理的应用
1、电解饱和食盐水制烧碱、氢气和氯气
2、电解精炼铜
3、电镀铜
4、电冶金