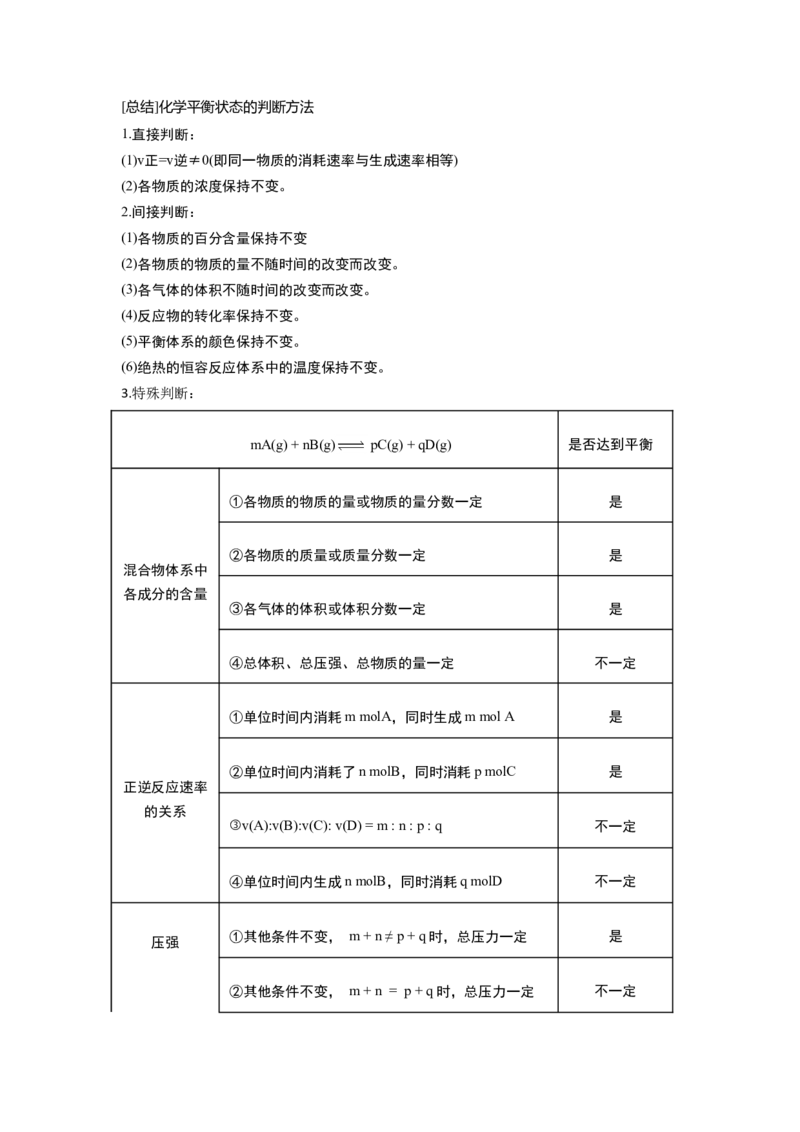文档内容
第二章 化学反应速率与化学平衡
第二节 化学平衡
第1课时 教学设计
【教学目标】
1.通过化学平衡状态的建立过程,知道化学平衡是一种动态平衡。
2.知道化学平衡状态的特征,判断反应是否达到化学平衡状态。
【教学重难点】
平衡状态的判断
【教学过程】
1.新课导入
[师]在科学研究和化工生产中,只考虑化学反应速率是不够的。例如,在工业生产中,除
了需要考虑使原料尽可能快地转化为产品,还需要考虑使原料尽可能多地转化为产品,这
就涉及到化学反应进行的限度,即化学平衡问题。
2.新课讲授
[板书]一、化学平衡的建立
[设疑]很多化学反应是可逆的。什么是可逆反应?可逆反应有什么特点?
[师]在相同条件下,既能向正反应方向进行又能向逆反应方向进行的化学反应。可逆反应
用 连接,把从左向右进行的反应称作正反应,从右向左的进行的反应称作逆反应。可
逆反应具有双向性、双同性、共存性。
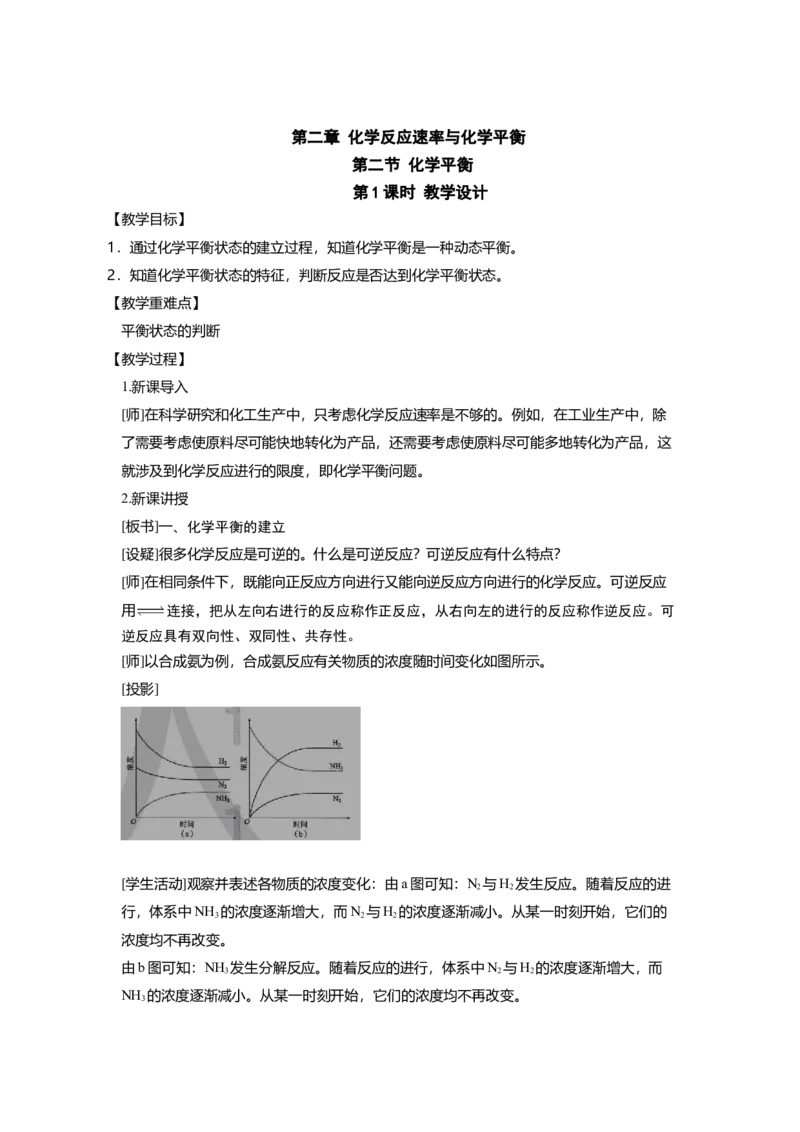
[师]以合成氨为例,合成氨反应有关物质的浓度随时间变化如图所示。
[投影]
[学生活动]观察并表述各物质的浓度变化:由a图可知:N 与H 发生反应。随着反应的进
2 2
行,体系中NH 的浓度逐渐增大,而N 与H 的浓度逐渐减小。从某一时刻开始,它们的
3 2 2
浓度均不再改变。
由b图可知:NH 发生分解反应。随着反应的进行,体系中N 与H 的浓度逐渐增大,而
3 2 2
NH 的浓度逐渐减小。从某一时刻开始,它们的浓度均不再改变。
3[师]a图表示的是合成氨的正反应,b图表示的是合成氨的逆反应,试分析反应开始时、过
程中及平衡时反应物、生成物质浓度的变化与正、逆反应速率的变化。
[生]开始时,反应物浓度最大,正反应速率最大,生成物浓度为0,逆反应速率为0;反应
过程中,反应物浓度逐渐减小,正反应速率也逐渐减小,生成物浓度逐渐增大,逆反应速
率也逐渐增大;一段时间后,达到平衡,此时各组分浓度保持不变,正反应速率等于逆反
应速率。
[师]我们可以借助图像来理解化学平衡的建立。
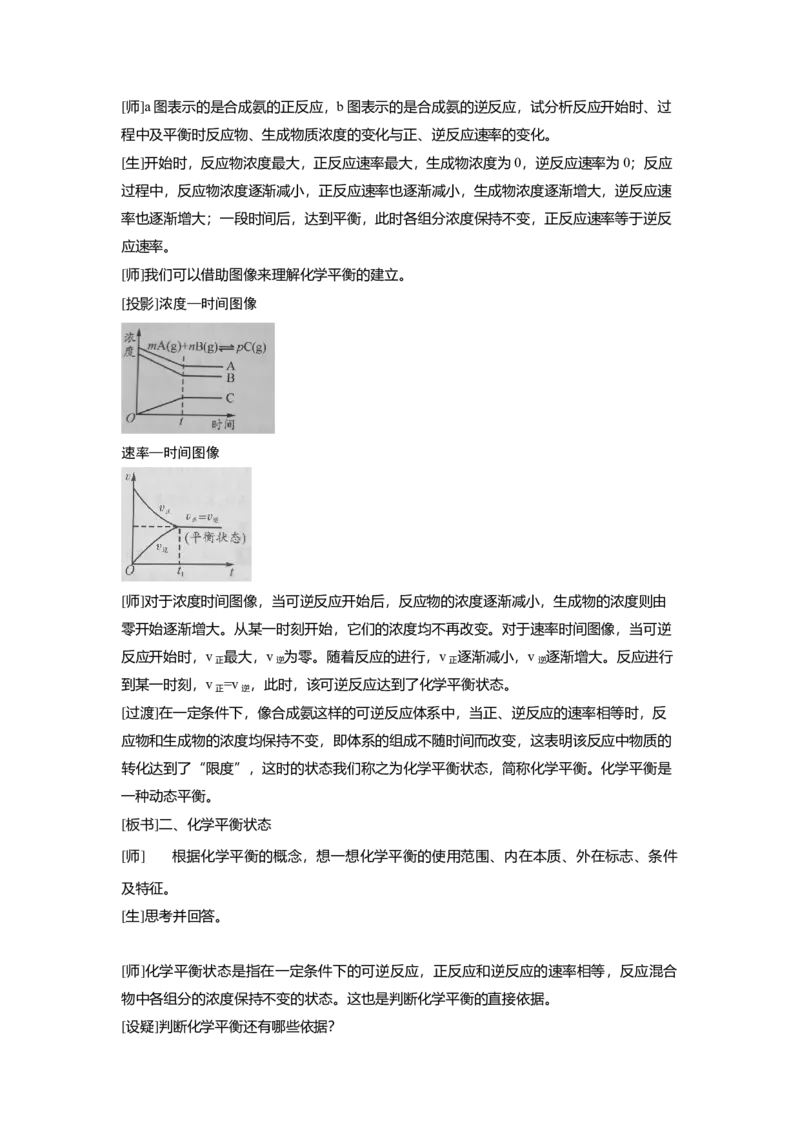
[投影]浓度—时间图像
速率—时间图像
[师]对于浓度时间图像,当可逆反应开始后,反应物的浓度逐渐减小,生成物的浓度则由
零开始逐渐增大。从某一时刻开始,它们的浓度均不再改变。对于速率时间图像,当可逆
反应开始时,v 最大,v 为零。随着反应的进行,v 逐渐减小,v 逐渐增大。反应进行
正 逆 正 逆
到某一时刻,v =v ,此时,该可逆反应达到了化学平衡状态。
正 逆
[过渡]在一定条件下,像合成氨这样的可逆反应体系中,当正、逆反应的速率相等时,反
应物和生成物的浓度均保持不变,即体系的组成不随时间而改变,这表明该反应中物质的
转化达到了“限度”,这时的状态我们称之为化学平衡状态,简称化学平衡。化学平衡是
一种动态平衡。
[板书]二、化学平衡状态
[师] 根据化学平衡的概念,想一想化学平衡的使用范围、内在本质、外在标志、条件
及特征。
[生]思考并回答。
[师]化学平衡状态是指在一定条件下的可逆反应,正反应和逆反应的速率相等,反应混合
物中各组分的浓度保持不变的状态。这也是判断化学平衡的直接依据。
[设疑]判断化学平衡还有哪些依据?[总结]化学平衡状态的判断方法
1.直接判断:
(1)v正=v逆≠0(即同一物质的消耗速率与生成速率相等)
(2)各物质的浓度保持不变。
2.间接判断:
(1)各物质的百分含量保持不变
(2)各物质的物质的量不随时间的改变而改变。
(3)各气体的体积不随时间的改变而改变。
(4)反应物的转化率保持不变。
(5)平衡体系的颜色保持不变。
(6)绝热的恒容反应体系中的温度保持不变。
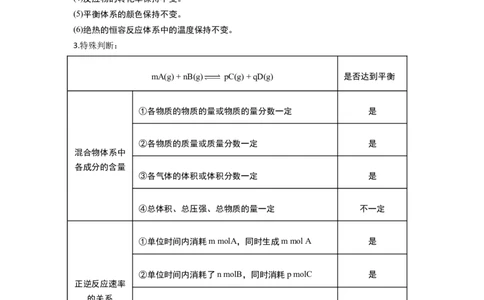
3.特殊判断:
mA(g) + nB(g) pC(g) + qD(g) 是否达到平衡
①各物质的物质的量或物质的量分数一定 是
②各物质的质量或质量分数一定 是
混合物体系中
各成分的含量
③各气体的体积或体积分数一定 是
④总体积、总压强、总物质的量一定 不一定
①单位时间内消耗m molA,同时生成m mol A 是
②单位时间内消耗了n molB,同时消耗p molC 是
正逆反应速率
的关系
③v(A):v(B):v(C): v(D) = m : n : p : q 不一定
④单位时间内生成n molB,同时消耗q molD 不一定
①其他条件不变, m + n ≠ p + q时,总压力一定 是
压强
②其他条件不变, m + n = p + q时,总压力一定 不一定① m + n ≠ p + q时,M一定 是
平均分子量M
② m + n = p + q时,M一定 不一定
温度
其他条件一定时,体系温度一定 是
体系密度
其它条件一定时,密度一定 不一定
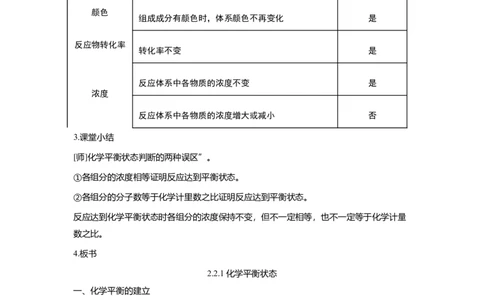
颜色
组成成分有颜色时,体系颜色不再变化 是
反应物转化率
转化率不变 是
反应体系中各物质的浓度不变 是
浓度
反应体系中各物质的浓度增大或减小 否
3.课堂小结
[师]化学平衡状态判断的两种误区”。
①各组分的浓度相等证明反应达到平衡状态。
②各组分的分子数等于化学计里数之比证明反应达到平衡状态。
反应达到化学平衡状态时各组分的浓度保持不变,但不一定相等,也不一定等于化学计量
数之比。
4.板书
2.2.1化学平衡状态
一、化学平衡的建立
二、化学平衡的状态
特征:逆、等、动、定、变
判断化学平衡状态的依据
v正=v逆≠0(即同一物质的消耗速率与生成速率相等)各物质的浓度保持不变。