文档内容
第六章 化学反应与能量
第二节 化学反应速率与限度
第1课时 化学反应的速率
1、了解化学反应速率的概念和表示方法。
2、能够进行化学反应速率的简单计算。
3、理解影响化学反应速率的因素及规律。
重点:化学反应速率的概念及其影响因素;
难点:化学反应速率的影响因素。
化学能与电能
一、化学反应速率
1.定义
化学反应速率是用来衡量化学反应过程进行的快慢的物理量。通常用单位时间 或
(均取正值)表示。
2.计算公式
3.单位
4.实例
某反应的反应物A浓度在5 min内由6 mol·L-1变成了2mol·L-1,则v(A)= 。
【课堂练习】
1、在某一化学反应中,生成物 B的浓度在5s内从0.5 mol/L变成2.0 mol/L,在这5s内B的化学反应速率
为_______。2、一个5L的容器中,盛入8.0 moL某气体反应物,5 min后,测得这种气体反应物还剩余6.8moL,这种
反应物的化学反应速率为___________。
【思考与发现】
反应:N(g)+3H(g) 2NH (g)在密闭的容器中进行,各物质浓度随时间变化如下:完成表格并
2 2 3
求在2 s内的这个反应的平均率。
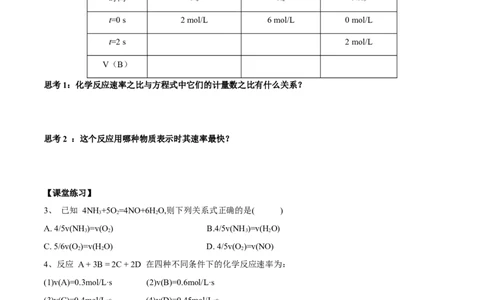
时间 N H NH
2 2 3
t=0 s 2 mol/L 6 mol/L 0 mol/L
t=2 s 2 mol/L
V(B)
思考1:化学反应速率之比与方程式中它们的计量数之比有什么关系?
思考2 :这个反应用哪种物质表示时其速率最快?
【课堂练习】
3、 已知 4NH +5O =4NO+6HO,则下列关系式正确的是( )
3 2 2
A. 4/5v(NH )=v(O) B.4/5v(NH )=v(HO)
3 2 3 2
C. 5/6v(O )=v(HO) D. 4/5v(O )=v(NO)
2 2 2
4、反应 A + 3B = 2C + 2D 在四种不同条件下的化学反应速率为:
(1)v(A)=0.3mol/L·s (2)v(B)=0.6mol/L·s
(3)v(C)=0.4mol/L·s (4)v(D)=0.45mol/L·s
则该反应速率的快慢顺序为 。
【思考与讨论】
对于下列反应,你是希望其反应速率越快越好还是越慢越好?
■钢铁腐蚀 ■ 食物腐坏 ■ 炼钢 ■ 合成氨
调控化学反应速率常常是决定化学实验成败或化工生产成本的关键。有哪些因素能够影响化学反应速率呢?
二、影响化学反应速率的因素
影响化学反应速率的因素
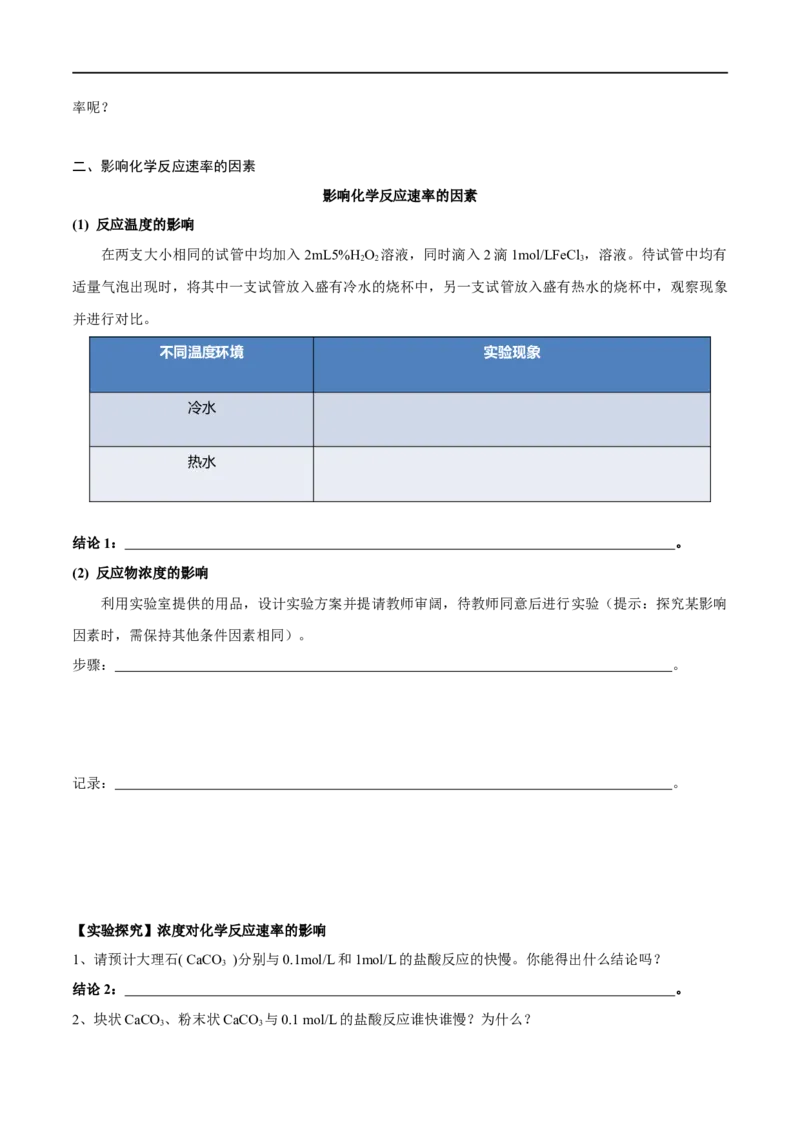
(1) 反应温度的影响
在两支大小相同的试管中均加入2mL5%H O 溶液,同时滴入2滴1mol/LFeCl ,溶液。待试管中均有
2 2 3
适量气泡出现时,将其中一支试管放入盛有冷水的烧杯中,另一支试管放入盛有热水的烧杯中,观察现象
并进行对比。
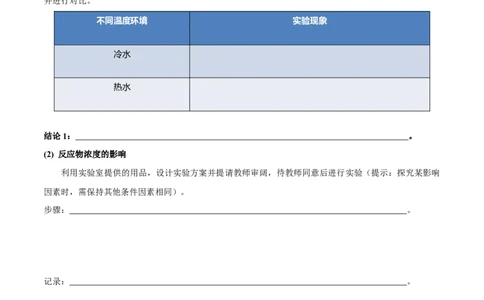
不同温度环境 实验现象
冷水
热水
结论1: 。
(2) 反应物浓度的影响
利用实验室提供的用品,设计实验方案并提请教师审阔,待教师同意后进行实验(提示:探究某影响
因素时,需保持其他条件因素相同)。
步骤: 。
记录: 。
【实验探究】浓度对化学反应速率的影响
1、请预计大理石( CaCO )分别与0.1mol/L和1mol/L的盐酸反应的快慢。你能得出什么结论吗?
3
结论2: 。
2、块状CaCO 、粉末状CaCO 与0.1 mol/L的盐酸反应谁快谁慢?为什么?
3 3结论3: 。
【实验探究】催化剂对化学反应速率的影响
现象 结论
加入MnO
2
加入FeCl
3
不加其他试剂
结论4: 。
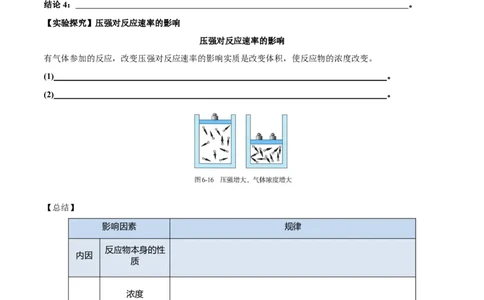
【实验探究】压强对反应速率的影响
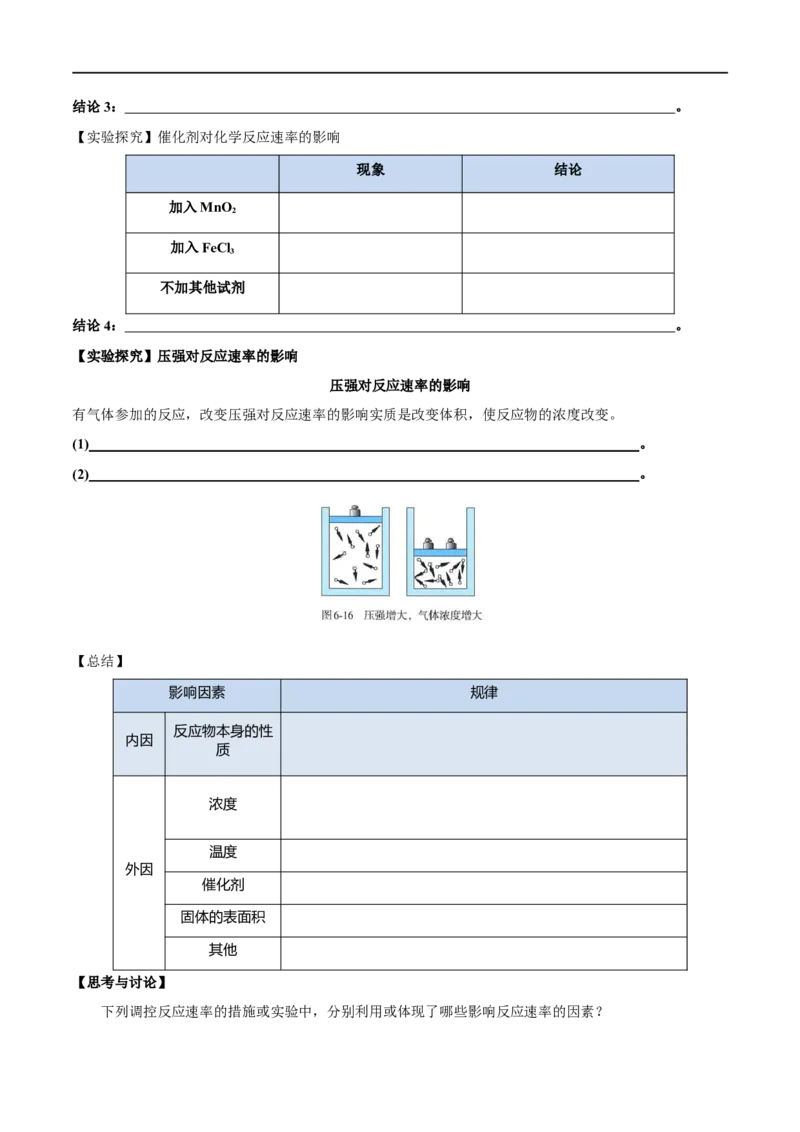
压强对反应速率的影响
有气体参加的反应,改变压强对反应速率的影响实质是改变体积,使反应物的浓度改变。
(1) 。
(2) 。
【总结】
影响因素 规律
反应物本身的性
内因
质
浓度
温度
外因
催化剂
固体的表面积
其他
【思考与讨论】
下列调控反应速率的措施或实验中,分别利用或体现了哪些影响反应速率的因素?(1)向炉膛内鼓风,用煤粉代替煤块可以使炉火更旺。
(2)把食物存放在冰箱里,在糕点包装内放置除氧剂可以延长食品保质期。
(3)做化学实验时,为加速反应的进行,通常将块状或颗粒状的固体药品研细并混匀,或者将固体试剂
溶于水配成溶液后再进行实验。
(4)铁在空气中和在纯氧中反应的剧烈程度明显不同。
【课堂练习】
1.下列关于化学反应速率的说法,不正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率的大小主要取决于反应物的性质
C.化学反应速率可以用单位时间内生成某物质的质量的多少来表示
D.化学反应速率常用单位有mol·L-1·s-1和mol·L-1·min-1
2.一定条件下,分别对反应C(s)+CO(g) 2CO(g)进行如下操作(只改变该条件):①升高反应体系的温
2
度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应
速率显著变大的是( )
A.①②③④ B.①③④
C.①② D.①③
3.已知合成氨反应N(g)+3H(g)2NH (g),其浓度数据如下:
2 2 3
N H NH
2 2 3
起始浓度/mol·L-1 1.0 3.0 0
2 s末浓度/mol·L-1 0.6 1.8 0.8
当用氨气浓度的增加来表示该化学反应的速率时,其速率为( )
A.0.2 mol·L-1·s-1 B.0.4 mol·L-1·s-1
C.0.6 mol·L-1·s-1 D.0.8 mol·L-1·s-1
4.把下列四种X溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此时,X
和盐酸缓慢地进行反应,其中反应最快的是( )
A.10 ℃ 20 mL 3 mol·L-1的X溶液
B.20 ℃ 30 mL 2 mol·L-1的X溶液
C.20 ℃ 10 mL 4 mol·L-1的X溶液
D.10 ℃ 10 mL 2 mol·L-1的X溶液
5.实验室用锌粒与2 mol·L-1硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )A.用锌粉代替锌粒
B.改用3 mol·L-1硫酸溶液
C.改用热的2 mol·L-1硫酸溶液
D.向该硫酸溶液中加入等体积的水