文档内容
第五章 化工生产中的重要非金属元素
第 2 节 氮及其化合物
第 1 课时 氮气与氮的固定 一氧化氮和二氧化氮
本节是人教版第五章第二节氮及其化合物的内容。本节内容主要包括:氮及氮的固定、一氧化
氮和二氧化氮、氨和铵盐、硝酸、酸雨及其防治。教材首先根据氮的原子结构知识,应用前一节掌
握的研究非金属单质性质的基本思路预测氮的化学性质,渗透条件对化学反应的影响,引出氮的固
定对人类生存的重要意义。之后,根据物质类别研究氮的化合物,包括一氧化氮、二氧化氮、硝酸、
氨和铵盐的化学性质。以工业合成氨、工业制硝酸的生产原理为载体,应用氧化还原反应原理,设
计含氮化合物的转化,使学生认识到从一种原料转化成多种产品,路径之一是通过氧化还原反应改
变主要元素的化合价,提升“变化观念”等学科核心素养。教材设置铵根离子的检验、实验室制取
氨的实验活动,让学生根据氨、铵根离子的性质和反应,选择合适的试剂,设计检验或者制取物质
的方案,提升其科学探究的能力。最后,教材编入“酸雨及其防治”内容以及“测定雨水的 pH”的
研究与实践活动,综合运用硫和氮及其化合物的相关知识,寻求证据参与社会性议题的讨论,分析
硫酸工业、合成氨工业对社会发展的价值和对环境的影响,有意识地渗透资源合理利用和环境保护
的意识。
《普通高中化学课程标准(2017版)》对本节的要求:结合真实情境中的应用实例或通过实验探
究,了解氮及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。结合
实例认识金属、非金属及其化合物的多样性,了解通过化学反应可以探索物质性质、实现物质转化,
认识物质及其转化在自然资源综合利用和环境保护中的重要价值。其情景素材建议为:“雷雨发庄
稼”;氮的循环与氮的固定;工业合成氨、工业制硫酸(或硝酸);氮肥的生产与合理使用;氯气、
氨气等泄漏的处理;酸雨的成因与防治;汽车尾气的处理。因此内容安排三个课时:第一课时为氮
气与氮的固定,一氧化氮和二氧化氮,第二课时为氨和铵盐,第硝酸和酸雨及防治。本节为第一课
时的内容。
【学习目标】
1、了解氮元素的存在及氮的固定。
2、掌握NO、NO 的性质。
23、了解NO、NO 、O 溶于水的简单计算(对生成硝酸的启示)。
2 2
【核心素养】
1、通过学习氮及氮的氧化物的知识培养学生论据推理与模型认知的化学核心素养。
2、通过氮的氧化物溶于水的实验进一步训练学生的操作技能,培养学生科学探究与实验创新
的化学核心素养。
1、氮气、一氧化氮、二氧化氮的化学性质为重点。
2、NO 溶于水的计算为难点。
x
多媒体、注射器、NO
【引入】
氮元素位于元素周期表的第二周期,VA族。氮原子的最外层有5个电子,既不容易得到3个
电子,也不容易失去5个电子。一般通过共用电子对与其他原子结合。在自然界里,氮元素主要以
氮分子的形式存在于空气中,部分氮元素存在于动植物体内的蛋白质中,还有部分氮元素存在于土
壤、海洋里的硝酸盐和铵盐中。
【讲解1】
一、氮气
(1) 氮气的物理性质
颜色 状态 气味 密度 溶解性
_____ 气体 _____ 密度与空气接近 ___溶于水
(2) 氮气的化学性质 氮气的结构
氮气的化学性质_____,通常很难与其他物质发生化学反应。① 还原性:氮气与氧气的反应,其化学方程式为 。
② 氧化性
a. N 与H 反应生成NH ,化学方程式为 。
2 2 3
b. 在点燃条件下与Mg反应,方程式为 。
【讲解2】
二、氮的固定
(1) 含义: 将大气中_______的氮转化为___________的过程叫做氮的固定。
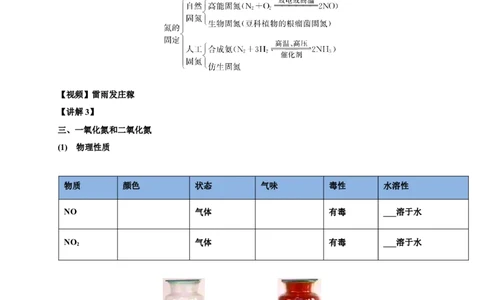
(2) 分类:
【视频】雷雨发庄稼
【讲解3】
三、一氧化氮和二氧化氮
(1) 物理性质
物质 颜色 状态 气味 毒性 水溶性
NO 气体 有毒 ___溶于水
NO 气体 有毒 ___溶于水
2
(2) 化学性质【实验5-5】实验
装置
在一支50 mL的注射器里充入20 mL NO,
实验 然后吸入5mL
打开弹簧夹,快速吸入10 mL空气后夹上
弹簧夹,观察现象,然后再振荡注射器
操作 水,用乳胶管和弹簧夹封住管口,振荡注
射器
现象
振荡后________________
结论:在一定条件下,NO与NO 可以相互转化。
2
反应的化学方程式为
①NO→NO : _____________________;
2
②NO →NO: __________________________(工业制取硝酸)。
2
【思考与讨论】
实验5-5发生了哪些化学反应?如果将注射器中的NO充分转化,可以采取什么措施?上述实
验对工业生成硝酸有什么启示?
【讲解3】
工业生成硝酸的启示
(1) 原理
解答氮的氧化物溶于水的计算问题首先明确原理,无论是单一气体(NO ),还是NO、NO 、
2 2
O 中的两者或三者的混合气体,反应的实质是 3NO +H O = 2HNO +NO,2NO+O = 2NO ,故若有
2 2 2 3 2 2
气体剩余只能是NO或O,不能是NO 。
2 2
1、 NO与O 同时通入水中
2
2NO+O ===2NO ①
2 2
3NO +H O===2HNO+NO ②
2 2 3
①×3+②×2 总的化学方程式为 4NO+3O +2H O===4HNO
2 2 3
② NO 和O 混合气体溶于水的计算
2 23NO +H O===2HNO+NO ①
2 2 3
2NO+O ===2NO ②
2 2
①×2+② 总的化学方程式为 4NO +O +2H O===4HNO
2 2 2 3
【思考与讨论】
(1) NO和NO 分别采用什么方法收集?
2
(2)NO 转化为NO的变化中,NO 只能作氧化剂吗?
2 2
【总结】【课堂练习】
1. 如图所示的试管中装有12 mL NO,然后间歇缓慢地通入8 mLO。有关最终状态的描述:①试管
2
内气体呈红棕色,②试管内气体呈无色,③试管内液面不变,④试管内液面上升,⑤试管内气体是
O,⑥试管内气体是NO。其中正确的是( )
2
A. ①③ B. ②④⑤ C. ②④⑥ D. ②③⑤
2. 同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO ,
2
②NO 和O ,③NO和N 。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积
2 2 2
分别为V、V、V,则下列关系正确的是( )
1 2 3
A.V>V >V B.V>V >V
1 2 3 1 3 2
C.V>V >V D.V>V >V
2 3 1 3 1 2
3. 在容积为672 mL的烧瓶中充满NO和NO 的混合气体,将其倒立在水槽里,去塞后再通入280
2
mL氧气,恰好完全反应,且液体充满烧瓶(气体体积都已折合为标准状况下的体积),下列有关叙
述正确的是( )
A. 总反应为NO+NO +O+HO === 2HNO
2 2 2 3
B. 总反应为4NO+8NO +5O+6HO === 12HNO
2 2 2 3
C. 生成硝酸的物质的量浓度均为0.030 mol·L-1
D. 生成硝酸的物质的量浓度约为0.060 mol·L-1
4. 用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:NO +NO+2NaOH===2NaNO +HO
2 2 2
2NO +2NaOH===NaNO +NaNO +HO
2 2 3 2
现有V L某NaOH溶液能完全吸收n mol NO 和m mol NO 组成的大气污染物。
2
(1)所用烧碱溶液的物质的量浓度至少为 mol·L-1
(2)若所得溶液中(NO -:NO -)=1:9,则原混合气体中NO 和NO的物质的量之比n:m=
3 2 2
。