文档内容
格致课堂
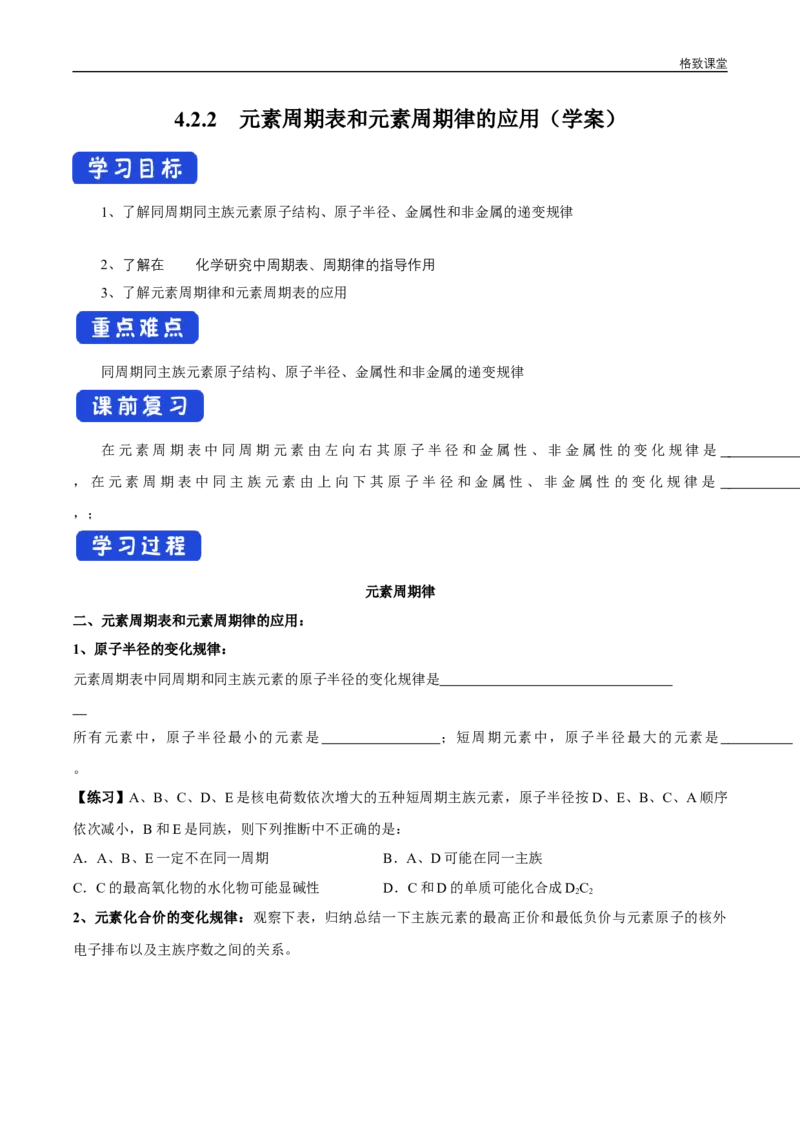
4.2.2 元素周期表和元素周期律的应用(学案)
1、了解同周期同主族元素原子结构、原子半径、金属性和非金属的递变规律
2、了解在 化学研究中周期表、周期律的指导作用
3、了解元素周期律和元素周期表的应用
同周期同主族元素原子结构、原子半径、金属性和非金属的递变规律
在元素周期表中同周期元素由左向右其原子半径和金属性、非金属性的变化规律是
,在元素周期表中同主族元素由上向下其原子半径和金属性、非金属性的变化规律是
,;
元素周期律
二、元素周期表和元素周期律的应用:
1、原子半径的变化规律:
元素周期表中同周期和同主族元素的原子半径的变化规律是
所有元素中,原子半径最小的元素是 ;短周期元素中,原子半径最大的元素是
。
【练习】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A顺序
依次减小,B和E是同族,则下列推断中不正确的是:
A.A、B、E一定不在同一周期 B.A、D可能在同一主族
C.C的最高氧化物的水化物可能显碱性 D.C和D的单质可能化合成DC
2 2
2、元素化合价的变化规律:观察下表,归纳总结一下主族元素的最高正价和最低负价与元素原子的核外
电子排布以及主族序数之间的关系。格致课堂
根据上面的表格,可以总结出来主族元素的化合价的规律有:
(1)
(2)
(3)
(4)
【练习】某主族元素R的最高正化合价与负化合价的代数和为4,下列有关叙述正确的是( )
A、R一定是第四周期元素
B、R的气态氢化物分子式为HR
2
C、R的气态氢化物比同周期其他元素的气态氢化物稳定
D、R的气态氢化物的水溶液显碱性
【练习】五种短周期元素的原子半径、最高正化合价及负化合价见下表( )
元素代号 L M Q R T
原子半径/nm 0.160 0.089 0.143 0.102 0.074
化合价 +2 +2 +3 +6,-2 -2
下列叙述正确的是
A.L的金属性比M的金属性弱
B.Q、T两元素间可形成两性化合物
C.T的单质是黄绿色气体
D.L、R两元素的简单离子的核外电子数可能相等
3、元素金属性和非金属性的变化规律:
同周期、同主族元素的金属性、非金属性变化的规律是
短周期主族元素金属性最强的元素是 ;非金属性最强的元素是 。
【思考与交流】根据之前的学习,总结比较元素的非金属性和金属性强弱的方法。
证明金属性强弱的方法有:格致课堂
(1)
(2)
证明非金属性强弱的方法有:
(1)
(2)
(3)
短周期主族元素的最高价氧化物的水化物中酸性最强的是 ;碱性最强的是
;气态氢化物稳定性最强的是 。
【练习】已知铍(Be)的原子序数为4。下列对铍及其化合物的叙述中,正确的是
A.铍的原子半径大于硼的原子半径
B.氯化铍分子的化学式为BeCl
2
C.氢氧化铍的碱性比氢氧化钙的弱
D.单质铍跟冷水反应产生氢气
【练习】电子层数相同的三种元素X、Y、Z,它们最高氧化物对应的水化物的酸性由强到弱的顺序是:
HXO>H YO >H ZO。下列判断中不正确的是( )
4 2 4 3 4
A.原子序数:XY>Z
C.元素的非金属性:X>Y>Z
D.气态氢化物的稳定性:X>Y>Z
【思考与交流】根据元素周期表和元素周期律,互相交流讨论,填写下表:
元素名称 硒 元素符号 Se
原子序数 34 金属还是非金属?
原子结构示意图
最高正价 最低负价
常见中间价 气态氢化物化学式
最高价氧化物 最高价氧化物对应水化物
与硫酸比较酸性 与硫化氢比较稳定性
在生产生活中,周期表和周期律还有更广泛的应用。由于周期表中位置相近的元素的性质相似,所以在一
定区域内寻找元素、发现物质的新用途是一种相当有效的方法。
(1)在周期表中金属和非金属的分界处可以找到 ,如 等。
(2)通常农药所含的 等元素在周期表中位置靠近,对这个区域内的元素进格致课堂
行研究,有助于研制出新品种的农药。科学家还在 中寻找耐高温、耐腐蚀的合
金元素以及制造催化剂的元素。
1.下列各组中,所有元素是按最高正化合价由高到底,最低负化合价绝对值由低到高顺序排列的是
A.Na、Mg、Al B.F、O、N C.N、O、F D.S、P、Si
2.元素 X的最低腐化合价和最高正化合价代数和等于4,X可能是
A.C B.Si C.S D.Be
3.根据中学化学教材所附元素周期表判断,下列叙述不正确的是
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
4.两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前 10号元素中,满足
上述关系的元素共有
A.1对 B.2对 C.3对 D.4对
5.下列说法正确的是
A.非金属元素R所形成的含氧酸盐(MRO )中的R元素必定呈现正价
a b
B.只有非金属能形成含氧酸或含氧酸盐
C.除稀有气体外的非金属元素都能生成不同价态的含氧酸盐
D.非金属的最高价含氧酸盐具有强氧化性
6.主族元素R最高正价氧化物对应水化物的化学式为HRO,则其氢化物的化学式是
2 3
A.HR B.RH C.HR D.RH
3 2 3
7.如图所示,已知A元素的最低化合价为-3价,它的最高价氧化物含氧56.21%,原子核内中子数比质
子数多1,试回答(均用具体的元素符号或化学式回答):
(1)写出它们的元素符号:
A________,B________,C________,D________。
(2)A、B、C、D的气态氢化物稳定性最差的是________。格致课堂
(3)A、B、C的原子半径由小到大的顺序是________。
(4)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是
___________________________________________________________。
【知识点填空答案】同周期元素由左向右原子半径依次减小(不包括稀有气体),同主族元素由上向下原
子半径依次增大;H;Na;C;同周期由左向右主族元素的最高正价逐渐有+1价升高至+7价(O和F一般
不呈现正价);同主族元素的最高正价和最低负价相同(注意O和F);主族元素的最高正价等于该元素
的原子最外层电子数,也等于其主族序数;非金属元素的最高正价和最低负价的绝对值之和等于 8(H的
最低负价为-1);B;B;同周期元素由左向右金属性减弱,非金属性增强;同主族元素由上向下金属性增
强非金属性减弱;Na;F;单质与水(或酸)反应生成氢气的难易(金属性越强反应越容易);最高价氧
化物的水化物——氢氧化物的碱性强弱(金属性越强氢氧化物的碱性越强);单质与氢气反应生成气态氢
化物的难易(非金属性越强反应越容易);最高价氧化物的水化物的酸性强弱(非金属性越强酸性越强);
气态氢化物的稳定性(非金属性越强气态氢化物越稳定);HClO ;NaOH;HF;非金属; ;
4
+6;-2;+4;HSe;SeO;HSeO;弱;弱;半导体材料;硅、锗、镓;氟、氯、硫、磷、砷;过渡元素;
2 3 2 4
【检测反馈答案】1.D 2.C 3.C 4.B 5.A 6.D
7.(1)P S Cl O (2)PH (3)ClHSO>HPO
3 4 2 4 3 4