文档内容
格致课堂
第四章 元素周期律
4.1.2 原子结构与元素的性质
1、知道碱金属元素、卤族元素的原子结构及特点。
2、能说出碱金属元素、卤族元素化学性质的相似性及递变性。
3、初步学会根据原子结构的特点,推测元素的化学性质。
1、碱金属元素、卤族元素化学性质的相似性及递变性。
2、能推测元素的化学性质。
我们把ⅠA 称为碱金属族,有哪些?元素符号怎么写?
VII A 族元素称为卤族元素,有哪些?元素符号怎么写?
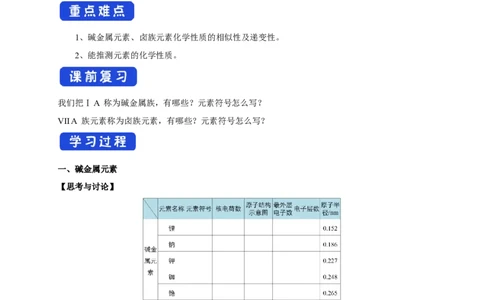
一、碱金属元素
【思考与讨论】
(1) 在周期表中,从上到下碱金属元素原子的核电荷数、原子半径的变化有什么特点?
(2) 观察碱金属元素的原子结构示意图,它们的原子核外电子排布有什么特点?从哪一点能够推断
出碱金属元素的化学性质具有相似性?格致课堂
【总结】通过分析上表可知,碱金属元素原子结构的共同点是 ,不同点是
,其变化规律是 。
【实验探究】
(1)回忆第二章学过的知识,钠有哪些化学性质?
(2)结合锂、钠和钾的原子结构特点,请你预测锂、钾可能具有哪些与钠相似的化学性质。
【分析和结论】
(1)通过实验、观察,讨论并总结钠、钾有哪些相似的化学性质,与你最初根据原子结构特点进
行的预测是否一致?
(2)从实验现象比较钾、纳与水反应的难易程度。由此,你能推断出锂与水反应的难易程度吗?
(3)通过比较碱金属与水反应的难易程度,你能发现与它们的原子结构有什么关系吗?由此,你
能推断出碱金属元素化学性质的相似性和递变规律吗?
【总结】
1、碱金属元素的化学性质的相似性
碱金属元素原子的最外层上都有 个电子,他们的化学性质相似,很容易 ,都能
和氧气与水发生反应。因此碱金属元素的化合价都是 价。
2、碱金属元素的化学性质的递变性
①与O 的反应
2
②与水的反应
2Na + 2HO = 2NaOH + H ↑(剧烈)
2 2
2K + 2HO = 2KOH + H ↑(更剧烈)
2 2
随着原子序数的递增,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,碱金属元素格致课堂
的原子失电子能力逐渐增强,金属性逐渐增强,单质还原性增强。
①与O 的反应越来越剧烈,产物更加复杂。
2
②与HO的反应越来越剧烈。
2
③最高价氧化物对应水化物的碱性逐渐增强,CsOH的碱性最强。
【归纳总结】碱金属元素的原子结构特点
二、卤族元素
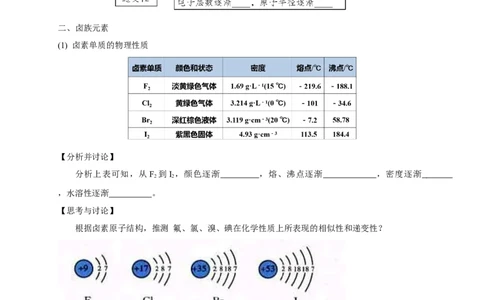
(1) 卤素单质的物理性质
【分析并讨论】
分析上表可知,从F 到I ,颜色逐渐 ,熔、沸点逐渐 ,密度逐渐
2 2
,水溶性逐渐 。
【思考与讨论】
根据卤素原子结构,推测 氟、氯、溴、碘在化学性质上所表现的相似性和递变性?
(2)卤素单质与氢气的反应格致课堂
【思考与讨论】
(1)根据卤素的原子结构,请你试着推测氟、氯、溴、碘在化学性质上表现出的相似性和递变性。
(2)根据卤素单质与氢气的反应事实,讨论随着原子核电荷数的增多,卤素单质与氢气反应的规
律性变化。
【总结】
从F 到I ,与H 反应所需要的条件逐渐 ,反应剧烈程度依次 ,生成气态氢
2 2 2
化物的稳定性依次 。
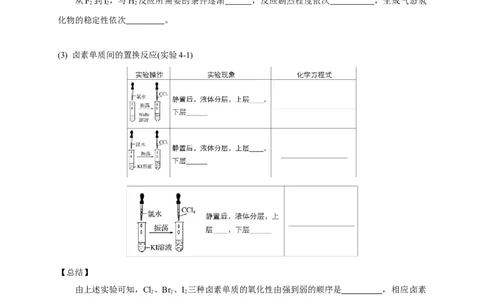
(3) 卤素单质间的置换反应(实验4-1)
【总结】
由上述实验可知,Cl、Br 、I 三种卤素单质的氧化性由强到弱的顺序是 ,相应卤素
2 2 2
离子的还原性由强到弱的顺序是 。
【归纳总结】格致课堂
【课后练习】
1.随着碱金属元素原子序数的增大,下列递变规律正确的是( )
A.原子半径逐渐增大
B.碱性逐渐减弱
C.单质熔、沸点逐渐升高
D.单质的氧化性逐渐增强
2.下列关于碱金属的叙述正确的是( )
A.钾与氧气或水反应比钠的反应剧烈,铷、铯的反应更剧烈
B.碱金属的密度随着原子序数的递增逐渐减小
C.碱金属元素的最高价氧化物对应的水化物的碱性随着原子序数的递增依次减弱
D.碱金属元素的阳离子的氧化性随着原子序数的递增依次增强
3.关于铯及其化合物的以下各种说法中不正确的是( )
A.氢氧化铯是一种强碱,比KOH的碱性强
B.铯与水或酸溶液反应剧烈,都生成氢气
C.Cs的还原性比Na强,故Na+的氧化性强于Cs+
D.Al的金属性大于Cs的金属性
4.随着卤族元素原子序数递增,下列说法正确的是( )
A.单质的熔、沸点逐渐降低
B.最高价氧化物对应水化物的酸性逐渐减弱(F除外)
C.单质的氧化性逐渐增强
D.气态氢化物的稳定性逐渐增强
5.下列对卤素的说法不符合递变规律的是( )
A.F、Cl、Br 、I 的氧化性逐渐减弱
2 2 2 2
B.HF、HCl、HBr、HI的热稳定性逐渐减弱
C.F-、Cl-、Br-、I-的还原性逐渐增强
D.卤素单质按F、Cl、Br 、I 的顺序颜色变浅,密度增大
2 2 2 2
6.下列说法正确的是( )
A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8
B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律
C.卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起
主要作用
D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl
4