文档内容
格致课堂
3.2.2 物质的量在化学方程式计算中的应用(学案)
1、了解新型合金
2、了解物质的量在化学方程式计算中的应用方法、计算格式和计算思路
物质的量在化学方程式计算中的应用方法、计算格式和计算思路
初中化学反应方程式中,物质的化学计量数代表的意义是 ;初中化
学计算的基本思路是 。
物质的量在化学方程式计算的应用
一、新型合金:
氢气是一种易燃易爆的气体,所以利用氢气的主要问题在于如何进行 。
储氢合金是一类能够 的材料。该材
料受热又会分解放出氢气,常见的储氢合金是 等。
除了储氢合金以外,新型合金还有: 等。
二、物质的量在化学方程式计算中的应用:
2Na + 2HO = 2NaOH + H↑
2 2
化学计量数之比:
扩大6.02×1023倍:
物质的量之比:
结论:
进行物质的量应用于化学方程式的计算时,须按以下步骤进行:
1.
2.
3.
4.格致课堂
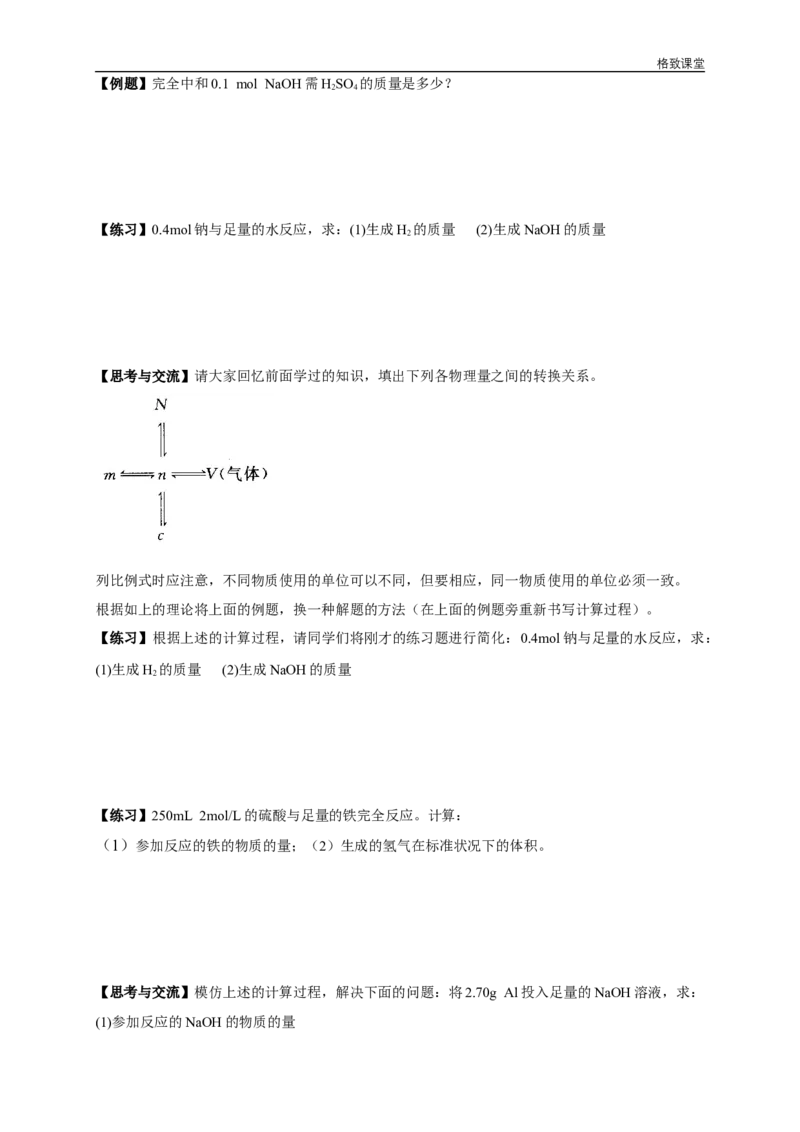
【例题】完全中和0.1 mol NaOH需HSO 的质量是多少?
2 4
【练习】0.4mol钠与足量的水反应,求:(1)生成H 的质量 (2)生成NaOH的质量
2
【思考与交流】请大家回忆前面学过的知识,填出下列各物理量之间的转换关系。
列比例式时应注意,不同物质使用的单位可以不同,但要相应,同一物质使用的单位必须一致。
根据如上的理论将上面的例题,换一种解题的方法(在上面的例题旁重新书写计算过程)。
【练习】根据上述的计算过程,请同学们将刚才的练习题进行简化:0.4mol钠与足量的水反应,求:
(1)生成H 的质量 (2)生成NaOH的质量
2
【练习】250mL 2mol/L的硫酸与足量的铁完全反应。计算:
(1)参加反应的铁的物质的量;(2)生成的氢气在标准状况下的体积。
【思考与交流】模仿上述的计算过程,解决下面的问题:将2.70g Al投入足量的NaOH溶液,求:
(1)参加反应的NaOH的物质的量格致课堂
(2)生成H 的体积(标准状况下)
2
【练习】用一定量的Fe与足量的1mol/L的HSO 溶液反应来制取H。若要制得2.24L H(标况),
2 4 2 2
试计算
(1)参加反应的HSO 的物质的量。
2 4
(2)参加反应的Fe的质量。
(3)所得FeSO 的物质的量。
4
(4)若将反应后的溶液稀释到500ml,则FeSO 的物质的量浓度是多少?
4
1.实验室用MnO 和浓盐酸制取氯气时,有14.6 g氯化氢被氧化,所得Cl 全部用石灰乳吸收
2 2
可制得漂白粉的质量是( )
A.14.3 g B.25.4 g C.28.6 g D.50.8 g
2.将足量铁粉加入100 mL 0.1 mol·L-1的CuSO 溶液中,充分反应后析出铜的质量为( )
4
A.32 g B.6.4 g C.0.64 g D.3.2 g
3.在500 mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体6.72 L,生
成物NaAlO 的物质的量浓度为(假定反应前后,溶液体积不变)( )
2
A.1 mol·L-1 B.0.4 mol·L-1 C.1.5 mol·L-1 D.2 mol·L-1
4.将1 mol Na和1 mol Al的混合物投入足量水中,产生气体在标准状况下的体积为( )
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
5.在500 mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体33.6 L,该
溶液中NaOH的物质的量浓度为( )
A.1 mol·L-1 B.2 mol·L-1 C.1.5 mol·L-1 D.3 mol·L-1
6.在一定条件下,钠与O 反应可生成1.5 g固体,若将相同质量的钠与80 mL 0.50 mol·L-1的
2格致课堂
盐酸反应,钠恰好完全转化生成NaCl,则1.5 g固体的成分是( )
A.NaO B.NaO C.NaO和NaO D.NaO 和NaO
2 2 2 2 2 2 2 2 2
7.把铁、铝混合物1.1 g溶于200 mL 5 mol·L-1盐酸中,反应后盐酸的浓度变为4.6 mol·L-1(溶
液体积变化忽略不计)。求:
(1)反应中消耗HCl的物质的量;
(2)该混合物中铝、铁的物质的量。
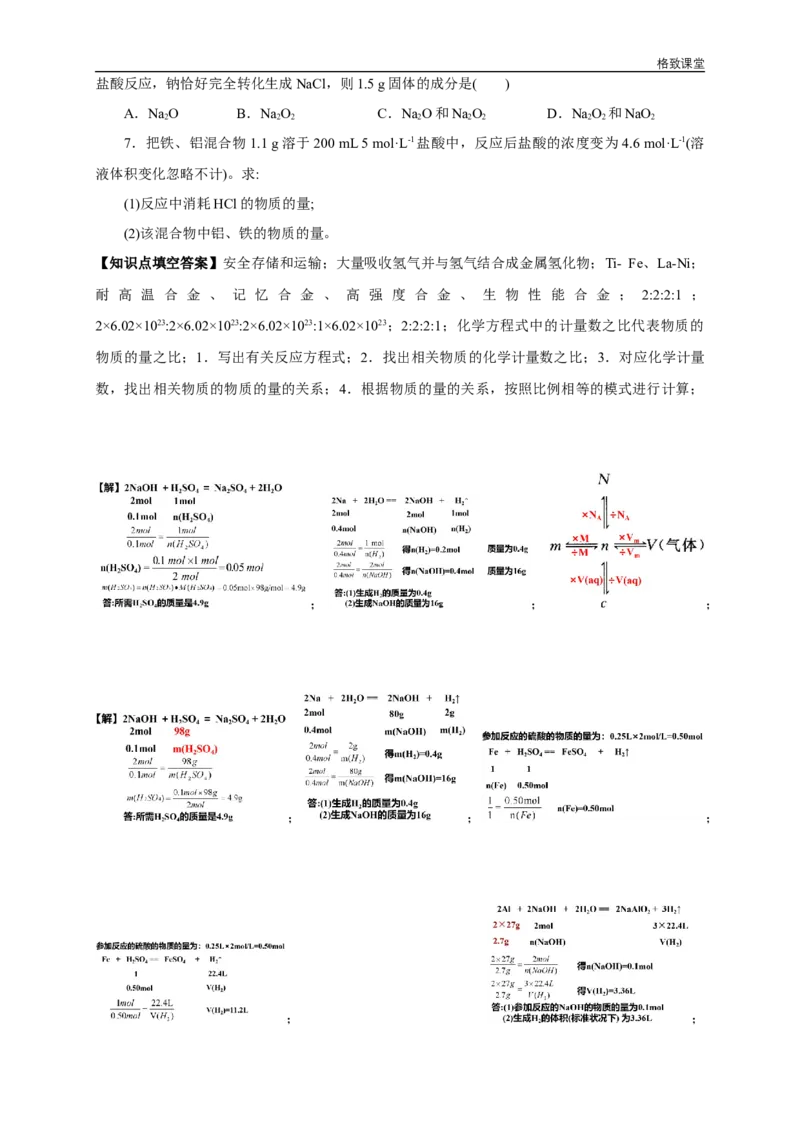
【知识点填空答案】安全存储和运输;大量吸收氢气并与氢气结合成金属氢化物;Ti- Fe、La-Ni;
耐 高 温 合 金 、 记 忆 合 金 、 高 强 度 合 金 、 生 物 性 能 合 金 ; 2:2:2:1 ;
2×6.02×1023:2×6.02×1023:2×6.02×1023:1×6.02×1023;2:2:2:1;化学方程式中的计量数之比代表物质的
物质的量之比;1.写出有关反应方程式;2.找出相关物质的化学计量数之比;3.对应化学计量
数,找出相关物质的物质的量的关系;4.根据物质的量的关系,按照比例相等的模式进行计算;
; ; ;
; ; ;
; ;格致课堂
【检测反馈答案】1.B 2.C 3.B 4.D 5.B 6.C
7.(1)0.08 mol (2)0.02 mol;0.01 mol