文档内容
格致课堂
3.1.1 铁的单质 铁的氧化物(学案)
1、掌握铁的单质氧化物的主要性质,了解其应用。
重点: 铁的单质和氧化物的性质
难点: 铁的单质和氧化物的性质
复习金属钠的性质填写:
钠与水(加酚酞)反应有5个现象:① (钠比水轻);②
(反应放热,钠熔点低);③迅速 (产生气体);④溶液使
变红(生成物呈碱性);⑤发出_______ 响声(反应生成了可燃性气体)。反应的化学方
程式为: ,反应的离子方程式 。
预习填写:
铁在地壳中的含量仅次于 、 和 ,具第 位,主要以 和
形式存在。在Fe O 中铁的化合价是 ,FeO中铁的化合价是 ,Fe O 中铁的化合价是
2 3 3 4
。
1、 铁与氧气点燃的化学方程式
2、 铁与氯气反应的化学方程式
3、 铁与硫单质的反应
4、 铁不能与冷、热水反应,但能否与水蒸气反应? 请设计一个简单的实验装置,使还
原铁粉与水蒸气反应
5、 铁与水蒸气反应现象
结论
6、铁的氧化物
俗名 物理性质(水溶性、色态 化学性质(稳定性、与酸反应的离子方程
等) 式)
FeO
Fe O
2 3格致课堂
Fe O
3 4
1、在由Fe、FeO、Fe O 组成的混合物中加入100mL2mol / L的盐酸,恰好使混合物溶
2 3
解,并放出448mL气体(标准状况下),此时溶液中无Fe3+离子,则下列判断正确的
是( )
A.混合物里三种物质反应时消耗盐酸的物质的量之比为1∶1∶3;
B.反应后所得溶液中的Fe2+与Cl - 的物质的量之比为1∶2;
C.混合物里,FeO的物质的量无法确定,但Fe比Fe O 的物质的量多;
2 3
D.混合物里,Fe O 的物质的量无法确定,但Fe比FeO的物质的量多。
2 3
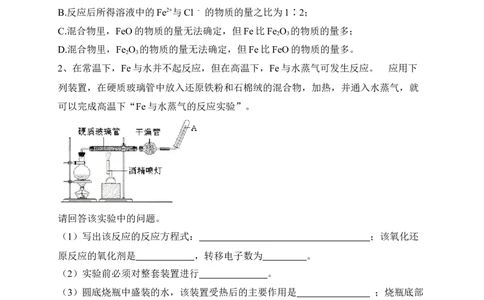
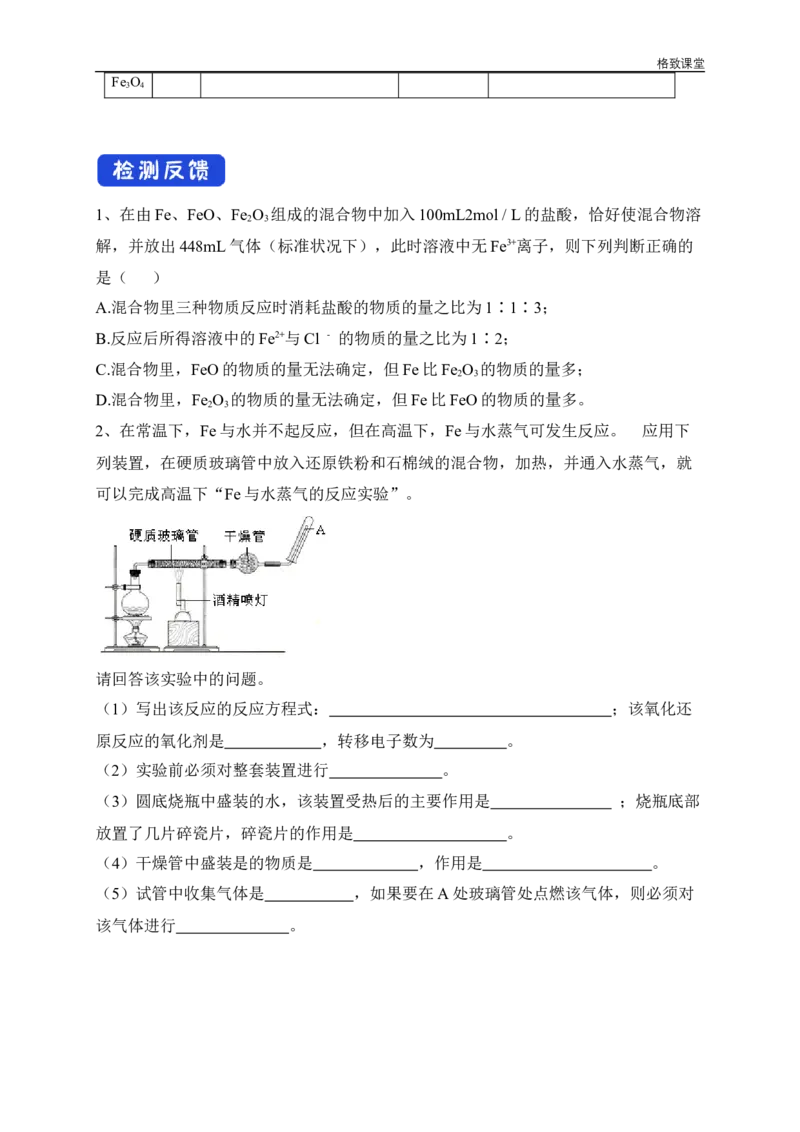
2、在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下
列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就
可以完成高温下“Fe与水蒸气的反应实验”。
请回答该实验中的问题。
(1)写出该反应的反应方程式: ;该氧化还
原反应的氧化剂是 ,转移电子数为 。
(2)实验前必须对整套装置进行 。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶底部
放置了几片碎瓷片,碎瓷片的作用是 。
(4)干燥管中盛装是的物质是 ,作用是 。
(5)试管中收集气体是 ,如果要在A处玻璃管处点燃该气体,则必须对
该气体进行 。