文档内容
格致课堂
2.1.2 钠的几种化合物 焰色试验(学案)
1、了解氧化钠和过氧化钠的性质
2、了解碳酸钠与碳酸氢钠的性质
3、了解焰色试验
氧化钠和过氧化钠、碳酸钠与碳酸氢钠的区别
碳酸钠、碳酸氢钠与盐酸反应的方程式为 ;以上
两种化合物各自的用途是 。钠在不同条件下与氧气反
应的方程式为
一、钠的氧化物
1、氧化钠:从物质组成或性质的角度判断,氧化钠属于
一般来说碱性氧化物具有的通性是:
(1)
(2)
(3)
由上,氧化钠可以发生的对应的反应为:
2、过氧化钠:过氧化钠与水反应的生成物只有氢氧化钠?
根据氧化还原判断,过氧化钠与水反应的生成物除氢氧化钠外还有 ;如何检验这种反应的生成
物?
【演示实验】向试管中加入过氧化钠固体,向其中滴加蒸馏水,将带火星的木条深入试管。用手轻轻触摸
试管外壁,最后向反应后的溶液中滴加酚酞。
实验现象 结论格致课堂
反应方程式为 ;并进行双线桥分析
为什么向放有过氧化钠的棉花上滴水会燃烧?
写出过氧化钠与二氧化碳的反应,并用双线桥进行分析:
过氧化钠与盐酸的反应:
过氧化钠不是碱性氧化物,其主要用途是
二、碳酸钠和碳酸氢钠:
1、碳酸钠的用途:
碳酸氢钠的用途:
【分组实验】在两只试管中分别加入少量碳酸钠和碳酸氢钠固体(各约1g),完成下列实验,并将实验现
象和相应的结论填入下表中。
碳酸钠 碳酸氢钠
(1)观察两者的外观
(2)分别加入几滴水,观察现象,插入温度计,观察其示数
的变化
(3)向(2)的试管中分别加5ml水,用力振荡,观察现象
(4)向(3)所得溶液中分别滴加1-2滴酚酞,观察现象
碳酸钠对热稳定,碳酸氢钠受热分解的方程式为
【学生活动】同学们互相讨论,分析上述实验,比较碳酸钠和碳酸氢钠的异同。
碳酸钠 碳酸氢钠
外观
加少量水
溶解性
热稳定性
溶液所显性质
用途
碳酸钠粉末遇水生成 ,该晶体在干燥的空气中会
逐渐失去结晶水转变为粉末( )
三、焰色试验:
【演示实验】将 (或者 )在酒精灯火焰上灼烧至颜色无变化,格致课堂
蘸取碳酸钠溶液,在火焰上灼烧,观察火焰颜色。将金属丝用 洗净,再蘸取硫酸铜溶液,
重复上述实验,观察火焰颜色。将金属丝用 洗净,再蘸取碳酸钾溶液,重复上述实验,透过
观察火焰颜色。
这种操作称为焰色试验。
钠的焰色为 ;钾的焰色为 ,需要透过 观察火焰
颜色,其作用为 。
1.在自然界中能存在的物质是 ( )
A.钠 B.氢氧化钠 C.过氧化钠 D.碳酸钠
2.NaO和NaO 的共同之处是 ( )
2 2 2
A.均是白色固体 B.都能与水反应生成碱
C.都具有漂白作用 D.都为碱性氧化物
3.在NaO 与水反应中,叙述正确的是 ( )
2 2
A.O 是还原产物 B.NaOH是氧化产物
2
C.NaO 是氧化剂,水是还原剂 D.NaO 中,-1价的氧既得电子,又失电子
2 2 2 2
4.下列说法中不正确的是 ( )
A.NaCO 和NaHCO 均可与HCl反应
2 3 3
B.NaCO 比NaHCO 易溶于水
2 3 3
C.NaCO 的稳定性比NaHCO 强
2 3 3
D.NaCO 能与石灰水反应而NaHCO 不反应
2 3 3
5.不能用来鉴别NaCO 和NaHCO 的方法是 ( )
2 3 3
A.分别加热 B.加澄清石灰水C.加稀盐酸 D.加BaCl
2
6.对2NaO+2CO ==2Na CO+O 下列说法正确的是 ( )
2 2 2 2 3 2
A.是氧化还原反应,NaO 是氧化剂,CO 是还原剂
2 2 2
B.是氧化还原反应,CO 是氧化剂,NaO 是还原剂
2 2 2
C.不是氧化还原反应,是碱性氧化和酸性氧化物反应
D.是氧化还原反应,NaO 既是氧化剂,又是还原剂
2 2
7.可以用来断定碳酸氢钠粉末中是否混有碳酸钠的实验方法是 ( )
A.加热时有无色气体放出
B.滴加盐酸时有无气泡放出格致课堂
C.溶于水后,滴加稀的氯化镁溶液有无白色沉淀生成
D.溶于水后,滴加澄清石灰水,有无白色沉淀生成
8.下列钠的化合物与其性质或用途不相符的是 ( )
A.NaO——淡黄色固体,可用作漂白剂
2 2
B.NaO——白色固体,性质不稳定
2
C.NaCO——性质稳定,可治疗胃酸过多
2 3
D.NaHCO ——受热易分解,可用作发酵粉
3
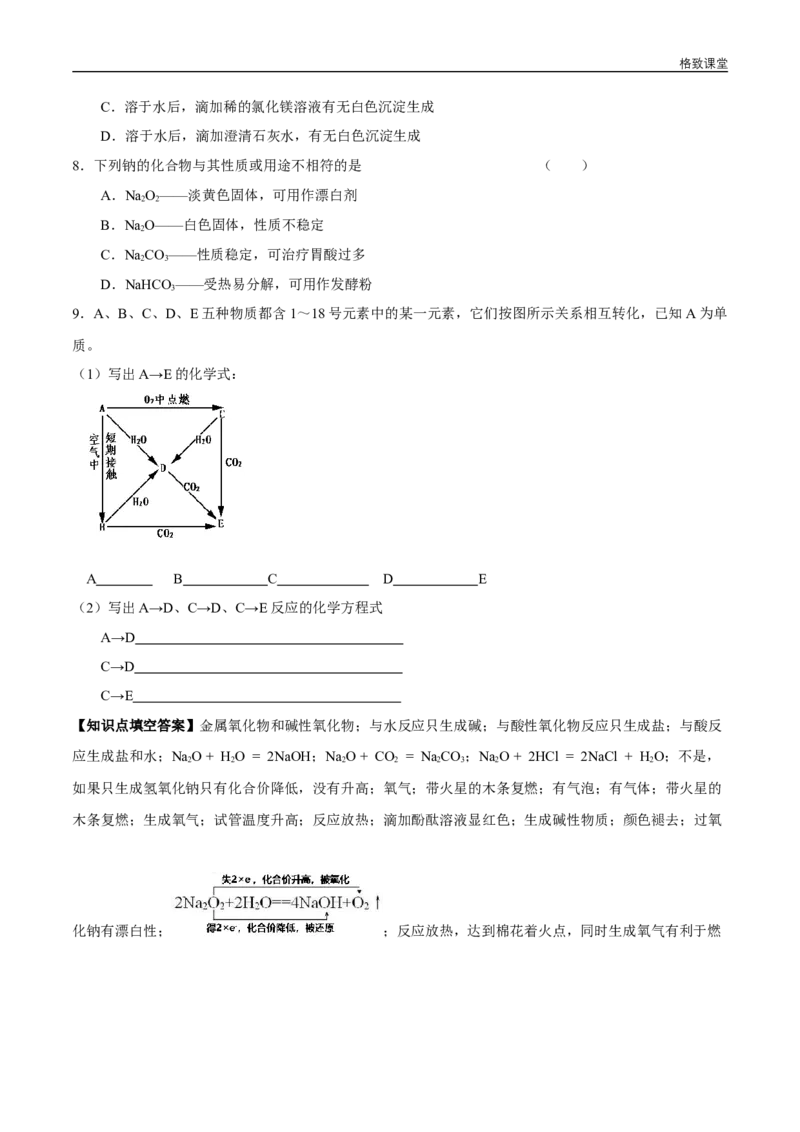
9.A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单
质。
(1)写出A→E的化学式:
A B C D E
(2)写出A→D、C→D、C→E反应的化学方程式
A→D
C→D
C→E
【知识点填空答案】金属氧化物和碱性氧化物;与水反应只生成碱;与酸性氧化物反应只生成盐;与酸反
应生成盐和水;NaO+ HO = 2NaOH;NaO+ CO = NaCO;NaO+ 2HCl = 2NaCl + HO;不是,
2 2 2 2 2 3 2 2
如果只生成氢氧化钠只有化合价降低,没有升高;氧气;带火星的木条复燃;有气泡;有气体;带火星的
木条复燃;生成氧气;试管温度升高;反应放热;滴加酚酞溶液显红色;生成碱性物质;颜色褪去;过氧
化钠有漂白性; ;反应放热,达到棉花着火点,同时生成氧气有利于燃格致课堂
烧; ;2NaO + 4HCl = 4NaCl + 2HO + O↑;在呼吸面具和潜艇中作
2 2 2 2
为供氧剂;碳酸钠:制肥皂、制玻璃、纺织、造纸;碳酸氢钠:治疗胃酸的药、制糕点;白色粉末;细小
的白色晶体;结块变成晶体,温度上升;少量溶解,温度下降;溶解;溶解一部分;溶液变红,颜色较深;
溶液变红,颜色较浅;2NaHCO NaCO + HO + CO↑;白色粉末;白色晶体;形成晶体,放热;溶
3 2 3 2 2
解,吸热;可溶,溶解度较大;可溶,溶解度较小;稳定,受热不分解;受热分解;碱性,较强;碱性,
较弱;工业碱;食用碱;带有结晶水的碳酸钠晶体(NaCO·xHO);风化;铂丝;干净的铁丝;盐酸;
2 3 2
盐酸;蓝色钴玻璃;很多金属及其化合物在灼烧时会使火焰呈现出特征颜色,根据这种现象可以定性判断
试样中所含的金属元素;胡各色;紫色;蓝色钴玻璃;滤去可能存在的钠盐发出的黄光。
【检测反馈答案】1.D 2.B 3.D 4.D 5.B 6.D 7.C 8.C
9.(1)A Na B Na O C Na O D NaOH E NaCO
2 2 2 2 3
(2)写出A→D、C→D、C→E反应的化学方程式
A→D 2Na+2H O==2NaOH+H↑
2 2
C→D 2Na O+2H O==4NaOH+O↑
2 2 2 2
C→E 2Na O+2CO ==2Na CO+O ↑
2 2 2 2 3 2