文档内容
格致课堂
第一章 物质及其变化
第 2节 离子反应
2.1 电解质的电离
1.了解电解质、非电解质和电离的概念。(重点)
2.会书写电离方程式。(重点)
3.从电离的角度认识酸、碱、盐。
重点:1.电解质
2.电离方程式
难点:电离概念的形成过程
初中化学学习中,对于酸碱盐的相关反应有哪些?初中关于物质导电性实验?
【实验探究】
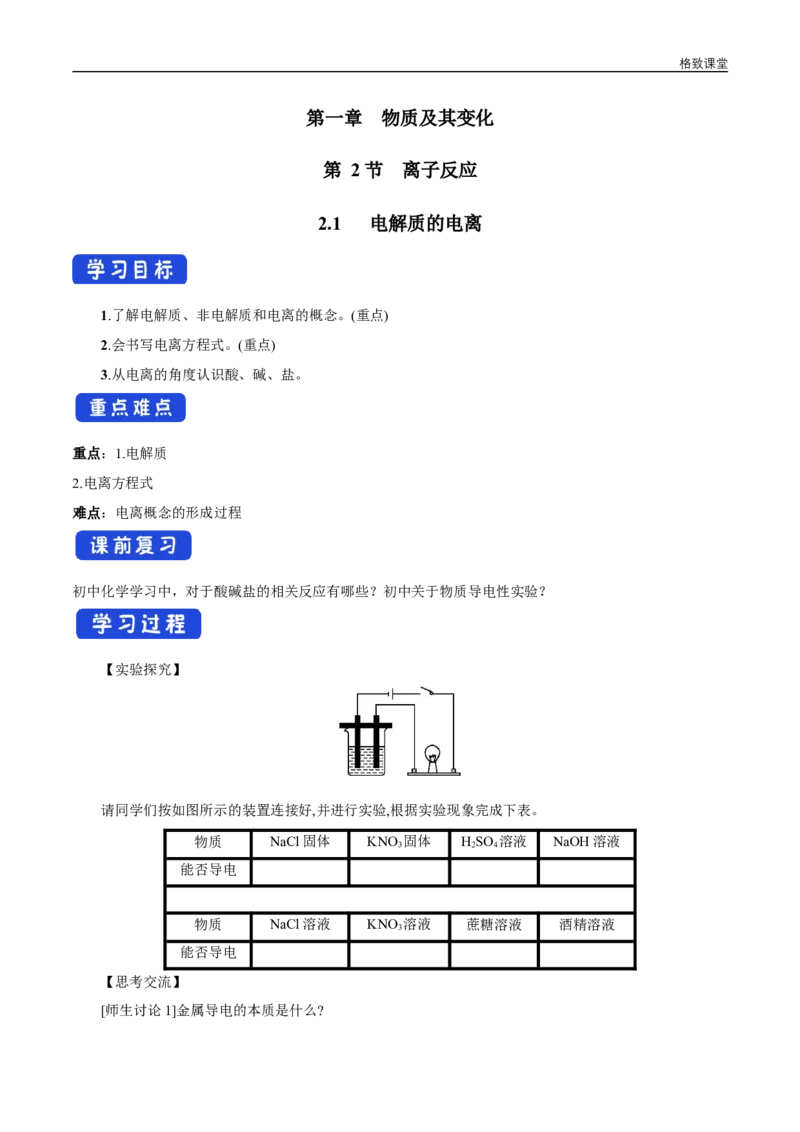
请同学们按如图所示的装置连接好,并进行实验,根据实验现象完成下表。
物质 NaCl固体 KNO 固体 HSO 溶液 NaOH溶液
3 2 4
能否导电
物质 NaCl溶液 KNO 溶液 蔗糖溶液 酒精溶液
3
能否导电
【思考交流】
[师生讨论1]金属导电的本质是什么?格致课堂
[师生讨论2]通过实验现象分析液态物质导电与否的条件?
[师生讨论3] KNO 溶液、熔融态KNO 和固态KNO 组成有何不同?
3 3 3
一、电解质和非电解质的概念
1.概念
电解质:在 状态下能导电的 。
非电解质:在 状态下都不能导电的 。
2.SO 属于化合物,溶于水也能导电,SO 属于电解质吗?
2 2
【练习1】下列物质哪些能导电?哪些是电解质?哪些是非电解质?
(1)金属铜 (2)碳棒 (3)O (4)H SO (5)液态 HCl (6)CH COOH (7)葡萄糖 (8)固态 NaCl
2 2 4 3
(9)CaCO 固体 (10)CuSO ·5H O (11)熔融状态的KNO (12)KOH水溶液 (13)酒精水溶液 (14)盐酸
3 4 2 3
(15)CaO (16)CO (17)H O (18)NH
2 2 3
二、电离
1.概念: 。
2.电离的表示——电离方程式
(1)概念: 。
(2)书写步骤:
三、从电离角度认识酸、碱、盐
1.酸:电离时生成的阳离子全部都是氢离子的化合物。
2.碱: 。
3.盐: 。
【练习2】书写下列物质的电离方程式:KCl、NaSO 、AgNO、BaCl 、NaHSO、NaHCO 。
2 4 3 2 4 3格致课堂
【练习3】下面叙述正确的是( )
A.NaCl溶液能导电,所以NaCl溶液是电解质
B.固态NaCl不导电,但NaCl是电解质
C.HCl水溶液能导电,所以HCl是电解质
D.SO 溶于水能导电,所以SO 是电解质
3 3
E.Cu能导电,所以是电解质
F.BaSO 的水溶液不能导电,所以BaSO 是非电解质
4 4
1.下列物质导电性最差的是( )
A.熔融的氢氧化钠 B.石墨棒
C.稀盐酸 D.固态氯化钾
2.下列物质中,属于电解质的是( )
A.CO B.HCl C.BaSO D.NaOH溶液
2 4
3.在下列化合物中,只有在水溶液中才能导电的电解质是( )
A.NaCl B.酒精 C.H SO D.KCl
2 4
4.下列物质既不是电解质,又不是非电解质的是( )
A.NaHSO B.Cu(OH) C.O D.HCl
4 2 2
5.下列物质的水溶液中存在溶质分子的是( )
A.HCl B.NaOH C.Na CO D.蔗糖
2 3
6.下列说法正确的是( )
A.酸、碱、盐都是电解质 B.电解质都是易溶于水的物质
C.氧化物都是电解质 D.氢化物都不是电解质
7.今有一种固体化合物X,X本身不导电,但熔化状态或溶于水中能够电离,下列关于该化合物X的说法
中,正确的是( )
A.X一定为电解质 B.X可能为非电解质
C.X只能是盐类 D.X可以是任何化合物
8下列电离方程式中正确的是( )
A.Ca(OH) ==Ca2++2OH
2
B.FeCl ==Fe2++Cl-
2格致课堂
C.H SO ==H++SO2-
2 4 4
D.Al (SO )==2Al3++3SO2-
2 4 3 4
9.关于酸、碱、盐的下列各种说法中正确的是( )
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,生成金属阳离子(或NH +)和酸根离子的是盐
4
D.NH Cl电离的电离方程式是:NHCl==NH ++Cl-,所以NH Cl是盐
4 4 4 4
参考答案
学习过程
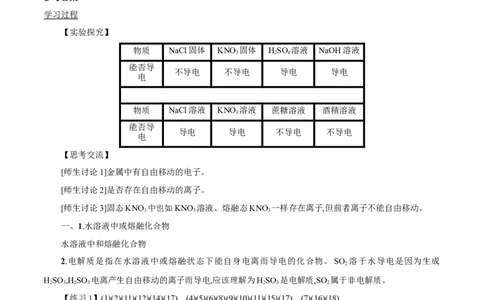
【实验探究】
物质 NaCl固体 KNO 固体 HSO 溶液 NaOH溶液
3 2 4
能否导
不导电 不导电 导电 导电
电
物质 NaCl溶液 KNO 溶液 蔗糖溶液 酒精溶液
3
能否导
导电 导电 不导电 不导电
电
【思考交流】
[师生讨论1]金属中有自由移动的电子。
[师生讨论2]是否存在自由移动的离子。
[师生讨论3]固态KNO 中也如KNO 溶液、熔融态KNO 一样存在离子,但前者离子不能自由移动。
3 3 3
一、1.水溶液中或熔融化合物
水溶液中和熔融化合物
2.电解质是指在水溶液中或熔融状态下能自身电离而导电的化合物。SO 溶于水导电是因为生成
2
HSO ,H SO 电离产生自由移动的离子而导电,应该理解为HSO 是电解质,SO 属于非电解质。
2 3 2 3 2 3 2
【练习1】(1)(2)(11)(12)(14)(17) (4)(5)(6)(8)(9)(10)(11)(15)(17) (7)(16)(18)
二、1.电解质在溶于水或受热熔化时,离解成自由移动的离子的过程
2.(1)用化学符号表示电解质电离成自由移动离子的式子
(2)①阴阳离子部分拆开写,但原子团不能拆,例如NH
4
+、SO
4
2-、OH-、NO
3
-、HCO
3
-等不能拆。
②构成物质的原子或原子团的个数在书写成离子时为化学计量数。
三、2.电离时生成的阴离子全部都是氢氧根离子的化合物
3.电离时生成金属阳离子(或N)和酸根阴离子的化合物
【练习2】KCl==K++Cl-格致课堂
NaSO ==2Na++SO 2-
2 4 4
AgNO==Ag++NO-
3 3
BaCl ==Ba2++2Cl-
2
NaHSO==Na++H++SO 2-
4 4
NaHCO ==Na++HCO-
3 3
【练习3】B、C
随堂检测
1.解析:石墨棒导电是因为自由电子的定向移动,熔融的氢氧化钠、稀盐酸存在自由移动的离子,可导电,
固态氯化钾因为无自由移动的离子,不导电。
答案:D
2.解析:电解质是指在水溶液中或熔融状态下能够导电的化合物。题目中只有B和C项是符合条件的,其
中HCl在水溶液中可以导电,BaSO 在熔融状态下可以导电。NaOH溶液是混合物;CO 通入水中虽可以导电,
4 2
但原因是生成了HCO,H CO 是电解质。
2 3 2 3
答案:BC
3.解析:电解质中,酸溶于水才能导电,熔融状态下不导电;强碱和盐,溶于水或熔融状态下均可导电。
答案:C
4.解析:电解质和非电解质的概念必须建立在化合物的基础上,氧气是单质,所以氧气既不是电解质,又不
是非电解质。
答案:C
5.解析:HCl、NaOH、NaCO 溶于水完全电离成离子。蔗糖是非电解质,溶于水不与水反应,不电离,仍以
2 3
分子形式存在。
答案:D
6.解析:氧化物有的是电解质,如NaO、CaO等离子化合物,有的不是电解质,如CO 、SO 等共价化合
2 2 2
物,C项错。氢化物有的是电解质,如HCl、HF等;有的不是电解质,如CH、NH 等,D项错。
4 3
答案:A
7.A 8.D
9.解析:本题考查从电离的角度对酸、碱、盐的认识。化合物电离时,生成的阳离子全部是氢离子的是酸,
所以A错;化合物电离时,生成的阴离子全部是氢氧根离子的是碱,所以B错;化合物电离时,生成金属阳离子
(或N)和酸根离子的是盐,所以C、D正确。
答案:CD格致课堂