文档内容
第2课时 杂化轨道理论
基础过关练
题组一 杂化轨道理论
1.鲍林曾获得诺贝尔奖不同奖项,杂化轨道理论是鲍林为了解释分子的空间结构提出的。下列对sp3、
sp2、sp杂化轨道的夹角大小的比较,得出的结论正确的是( )
A.sp杂化轨道的夹角最大
B.sp2杂化轨道的夹角最大
C.sp3杂化轨道的夹角最大
D.sp3、sp2、sp杂化轨道的夹角大小相等
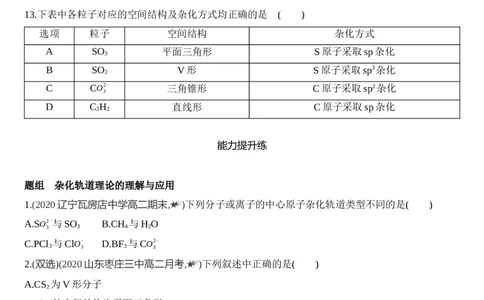
2.下列图形属于sp杂化轨道的是( )
3.(2020山东济宁高二期末)氯化亚砜(SOCl )是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下
2
列关于氯化亚砜分子的空间结构和中心原子(S)采取的杂化方式的说法正确的是( )
A.三角锥形、sp3 B.平面三角形、sp3
C.平面三角形、sp2 D.三角锥形、sp2
4.s轨道和p轨道杂化的类型不可能有( )
A.sp杂化 B.sp2杂化
C.sp3杂化 D.sp4杂化
5.在 分子中,C—Br键采用的成键轨道是( )
A.sp-p B.sp2-s C.sp2-p D.sp3-p
6.下列有关sp2杂化轨道的说法错误的是( )
A.由同一能层上的s轨道与p轨道杂化而成B.共有3个能量相同的杂化轨道
C.每个sp2杂化轨道中s能级成分占三分之一
D.sp2杂化轨道最多可形成2个σ键
7.下列分子中,中心原子的杂化轨道类型相同的是( )
A.CO 与SO B.CH 与NH
2 2 4 3
C.BeCl 与BF D.C H 与C H
2 3 2 4 2 2
8.在1个乙烯分子中有5个σ键和1个π键,下列说法正确的是( )
深度解析
A.sp2杂化轨道形成σ键,未参与杂化的2p轨道形成π键
B.sp2杂化轨道形成π键,未参与杂化的2p轨道形成σ键
C.C—H是sp2杂化轨道形成的σ键, 是未参与杂化的2p轨道形成的
D. 是sp2杂化轨道形成的σ键,C—H是未参与杂化的2p轨道形成的π键
9.下列关于杂化轨道的叙述中,不正确的是( )
深度解析
A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
C.NH 和CH 两个分子中中心原子N和C都是通过sp3杂化轨道成键
3 4
D.用杂化轨道理论与VSEPR模型分析分子空间结构的结果常常相互矛盾
题组二 杂化轨道类型与分子空间结构的关系
10.(2020河南洛阳高二期末)下列分子中,空间结构是平面三角形的是( )
A.CH B.NH
4 3
C.BF D.CO
3 2
11.氨气分子的空间结构是三角锥形,而甲烷分子的空间结构是正四面体形,这是因为( )
A.两种分子的中心原子的杂化轨道类型不同,NH 中N原子为sp2杂化,而CH 中C原子是sp3杂化
3 4
B.NH 分子中氮原子形成3个杂化轨道,CH 分子中碳原子形成4个杂化轨道
3 4
C.NH 分子中中心原子上有一对未成键的孤电子对,它对成键电子对的排斥作用较强
3
D.氨气是四原子化合物,甲烷为五原子化合物
12.甲烷分子(CH )失去一个H+,形成甲基阴离子(CH-),在这个过程中,下列说法不合理的是( )
4 3
A.碳原子的杂化轨道类型发生了改变B.微粒的空间结构发生了改变
C.微粒的稳定性发生了改变
D.微粒中的键角发生了改变
13.下表中各粒子对应的空间结构及杂化方式均正确的是 ( )
选项 粒子 空间结构 杂化方式
A SO 平面三角形 S原子采取sp杂化
3
B SO V形 S原子采取sp3杂化
2
C CO2- 三角锥形 C原子采取sp2杂化
3
D C H 直线形 C原子采取sp杂化
2 2
能力提升练
题组 杂化轨道理论的理解与应用
1.(2020辽宁瓦房店中学高二期末, )下列分子或离子的中心原子杂化轨道类型不同的是( )
A.SO2-与SO B.CH 与H O
3 3 4 2
C.PCl 与ClO- D.BF 与CO2-
3 3 3 3
2.(双选)(2020山东枣庄三中高二月考, )下列叙述中正确的是( )
A.CS 为V形分子
2
B.ClO-的空间结构为平面三角形
3
C.SF 中有6对完全相同的成键电子对
6
D.SiF 和SO2-的中心原子均为sp3杂化
4 3
3.(2020河南林州一中高二检测, )关于原子轨道的说法正确的是( )
A.中心原子采取sp3杂化轨道成键的分子,其空间结构都是四面体形
B.CH 中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混杂而形成的
4
C.sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混杂形成的一组能量相同的新轨道D.凡AB 型的共价化合物,其中心原子A均采取sp3杂化轨道成键
3
4.(2020河北正定中学高二月考, )下列关于三氯化磷分子的叙述不正确的是( )
A.PCl 分子中三个共价键的键长和键角都相等
3
B.PCl 分子中的P—Cl键属于极性共价键
3
C.PCl 分子中三个共价键键能相等
3
D.PCl 分子中磷原子采取sp2杂化
3
5.(2020天津第二十中学高二检测, )根据杂化轨道理论和价层电子对互斥模型,判断下列分子或离子
的空间结构正确的是( )
分子 中心原子 价层电子 分子或离子
选项
或离子 杂化方式 对互斥模型 的空间结构
A SO sp 直线形 直线形
2
B HCHO sp2 平面三角形 三角锥形
C NF sp2 四面体形 平面三角形
3
D NH+ sp3 正四面体形 正四面体形
4
6.(2019四川雅安中学高二上第一次月考, )下列分子的空间结构可用sp2杂化轨道来解释的是( )
①BF ② ③ ④C H ⑤N H ⑥苯分子
3 2 2 2 4
A.①②③ B.①③⑥ C.②③⑤ D.③④⑥
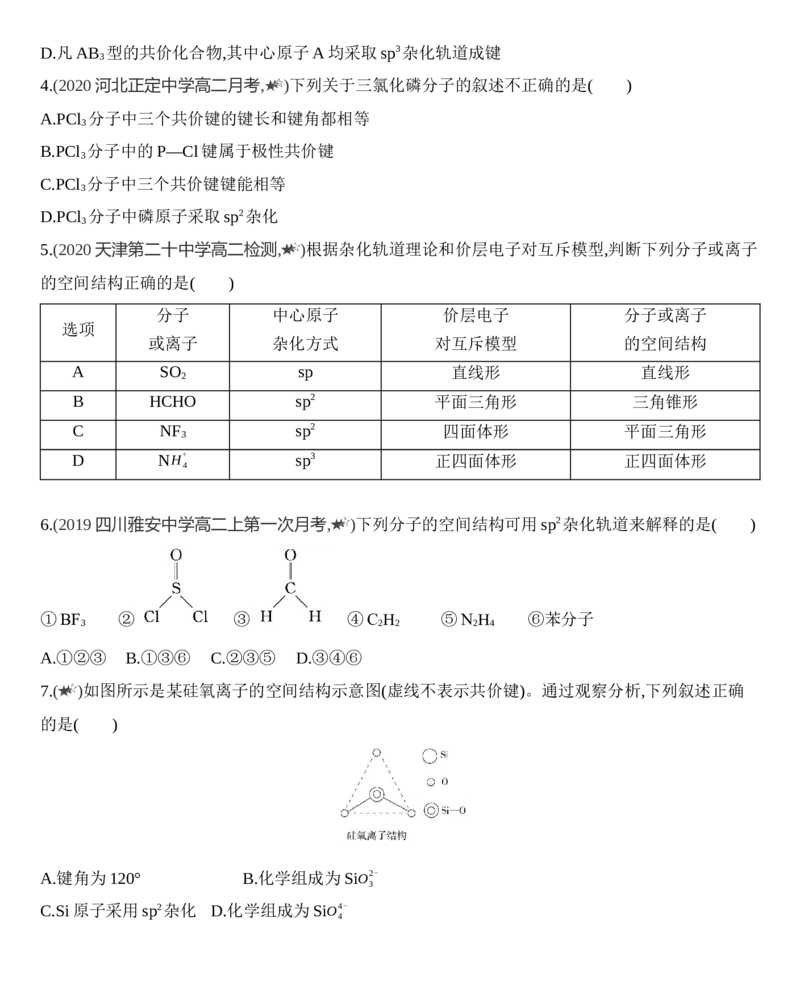
7.( )如图所示是某硅氧离子的空间结构示意图(虚线不表示共价键)。通过观察分析,下列叙述正确
的是( )
A.键角为120° B.化学组成为SiO2-
3
C.Si原子采用sp2杂化 D.化学组成为SiO4-
48.(2019四川蓉城名校联盟高二期中, )推理是学习化学知识的一种重要方法。下列推理合理的是(
)
A.SO 中硫原子采取sp2杂化,则CO 中碳原子也采取sp2杂化
2 2
B.NH 分子的空间结构是三角锥形,则NCl 分子的空间结构也是三角锥形
3 3
C.H O分子的键角是105°,则H S分子的键角也是105°
2 2
D.PCl 分子中每个原子最外层达到8电子稳定结构,则BF 分子中每个原子最外层也能达到8电子稳
3 3
定结构
9.( )下列关于杂化轨道的叙述中,不正确的是( )
A.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
B.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为四面体结构
C.杂化前后的轨道数目不变,但轨道的形状发生了改变
D.sp3、sp2、sp杂化轨道的夹角分别为109°28'、120°、180°
10.( )回答下列问题:
(1)下列微粒中按键角由大到小的顺序排列为 (用编号填写)。
①HCN ②SiF ③SCl ④CO2- ⑤H O+
4 2 3 3
(2)ClO-、ClO-、ClO-、ClO-中Cl都是以sp3杂化轨道与O原子成键,将它们的空间结构填入表格中:
2 3 4
离子 ClO- ClO- ClO- ClO-
2 3 4
空间结构
(3)S单质的常见形式为S ,其结构如图所示,S原子采取的杂化方式是 。
8
(4)肼(N H )分子可视为NH 分子中的一个氢原子被—NH (氨基)取代形成的另一种氮的氢化物。N H
2 4 3 2 2 4
分子中氮原子的杂化轨道类型是 ,N H 分子中的六个原子 (填“在”或“不在”)
2 4
同一个平面上。
答案全解全析
基础过关练
1.A 2.D 3.A 4.D 5.C 6.D 7.B 8.A9.D 10.C 11.C 12.A 13.D
1.A sp3、sp2、sp杂化轨道的夹角分别为109°28'、120°、180°。
2.D sp杂化轨道夹角为180°,C项属于未杂化的p轨道。
3.A 根据价层电子对互斥模型确定微粒的空间结构,SOCl 中S原子形成2个S—Cl键,1个 键,
2
价层电子对数=σ键个数+孤电子对数=3+6-1-1-1×2=4,杂化轨道数是4,故S原子采取sp3杂化,中心
2
原子上有一对孤电子对,分子空间结构为三角锥形,故选A。
4.D np能级有三个轨道:np 、np 、np ,当s轨道和p轨道杂化时只有三种类型:
x y z
①sp杂化,即一个s轨道和一个p轨道的杂化;②sp2杂化,即一个s轨道和两个p轨道的杂化;③sp3杂
化,即一个s轨道和三个p轨道的杂化。
5.C 分子中的两个碳原子都采取sp2杂化,溴原子的价电子排布式为4s24p5,4p轨道上有
一个未成对电子,与碳原子的一个sp2杂化轨道成键。
6.D 参与杂化的轨道的能量是相近的,同一能层上s轨道与p轨道的能量差异不是很大,可形成sp2杂
化轨道,A项正确;形成的杂化轨道能量相同,B项正确;sp2杂化轨道是由一个s轨道与2个p轨道杂化
而成的,C项正确;sp2杂化轨道最多可形成3个σ键,D项错误。
7.B CO 中C原子为sp杂化,SO 中S原子为sp2杂化,A不正确;CH 中C原子为sp3杂化,NH 中N原
2 2 4 3
子为sp3杂化,B正确;BeCl 中Be原子为sp杂化,BF 中B原子为sp2杂化,C不正确;C H 中C原子为
2 3 2 4
sp2杂化,C H 中C原子为sp杂化,D不正确。
2 2
8.A 在乙烯分子中碳原子与相连的氢原子、碳原子形成平面三角形,所以乙烯分子中每个碳原子均
采取sp2杂化,其中杂化轨道形成σ键,未参与杂化的2p轨道形成π键。
归纳总结 杂化轨道与共价键类型
杂化轨道只能用于形成σ键或用来容纳未参与成键的孤电子对,不能用于形成π键;未参与杂化的p轨
道可用于形成π键。
9.D 中心原子采取sp3杂化轨道成键的分子可能是正四面体形(如CH )、三角锥形(如NH )或者V形
4 3
(如H O),A正确;π键是由未参与杂化的轨道“肩并肩”重叠形成的,杂化轨道只用于形成σ键或用于
2
容纳孤电子对,B正确;正四面体形的CH 和三角锥形的NH 中,中心原子N和C都是通过sp3杂化轨道
4 3成键,C正确;杂化轨道理论和VSEPR模型都是为了解释分子的空间结构而提出的理论,两者不矛盾,可
以先通过VSEPR模型判断出分子的空间结构,再判断出中心原子的杂化轨道类型,D错误。
特别提醒 (1)在形成多原子分子时,中心原子价电子层上的某些能量相近的原子轨道(ns、np)发生杂
化,双原子分子中,不存在原子轨道的杂化。
(2)杂化过程中,原子轨道总数不变,即杂化轨道的数目与参与杂化的原子轨道数目相等。
(3)杂化过程中,轨道的形状发生变化,但杂化轨道的形状相同,能量相同,方向不同。
10.C CH 的中心碳原子为sp3杂化,空间结构为正四面体形,A不符合题意;NH 的中心氮原子为sp3杂
4 3
化,空间结构为三角锥形,B不符合题意;BF 的中心硼原子为sp2杂化,空间结构为平面三角形,C符合题
3
意;CO 的中心碳原子为sp杂化,空间结构为直线形,D不符合题意。
2
11.C NH 和CH 中的中心原子都是sp3杂化,都形成夹角为109°28'的四个杂化轨道,只是NH 分子中
3 4 3
N原子利用其中3个sp3杂化轨道与3个H原子的1s轨道成键,另一个sp3杂化轨道被孤电子对占据,
所以NH 分子为三角锥形,而CH 分子中4个sp3杂化轨道全部用于形成4个C—H键,所以CH 分子
3 4 4
为正四面体形。
12.A CH 为正四面体形,而CH-为三角锥形,微粒的空间结构、键角、稳定性均发生改变,但中心原子
4 3
杂化轨道类型不变,都是sp3杂化。
13.D A项,SO 分子中硫原子的价层电子对数=3+1×(6-3×2)=3,不含孤电子对,采取sp2杂化,空间结构
3
2
为平面三角形,错误;B项,SO 分子中硫原子的价层电子对数=2+1×(6-2×2)=3,含1对孤电子对,采取sp2
2
2
杂化,空间结构为V形,错误;C项,C
O2-
中碳原子价层电子对数=3+1×(4+2-3×2)=3,不含孤电子对,采取
3 2
sp2杂化,空间结构为平面三角形,错误;D项,乙炔(CH CH)分子中每个碳原子均形成2个σ键和2个
π键,价层电子对数是2,为sp杂化,空间结构为直线形,正确。
能力提升练
1.A 2.CD 3.C 4.D 5.D 6.B 7.D 8.B
9.A1.A A项,SO2-中S原子价层电子对数为4,杂化轨道类型是sp3,SO 中S原子价层电子对数为3,杂化
3 3
轨道类型是sp2,故A符合题意;B项,CH 中C原子价层电子对数为4,杂化轨道类型是sp3,H O中O原
4 2
子价层电子对数为4,杂化轨道类型是sp3,故B不符合题意;C项,PCl 中P原子价层电子对数为4,杂化
3
轨道类型是sp3,ClO-中Cl原子价层电子对数为4,杂化轨道类型是sp3,故C不符合题意;D项,BF 中B
3 3
原子价层电子对数为3,杂化轨道类型为sp2,CO2-中C原子价层电子对数为3,杂化轨道类型为sp2,故D
3
不符合题意。
2.CD CS 分子中,碳原子采取sp杂化,为直线形,A错误;ClO-的中心原子价层电子对数为4,孤电子对
2 3
数为1,所以是三角锥形,B错误;SF 的中心原子价层电子对数为6,无孤电子对,呈正八面体结构,有6对
6
完全相同的成键电子对,C正确;SiF 和SO2-的中心原子价层电子对数为4,都是sp3杂化,D正确。
4 3
3.C 中心原子采取sp3杂化的分子,VSEPR模型是四面体形,但其空间结构不一定是四面体形,如:水和
氨气分子中中心原子均采取sp3杂化,但H O是V形分子,NH 是三角锥形分子,故A错误;CH 中sp3杂
2 3 4
化轨道是由中心碳原子的能量相近的2s轨道和3个2p轨道杂化形成的,故B错误;同一个原子中能量
相近的s轨道和p轨道混杂可形成一组能量相同的新轨道,故C正确;BF 中B原子的价层电子对数为
3
3,杂化轨道类型为sp2,故D错误。
4.D PCl 分子中三个P—Cl键完全相同,所以其键长、键能、键角都相等,故A、C正确;不同非金属
3
元素原子之间形成极性共价键,则分子中P—Cl键是极性共价键,故B正确;PCl 分子中中心磷原子的
3
价层电子对数为3+5-1×3=4,为sp3杂化,故D错误。
2
5.D SO 分子中心原子杂化方式为sp2,价层电子对互斥模型为平面三角形,含有一对孤电子对,分子的
2
空间结构为V形,A错误;HCHO分子中心原子杂化方式为sp2,价层电子对互斥模型为平面三角形,没
有孤电子对,分子的空间结构为平面三角形,B错误;NF 分子中心原子杂化方式为sp3,价层电子对互斥
3
模型为四面体形,含有一对孤电子对,分子的空间结构为三角锥形,C错误;NH+的中心原子杂化方式为
4
sp3,价层电子对互斥模型为正四面体形,没有孤电子对,离子的空间结构为正四面体形,D正确。6.B ①BF 分子中硼原子杂化轨道数为3,所以采取sp2杂化,故正确;② 分子中硫原子杂化轨
3
道数为4,所以采取sp3杂化,故错误;③ 分子中碳原子杂化轨道数为3,所以采取sp2杂化,故正
确;④ 分子中每个碳原子杂化轨道数为2,所以采取sp杂化,故错误;⑤N H 分子中每个氮原
2 4
子杂化轨道数为4,所以采取sp3杂化,故错误;⑥苯分子中每个碳原子杂化轨道数为3,所以采取sp2杂化,
故正确。
7.D 由结构示意图可知,Si位于正四面体的中心,键角为109°28',A错误;Si原子核外最外层有4个电
子,Si原子形成4个Si—O键,O原子核外最外层有6个电子,Si的化合价为+4价,O的化合价为-2价,化
学组成为SiO4-,B错误、D正确;Si原子形成4个Si—O σ键,Si上没有孤电子对,Si原子采用sp3杂化,C
4
错误。
8.B 一个二氧化碳分子中含有2个σ键且中心原子不含孤电子对,所以碳原子采取sp杂化而不是sp2
杂化,A错误;NH 、NCl 中N原子都采取sp3杂化,有1对孤电子对,所以分子的空间结构都是三角锥形,
3 3
B正确;S的电负性比O小,而且原子半径大,所以S—H键上的电子对偏向S并没有H O中O—H键上
2
的电子对偏向O那么严重,所以排斥力也相应比较小,键角也稍小,C错误;BF 分子中B元素化合价为
3
+3价,B原子最外层未达8电子结构,D错误。
9.A 杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对,不能用于形成π键,A错误;分子中
中心原子通过sp3杂化轨道成键时,该分子是否是四面体结构,还与该中心原子是否有孤电子对有关,若
无孤电子对,则为四面体结构,B正确;杂化前后轨道的数目不变,但轨道的形状会发生变化,C正确;sp3
杂化轨道为正四面体形,夹角为109°28',sp2杂化轨道为平面三角形,夹角是120°,sp杂化轨道为直线形,
夹角是180°,D正确。
10.答案 (1)①④②⑤③
(2)直线形 V形 三角锥形 正四面体形
(3)sp3(4)sp3 不在
解析 (1)①HCN中的C原子采取sp杂化,键角为180°;②SiF 中Si原子杂化轨道数为4,采取sp3杂化,
4
键角为109°28';③SCl 中S原子杂化轨道数为4,采取sp3杂化,含有2对孤电子对,分子为V形结构,键
2
角约为105°;④CO2-中C原子的杂化轨道数为3,所以C原子采取sp2杂化,分子为平面三角形结构,键
3
角为120°;⑤H O+中O原子的杂化轨道数为4,所以O原子采取sp3杂化,O原子上含有1对孤电子对,
3
分子为三角锥形结构,键角约为107°。所以各微粒按键角由大到小的顺序排列为①④②⑤③。
(2)ClO-中两原子构成直线形结构,ClO-、ClO-、ClO-中Cl采取sp3杂化,孤电子对数分别为2、1、0,所
2 3 4
以空间结构分别为V形、三角锥形、正四面体形。
(3)由题图结构可知,每个硫原子形成2个共价键,且含有2对孤电子对,S原子的杂化轨道数为4,故硫原
子采取sp3杂化。
(4)N H 分子中,每个N原子形成3个σ键,N原子上有1对孤电子对,故N原子采取sp3杂化;1个N原
2 4
子和与其相连的2个H原子及另外1个N原子形成类似NH 的三角锥形结构,故六个原子不可能共面。
3