文档内容
高 2019 级 2019—2020 学年度第一学期期中模块考试
化学试题 2019.11
Ⅰ选择题部分
(本部分共24个小题,每个小题只有一个选项最符合题意,每小题2分,共48分)
1.下列说法中,正确的是( )
A.1771年,法国科学家拉瓦锡发现元素周期律,把化学元素及其化合物纳入一个统一的理论体系
B.化学科学与其他科学分支的联系不密切
C.化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中
D.化学家可以在微观层面上操纵分子和原子,组装分子材料、分子器件和分子机器
2.2018年,一档《辉煌中国》电视纪录片,让“厉害了,我的国”成了不少人的口头禅。我国科技
创新成果卓越,下列成果中获得诺贝尔奖的是( )
A.侯德榜发明联合制碱法 B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发石油炼制催化剂 D.张青莲主持测定了几种元素相对原子质量的新值
3.保护环境是每一个公民的责任。下列做法有利于保护环境的是( )
①推广使用无磷洗衣粉 ②城市垃圾分类处理 ③推广使用一次性木质筷子
④推广使用清洁能源 ⑤过量使用化肥、农药 ⑥推广使用无氟冰箱。
A.①②④⑤ B.①②④⑥ C.②③④⑥ D.③④⑤⑥
4.战国所著《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为
“蜃”。蔡伦改进的造纸术,第一步沤浸树皮脱胶的碱液可用“蜃”溶于水制得。“蜃”的主要成
分是( )
A.CaO B.NaHCO C.SiO D.CaCO
3 2 3
5.下列有关物质分类或归类正确的一组是( )
①液氨、液氯、干冰均为化合物 ②盐酸、合金、氨水均为混合物
③明矾、小苏打、醋酸、硫酸均为电解质 ④碘酒、氢氧化钠溶液、豆浆均为胶体
⑤Na O,Na CO ,NaHCO ,Na SiO 均为钠盐
2 2 3 3 2 3
A. ①和② B.②和③ C.③和④ D. ②③⑤
6.春秋季节在我市常出现大雾天气,对于这种现象下列说法正确的是( )
A.大雾是由于空气中的SO 超标造成的 B.大雾可看作是一种分散剂为水的分散系
2
C.大雾可看作是一种胶体 D.大雾是由于空气中的粉尘超标造成的7.下列操作过程中一定有氧化还原反应发生的是( )
A. B. C. D.
8.粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。为了
除去粗盐中的Ca2+, Mg2+, SO 2-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作
4
中选取必要的步骤和正确的操作顺序( )
①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na CO 溶液;⑤加过量BaCl 溶液。
2 3 2
A. ④②⑤ B. ②⑤④①③ C. ④①②⑤③ D. ①④②⑤③
9.下列离子方程式,书写正确的是( )
A.盐酸与石灰石反应:CO 2ˉ+2H+ = CO ↑+H O
3 2 2
B.铁与稀盐酸反应:2Fe+6H+ = 2Fe3++3H ↑
2
C.氢氧化铁胶体的制备:FeCl + 3H O = Fe(OH) +3HCl
3 2 3
D.硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH¯+Cu2++SO 2ˉ = BaSO ↓+Cu(OH) ↓
4 4 2 [来源:学+科+网]
10.科学家开发出一种低成本光伏材料—蜂窝状石墨烯。生产原理是Na O+2CO
2
Na CO +C(石墨烯),然后除去Na CO ,即可制得蜂窝状石墨烯。下列说法不正确的是( )
2 3 2 3
A.该生产石墨烯的反应属于氧化还原反应
B.石墨烯与金刚石互为同素异形体
C.Na O属于碱性氧化物,CO属于酸性氧化物,Na CO 属于盐
2 2 3
D.自然界中钠元素以化合态形式存在
11.磁流体是电子材料的新秀,它既具有固体磁性材料的磁性,又具有液体的流动性。制备时将含
等微粒个数的FeSO 溶液和Fe (SO ) 溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶
4 2 4 3
液,即可生成黑色的、分散质粒子的直径为 5.5 36nm 的磁流体 。下列说法中正确的是(
~
)
A.所得到的分散系属于浊液 B.用一束光照射该分散系时,可以看到一条光亮的“通路”
C.该分散系不能透过滤纸 D.该分散系的分散质为Fe(OH)
3
12.下列叙述中正确的是( )
序号 氧化剂 还原剂 其他反应物 氧化产物 还原产物① Cl FeCl FeCl
2 2 3
② KMnO H O H SO O MnSO
4 2 2 2 4 2 4
③ KClO HCl(浓) Cl Cl
3 2 2
④ KMnO HCl(浓) Cl MnCl
4 2 2
A.表中第①组反应中FeCl 只是还原产物 B.氧化性比较:KMnO >Fe3+>Cl
3 4 2
C.还原性比较:H O >Mn2+>Cl- D.第④组中的HCl既作还原剂,又起到酸的作用
2 2
13.如表所示,陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
A 碳酸钠溶液可用于治疗胃病 NaCO 可与盐酸反应 Ⅰ对,Ⅱ对,有
2 3
B 向滴有酚酞的水溶液中加入 NaO 与水反应生成NaOH Ⅰ对,Ⅱ错,无
2 2
NaO 变红色
2 2
C 金属钠具有强还原性 高压钠灯发出透雾性强的黄光 Ⅰ对,Ⅱ对,有
D 过氧化钠可为航天员供氧 NaO 能与CO 和HO反应生成O Ⅰ对,Ⅱ对,有
2 2 2 2 2
14.离子的摩尔导电率可用来衡量电解质溶液中离子导电能力的强弱,摩尔导电率越大,离子在溶
液中的导电能力越强。已知Ca2+、OH-、HCO-的摩尔导电率分别为0.60、1.98、0.45,据此可判断,
3
向饱和澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是(
)
15.化学实验中若使某步的有害产物作为另一步的反应物,
形成一个循环,则可不再向环境排放该种有害物质。在如
图所示有编号的反应中,属于氧化还原反应的有( )
A.3个 B.4个 C.5个 D.6个
16.将一块金属钠投入到滴有紫色石蕊试液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其
中正确的有( )
①钠投入水中,先沉入水底,后浮出水面 ②钠立即与水反应,并有气体产生
③反应后溶液变红 ④钠熔成闪亮的小球
⑤小球在水面上四处游动 ⑥有“嘶嘶”的响声发出.
A.①②③④ B.②③④⑤ C.②④⑤⑥ D.③④⑥17.小王同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及
时制止。原因是CO 可以支持镁燃烧发生以下反应:2Mg+CO 2MgO+C,下列关于该反应
2 2
的判断正确的是( )
[来源:学*科*网]
A.Mg元素化合价由0价升高到+2价,所以MgO是还原产物
B.由此反应可以判断氧化性CO >MgO,还原性Mg>C
2
C.CO 作氧化剂,表现氧化性,发生氧化反应
2
D.Mg原子得到的电子数目等于碳原子失去的电子数目
18.下述对焰色反应实验操作注意事项的说明,正确的是( )。
①钾的火焰颜色要透过蓝色钴玻璃观察;
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质;
[来源:学科网]
③每次实验后,要将铂丝用盐酸洗净;
④实验时最好选择本身颜色较浅的火焰;
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确
C.仅有⑤不正确 D.全正确
19.制备氰氨基化钙的化学方程式为CaCO +2HCN=CaCN +CO↑+H ↑+CO ↑,下列说法正确的是(
3 2 2 2
)
[来源:学科网]
A. 氢元素被氧化,碳元素被还原 B. HCN被氧化,CaCO 被还原
3
C. HCN是氧化剂,CaCO 是还原剂 D. CaCN 是氧化产物,H 为还原产物
3 2 2
20.下列实验装置不能达到实验目的的是( )
21.已知在碱性溶液中可发生如下反应:
2R(OH) +3ClO-+4OH-===2RO n-+3Cl-+5HO,则RO n-中R的化合价是( )
3 4 2 4
A.+3 B.+4 C.+5 D.+6
22.现有两瓶失去标签的同浓度的Na CO 和NaHCO 无色溶液,下述鉴别方法不合理的是( )
2 3 3
①用干燥的pH试纸检验,pH大的是Na CO
2 3②取同量的溶液于两支试管中,加热,有气泡产生的是NaHCO
3
③取同量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO
3
④取同量的溶液于两支试管中,滴加Ba(OH) 溶液,生成白色沉淀的是Na CO
2 2 3
⑤取同量的溶液于两支试管中,滴加BaCl 溶液,生成白色沉淀的是Na CO
2 2 3
A. ①⑤ B.③⑥ C.②④ D.②⑤
23.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中共存的是( )
A. 所含溶质为NaHSO 的溶液:加入K+、CO 2-、NO -、Na+
4 3 3
B. 滴加酚酞变红的溶液:加入SO 2-、Cu2+、K+、Cl -
4
C. 常温下,加入铁粉能生成H 的溶液:加入Na+、Ca2+、Cl -、HCO -
2 3
D. 含有大量SO 2-的溶液:加入K+、Cu2+、Cl-、NO -
4 3
24.《本草纲目》中记载“(火药)乃焰消(KNO )、硫磺、杉木炭所合,以为烽燧铳机诸药者”.
3
火药燃烧爆炸时发生的反应为:S+2KNO +3C K S+N ↑+3CO ↑,下列有关说法正确的是(
3 2 2 2
)
A.黑火药属于纯净物 B.该反应中硫元素的化合价升高
C.黑火药爆炸时,发生了氧化还原反应 D.该反应属于置换反应
Ⅱ非选择题部分
(本部分共四个题,每空2分,共52分)
25(10分)下表是生活生产中常见的物质,表中列出了它们的一种主要成分(其它成分未列出)
编号 ① ② ③ ④ ⑤ ⑥
名称 天然气 白酒 醋酸 小苏打 消石灰 铜线
成分 CH CHOH CHCOOH NaHCO Ca(OH) Cu
4 2 5 3 3 2
(1)请你对表中①~⑦的主要成分进行分类(填编号)
是电解质的是 ,是非电解质的是 。
(2)写出④在水中的电离方程式 。
(3)写出下列反应的离子方程式:
用④治疗胃酸过多(主要成分为盐酸) 。
用③除水垢的离子方程式 。26(12分)金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年
才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融)
2Na+Cl↑。回答下列有关单质钠的问题:
2
(1)下列各项中属于保存金属钠的正确方法是 。
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是 。
A.NaO B.NaO C.NaOH D.NaCO
2 2 2 2 3
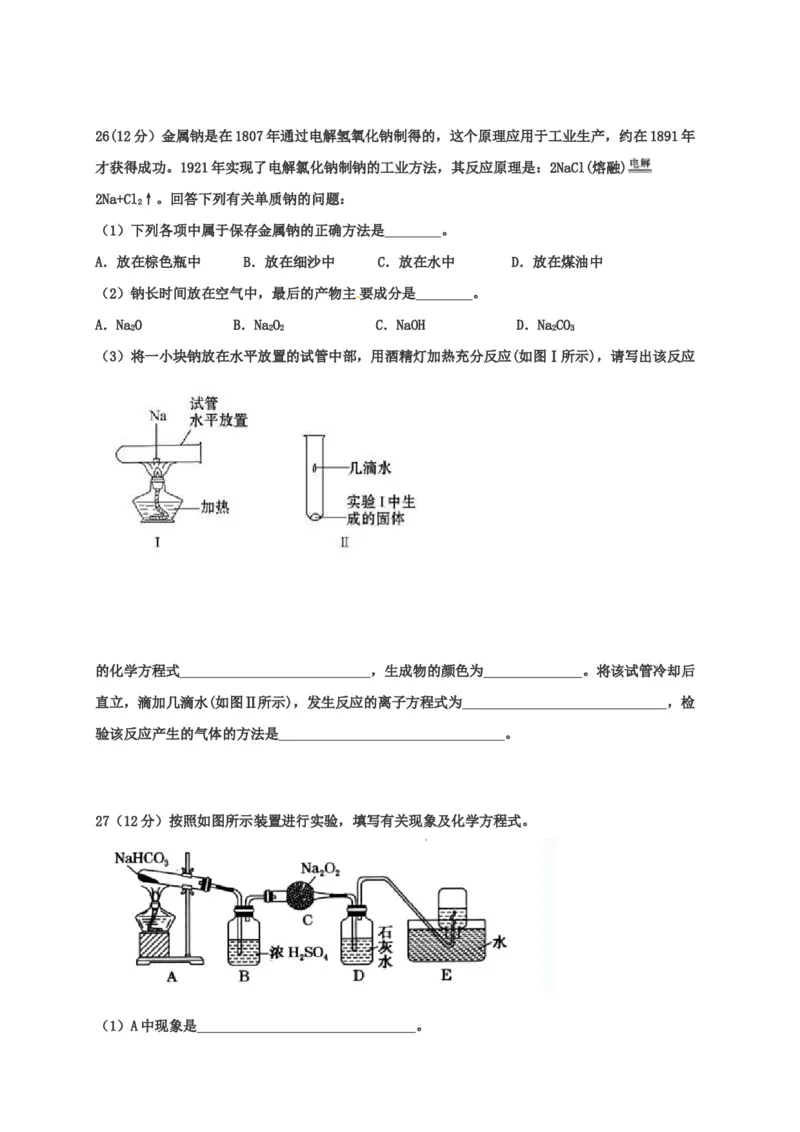
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),请写出该反应
的化学方程式 ,生成物的颜色为 。将该试管冷却后
直立,滴加几滴水(如图Ⅱ所示),发生反应的离子方程式为 ,检
验该反应产生的气体的方法是 。
27(12分)按照如图所示装置进行实验,填写有关现象及化学方程式。
(1)A中现象是 。(2)B中浓硫酸的作用是 。
(3)C中发生反应的化学方程式为 。
(4)D中的现象是 ,发生反应的离子方程式是
。
(5)E中收集的气体是 (填名称)。
28(18分)氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是 。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH 和Cl 反应的方程式为: NH+ Cl— N+ HCl
3 2 3 2 2
①该反应中被氧化的元素是 (填元素名称),氧化剂是 (填化学式)。
②配平该方程式: NH + Cl — N + HCl
3 2 2
③根据上述反应,工业生产中常用喷洒氨水的方法来检查是否有Cl 泄漏,若Cl 有泄漏,可以观察
2 2
到的现象是 ,产生该现象的反应方程式为 。
(3)“地康法”制氯气的反应原理图示如下:
①反应I的化学方程式为 。
②反应II属于 反应。(填四种基本反应类型之一)。
③若要制得a个氯气分子,则整个反应中转移电子的个数为 个。高一期中化学检测答案
1-5DBBAB;6-10CDBDC;11-15BDDDA;16-20CBDDD;21-24DCDC;
25(1)③④⑤;①②;
(2)NaHCO =Na++HCO -;
3 3
(3)HCO -+H+=H O+CO ↑;
3 2 2
CaCO +2CH COOH=Ca2++2CH COO-+H O+CO ↑;
3 3 3 2 2
26(1)D; (2)D;
(3)2Na+O Na O ;淡黄色 ;
2 2 2
2Na O +2H O=4Na++4OH-+O ↑;
2 2 2 2
用带火星的木条放在试管口,看是否复燃;
27(1)试管口有无色液体生成;
(2)干燥CO 气体;
2
(3)2CO +2Na O =2Na CO +O ;
2 2 2 2 3 2
(4)石灰水变浑浊;
CO +Ca2++2OH-=CaCO ↓+H O;
2 3 2
(5)氧气。
28(1)a;
[来源:学§科§网Z§X§X§K]
(2)①氮;Cl ;
2
②2,3,1,6;
③有白烟产生;
HCl+NH =NH Cl;
3 4
(3)2HCl+CuO=CuCl +H O;
2 2
置换反应;
2a。