文档内容
实验活动3 盐类水解的应用(精练)
题组一 溶液酸碱性的判断
1.(2022广西)水溶液呈碱性的盐是
A.NaOH B.NaNO C.NaC O D.NaHSO
3 2 2 4 4
【答案】C
【解析】A. NaOH是强碱,在水溶液中电离出氢氧根,故A不选;
B. NaNO 是强酸强碱盐,其水溶液呈中性,故B不选;
3
C. Na C O 是强碱弱酸盐,C O 在水溶液中水解生成氢氧根,溶液呈碱性,故C选;
2 2 4 2
D. NaHSO 在水溶液中电离产生氢离子、钠离子、硫酸根离子,溶液呈酸性,故D不选;
4
正确答案是C。
2.(2022银川)物质的量浓度相同的NaX、NaY和NaZ三种盐溶液,若它们的pH依次为8、9、10,则HX、
HY、HZ的酸性由强到弱的排列顺序是( )
A.HX、HZ、HY B.HZ、HY、HX
B.HX、HY、HZ D.HY、HZ、HX
【答案】C
【解析】组成盐的酸根对应的酸越弱,该酸根的水解程度越大,物质的量浓度相同时,该盐溶液的碱性越
强,pH越大,则HX、HY、HZ的酸性由强到弱的排列顺序是HX、HY、HZ。
3.(2022·诸暨)下列物质的水溶液呈碱性且属于盐是( )
A.苯甲酸钠 B. C.HCl D.
【答案】A
【解析】A.苯甲酸钠属于强碱弱酸盐,其水溶液呈碱性,属于盐类,A选;
B. 与水反应生成NaOH,溶液呈碱性,属于金属氧化物,不属于盐类,B不选;
C.HCl电离出氢离子,溶液呈酸性,属于酸类,不属于盐类,C不选;
D. 是强酸强碱盐,溶液呈中性,D不选;
故答案为:A。
题组二 盐类水解在生活中的应用
1.(2022雅安)下列事实不属于盐类水解应用的是( )A.NH Cl与ZnCl 溶液可作焊接金属中的除锈剂
4 2
B.实验室通常在HCl气氛中加热MgCl •6H O制MgCl
2 2 2
C.实验室配制FeCl 溶液时加入少量稀盐酸
3
D.实验室用Zn和稀硫酸制氢气时加入少量CuSO 溶液
4
【答案】D
【解析】A.NH Cl与ZnCl 溶液可作焊接金属中的除锈剂,主要是NH Cl与ZnCl 溶液水解显酸性,酸和
4 2 4 2
铁锈反应,故A不符合题意;
B.实验室通常在HCl气氛中加热MgCl •6H O制MgCl ,加HCl的目的是抑制镁离子水解,故B不符合题
2 2 2
意;
C.实验室配制FeCl 溶液时加入少量稀盐酸,目的是抑制铁离子水解,防止溶液变浑浊,故C不符合题意;
3
D.实验室用Zn和稀硫酸制氢气时加入少量CuSO 溶液,锌置换出铜形成Zn−Cu−HSO 原电池,加快反
4 2 4
应速率,与水解无关,故D符合题意。
故答案为:D。
2.(2022新乡)化学与生活密切相关。下列物质的用途与水解有关的是( )
A.草木灰去除餐具的油污 B.硫酸铜对游泳池进行消毒
C.FeCl 溶液腐蚀铜制线路板 D.钡餐用于胃肠道造影检查
3
【答案】A
【解析】A.草木灰的主要成分为碳酸钾,碳酸根离子水解使溶液显碱性,从而去除餐具的油污,A符合
题意;
B.细菌的细胞壁主要是肽聚糖结构,硫酸铜做消毒剂,起作用离子是铜离子,因为铜离子有破坏肽聚糖
结构的作用,能损伤细胞壁而使细菌变形或杀伤细菌,所以可以用来杀菌,与水解无关,B不符合题意;
C.FeCl 溶液腐蚀铜制线路板,是氯化铁与铜发生氧化还原反应生成氯化铜和氯化亚铁,利用了铁离子的
3
氧化性,与水解无关,C不符合题意;
D.用于消化道检查的钡餐是药用硫酸钡,硫酸钡不溶于水和脂质,不会被胃肠道黏膜吸收,对人基本无
毒性,钡餐造影即消化道钡剂造影,是指用硫酸钡作为造影剂,在X线照射下显示消化道有无病变的一种
检查方法,与水解无关,D不符合题意;
故答案为:A。
3.(2021金台)下列表述中,与盐类水解有关的是( )
①明矾和FeCl 可作净水剂
3
②为保存FeCl 溶液,要在溶液中加少量铁粉
2
③AlCl 溶液蒸干,灼烧,最后得到的主要固体产物是Al O
3 2 3④NHCl与ZnCl 溶液可作焊接中的除锈剂
4 2
⑤实验室盛放NaOH溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥用NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
⑦草木灰与铵态氮肥不能混合施用
A.①②③⑤⑥⑦ B.①③④⑥⑦
C.①③⑤⑥⑦ D.全有关
【答案】B
【解析】①铝离子和铁离子水解生成胶体,具有吸附悬浮杂质的作用,起到净水的作用,故①和水解有关
②亚铁离子极易被氧化为Fe3+,加入铁粉可以把Fe3+还原为Fe2+离子,故②和水解无关;
③蒸干氯化铝溶液促进铝离子的水解,氯化氢挥发得到水解产物氢氧化铝,氢氧化铝灼烧得到氧化铝,故
③和水解有关;
④铵根离子、锌离子水解显酸性,因此能和铁锈反应,能起到除锈的作用,故④和水解有关;
⑤氢氧化钠溶液和玻璃中的二氧化硅反应,生成硅酸钠是矿物胶粘结瓶口和瓶塞,故⑤与水解无关;
⑥碳酸氢根离子水解显碱性,铝离子水解显酸性,二者水解相互促进生成二氧化碳和氢氧化铝,故⑥和水
解有关;
⑦草木灰是碳酸钾,水解显碱性,铵盐水解显酸性,混合水解会相互促进生成二氧化碳和氨气,减弱肥效,
故⑦和水解有关;
故答案为:B。
4.(2022辽宁)下列事实:
① 溶液呈酸性;
②长期施用化肥 会使土壤酸性增强,发生板结;
③配制 溶液时,用稀盐酸溶解 固体;
④ 溶液中 ;
⑤氯化铵溶液可去除金属制品表面的锈斑;
⑥蒸干 溶液,往往得不到 固体。
其中与盐类的水解有关的有( )
A.仅①②③⑤ B.仅②③④⑤⑥
C.仅①④⑤⑥ D.仅①②③④⑤【答案】B
【解析】①中 为强酸强碱的酸式盐,溶液显酸性是因为 电离出 ,和盐的水解
无关;②中是 水解使土壤酸性增强;③中 电离产生的 会抑制 水解;④中是因
水解的程度大于其电离的程度,故c(HS)>c(S2-);⑤中 水解产生的 与锈斑中的Fe O
2 2 3
反应;⑥加热会促进 水解,蒸干FeCl 溶液往往得到的是Fe O;
3 2 3
综上所述,②③④⑤⑥符合题意,
故答案为:B。
5.(2021黑龙江)下列说法与盐类的水解有关的有几项( )
①氯化铵与氯化锌溶液可作焊接金属过程中的除锈剂
②用碳酸氢钠与硫酸铝两种溶液可作泡沫灭火剂
③配制硫酸亚铁溶液时需加入少量铁粉
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤比较氯化铵和硫化钠等盐溶液的酸碱性
⑥草木灰与铵态氮肥不能混合施用
⑦Na SO 溶液蒸干后得到NaSO 固体
2 3 2 4
A.4项 B.5项 C.6项 D.7项
【答案】B
【解析】①NH Cl与ZnCl 溶液中的铵根和锌离子会发生水解,导致溶液显示酸性,酸可以和金属锈的成
4 2
分反应而除锈,故①与盐类的水解有关;
②NaHCO 与Al (SO ) 两种溶液中的碳酸根离子和铝离子双水解会生成二氧化碳来灭火,二者可作泡沫灭
3 2 4 3
火剂,故②与盐类的水解有关;
③硫酸亚铁配制中要加硫酸和铁粉,铁粉的作用是防止亚铁离子被氧化,故③与盐类的水解无关;
④Na CO 溶液中的碳酸根水解显示碱性,磨口玻璃塞的成分中二氧化硅可以和碱反应,会导致瓶塞和瓶口
2 3
黏在一起,故④与盐类的水解有关;
⑤铵根离子水解显酸性、硫离子水解溶液显碱性,故⑤与盐类的水解有关;
⑥铵根离子水解呈酸性,草木灰中的碳酸根离子水解显碱性,二者发生相互促进的水解反应,生成氨气,
挥发降低肥效,故⑥与盐类的水解有关;
⑦Na SO 溶液蒸干过程中,NaSO 被氧化为NaSO 固体,故⑦与盐类的水解无关;
2 3 2 3 2 4综上所述,与盐类的水解有关的有5个,故B符合题意。
故答案为:B。
题组三 离子浓度的比较
1.(2022湖南)下列有关电解质溶液的说法正确的是( )
A.向0.1mol/L CH COOH溶液中加入少量水,溶液中 减小
3
B.将CHCOONa溶液从20℃升温至30℃,溶液中 减小
3
C.向盐酸中加入氨水至中性,溶液中
D.室温下,pH=11的CHCOONa溶液与pH=11的NaOH溶液中水的电离程度相同
3
【答案】B
【解析】A.K= ,加水虽促进电离,n(CHCOO-)增大,但c(CHCOO-)减小,K
a 3 3 a
保持不变,则溶液中 增大,A项不符合题意;
B.20℃升温至30℃,促进CHCOO-水解,且K 增大,则溶液中 减小,B
3 h
项符合题意;
C.向盐酸中加入氨水呈中性,则c(H+)=c(OH-),电荷守恒可知,溶液中 ,即
=1,C项不符合题意;
D.CHCOONa溶液中CHCOO-发生水解反应促进水的电离,NaOH电离出OH-抑制水的电离,两者溶液
3 3
中水的电离程度不相同,D项不符合题意;
故答案为:B。
2.(2022·金山)常温下,用0.100 mol·L-1 NaOH(aq)滴定20.00 mL c mol·L-1二元酸HA,滴定曲线如图所
2
示,下列叙述正确的是( )A.HA电离:HA→2H++A2-
2 2
B.a点:c(HA-)>c(Na+)>c(H+)>c(A2-)>c(OH-)
C.b点:c(H+)=c(A2-)+c(OH-)
D.c点:c(Na+)<c(HA-)+2c(A2-)
【答案】C
【解析】A.根据图示可知:未滴定NaOH溶液时,溶液pH接近1,说明H2A第一步完全电离,当加入
NaOH溶液40 mL时,二者恰好反应产生NaA,此时溶液pH=7.26>7,说明A2-发生水解反应产生了
2
HA-,导致溶液中c(OH-)>c(H+),溶液显碱性,说明NaA是强碱弱酸盐,HA第一步完全电离,第二步存
2 2
在电离平衡,电离方程式为:HA =H++HA-,HA- H++A2-,A不符合题意;
2
B.a点反应时得到HA与NaHA的混合溶液,HA第一步完全电离,HA-也电离产生H+,所以c(H+)>
2 2
c(Na+),B不符合题意;
C.b点溶液为NaOH与HA按1:1反应产生NaHA,溶液中存在电荷守恒:c(Na+)+c(H+)=c(HA-)+2c(A2-)
2
+c(OH-),也存在物料守恒:c(Na+)=c(HA-)+c(A2-),所以c(H+)= c(A2-)+c(OH-),C符合题意;
D.c点溶液为NaA溶液,存在电荷守恒:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-),溶液显碱性,则c(H+)<
2
c(OH-),所以c(Na+)>c(HA-)+2c(A2-),D不符合题意;
故答案为:C。
3.(2022·赤峰)25℃时,向一定浓度的 溶液中滴入 溶液,粒子浓度与混合溶液 的
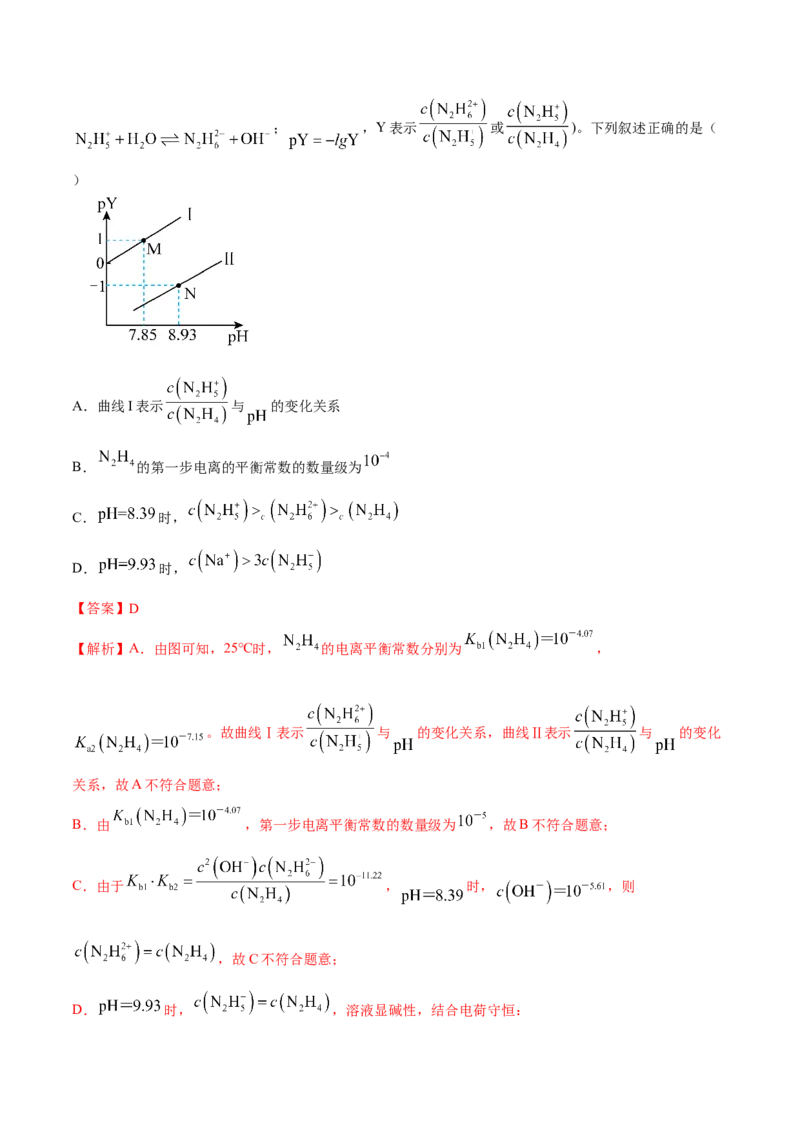
变化关系如图所示。已知:肼在水中的电离方程式: ,; ,Y表示 或 )。下列叙述正确的是(
)
A.曲线I表示 与 的变化关系
B. 的第一步电离的平衡常数的数量级为
C. 时,
D. 时,
【答案】D
【解析】A.由图可知,25℃时, 的电离平衡常数分别为 ,
。故曲线Ⅰ表示 与 的变化关系,曲线Ⅱ表示 与 的变化
关系,故A不符合题意;
B.由 ,第一步电离平衡常数的数量级为 ,故B不符合题意;
C.由于 , 时, ,则
,故C不符合题意;
D. 时, ,溶液显碱性,结合电荷守恒:和物料守恒:
,可知, ,故D符合题意;
故答案为:D。
4.(2022·成都)常温下,向某浓度的二元弱酸HX溶液中逐滴加入NaOH稀溶液,所得溶液中三种微粒
2
HX、HX-、X2-的物质的量分数(δ)与溶液pH的关系如图所示。下列叙述错误的是( )
2
A.M →A反应的离子方程式为: HX+OH- = HX- + H O
2 2
B.B点的溶液中: c(Na+)> 3c(X2-)
C.NaHX溶液中: c(OH-)+ c(X2-)= c(H+) + c(H X)
2
D.外界条件不变时,加入NaOH稀溶液的过程中, =10, 且始终保持不变
【答案】D
【解析】A.HX与NaOH反应生成HXNa和水,M →A反应的离子方程式为: HX+OH- = HX- + H O,
2 2 2
A不符合题意;
B.B点为NaHX与NaX的混合溶液,c(X2-)= ,根据物料守恒c(Na+)= c(X2-)+ = 3c(X2-),
2
但是X2-发生水解,则溶液中: c(Na+)> 3c(X2-),B不符合题意;
C.NaHX溶液中: c(OH-)+ c(X2-)= c(H+) + c(H X),符合质子守恒,C不符合题意;
2
D.A点 ,B点 ,外界条件不变时,加入NaOH稀溶液的过程中, =10-3,D符合题意;
故答案为:D。
5.(2022成都期末)下列说法正确的是( )
A. 溶液中:
B. 溶液和 溶液均显中性,两种溶液中水的电离程度相等
C. 溶液加适量的水稀释后,溶液中 的值变大
D.常温下, 值相等的 三种溶液的浓度大小关系为
【答案】C
【解析】A. 为强碱弱酸盐,亚硫酸氢根的电离大于水解,溶液显酸性,故
,A不符合题意;
B.醋酸铵是弱酸弱碱盐,水溶液中发生水解,促进水的电离,醋酸根离子的水解程度和铵根离子的水解
程度相近,溶液呈现中性, 是强酸强碱盐,对水的电离无影响,B不符合题意;
C. 溶液存在水解平衡: ,加适量的水稀释后,碳酸氢根离子浓度
减小,温度不变水解平衡常数不变,则溶液中 的值变大,C符合题意;
D.酸性:醋酸>碳酸>次氯酸,酸性越弱,其酸根的水解能力越强,相同浓度下盐溶液的pH值越大,故
等pH的 三种溶液的浓度大小关系为,D不符合题意;
故答案为:C。
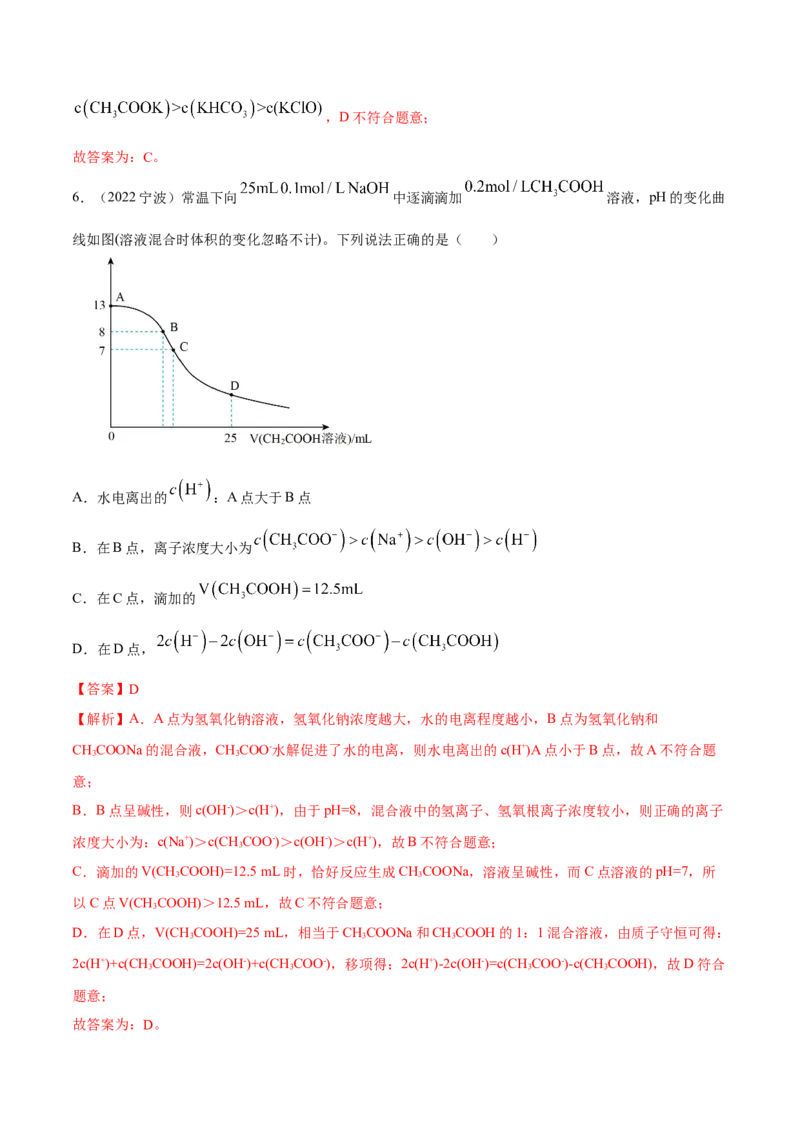
6.(2022宁波)常温下向 中逐滴滴加 溶液,pH的变化曲
线如图(溶液混合时体积的变化忽略不计)。下列说法正确的是( )
A.水电离出的 :A点大于B点
B.在B点,离子浓度大小为
C.在C点,滴加的
D.在D点,
【答案】D
【解析】A.A点为氢氧化钠溶液,氢氧化钠浓度越大,水的电离程度越小,B点为氢氧化钠和
CHCOONa的混合液,CHCOO-水解促进了水的电离,则水电离出的c(H+)A点小于B点,故A不符合题
3 3
意;
B.B点呈碱性,则c(OH-)>c(H+),由于pH=8,混合液中的氢离子、氢氧根离子浓度较小,则正确的离子
浓度大小为:c(Na+)>c(CHCOO-)>c(OH-)>c(H+),故B不符合题意;
3
C.滴加的V(CH COOH)=12.5 mL时,恰好反应生成CHCOONa,溶液呈碱性,而C点溶液的pH=7,所
3 3
以C点V(CH COOH)>12.5 mL,故C不符合题意;
3
D.在D点,V(CH COOH)=25 mL,相当于CHCOONa和CHCOOH的1:1混合溶液,由质子守恒可得:
3 3 3
2c(H+)+c(CH COOH)=2c(OH-)+c(CH COO-),移项得:2c(H+)-2c(OH-)=c(CH COO-)-c(CHCOOH),故D符合
3 3 3 3
题意;
故答案为:D。7.(2022山西)常温时,向20mL0.01mol·L-1的HA溶液中滴加0.01mol·L-1NaOH溶液,混合溶液的pH与
微粒浓度变化的关系如图所示。下列说法不正确的是( )
A.c点溶液对应的pH为5.2
B.b点对应的NaOH溶液体积大于10.00mL
C.a点溶液中:c(HA)>c(A-)>c(Na+)>c(H+)>c(OH-)
D.常温时,HA的K=10-4.2
a
【答案】B
【解析】A.根据分析,c点c(H+)=10-5.2mol/L,pH=5.2,A不符合题意;
B.若加10mLNaOH,溶液中HA与A-为1:1,A-的水解常数K= = =10-9.8,K>K,因此HA的
h a h
电离大于A-的水解,即c(HA)<c(A-),在b点时,c(HX)= c(A-),因此b点对应的NaOH溶液体积小于
10.00mL,B符合题意;
C.a点lg =-1,因此c(HA)=10c(A-),c(HA)>c(A-)由于HA可以电离出A-,因此c(A-)>c(Na+),根
据分析,pH为3.2,因此c(H+)>c(OH-),离子的大小关系为c(HA)>c(A-)>c(Na+)>c(H+)>c(OH-),C不符
合题意;
D.根据分析,电离常数Ka= = c(H+)=10-4.2;D不符合题意;
故答案为:B。
8.(2022·江苏)室温下,通过下列实验探究NaHCO 、NaHSO 溶液的性质:
3 3
实验 实验操作和现象
1 用pH试纸测定浓度为0.1mol·L-1NaHSO 溶液的pH,pH≈5
3
2 用pH试纸测定浓度为0.1mol·L-1NaHCO 溶液的pH,pH≈8
3
3 将浓度均为0.1mol·L-1的NaHSO 和Ba(OH) 溶液等体积混合,产生白色沉淀
3 2
下列说法正确的是( )A.实验1可得0.1mol·L-1NaHSO 溶液中:K (H SO )·K (H SO )<10-10
3 a1 2 3 a2 2 3
B.实验2可得0.1mol·L-1NaHCO 溶液中:c(HCO )>c(CO )>c(HCO)
3 2 3
C.实验3所得溶液中:c(Ba2+)·c(SO )=2.5×10−3
D.浓度均为0.1mol·L-1的NaHSO 和NaHCO 两份溶液中:c(HCO )+2c(CO )<c(HSO )+2c(SO )
3 3
【答案】D
【解析】A.K (H SO )·K (H SO )= · = ,溶液的
a1 2 3 a2 2 3
pH≈5,所以c(H+)≈10-5,c2(H+)≈10-10,溶液显酸性说明HSO 的电离程度大于水解程度,所以c(SO )>
c(HSO ),所以 >1,则K (H SO )·K (H SO )>10-10,A不符合题意;
2 3 a1 2 3 a2 2 3
B.溶液pH≈8,显碱性,则HCO 的水解程度大于电离程度,水解和电离都是微弱的,所以c(HCO )>
c(HCO)>c(CO ),B不符合题意;
2 3
C.等浓度的NaHSO 和Ba(OH) 溶液等体积混合后发生反应:NaHSO+Ba(OH) =BaSO +NaOH+HO,若
3 2 3 2 3 2
BaSO 不是沉淀,则溶液中c(Ba2+)=c(SO )=0.05mol/L,c(Ba2+)·c(SO )=2.5×10−3,但BaSO 为白色沉淀,
3 3
所以c(Ba2+)·c(SO )<2.5×10−3,C不符合题意;
D.NaHSO 溶液中存在电荷守恒:c(Na+)+c (H+)=c(HSO )+2c(SO )+c (OH-),所以c(HSO )+2c(SO
3 1 1 1
)=c (Na+)+c (H+)-c (OH-),同理可得NaHCO 溶液中c(HCO )+2c(CO )=c (Na+)+c (H+)-c (OH-),两溶液中
1 1 1 3 2 2 2
钠离子浓度相同,而NaHSO 溶液的pH更小,所以c(H+)-c (OH-)>c(H+)-c (OH-),则c(HCO )+2c(CO )
3 1 1 2 2
<c(HSO )+2c(SO ),D符合题意;故答案为:D。
题组四 蒸干的产物判断
1.(2022广安)下列物质的水溶液加热蒸干、灼烧不变质的是( )
A. B. C. D.
【答案】D
【解析】A.NH Cl加热分解为氨气和HCl,故A不选;
4
B.NaHCO 加热分解为NaCO、CO 和水,故B不选;
3 2 3 2
C.AlCl 溶液中的Al3+水解生成Al(OH) 和HCl,加热能促进水解和HCl的挥发,所以加热蒸干后得到
3 3
Al(OH) ,灼烧时 Al(OH) 分解为Al O 和水,故C不选;
3 3 2 3
D.NaCl溶液加热蒸干并灼烧,不会发生分解以及水解反应,得到的仍为NaCl固体,故D选;
故答案为:D。
2.(2022浙江)蒸干含有下列溶质的溶液,能得到原溶质的是( )
A.CuSO B.NaSO C.NaHCO D.NH Cl
4 2 3 3 4
【答案】A
【解析】A.加热虽然能促进Cu2+离子水解,但硫酸是难挥发的高沸点酸,水解生成的硫酸能与氢氧化铜
反应,在空气中蒸干后依然得到硫酸铜,A符合题意;
B.亚硫酸钠具有还原性,易被空气中的氧气氧化生成硫酸钠,在空气中蒸干后得到硫酸钠,无法得到亚
硫酸钠,B不符合题意;
C.NaHCO 受热分解为碳酸钠、CO 和HO,最后得到的是碳酸钠固体,C不符合题意;
3 2 2
D.蒸干NH Cl溶液时,会生成氨气和氯化氢,D不符合题意;
4
故答案为:A。
3.(2022抚顺)蒸干并灼烧下列物质的水溶液,仍能得到该物质的是( )
A.氯化铝 B.碳酸氢钠 C.硫酸亚铁 D.碳酸钠
【答案】D
【解析】A、蒸干灼烧氯化铝溶液,由于铝离子的水解,氯化氢的挥发,故最终得到的是氧化铝,A不符
合题意;
B、蒸干灼烧碳酸氢钠溶液,碳酸氢钠受热易分解,故最终得到的是碳酸钠,B不符合题意;
C、蒸干灼烧硫酸亚铁溶液,亚铁离子易被氧化,故最终得到的是硫酸铁,C不符合题意;
D、蒸干灼烧碳酸钠溶液,由于碳酸钠对热稳定,也不易被氧化,故最终仍然得到碳酸钠,D符合题意;故答案为:D。
4.(2022·宝山)向NaBr、NaI混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,剩余固体的组成
可能是:( )
A.NaCl、NaBr、NaI B.NaCl、NaBr、I
2
C.NaCl、NaI D.NaCl、NaI、Br
2
【答案】A
【解析】已知Br-的还原性弱于I-,即向NaBr、NaI混合液中,通入一定量氯气,则先氧化I-,反应为:2I-
+Cl=I +2Cl-,当I-完全消耗后,才氧化Br-,反应为:2Br-+Cl=Br +2Cl-,据此分析解题:
2 2 2 2
A.当通入的氯气很少,NaI过量时,生成的I 易升华,则剩余固体为NaCl、NaBr、NaI,A符合题意;
2
B.由于生成的I 易升华,故固体不可能还含有I,B不合题意;
2 2
C.由于Br-的还原性弱于I-,通入氯气时先氧化I-而不是Br-,即当NaI过量时,不可能NaBr被氧化,即固
体不可能是NaCl、NaI ,C不合题意;
D.由于Br-的还原性弱于I-,通入氯气时先氧化I-而不是Br-,即当NaI过量时,不可能NaBr被氧化,且
Br 易挥发,即固体不可能是NaCl、NaI、Br ,D不合题意;
2 2
故答案为:A。
5.(2022·呼和浩特)在含有NaBr和NaI的溶液中通入足量的 ,然后把溶液蒸干并将剩余残渣灼烧,
最后留下的物质是( )
A.NaCl和NaBr的混合物 B.NaCl和
C.NaCl D.NaCl、 和
【答案】C
【解析】在含有NaBr和NaI的溶液中通入足量的Cl,发生反应2NaBr+Cl = 2NaCl+Br 、2NaI+Cl =
2 2 2 2
2NaCl+I ,把溶液蒸干并将剩余残渣灼烧,溴易挥发、碘易升华,最后留下的物质是NaCl,
2
故答案为:C。
6.(2022·银川)某样品含有氢氧化钾、碳酸钾和水三种物质。室温下,向该样品中加入溶质质量分数为
14.6%的稀盐酸100g,恰好完全反应得到中性溶液,蒸干溶液得到固体质量为( )
A.74.5g B.29.8g C.10g D.7.45g
【答案】B
【解析】样品中加入盐酸,氢氧化钾、碳酸钾分别与盐酸恰好完全反应得到中性溶液,则得到KCl溶液,已知消耗溶质质量分数为14.6%的稀盐酸100g,则 ,反应过程中氯元
素守恒,则反应生成的、蒸干溶液得到固体中 、质量为
;
故答案为:B。
7.(2022·奉化)在含有NaBr和NaI的溶液中通入足量Cl,然后把溶液蒸干,并将所得固体灼烧,最后
2
剩余的物质是( )
A.NaCl B.NaCl和I
2
C.NaCl和NaBr D.NaCl、NaBr和I
2
【答案】A
【解析】向含有NaBr、NaI的混合溶液中通入过量的Cl 充分反应,发生:Cl+2NaI=2NaCl+I ,
2 2 2
Cl+2NaBr=2NaCl+Br ,加热时Br 易挥发,I 易升华,最后剩余的固体为NaCl,
2 2 2 2
故答案为:A。
8.(2022张家口)48.9g由NaO、NaO、NaCO、NaOH组成的混合物与300g质量分数为14. 6%的盐酸
2 2 2 2 3
恰好反应,蒸干反应后的溶液,最终得到的固体的质量为( )
A.70.2 g B.64.4 g C.58.5 g D.46.8 g
【答案】A
【解析】NaO、NaO、NaCO、NaOH的混合物与盐酸恰好反应,所得溶液中溶质为NaCl,溶液蒸干所
2 2 2 2 3
得固体为NaCl,根据氯原子守恒可得:n(NaCl)=n(HCl),盐酸中氯化氢的质量为:m(HCl)
=300g×14.6%=43.8g,则n(NaCl)=n(HCl)=43.8g÷36.5g/mol=1.2mol,所以最终得到NaCl的质量为:
1.2mol×58.5g/mol=70.2g。
故答案为:A。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育