文档内容
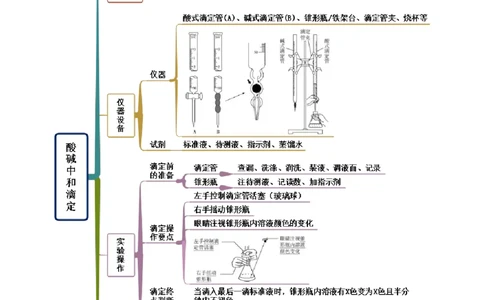
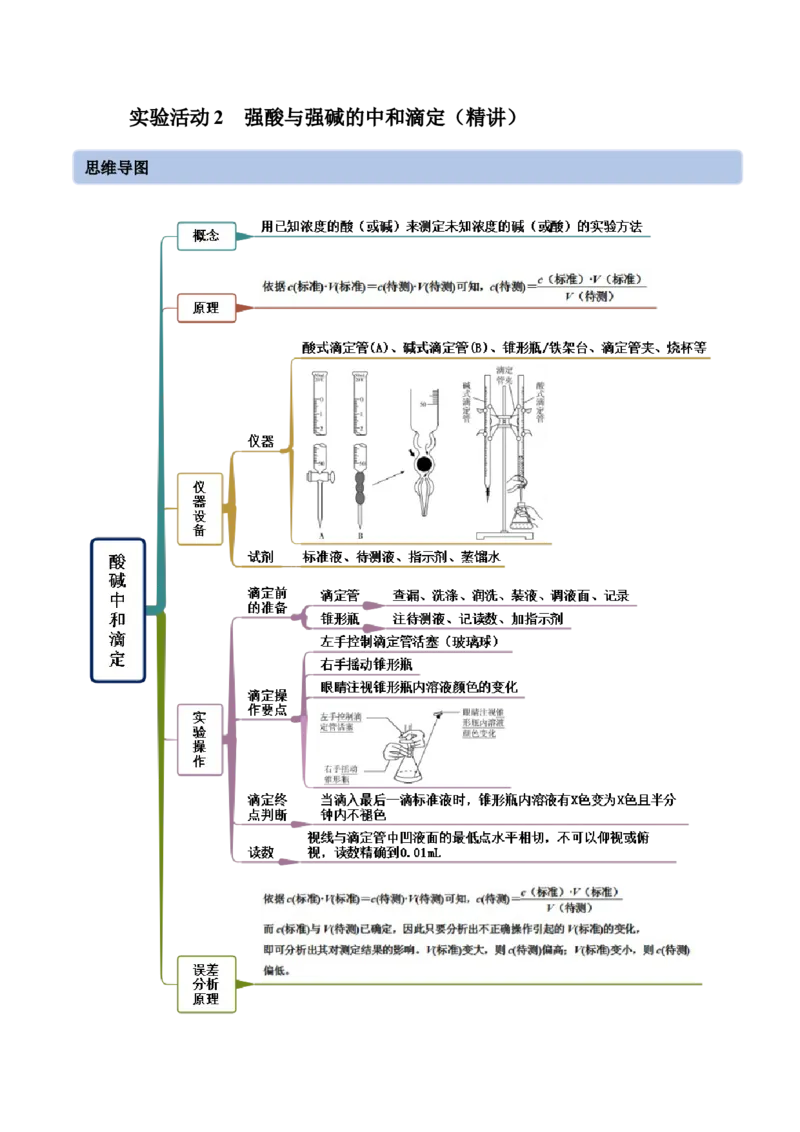
实验活动2 强酸与强碱的中和滴定(精讲)
思维导图例题精讲
【例1】(2022高二·咸阳)实验小组欲用0.5000mol•L-1标准NaOH溶液标定未知浓度的HSO 溶液,其操
2 4
作分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.5000mol•L-1标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④量取20.00mL待测液注入润洗过的锥形瓶中,并加入2滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2~3次。
请回答下列问题:
(1)以上步骤有错误的为 个。
(2)排除碱式滴定管中气泡的方法应采用如图所示操作中的 (填序号)。
(3)步骤⑤滴定时眼睛应注视;到达滴定终点的现象是 。
(4)以下是实验数据记录表:
标准NaOH溶液体积(mL)
滴定次数 待测液体积(mL)
滴定前 滴定后
1 20.00 0.00 18.10
2 20.00 2.20 18.40
3 20.00 2.00 18.16
根据表中数据计算该HSO 溶液的物质的量浓度为 mol/L。
2 4
(5)下列操作可能使所测HSO 溶液的浓度偏高的是____(填字母)。A.锥形瓶装液前,留有少量蒸馏水
2 4
A.碱式滴定管盛装标准液前未润洗
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.滴定过程中刚变色就立即停止滴定【例2】(2022高二·浙江)硫酸亚铁铵 是一种重要的化学试剂,样品中铁含
量的测定可以采用酸性高锰酸钾滴定的方法。高锰酸钾标准溶液可用性质稳定、摩尔质量较大的基准物质
草酸钠( )进行标定。实验步骤如下:
步骤一:先粗略配制浓度约为 的高锰酸钾溶液250mL:
步骤二:称取草酸钠固体mg放入锥形瓶中,加入适量水溶解并加硫酸酸化,加热到70~80℃立即用
滴定,从而标定 浓度为 ;
步骤三:称取样品2.031g,放入锥形瓶并用适量水溶解,然后分成三等份;
步骤四:用标准 溶液滴定步骤三所配样品溶液,三次实验达到终点时消耗标准液体积如下:
序号 滴定前读数/mL 滴定后读数/mL
1 0.10 20.15
2 2.20 25.30
3 1.30 21.25
(1)写出用草酸标定高锰酸钾反应原理的离子方程式 。
(2)步骤一中至少需要用到的玻璃仪器有烧杯、 、 。
(3)步骤二中需要对m的值进行预估,你的预估依据是 。
a.所加硫酸的体积和浓度 b.反应的定量关系
c.滴定管的最大容量 d.用于溶解草酸钠的水的体积
(4)在测定过程中,选出正确的滴定操作并排序 :检查是否漏水→蒸馏水洗涤→标准液润
洗滴定管→( )→( )→( )→( )→到达滴定终点,停止滴定,记录读数
a.轻轻转动酸式滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.调整管中液面,用胶头滴管滴加标准液恰好到“0”刻度
d.锥形瓶放于滴定管下,边摇边滴定,眼睛注视锥形瓶内颜色变化
e.装入标准 溶液至“0”刻度以上2~3mL,固定好滴定管
f.锥形瓶放于滴定管下,边摇边滴定,眼睛注视滴定管内液面变化
g.将滴定管尖向上弯曲,轻轻挤压玻璃珠使滴定管的尖嘴部分充满溶液至无气泡(5)样品中铁元素的质量分数为 。
(6)以下操作会造成测定结果偏低的是____。
A.达到滴定终点读取数据时,俯视视滴定管液面
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
D.溶液颜色变化后,立即读数
【一隅三反】
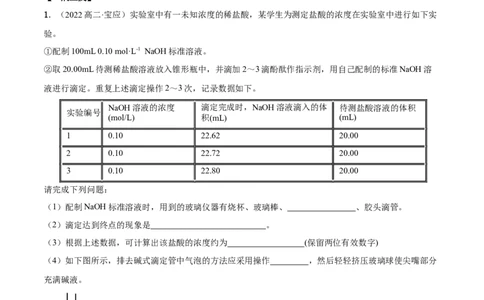
1.(2022高二·宝应)实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实
验。
①配制100mL 0.10 mol·L-1 NaOH标准溶液。
②取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶
液进行滴定。重复上述滴定操作2~3次,记录数据如下。
NaOH溶液的浓度 滴定完成时,NaOH溶液滴入的体 待测盐酸溶液的体积
实验编号
(mol/L) 积(mL) (mL)
1 0.10 22.62 20.00
2 0.10 22.72 20.00
3 0.10 22.80 20.00
请完成下列问题:
(1)配制NaOH标准溶液时,用到的玻璃仪器有烧杯、玻璃棒、 、胶头滴管。
(2)滴定达到终点的现象是 。
(3)根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)
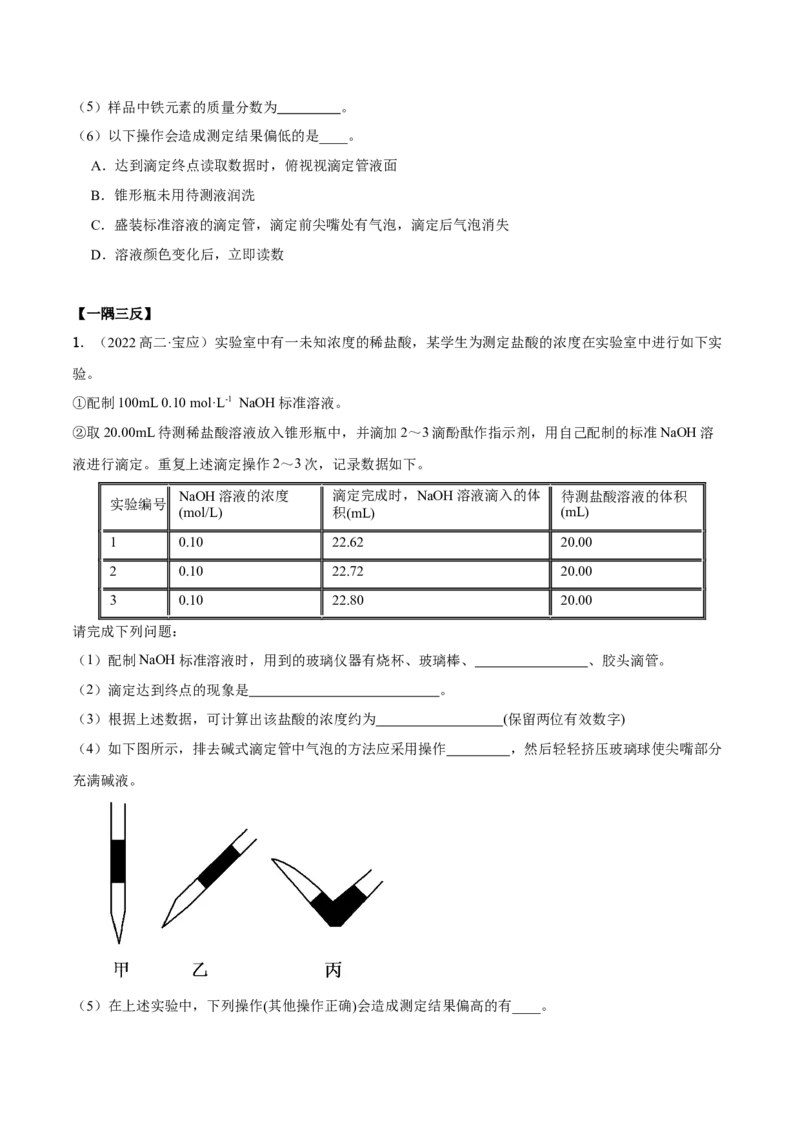
(4)如下图所示,排去碱式滴定管中气泡的方法应采用操作 ,然后轻轻挤压玻璃球使尖嘴部分
充满碱液。
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有____。A.滴定终点读数时俯视读数
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.称量前NaOH固体中混有NaCO 固体
2 3
E.碱式滴定管尖嘴部分有气泡,滴定后消失
F.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
G.配制好的NaOH标准溶液保存不当,部分与空气中的CO 反应生成了NaCO
2 2 3
2.(2022高二·浙江)硫代硫酸钠(Na SO)是中学阶段常见的化学试剂。
2 2 3
(1)I.它在酸性条件下不稳定,可与稀硫酸发生反应: 。现利用该反
应探究外界条件对反应速率的影响。
实验编 0.1mol/L Na SO 溶液体 0.1mol/L H SO 溶液体 水的体 温 出现浑浊所用时
2 2 3 2 4
号 积/mL 积/mL 积/mL 度/℃ 间/s
1 4.0 3.0 1.0 20
2 2.0 3.0 V 20
1
3 V 3.0 3.0 30
2
完成此实验设计,其中:V= ,V=
1 2
(2)对比实验1、2可探究 对反应速率的影响。
(3)II.硫代硫酸钠易与空气中的CO、O 等反应而变质,现有研究性学习小组同学,测定实验室储存的
2 2
NaSO 样品的纯度。方法如下:准确称取10.00g样品,用蒸馏水溶解并定容至250mL,准确移取该溶液
2 2 3
25.00mL于锥形瓶中,加入2滴淀粉溶液,用0.1000mol/L碘的标准溶液滴定。反应原理为
。
滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→ →开始滴定。
a.烘干 b.装入滴定液至零刻度以上 c.调整滴定液液面至零刻度或零刻度以下 d.用洗耳球吹出润洗液
e.排除气泡 f.用滴定液润洗滴定管2至3次 g.记录起始读数
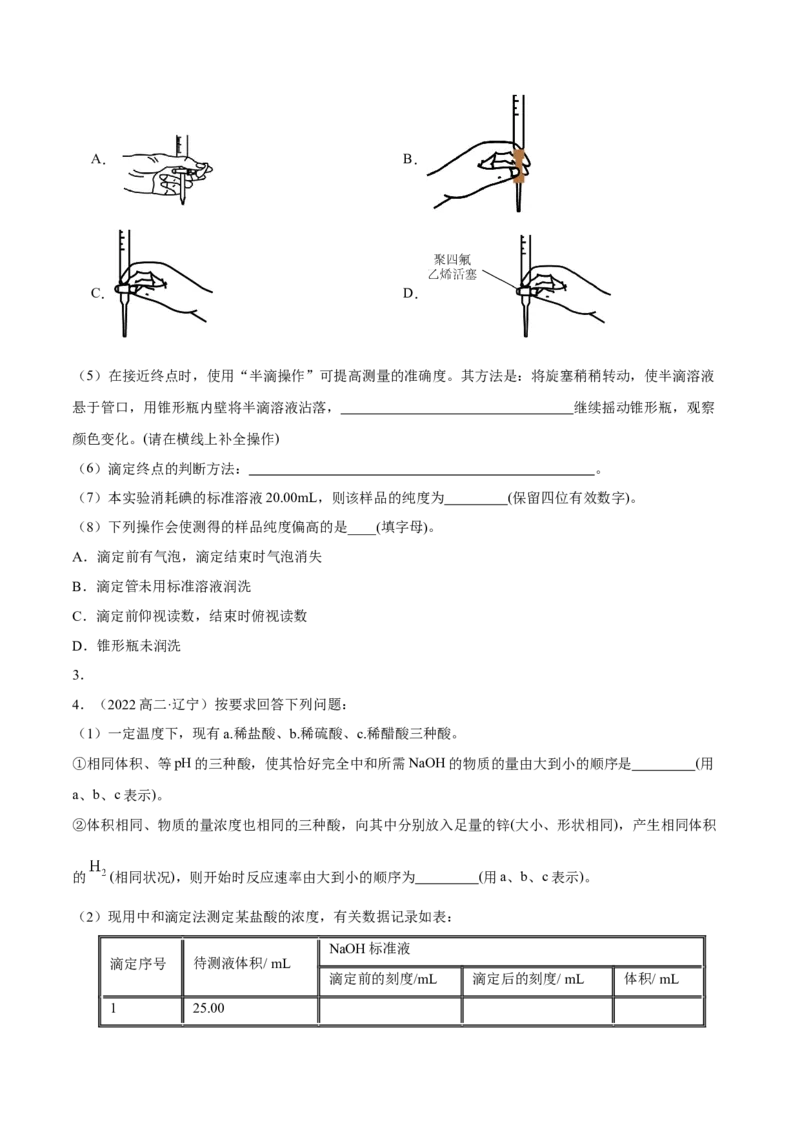
(4)本实验滴定过程中操作滴定管的图示正确的是____(填字母)A. B.
C. D.
(5)在接近终点时,使用“半滴操作”可提高测量的准确度。其方法是:将旋塞稍稍转动,使半滴溶液
悬于管口,用锥形瓶内壁将半滴溶液沾落, 继续摇动锥形瓶,观察
颜色变化。(请在横线上补全操作)
(6)滴定终点的判断方法: 。
(7)本实验消耗碘的标准溶液20.00mL,则该样品的纯度为 (保留四位有效数字)。
(8)下列操作会使测得的样品纯度偏高的是____(填字母)。
A.滴定前有气泡,滴定结束时气泡消失
B.滴定管未用标准溶液润洗
C.滴定前仰视读数,结束时俯视读数
D.锥形瓶未润洗
3.
4.(2022高二·辽宁)按要求回答下列问题:
(1)一定温度下,现有a.稀盐酸、b.稀硫酸、c.稀醋酸三种酸。
①相同体积、等pH的三种酸,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是 (用
a、b、c表示)。
②体积相同、物质的量浓度也相同的三种酸,向其中分别放入足量的锌(大小、形状相同),产生相同体积
的 (相同状况),则开始时反应速率由大到小的顺序为 (用a、b、c表示)。
(2)现用中和滴定法测定某盐酸的浓度,有关数据记录如表:
NaOH标准液
滴定序号 待测液体积/ mL
滴定前的刻度/mL 滴定后的刻度/ mL 体积/ mL
1 25.002 25.00 1.50 31.50 30.00
3 25.00 5.00 31.34 26.34
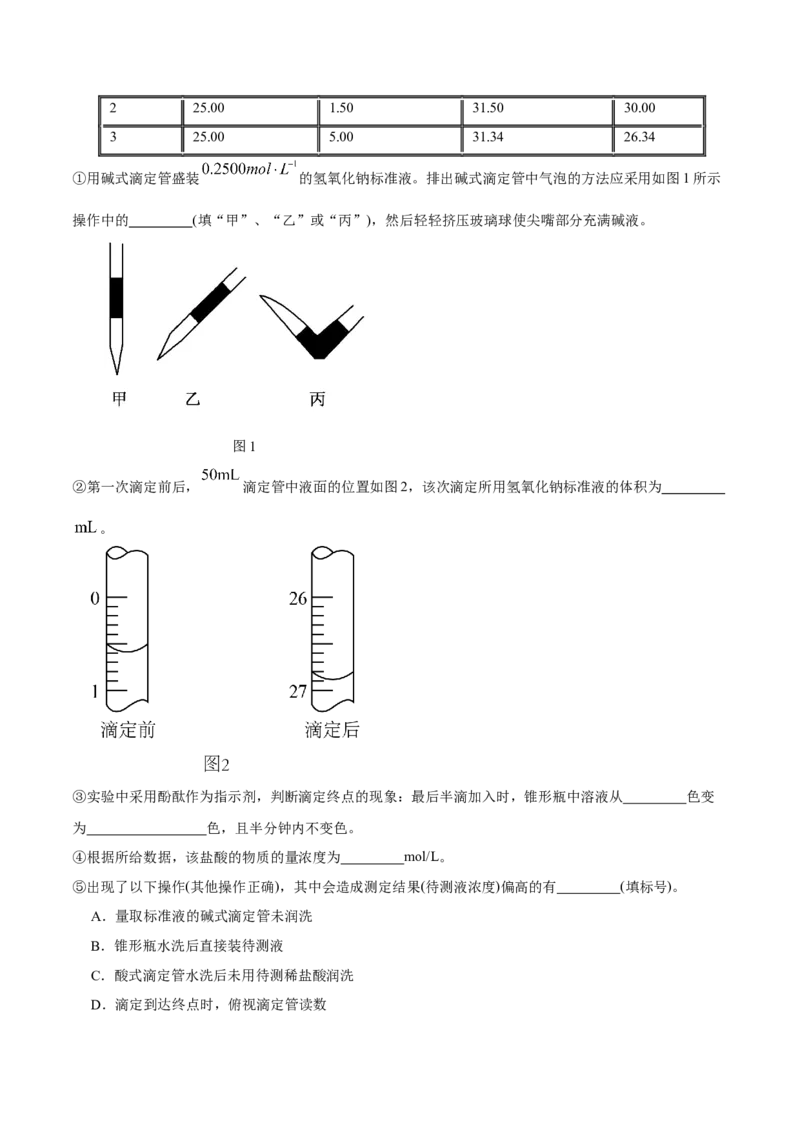
①用碱式滴定管盛装 的氢氧化钠标准液。排出碱式滴定管中气泡的方法应采用如图1所示
操作中的 (填“甲”、“乙”或“丙”),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
图1
②第一次滴定前后, 滴定管中液面的位置如图2,该次滴定所用氢氧化钠标准液的体积为
。
③实验中采用酚酞作为指示剂,判断滴定终点的现象:最后半滴加入时,锥形瓶中溶液从 色变
为 色,且半分钟内不变色。
④根据所给数据,该盐酸的物质的量浓度为 mol/L。
⑤出现了以下操作(其他操作正确),其中会造成测定结果(待测液浓度)偏高的有 (填标号)。
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸润洗
D.滴定到达终点时,俯视滴定管读数E.滴定前碱式滴定管尖嘴部分有气泡,滴定后气泡消失
4.(2022高二·乐山)硫代硫酸钠(Na SO),又名大苏打,在化学实验中应用广泛。实验室进行如下实验
2 2 3
测定某硫代硫酸钠样品的纯度(杂质不参与反应)。
步骤I:准确称取10.00g产品,溶于蒸馏水配成250.00mL溶液。
步骤II:取25.00mL注入锥形瓶,加入指示剂,用0.05mol·L-1标准碘溶液滴定。(已知:2SO +I =S O
2 2 4
(无色)+2I-),回答下列问题:
(1)步骤II中选用的指示剂为 ,滴定终点的现象为 。
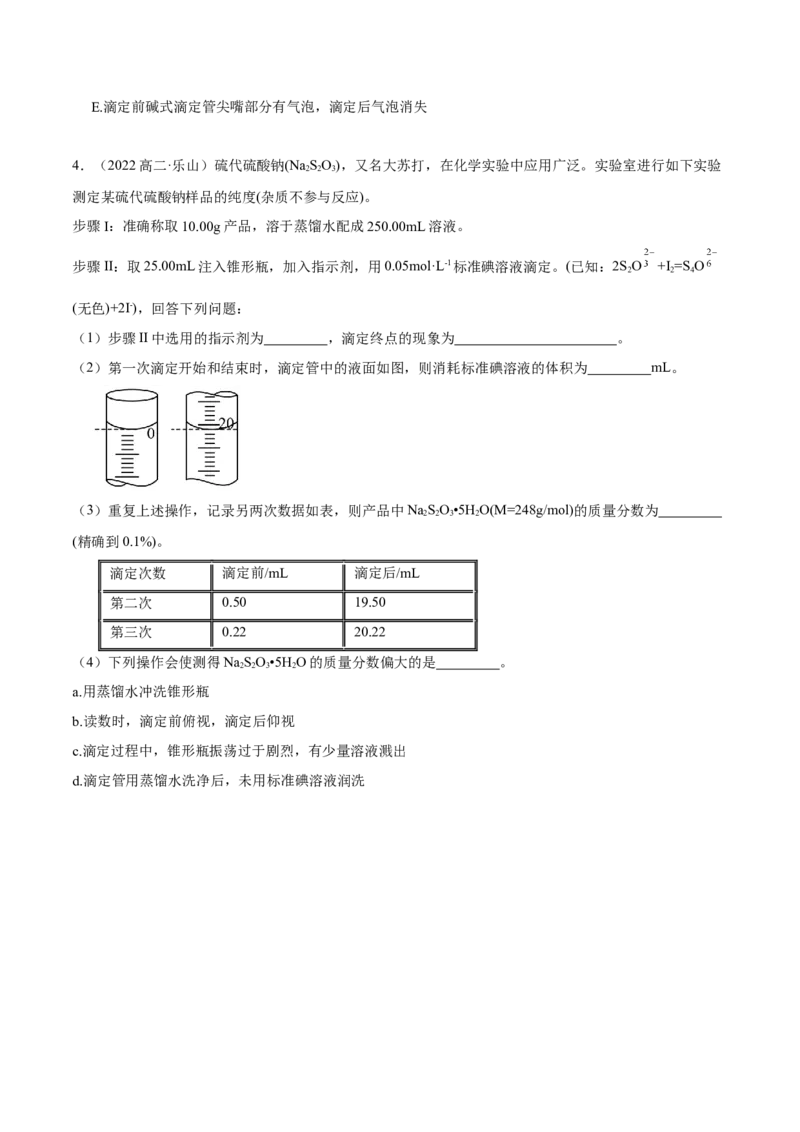
(2)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为 mL。
(3)重复上述操作,记录另两次数据如表,则产品中NaSO•5H O(M=248g/mol)的质量分数为
2 2 3 2
(精确到0.1%)。
滴定次数 滴定前/mL 滴定后/mL
第二次 0.50 19.50
第三次 0.22 20.22
(4)下列操作会使测得NaSO•5H O的质量分数偏大的是 。
2 2 3 2
a.用蒸馏水冲洗锥形瓶
b.读数时,滴定前俯视,滴定后仰视
c.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
d.滴定管用蒸馏水洗净后,未用标准碘溶液润洗倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育