文档内容
实验活动2 强酸与强碱的中和滴定(精练)
1.(2022高二·浙江)下列说法错误的是( )
A.用润湿的pH试纸测稀NaOH溶液的pH,测定值偏小
B.将pH=3的醋酸溶液稀释1000倍得到pH<6醋酸溶液
C.酸碱中和滴定时,若不小心滴过了头,可向锥形瓶内再滴加少量待测液,继续滴定到终点
D.用酸式滴定管量取20.00mL的盐酸溶液,结束时仰视读数,会使所量液体体积偏大
2.(2022广东)下列关于酸碱中和滴定实验的说法正确的是( )
A.用碱式滴定管量取 的 溶液
B.锥形瓶使用前用待测液润洗
C.用标准盐酸滴定某氨水溶液,应选用甲基橙作指示剂
D.用标准盐酸滴定某氨水溶液,滴定终点时俯视读数,导致测定结果偏高
3.(2022高二下·赤峰期末)酸碱中和滴定实验中,下列说法正确的是( )
A.中和滴定操作中所需标准溶液越浓越好,指示剂一般加入
B.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
C.酸碱指示剂的变色点就是反应终点
D.滴定前滴定管中的液体液面处于 处,滴定过程中用去 的液体,此时滴定管中剩余液体
的体积为
4.(2022高二·大庆)室温下,用 0. 100 mol·L-1 NaOH溶液分别滴定 20.00 mL 0.100 mol ·L-1 的盐酸
和醋酸,滴定曲线如图所示。下列说法不正确的是( )
A.pH=7 时,滴定醋酸消耗的 V(NaOH)等于 20.00 mL
B.Ⅱ表示的是滴定盐酸的曲线
C.初始时盐酸的浓度为 0. 10mol/LD.滴定醋酸溶液、盐酸时,均可选择酚酞溶液做指示剂
8.(2021高二·芜湖)下列关于酸碱中和滴定实验的说法错误的是( )
A.指示剂变色点必须在滴定突跃范围内
B.酸碱滴定实验中,用待测溶液润洗锥形瓶以减小实验误差
C.若装标准溶液的滴定管在滴定前尖嘴处有气泡,则测得结果不可靠
D.滴定管用蒸馏水洗净后,不能使用高温烘箱进行快速烘干
9.(2022高二上·深圳期中)
(1)Ⅰ.为测定某盐酸的浓度,用已知浓度的氢氧化钠溶液滴定。 酸式滴定管排气泡的方法是
。
(2)在待测液中滴加几滴酚酞,用氢氧化钠标准溶液滴定,直至 ,即为滴定终点。
(3)下列操作造成滴定结果偏高的是 (填字母)。
a.滴定过程中向锥形瓶中加入少量蒸馏水
b.其他操作均符合题意,滴定终点读数时俯视滴定管的刻度
c.未用用氢氧化钠标准溶液润洗碱式滴定管
d.滴定终点读数时发现滴定管尖嘴处悬挂一滴液体
e.未用待测盐酸润洗酸式滴定管
f.滴定前无气泡,滴定后尖嘴部分有气泡
(4) 常用于氧化还原滴定。滴定时应将 加入 滴定管中(填“酸式”或“碱
式”);在规格为25mL的滴定管中,若 溶液起始读数是5mL,此时滴定管中 的实际体
积为 (填标号)。
A.1.5mL B.20mL C.大于20mL D.小于20mL
(5)Ⅱ.某实验小组用0.55mol/L的NaOH溶液和0.25mol/L的 溶液进行中和热的测定。取
50mLNaOH溶液和50mL 溶液在 中(填仪器名称)进行实验。数据如下:起始温度 /℃
实验次数 终止温度 /℃
NaOH 平均值
1 25.2 25.0 25.1 28.5
2 26.2 26.4 26.3 32.5
3 25.3 25.3 25.3 28.8
4 26.1 26.5 26.3 29.6
近似认为50mL 0.55mol/L NaOH溶液和50mL0.25mol/L的 溶液的密度都是1g/mL,中和后生成溶液
的比热容 ,则测得中和热 kJ/mol(精确到小数点后一位)。
10.(2022高二上·嘉兴期中)某学生用 0.1000mol/L KOH 溶液滴定未知浓度的盐酸溶液,其操作可分解
为如下几步:
①移取 25.00mL 待测的盐酸溶液注入洁净的锥形瓶,并加入 2-3 滴酚酞
②用标准溶液润洗滴定管 2-3 次
③把盛有标准溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液
④取标准 KOH 溶液注入 至 0 刻度以上 2-3cm
⑤调节液面至 0 或 0 刻度以下,记下读数
⑥把锥形瓶放在滴定管的下面,用标准 KOH 溶液滴定至终点,记下滴定管液面的刻度
(1)正确操作的顺序是(用序号填写) .
(2)步骤④中的滴定管是: (填“酸式滴定管”或“碱式滴定管”)。
(3)当步骤⑥待测液由 色变为 色,且半分钟内不变化即达到终点,KOH
溶液开始时读数及恰好反应时的读数见表。
实验编号 待测盐酸溶液体积(mL) 滴定开始读数(mL) 滴定结束读数(mL)
① 25.00 0.00 19.95
② 25.00 1.10 18.30
③ 25.00 0.20 20.25
请计算待测的盐酸的物质的量浓度 mol/l(小数点后面保留 4 位数字 )。
(4)由于操作失误,使得上述所测盐酸溶液的浓度偏高的是 _。
A.滴定达到终点时,俯视滴定管内液面读数
B.碱式滴定管用蒸馏水洗净后立即取用氢氧化钾溶液进行滴定C.锥形瓶用蒸馏水洗净后未干燥就装入盐酸待测液
D.滴定时碱式滴定管中氢氧化钾溶液洒落在锥形瓶外
11.(2020二上·宜春期末)(1)Ⅰ某学生用已知物质的量浓度的硫酸来测定未知物质的量浓度的
溶液时,选择酚酞作指示剂。回答下列问题:
用标准的硫酸滴定待测的 溶液时,终点现象是: 。
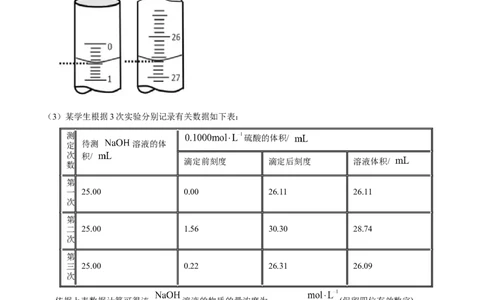
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用硫酸溶液的体积为 。
(3)某学生根据3次实验分别记录有关数据如下表:
测
硫酸的体积/
定 待测 溶液的体
次 积/
滴定前刻度 滴定后刻度 溶液体积/
数
第
一 25.00 0.00 26.11 26.11
次
第
二 25.00 1.56 30.30 28.74
次
第
三 25.00 0.22 26.31 26.09
次
依据上表数据计算可得该 溶液的物质的量浓度为 (保留四位有效数字)。
(4)下列操作中可能使所测 溶液的浓度数值偏低的是____(填字母)。A.酸式滴定管未用标准硫
酸润洗就直接注入标准硫酸
A.读取硫酸体积时,开始仰视读数,滴定结束时俯视读数
B.酸式滴定管在滴定前有气泡,滴定后气泡消失
C.锥形瓶用水洗涤后,用待测液润洗(5)酸碱中和滴定原理也可用于其它类型的滴定。如:一种测定水样中 的浓度的实验步骤如下:
第1步:向锥形瓶中加入处理后的水样25.00 ,加入几滴 溶液作为指示剂。
第2步:加入 溶液(过量),充分摇匀。
第3步:用 标准溶液进行滴定,至终点时消耗标准溶液 。
计算该水样中 的物质的量浓度为 (已知:
, , )。
(6)Ⅱ、某实验小组用 溶液和0.50 硫酸溶液进行中和热的测定取
溶液和30 硫酸溶液进行实验,测得起止温度差的平均值为4.0℃。近似认为
溶液和0.50 硫酸溶液的密度都是1 ,中和后生成溶液的比热容
。则计算得中和热 (取小数点后一位)。
(7)上述实验结果与-57.3 有偏差,产生偏差的原因可能是 (填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取 溶液的体积时仰视刻度线读数
c.分多次把 溶液倒入盛有硫酸的小烧杯中
d.用温度计测定 溶液起始温度后直接测定 溶液的温度
12.(2022高二东城)CHCOONa溶液是常见的强碱弱酸盐,可由醋酸和NaOH溶液反应得到。
3
(1)CHCOONa水溶液呈 (填“酸”或“碱”)性。
3
(2)CHCOONa在溶液中发生水解反应的离子方程式是 。
3
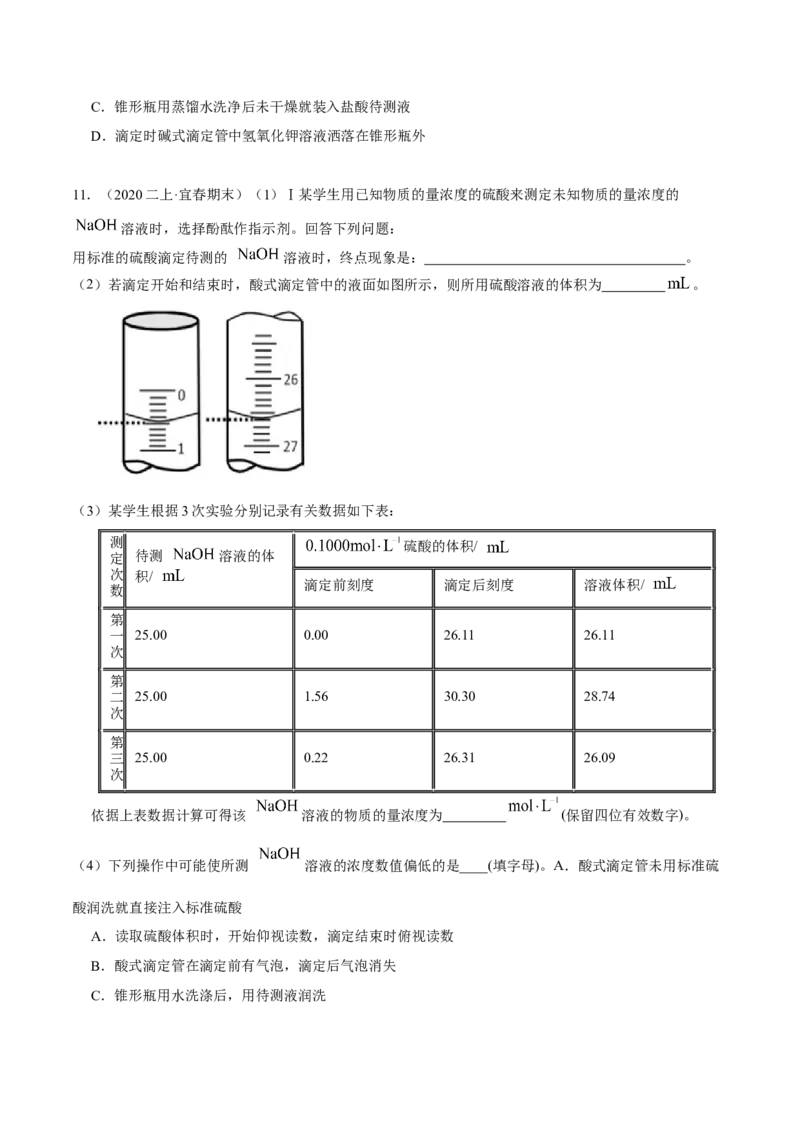
(3)用0.1000 mol/L NaOH分别滴定25.00mL 0.1000 mol/L盐酸和25.00 mL 0.1000mol/L醋酸,滴定过程中pH变化曲线如下图所示。
①在上述滴定过程中,不需要使用的玻璃仪器 (填序号)。
A.容量瓶 B.碱式滴定管 C.锥形瓶 D.胶头滴管
②由图中数据可判断滴定盐酸的pH变化曲线如图,判断的理由如下(答出2点):
i.起始未滴加NaOH溶液时, 。
ii. 。
③滴定CHCOOH溶液的过程中,当滴加12.50mL NaOH溶液时,溶液中各离子浓度由大到小的顺序是
3
(用符号“c”及“>”表示)。
(4)向0.1 mol/ L CH COONa溶液中逐滴加入0.1mol/L盐酸至恰好反应。反应过程中,你认为
3
CHCOONa的水解平衡向 (填“左”或“右”)移动,分析的过程:当滴入稀盐酸后,
3
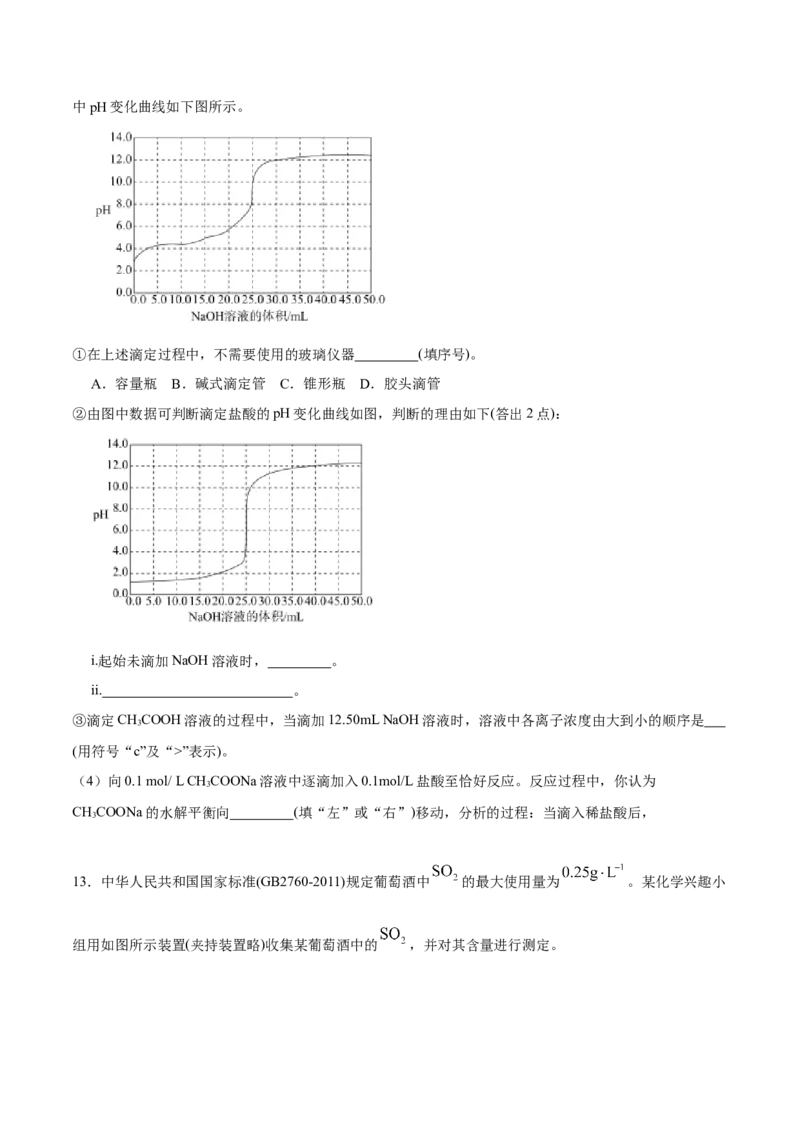
13.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中 的最大使用量为 。某化学兴趣小
组用如图所示装置(夹持装置略)收集某葡萄酒中的 ,并对其含量进行测定。(1)B中加入300.00mL葡萄酒和适量硫酸,加热使 全部逸出并与C中 完全反应,C中发生
反应的化学方程式为 。
(2)除去C中过量的 后,用 标准溶液进行滴定,该标准液应置于
(填“酸式”或“碱式”)滴定管中,若用容量为50mL的滴定管进行实验,当滴定管中的凹液面最低处在
刻度“15”处时,则管内液体的体积 (填标号)。
A.=15mL B.=35mL C.<15mL D.>35mL
(3)该兴趣小组选择用酚酞作指示剂,达到滴定终点的标志为 。
(4)①滴定开始和结束时,滴定管中液面如图所示,则起始读数为 mL,终点读数为
mL,所用NaOH溶液的体积为 mL。
②根据消耗的NaOH溶液的量,计算该葡萄酒中 含量为 。
(5)下列操作可能使测定的葡萄酒中 含量偏低的是___________(填标号)。
A.滴定管未用标准液润洗就直接注入NaOH标准溶液
B.滴定管在滴定前无气泡,滴定后尖嘴处有气泡
C.滴定结束后,滴定管尖嘴处悬挂一滴液滴
D.读取NaOH溶液体积时,滴定前读数符合题意,滴定后俯视读数14.(2022高二上·联合期中)高锰酸钾是一种重要的化学试剂,利用高锰酸钾完成以下两个实验:
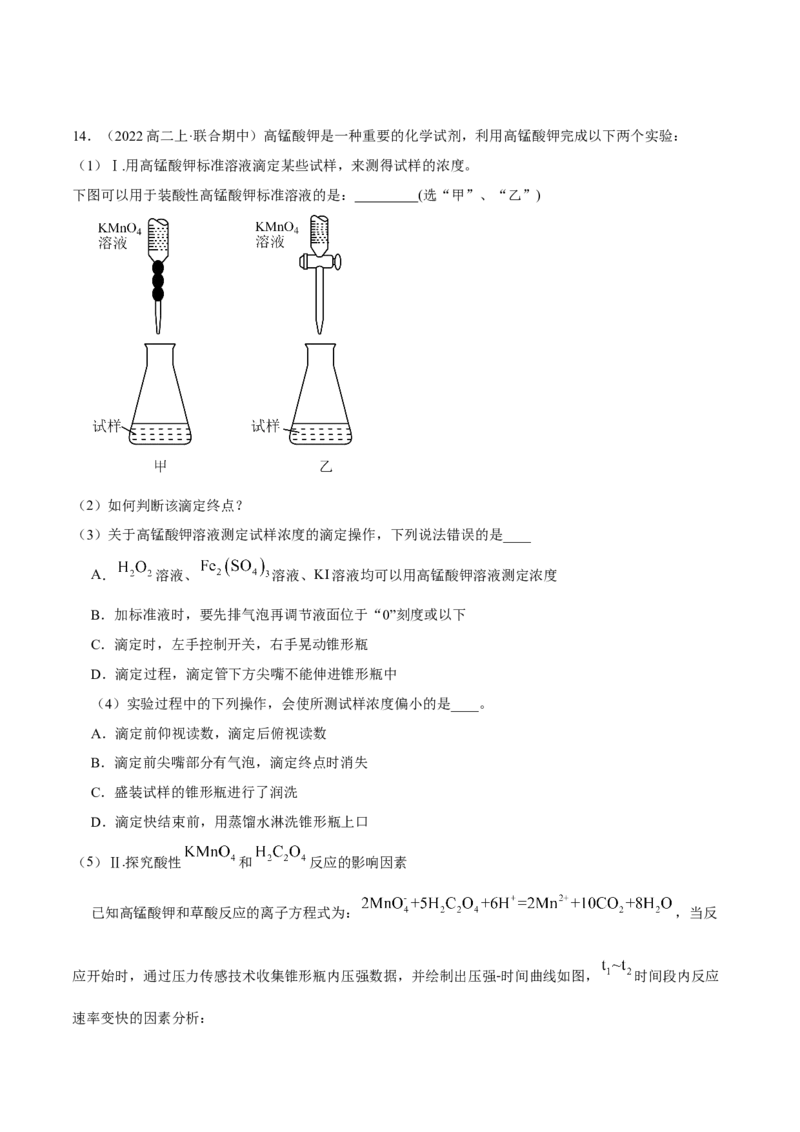
(1)Ⅰ.用高锰酸钾标准溶液滴定某些试样,来测得试样的浓度。
下图可以用于装酸性高锰酸钾标准溶液的是: (选“甲”、“乙”)
(2)如何判断该滴定终点?
(3)关于高锰酸钾溶液测定试样浓度的滴定操作,下列说法错误的是____
A. 溶液、 溶液、KI溶液均可以用高锰酸钾溶液测定浓度
B.加标准液时,要先排气泡再调节液面位于“0”刻度或以下
C.滴定时,左手控制开关,右手晃动锥形瓶
D.滴定过程,滴定管下方尖嘴不能伸进锥形瓶中
(4)实验过程中的下列操作,会使所测试样浓度偏小的是____。
A.滴定前仰视读数,滴定后俯视读数
B.滴定前尖嘴部分有气泡,滴定终点时消失
C.盛装试样的锥形瓶进行了润洗
D.滴定快结束前,用蒸馏水淋洗锥形瓶上口
(5)Ⅱ.探究酸性 和 反应的影响因素
已知高锰酸钾和草酸反应的离子方程式为: ,当反
应开始时,通过压力传感技术收集锥形瓶内压强数据,并绘制出压强-时间曲线如图, 时间段内反应
速率变快的因素分析:甲同学:该反应放热,体系温度升高,成为主导影响因素
乙同学:根据自己的解析设计以下实验方案进行验证:
试管中所加试剂及其用量/L
实
实验 再向试管中 溶液褪至
验
温度/ 加入某种固 无色所需
编
稀 体 时间/min
号 溶液 溶液
溶液
① 25 2.0 3.0 2.0 3.0 无
② 25 2.0 3.0 2.0 3.0
根据实验设计,你推测乙同学认为反应加快的因素是什么? 。
(6)若观察到 ,则乙同学分析的影响因素是合理的。
15.(2022高二上·通州期中)碳酸氢钠属于抗酸药,用于碱化尿液及酸血症,也可用于胃酸过多,在潮
湿空气中缓缓分解。某化学小组用如下方法对某品牌碳酸氢钠片中的含量进行了探究(可能含有少量
NaCO,药品中不含干扰测定的物质)。
2 3
【鉴别】
a.取铂丝,用盐酸湿润后,蘸取药品粉末,在无色火焰中燃烧,火焰显黄色。
b.向本品水溶液中加盐酸产生泡沸现象。
【检查】配置药品质量分数为0.8%的水溶液,测pH为8.3。
【含量测定】小组采用滴定法进行含量测定:
I.用已准确称量的药品固体ag配制一定体积的溶液VmL。(此时主要溶质为NaHCO 和少量NaCO)
3 2 3
II.取VmL上述溶液于锥形瓶中,加入酚酞指示剂2—3滴。
1
III.用1mol/L盐酸标准溶液滴定II中溶液至第一终点时,消耗盐酸溶液VmL。 (此时溶质为NaCl和
2
NaHCO )
3IV.再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,又消耗盐酸溶液VmL。
3
已知:HCO 的电离平衡常数 ;
2 3
常用的酸碱指示剂及其变色范围如下:
酚酞:pH<8.2无色、8.210红色
甲基橙:pH<3.1红色、3.14.4黄色
(1)请写出“鉴别”中产生泡沸现象主要反应的离子反应方程式: 。
(2)请结合化学用语解释“检查”中水溶液pH为8.3的主要原因(不考虑杂质影响):
(3)“含量测定”的步骤I中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
(4)滴定过程中应选择如图所示滴定管 (填字母)。
(5)步骤V中第二步滴定用甲基橙滴定至终点的现象是由 色变为橙色。
(6)药品中碳酸氢钠的质量分数为 。(碳酸氢钠摩尔质量: )倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育