文档内容
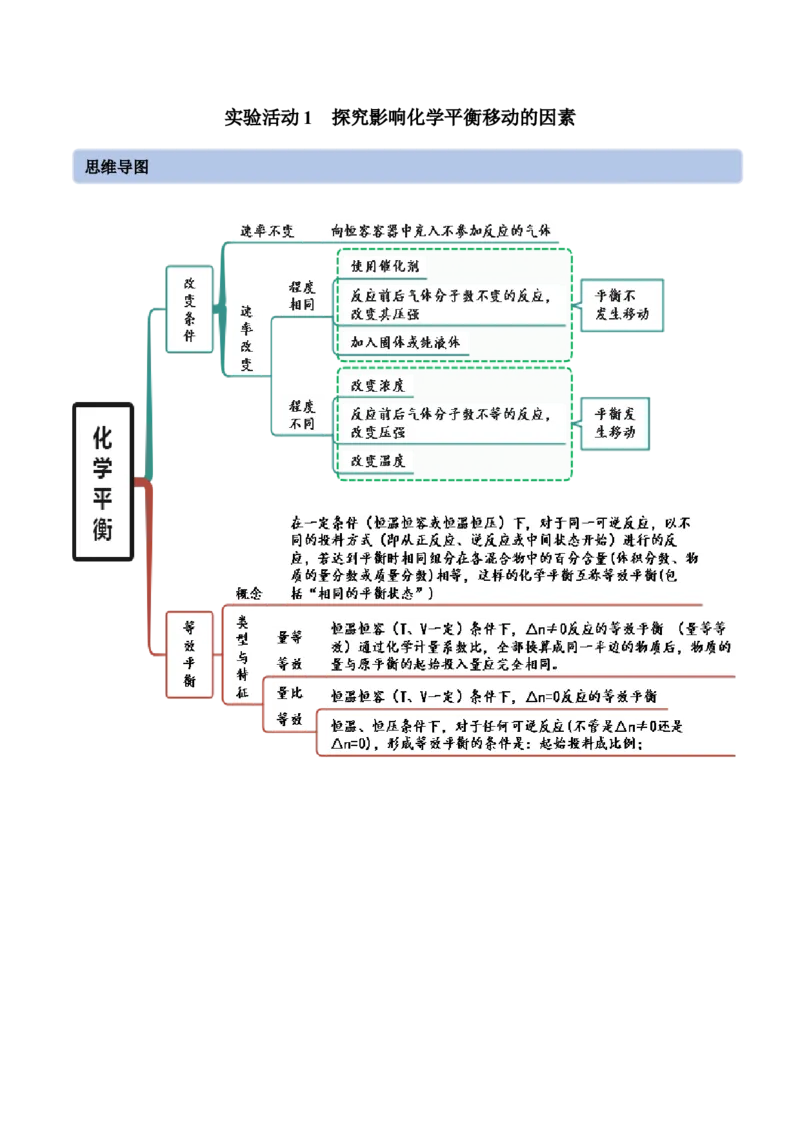
实验活动1 探究影响化学平衡移动的因素
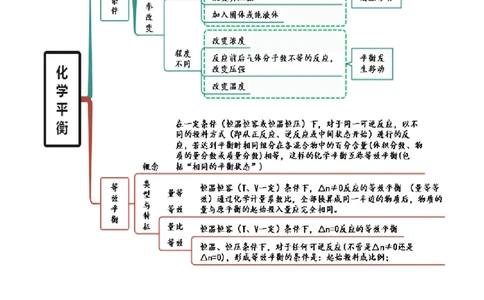
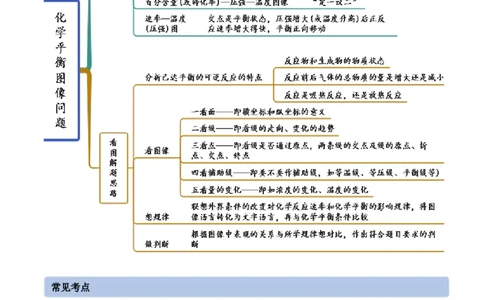
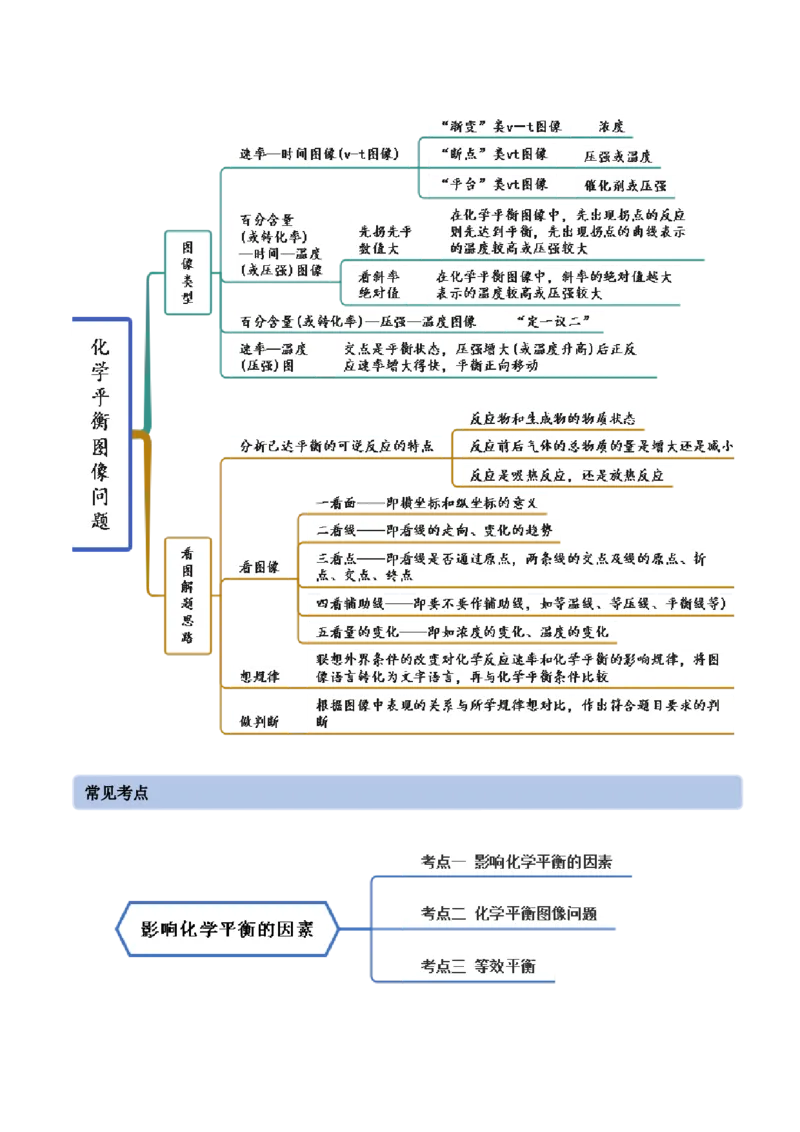
思维导图常见考点考点一 影响化学平衡的因素
【例1】(2022·云南保山·高二期中)反应X(g)+Y(g) 3Z(g) H<0,达到平衡时,下列说法正确的是
A.减小容器体积,平衡向右移动 B.恒容⇌时充入H△e气,Z的产率增大
C.增大c(X),X的转化率增大 D.降低温度,Y的转化率增大
【一隅三反】
1.(2022·广东潮州·高二期末)无水氯化铝是一种重要的催化剂,工业上由Al O 制备无水氯化铝的反应
2 3
为:2Al O(s)+6Cl (g) 4AlCl (g)+3O(g) ΔH>0。下列分析正确的是
2 3 2 3 2
A.增大Al O 用量,化学平衡不移动
2 3
B.电解熔融的Al O 和AlCl 均能得到单质铝
2 3 3
C.增大压强(即压缩气体),化学平衡向正反应方向移动
D.其他条件不变时,升高温度,正反应速率加快,逆反应速率减慢
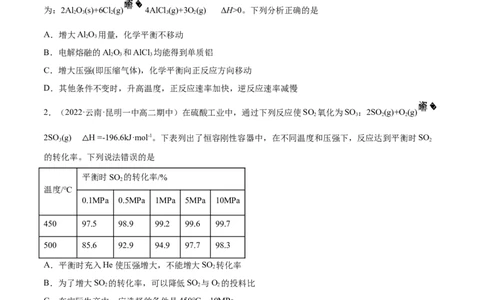
2.(2022·云南·昆明一中高二期中)在硫酸工业中,通过下列反应使SO 氧化为SO :2SO (g)+O(g)
2 3 2 2
2SO (g) H =-196.6kJ·mol-1。下表列出了恒容刚性容器中,在不同温度和压强下,反应达到平衡时SO
3 2
的转化率。△下列说法错误的是
平衡时SO 的转化率/%
2
温度/℃
0.1MPa 0.5MPa 1MPa 5MPa 10MPa
450 97.5 98.9 99.2 99.6 99.7
500 85.6 92.9 94.9 97.7 98.3
A.平衡时充入He使压强增大,不能增大SO 转化率
2
B.为了增大SO 的转化率,可以降低SO 与O 的投料比
2 2 2
C.在实际生产中,应选择的条件是450℃,10MPa
D.在实际生产中,选定的温度为400~500℃,主要原因是考虑催化剂的活性最佳
3.(2021·贵州·高二学业考试)在密闭容器中发生反应:C(s)+HO(g) CO(g)+H(g) H>0,达到
2 2
△
平衡后,其他条件不变时,下列措施能使平衡向逆反应方向移动的是
A.减小压强 B.降低温度 C.移走CO D.加入催化剂考点二 化学平衡的图像问题
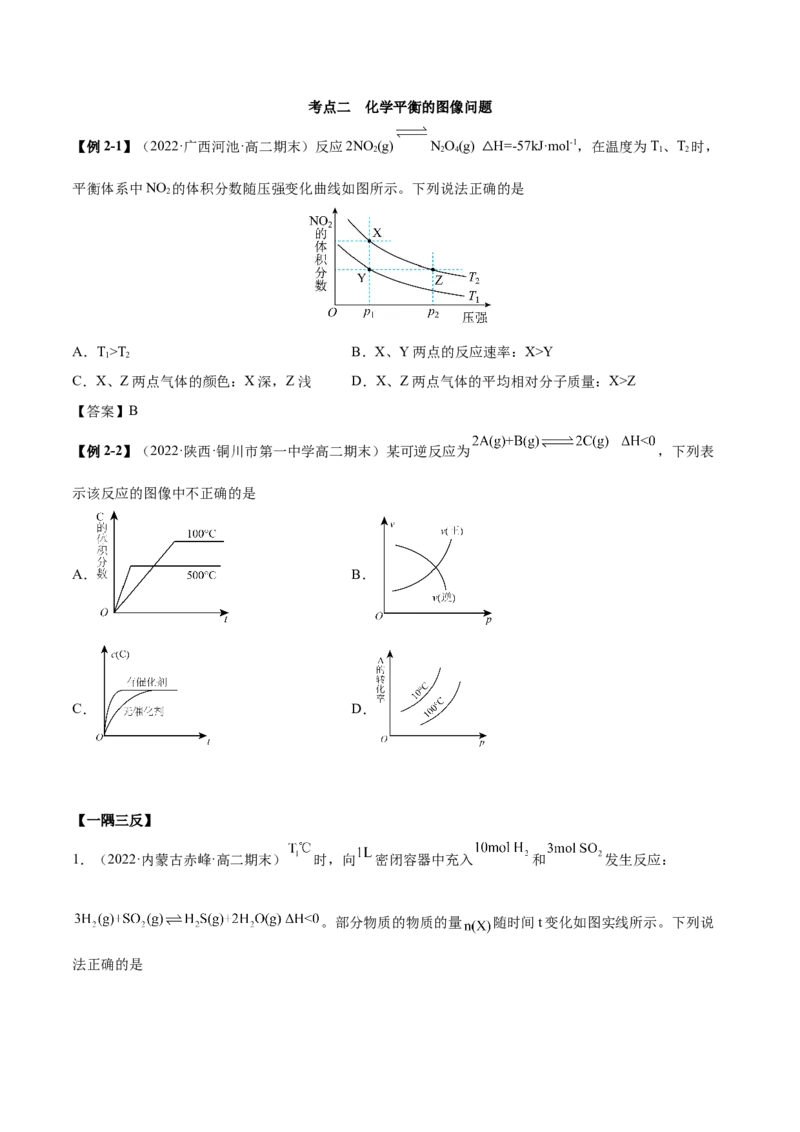
【例2-1】(2022·广西河池·高二期末)反应2NO (g) NO(g) H=-57kJ·mol-1,在温度为T、T 时,
2 2 4 1 2
△
平衡体系中NO 的体积分数随压强变化曲线如图所示。下列说法正确的是
2
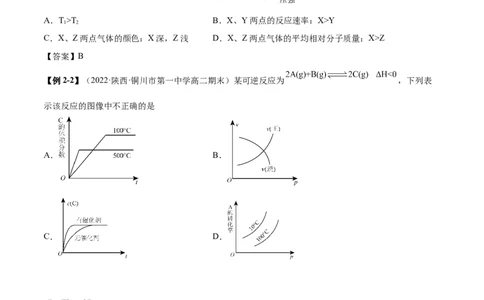
A.T>T B.X、Y两点的反应速率:X>Y
1 2
C.X、Z两点气体的颜色:X深,Z浅 D.X、Z两点气体的平均相对分子质量:X>Z
【答案】B
【例2-2】(2022·陕西·铜川市第一中学高二期末)某可逆反应为 ,下列表
示该反应的图像中不正确的是
A. B.
C. D.
【一隅三反】
1.(2022·内蒙古赤峰·高二期末) 时,向 密闭容器中充入 和 发生反应:
。部分物质的物质的量 随时间t变化如图实线所示。下列说
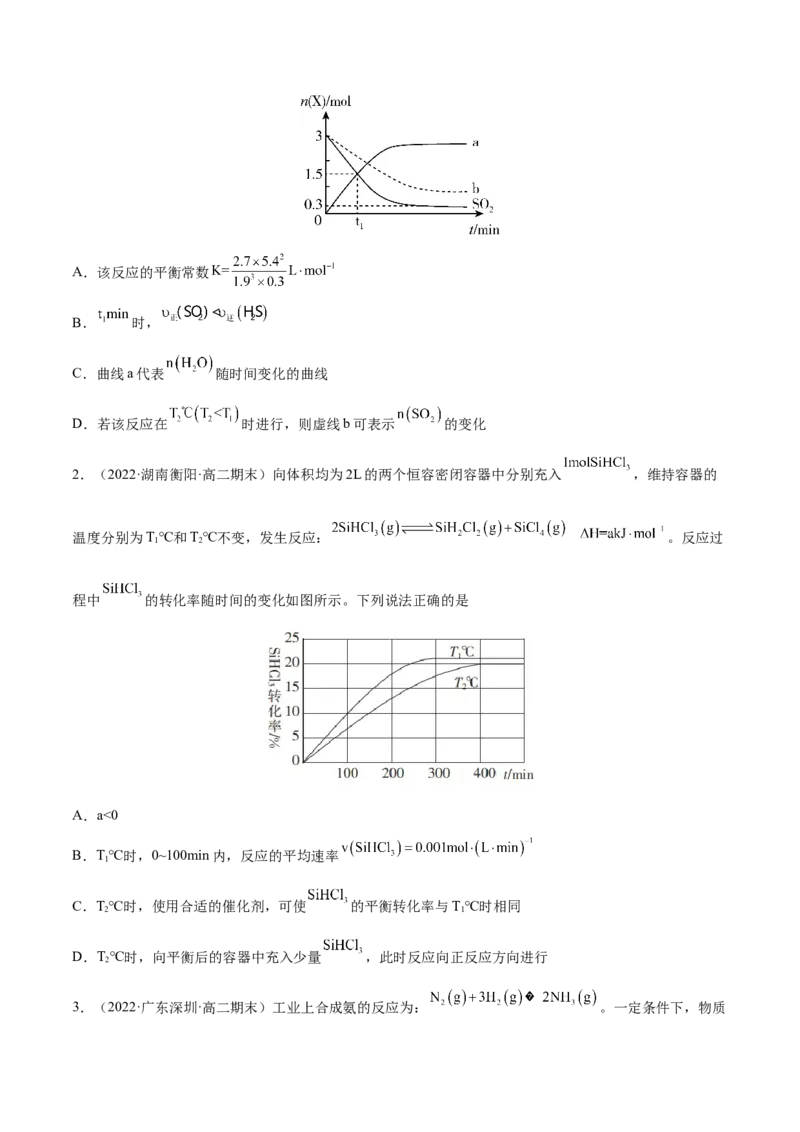
法正确的是A.该反应的平衡常数
B. 时,
C.曲线a代表 随时间变化的曲线
D.若该反应在 时进行,则虚线b可表示 的变化
2.(2022·湖南衡阳·高二期末)向体积均为2L的两个恒容密闭容器中分别充入 ,维持容器的
温度分别为T℃和T℃不变,发生反应: 。反应过
1 2
程中 的转化率随时间的变化如图所示。下列说法正确的是
A.a<0
B.T℃时,0~100min内,反应的平均速率
1
C.T℃时,使用合适的催化剂,可使 的平衡转化率与T℃时相同
2 1
D.T℃时,向平衡后的容器中充入少量 ,此时反应向正反应方向进行
2
3.(2022·广东深圳·高二期末)工业上合成氨的反应为: 。一定条件下,物质的量之比为1:3的 和 在恒容密闭容器中反应,下图曲线a表示该反应在温度T下 的浓度c
随时间t的变化,曲线b表示该反应在某一起始反应条件改变时 的浓度c随时间t的变化。下列叙述不
正确的是
A.温度T下,在 时间内,
B.温度T下,该反应的平衡常数
C.M点的 大于N点的
D.曲线b先达到平衡,表明反应速率比较快,可能是使用了更高效的催化剂
4.(2022·全国·高二)在容积可变的密闭容器中存在如下反应:CO(g)+HO(g) CO(g)+H(g) H<0,下
2 2 2
列对图像的分析中正确的是 ⇌ △
A.图I研究的是t 时增大压强对反应速率的影响
0
B.图II研究的一定是t 时使用了催化剂对反应速率的影响
0
C.图III研究的是温度对化学平衡的影响,且甲的温度较高
D.图IV研究的可能是压强对化学平衡的影响,且a的压强较高
5.(2022·广西·桂林市临桂区五通中学高二期中)反应2A(g)+B(g) 2C(g); H<0,下列图象正确的
△
是A. B.
C. D.
考点三 等效平衡
【例3-1】(2022·河北·石家庄二中高一期末)三个恒容密闭容器中(容积均相等)按不同方式投料,发生反
应N(g)+3H(g)=2NH (g) H<0,相关数据如下,下列说法正确的是
2 2 3
△容器1 容器2 容器3
反应温度T/K 770 770 800
反应物投入量 1molN 、3molH 4molNH 1molN 、3molH
2 2 3 2 2
平衡v (H ) mol/(L·min) v v v
正 2 1 2 3
平衡c(NH ) mol/L c c c
3 1 2 3
平衡转化率α α (N ) α (NH ) α (N )
1 2 2 3 3 2
A.v>v B.c<2c C.c>2c D.α +α >1
1 3 2 1 2 3 1 2
【例3-2】如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和
1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g) 2C(g),反应达到平衡后,恢复
到反应发生前时的温度。下列有关说法不正确的是A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
B.达到平衡后,隔板K最终停留在左侧刻度0~2之间
C.到达平衡时,甲容器中C的物质的量等于乙容器中C的物质的量
D.若平衡时K停留在左侧1处,则活塞仍停留在6刻度右侧
【一隅三反】
1.(2022·黑龙江·哈尔滨市第六中学校高二期末)在恒温恒压下,向密闭容器中充入4molSO 和2molO ,
2 2
发生如下反应:2SO (g)+O(g) 2SO (g) H<0。2min后,反应达到平衡,生成SO 为1.4mol,同时
2 2 3 3
△
放出热量QkJ。则下列分析正确的是
A.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ
B. 后,向容器中再通入一定量的SO 气体,重新达到平衡时,SO 的含量降低
3 2
C.若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO )大于1.4mol
3
D.若反应开始时容器体积为2L,则v(SO )=0.7mol·L-1·min-1
3
2.(2022·甘肃·玉门市教育局教育研究室高二期中)某密闭容器中充入1molN 、3molH ,在温度恒定时
2 2
达平衡,测得NH 为0.6mol。若该容器起始时充入2molN 、6molH ,同温下达到平衡,对容器内NH 物质
3 2 2 3
的量的说法正确的是
A.若为恒容容器,n(NH )<1.2mol B.若为恒压容器,n(NH )=0.6mol
3 3
C.若为恒容容器,n(NH )=1.2mol D.若为恒压容器,n(NH )=1.2mol
3 3
3.(2021·新疆师范大学附属中学高二阶段练习)在温度均为T℃的密闭容器中发生反应:2SO (g)+O(g)
2 2
2SO (g) ΔH<0。下列说法正确的是
3
起始物质的量/mol
达平衡时SO
容器编 3
容器类型 初始体积 达平衡需要的时间/min
号
物质的量/mol
SO O SO
2 2 3
Ⅰ 恒温恒容 1.0L 2 1 0 1.6 5
Ⅱ 恒温恒压 1.0L 2 1 0 a t
A.a<1.6,t<5
B.选择不同的催化剂,该反应的反应速率和平衡转化率都将不同
C.反应达到平衡时,装置Ⅱ中SO 平均反应速率v>0.32mol·L-1·min-1
2
D.若起始时向容器Ⅰ中充入1molSO 、0.5molO,达平衡时SO 物质的量大于0.8mol
2 2 34.(2022·山西·朔州市朔城区第一中学校高二开学考试)相同温度下,在体积相等的三个恒容密闭容器中
发生可逆反应: ,实验测得起始,平衡时的有关数据如下表,
下列叙述正确的是
起始各物质的物质的量/
平衡时反应中的能量变化
容器编号
① 2 1 0 放出热量
② 2 2 0 放出热量
③ 4 2 0 放出热量
A. 的转化率②>①>③
B.三个容器内反应的平衡常数③>①>②
C.达到平衡时 的体积分数①>③
D.放出热量大小关系:倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育