实验活动1 探究影响化学平衡移动的因素
题组一 影响化学平衡的因素
1.(2022·广西河池·高二阶段练习)一定温度下发生反应:H(g)+I (g) 2HI(g)ΔH<0。达到平衡后,改
2 2
变下列条件,可以使混合气体颜色加深的是
A.恒温恒容充入氦气 B.恒温恒压充入氦气
C.降低温度 D.缩小容器的容积
【答案】D
【解析】A.恒温恒容充入不参加反应的氦气,平衡体系中各物质的浓度不变,化学平衡不移动,混合气
体颜色不变,故A错误;
B.恒温恒压充入氦气,容器体积增大,I(g)的浓度减小,颜色变浅,故B错误;
2
C.该反应是放热反应,降低温度,平衡向正反应方向移动,碘蒸气的浓度减小,混合气体颜色变浅,故
C错误;
D.该反应是气体体积不变的反应,缩小容器的容积,气体压强增大,化学平衡不移动,碘蒸气的浓度增
大,混合气体颜色加深,故D正确;
故选D。
2.(2022·河北武强中学高二期中)2NO(g)+O (g) 2NO (g)体系中能使该反应的反应速率增大,且平衡向
2 2
正反应方向移动的是 ⇌
A.及时分离出NO 气体 B.扩大容器体积
2
C.增大O 的浓度 D.选择高效催化剂
2
【答案】C
【解析】A.及时分离出NO 气体,平衡向生成二氧化氮的方向移动,正向移动;但是反应物浓度减小,
2
反应速率减小,A错误;
B.反应为气体分子数减小的反应,扩大容器体积,平衡逆向移动,且物质的浓度均减小,反应速率减慢,
B错误;
C.增大O 的浓度,平衡正向移动,反应物浓度变大,反应速率变大,C正确;
2
D.选择高效催化剂可加快反应速率,但不改变平衡移动,D错误;
故选C。
3.(2022·广西·宾阳中学高二期末)已知2NO (g) NO(g),用如图针筒装入一定量的NO 和NO 并进行
2 2 4 2 2 4
如下实验。下列说法正确的是 ⇌A.初态到末态颜色变浅,平衡正向移动
B.平均摩尔质量:末态大于初态
C.c(NO ):初态比末态2倍稍大
2
D.初态到末态n(N O)减小
2 4
【答案】D
【解析】A.初态到末态体积增大,压强减小,平衡逆向移动,但体积增大引起的浓度变小,颜色变浅,
故A错误;
B.初态到末态体积增大,压强减小,平衡逆向移动,气体总质量不变,但总物质的量增大,平均摩尔质
量,末态小于初态,故B错误;
C.初态到末态体积增大2倍,若平衡不移动,则末态c( NO )是初态的一半,但压强减小,平衡逆向移动,
2
故c( NO),初态比末态2倍略小,故C错误;
2
D.初态到末态体积增大,压强减小,平衡逆向移动,初态到末态n(N O )减小,故D正确;
2 4
故选:D。
4.(2021·辽宁·沈阳市第一二〇中学高二开学考试)下列叙述及解释正确的是
A.2NO (红棕色) NO(无色) H<0,在达到平衡后,对平衡体系采取缩小容积、增大压强的措施,
2 2 4
△
因为平衡向正反应方向移动,故体系颜色变浅
B.H(g)+I (g) 2HI(g) H<0,在达到平衡后,对平衡体系采取增大容积、减小压强的措施,因为
2 2
△
平衡不移动,故体系颜色不变
C.N(g)+3H(g) 2NH (g),在达到平衡后,保持压强不变,充入He,平衡向左移动
2 2 3
D.2C(s)+O(g) 2CO(g)在达到平衡后,加入碳,平衡向正反应方向移动
2
【答案】C
【解析】A.2NO (红棕色) NO(无色) H<0,在达到平衡后,对平衡体系采取缩小容积、增大压
2 2 4
△
强的措施,虽平衡向正反应方向移动,但NO 的浓度比缩小体积前大,体系颜色加深,故A错误;
2
B.H(g)+I (g) 2HI(g) H<0,在达到平衡后,对平衡体系采取增大容积、减小压强的措施,平衡
2 2
△不移动,I(g)的浓度增大,体系颜色加深,故B错误;
2
C.N(g)+3H(g) 2NH (g),在达到平衡后,保持压强不变,充入He,容器体积变大,相当于减压,平
2 2 3
衡向左移动,故C正确;
D.碳是固体,2C(s)+O(g) 2CO(g)在达到平衡后,加入碳,平衡不移动,故D错误;
2
选C。
5.(2022·湖北·高二期中)实验表明,反应NO +CO NO+CO 的速率与浓度关系为v=kc(NO ),其
2 2 2
中k为速率常数,恒温时k是定值。下列说法正确的是
A.增大c(CO),反应速率明显加快
B.恒压时,充入稀有气体该反应速率减慢
C.升高温度化学平衡常数不变
D.将产物从体系中分离出去平衡逆向移动
【答案】B
【解析】A.速率与浓度关系为v=kc(NO ),则增大c(CO),反应速率不变,故A错误;
2
B.恒压体系充入稀有气体使体积增大,c(NO )减小,所以反应速率减慢,故B正确;
2
C.平衡常数受温度影响,升高温度化学平衡常数变化,故C错误;
D.将产物从体系中分离出去,生成物浓度减小,平衡正向移动,故D错误;故选B。
6.(2022·贵州·毕节市第一中学高二阶段练习)有一处于平衡状态的反应:3A(s)+2B(g) 3C(g),
ΔH>0。为了使平衡向生成C的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂
A.①③ B.①③⑤ C.①④ D.②④⑤
【答案】C
【解析】3A(s)+2B(g) 3C(g),ΔH>0,正反应是气体体积增大的吸热反应;
①升高温度,平衡向正向(放热)反应移动;
②降低温度,平衡向逆向(吸热)反应移动;
③压强增大,平衡向逆向(气体体积减小)方向移动;
④降低压强,平衡向正向(气体体积增大)方向移动;
⑤加催化剂不会引起化学平衡的移动;
①④符合题意,故选C。7.(2021·新疆·乌鲁木齐市第三十一中学高二期中)可逆反应 ,在一定条件
下达到平衡,若改变条件,将变化情况 增大、减小、不变 填入空格:
(1)升高温度, _______, _______, 转化率_______。
(正) (逆)
(2)使用催化剂, _______, _______, 的物质的量_______。
(正) (逆)
(3)保持温度和压强不变加入稀有气体,则 的物质的量_______, 的转化率_______。
(4)保持温度和体积不变加入稀有气体,则 的转化率_______。
(5)若温度和体积不变,反应从正反应开始至平衡,在这个变化过程中,容器内气体的密度_______。
【答案】(1) 增大 增大 减小
(2) 增大 增大 不变
(3) 减小 减小
(4)不变
(5)不变
【解析】(1)升高温度任何反应的反应速率均加快,则升高温度, 增大, 增大,升高温度,平衡向
(正) (逆)
着吸热反应方向移动,即向逆向移动, 转化率减小,故答案为:增大;增大;减小;
(2)使用催化剂,能够同等幅度的加快正、逆反应速率,导致 增大, 增大,但平衡不移动, 的物
(正) (逆)
质的量不变,故答案为:增大;增大;不变;
(3)保持温度和压强不变加入稀有气体,则反应体系容器体积增大,相当于减小平衡体系的压强,平衡向着
气体体积增大的方向移动,即向逆反应方向移动,则 的物质的量减小, 的转化率减小,故答案为:减
小;减小;
(4)保持温度和体积不变加入稀有气体,则反应体系的容器体积不变,各物质的浓度不变,正逆反应速率不
变,仍然相等,平衡不移动,则 的转化率不变,故答案为:不变;
(5)若温度和体积不变,反应从正反应开始至平衡,在这个变化过程中,根据质量守恒定律可知,反应前后
气体的质量不变,则容器内气体的密度不变,故答案为:不变。
题组二 化学平衡的图像问题
1.在密闭容器中,反应X(g)+Y(g) 2XY(g) ΔH<0,达到甲平衡,在仅改变某一条件后达到乙平衡,
2 2
对改变的条件下列分析正确的是A.图I是增大反应物的浓度 B.图Ⅱ一定是加入催化剂的变化情况
C.图Ⅲ是增大压强 D.图Ⅲ是升高温度
【答案】D
【解析】A.图I在某一时刻正逆反应速率都增大,若只是增大反应物的浓度,只有正反应速率增大,逆
反应速率不变,A错误;
B.图Ⅱ正逆速率都增大,但增大程度相同,可能是增大压强或加入催化剂的变化情况,因为该反应是前
后气体分子数相同的反应,增大压强,正逆速率都增大,但仍相等,平衡不移动,B错误;
C.图Ⅲ改变条件速率增大,但平衡逆向移动,可能是升温,该反应是气体前后分子数相同的反应,故增
大压强,正逆反应速率都增大,但平衡不移动,C错误;
D.图Ⅲ改变条件速率增大,但平衡逆向移动,可能是升温,D正确;
故选D。
2.(2022·湖北·高二期中)有一化学反应mA(s)+n B(g) p C(g)+q D(g),如图表示的是A的转化率与
压强、温度的关系。下列叙述正确的是
A.正反应是吸热反应: m+n>p+q B.正反应是放热反应: m+n
p+q D.逆反应是吸热反应: np+q,A错误;
B.正反应为吸热反应,B错误;
C.正反应为吸热反应,因此逆反应为放热反应;由分析可知,n>p+q,C正确;D.由C选项可知,逆反应是放热反应,且 n>p+q,D错误;
因此本题选C。
3.(2022·云南·弥勒市一中高二期末)在某密闭容器中,可逆反应: 符合图中(Ⅰ)所
示关系, 表示C气体在混合气体中的体积分数。由此判断下列说法不正确的是
A.
B.正反应为放热反应
C. ,Y轴表示B的转化率
D. ,Y轴表示混合气体的平均相对分子质量
【答案】A
【解析】温度越高,反应越先达到平衡,依据图(I),压强都为p 时,T 下先达到平衡,则T>T,而温度
2 1 1 2
越高,C的体积分数越小,说明升高温度平衡逆向移动,该反应正反应为放热反应;压强越大,越先达到
平衡,依据图(I),温度都为T 时,p 下先达到平衡,则p>p,而压强越大,C的体积分数越大,说明增大
1 2 2 1
压强,平衡正向移动,该反应正反应为气体分子数减小的反应,1+1>x,即x<2。
A.由分析可知,x<2,A错误;
B.由分析可知,该反应正反应为放热反应,B正确;
C.由分析可知,温度相同时,压强增大,平衡正向移动,B的转化率增大,则图(II)中, ,Y轴可
表示B的转化率,C正确;
D.由分析可知,该反应为气体分子数减小的反应,依据质量守恒定律,气体质量一直不变,则温度相同
时,压强增大,平衡正向移动,混合气体的平均相对分子质量增大,则图(II)中, ,Y轴可表示混合
气体的平均相对分子质量,D正确;
答案选A。
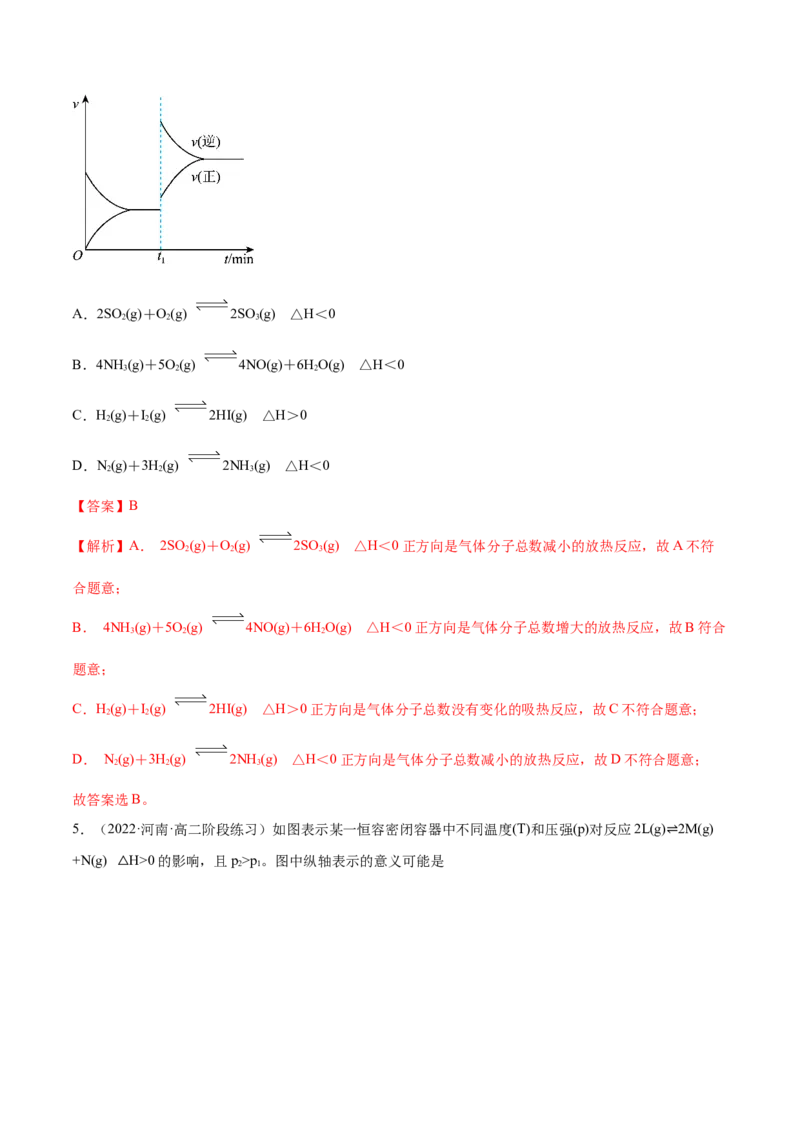
4.(2022·上海交大附中高二阶段练习)如图为某化学反应的速率与时间的关系示意图。在t 时刻升高温
1
度或者增大压强,速率的变化都符合示意图的反应是A.2SO (g)+O(g) 2SO (g) △Η<0
2 2 3
B.4NH (g)+5O(g) 4NO(g)+6HO(g) △Η<0
3 2 2
C.H(g)+I(g) 2HI(g) △Η>0
2 2
D.N(g)+3H(g) 2NH (g) △Η<0
2 2 3
【答案】B
【解析】A. 2SO (g)+O(g) 2SO (g) △Η<0正方向是气体分子总数减小的放热反应,故A不符
2 2 3
合题意;
B. 4NH (g)+5O(g) 4NO(g)+6HO(g) △Η<0正方向是气体分子总数增大的放热反应,故B符合
3 2 2
题意;
C.H(g)+I(g) 2HI(g) △Η>0正方向是气体分子总数没有变化的吸热反应,故C不符合题意;
2 2
D. N(g)+3H(g) 2NH (g) △Η<0正方向是气体分子总数减小的放热反应,故D不符合题意;
2 2 3
故答案选B。
5.(2022·河南·高二阶段练习)如图表示某一恒容密闭容器中不同温度(T)和压强(p)对反应2L(g) 2M(g)
+N(g) H>0的影响,且p>p。图中纵轴表示的意义可能是 ⇌
2 1
△A.容器中混合气体的密度 B.混合气体中M的百分含量
C.平衡常数K D.
【答案】B
【解析】A.恒容条件下反应,容器体积不变,气体总质量不变,密度一直保持不变,改变压强无影响,A
错误;
B.该反应正向气体分子数减少,增大压强,平衡逆向移动,混合气体中M的百分含量减小,B正确;
C.平衡常数只与温度有关,相同温度下,不同压强条件下的平衡常数应相同,C错误;
D.该反应正向气体分子数减少,增大压强,平衡逆向移动,混合气体中M的物质的量减少,L的物质的
量增加,n(L)/n(M)比值增大,D错误;
故选B。
6.(2021·贵州·高二学业考试)在体积一定的密闭容器中发生反应:mA(g)+nB(g) pC(g),C的百分
含量在不同压强下随时间的变化如图所示。下列判断正确的是
A.P>P ;m+nP ;m+n>p
1 2 1 2
C.P
p D.P
P ;压强增大,C的百分含量减少,即加压平衡逆向移动,
1 1 2
因此正反应是气体体积增大的反应,则m+nK
A B C A B C
C.若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为5L
D.若增大H 的浓度,则CO 和H 的平衡转化率(α)均会增大
2 2
【答案】B
【解析】A.由图可知,C点的反应温度高于B点,温度越高,反应速率越大,则C点的速率比B点的大,
故A不符合题意;
B.平衡常数是温度函数,温度不变,平衡常数不变,由图可知,A、B、C三点的温度大小顺序为
C>A=B,温度升高,一氧化碳的平衡转化率减小,说明平衡向逆反应方向移动,该反应是放热反应,反应
的化学平衡常数减小,则A、B、C三点的平衡常数K 、K 、K 的大小关系为K =K >K ,故B符合题意;
A B C A B C
C.由图可知,A、B的反应温度相同,反应的平衡常数相等,A点一氧化碳的转化率为50%,由容器的体
积为10L可知,平衡时一氧化碳、氢气、甲醇的浓度为(1—1×50%)mol/L=0.5mol/L、(2—1×50%×2)mol/
L=1mol/L、1×50%mol/L=0.5mol/L,反应的平衡常数K = =1;B点一氧化碳的转化率为80%,由容
A
器的体积为5L可知,平衡时一氧化碳、氢气、甲醇的浓度为(2—2×50%)mol/L=1mol/L、(4—
2×50%×2)mol/L=2mol/L、2×50%mol/L=1mol/L,反应的平衡常数K = =0.25, 由计算结果可知,A、
B
B的平衡常数不相等,则若达到平衡状态A时,容器的体积为10L,在平衡状态B时容器的体积不可能为
5L,故C不符合题意;
D.增大氢气浓度,平衡向正反应方向移动,氢气的转化率减小,故D不符合题意;
故选B。
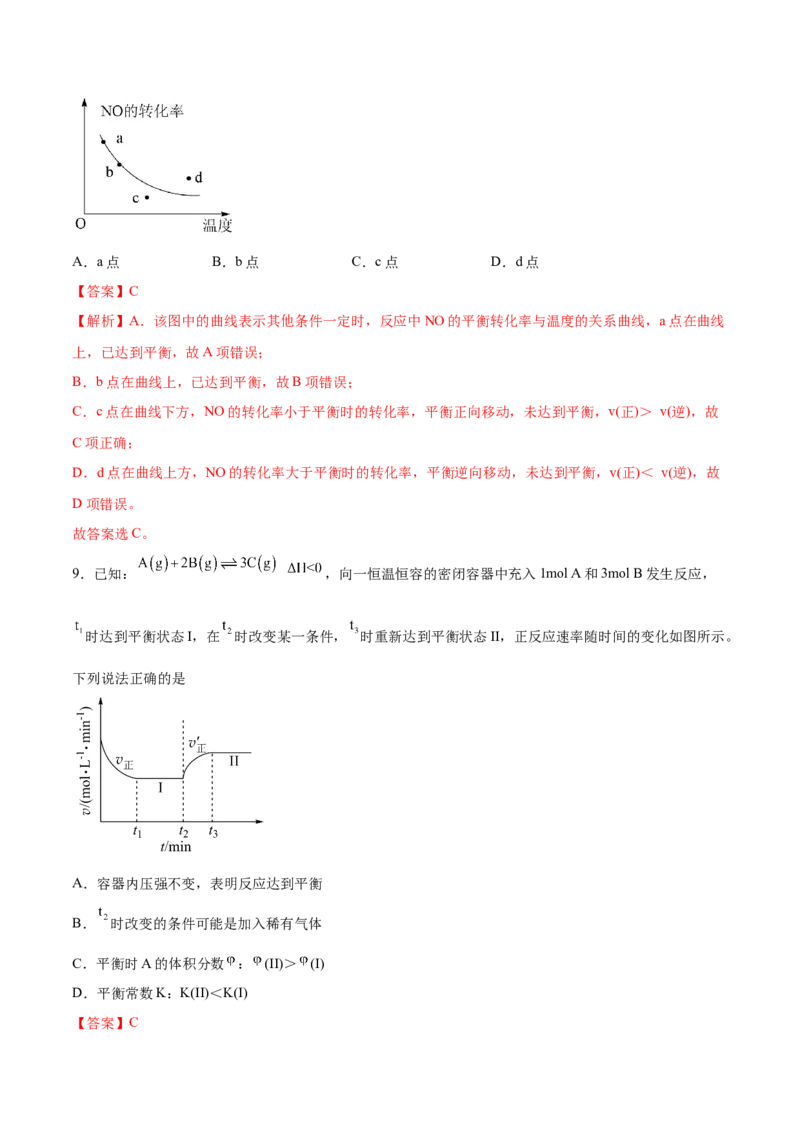
8.2NO+O 2NO ,图中的曲线是表示其他条件一定时,反应中NO的平衡转化率与温度的关系曲线,
2 2
图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)> v(逆)的是A.a点 B.b点 C.c点 D.d点
【答案】C
【解析】A.该图中的曲线表示其他条件一定时,反应中NO的平衡转化率与温度的关系曲线,a点在曲线
上,已达到平衡,故A项错误;
B.b点在曲线上,已达到平衡,故B项错误;
C.c点在曲线下方,NO的转化率小于平衡时的转化率,平衡正向移动,未达到平衡,v(正)> v(逆),故
C项正确;
D.d点在曲线上方,NO的转化率大于平衡时的转化率,平衡逆向移动,未达到平衡,v(正)< v(逆),故
D项错误。
故答案选C。
9.已知: ,向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应,
时达到平衡状态I,在 时改变某一条件, 时重新达到平衡状态II,正反应速率随时间的变化如图所示。
下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B. 时改变的条件可能是加入稀有气体
C.平衡时A的体积分数 : (II)> (I)
D.平衡常数K:K(II)<K(I)
【答案】C【解析】A.容器内发生的反应为A(g)+2B(g) 3C(g),该反应是气体分子数不变的可逆反应,所以在恒温
恒容条件下,气体的压强始终保持不变,则容⇌器内压强不变,不能说明反应达到平衡状态,A错误;
B.根据图像变化曲线可知,t t 过程中,t 时v正ˊ瞬间不变,平衡过程中不断增大,则说明反应向逆反
2 3 2
应方向移动,且不是“突变”图∼像,属于“渐变”过程,所以排除温度与催化剂等影响因素,改变的条件
为:向容器中加入C,B错误;
C.最初加入体系中的A和B的物质的量的比值为1:3,当向体系中加入C时,平衡逆向移动,最终A和
B各自物质的量增加的比例为1:2,因此平衡时A的体积分数φ(II)>φ(I),C正确;
D.平衡常数K与温度有关,因该反应在恒温条件下进行,所以K保持不变,D错误;故选C。
题组三 等效平衡
1.(2022·甘肃张掖·高二期末) 和 分别为A、B在两个恒容容器中平衡体系A(g) 2B(g)和2A(g)
B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
A. 、 均减小 B. 、 均增大
C. 减小, 增大 D. 增大, 减小
【答案】C
【解析】在恒温、恒容条件下,对于反应A(g) 2B(g),增加A的物质的量,所到达的平衡状态可以等效
为增大压强,平衡向逆反应方向移动,A的转化率减小,即α 减小;
1
对于反应:2A(g) B(g),增加A的物质的量,所到达的平衡状态可以等效为增大压强,增大压强平衡向
生成B的方向移动,A的转化率增大,即α 增大;
2
答案选C。
2.在恒温恒容的密闭容器中充入 A和 B,发生反应: ,达平衡时,
C为 ,如果此时移走 A和 B,在相同的温度下再次达平衡时C的物质的量为
A. B.
C.小于 D.大于 ,小于
【答案】C
【解析】根据题意可以理解为将原容器分为两部分,每部分充入1molA和0.5molB,达到平衡是C物质的
量为0.2mol,将其中一部分移走,剩余0.2 molC,恢复到原容器即增大体积,减小压强,平衡向体积增大
即逆向移动,C物质的量减小,因此在相同的温度下再次达平衡时C的物质的量为小于 ,故C符合题意。综上所述,答案为C。
3.(2021·广西·宾阳中学高二期中)甲、乙两容器都发生反应 2A(g)+B(g) xC(g),两容器温度和初始压
强都相同。甲容器中充入 2 mol A 和1 mol B,达平衡后,C在平衡混合气⇌中的体积分数为φ、物质的量为
n;乙容器中充入 1.4 mol A,0.7 mol B 和 0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ、物质
1
的量为n 下列说法中正确的是
2.
A.若甲、乙两容器均为恒容容器,则x一定等于2
B.若甲、乙两容器均为恒压容器,则x一定等于3
C.若甲为恒容容器、乙为恒压容器,且 x=3,则 n 必大于n
1 2
D.若甲为恒压容器、乙为恒容容器,且 x≠3,则 n 必大于n
1 2
【答案】C
【解析】A.在恒温恒容下,甲容器中充入 2 mol A 和1 mol B与乙容器中充入 1.4 mol A,0.7 mol B 和
0.6 mol C,达平衡后,C在平衡混合气中的体积分数为φ,说明两个平衡为等效平衡,按化学计量数转化,
应满足:n(A)=2mol,n(B)=1mol,则 ,解得x=2,另外,对于反应前后气体的计量数
之和相等的反应,物质的投料比成相同比例时也是等效平衡,所以x=3也是正确的,所以x可能为2或
3,A项错误;
B.若甲、乙两容器均为恒压容器,只要反应物成比例就是等效平衡,开始甲容器充入2mol A和1mol B与
乙容器中充入1.4mol A,0.7mol B和0.6mol C,无论x取何值,都满足n(A):n(B)=2:1,B项错误;
C.若甲为恒容容器,乙为恒压容器,且x=3,则反应前后气体体积相等,气体的物质的量始终不变,所以
n 等于3mol,n 等于1.4mol+0.7mol+0.6mol=2.7mol,n>n,C项正确;
1 2 1 2
D.若甲为恒压容器、乙为恒容容器,且 x≠3,当x=2时,开始甲容器充入2mol A和1mol B与乙容器中
充入1.4mol A,0.7mol B和0.6mol C,达平衡后,C的体积分数为φ,说明二者是等效平衡,此时n=n,
1 2
D项错误;
答案选C。
4(2021·甘肃·兰州一中高二期中) ,向恒温、恒容的三个密
闭容器中分别充入气体:(甲) 和 ,(乙) 和 ,(丙) 。反应达平衡
时, 的质量m满足下列关系的是
A.(甲)>m(丙)>2m(乙) B.m(甲)=m(丙)>2m(乙)C.m(甲)=m(丙)<2m(乙) D.m(甲)<m(丙)<2m(乙)
【答案】B
【解析】用一边倒法可知, (甲)的投料 和 ,(丙)的投料 相同,则甲和丙建立的
是等同平衡:反应达平衡时, 的质量m(甲)=m(丙), (乙)的投料 和 是甲的一半,若
乙的容积也减半,则二者也是等效平衡、乙中三氧化硫的量是甲的一半,实际情况则容器容积相同:则乙
平衡等效于甲平衡扩容减压后移动所得,减压 左移,则反应
达平衡时, 的质量m(丙)>2m(乙),故m(甲)=m(丙)>2m(乙);
答案选B。
5.相同温度下,在两个相同的密闭容器中发生反应: ,两容
器中各物质起始的物质的量及平衡时的相关数据如下表所示:
容 起始 起始 起始 平衡转化 平衡转化 反应开始至平衡时热效
器 CO 率 率 应
Ⅰ 1mol 2mol 0mol 放热
Ⅱ 0mol 0mol 1mol 吸热
则下列关系正确的是
A. B. C. D.
【答案】B
【解析】A.根据题中信息可以得到容器Ⅰ和Ⅱ是等效平衡,正逆反应的转化率相加等于1,即 ;
正反应放出的热量数值加上逆反应吸收的热量数值之和等于Q,即 ,故B正确。
综上所述,答案为B。
6.一定温度下,某密闭容器中充入 和 ,发生反应 。在达到平衡后,生成 。当温度不变时,若起始加入的 、 、AB的物质的量分别为:x,y,z,则下列说法正
确的是
A.若保持恒容,当 , ,则达新平衡状态时 和 的转化率一定升高
B.若保持恒压,当 ,z为任意值,则达新平衡状态时AB的物质的量为
C.若保持恒容,当 ,则达新平衡状态时 的体积分数与原平衡时相同
D.若保持恒压,当 , ,则达新平衡状态时 的体积分数与原平衡时可能相同
【答案】D
【解析】A.若保持恒容,当x:y<1:2,z=0,B (g)浓度增大,A 的转化率增大,B 的转化率降低,故
2 2 2
A错误;
B.若保持恒压,当x:y=1:2,z为0时,两平衡等效,因此AB的量无法表示,故B错误;
C.若保持恒容,应用极值转化后,相当于投料比为1:1,与原平衡不等效,新平衡状态时A 的体积分数
2
与原平衡不同,故C错误;
D.若保持恒压,当x:y<1:2,z>0,满足(x+ ):(y+ )=1:2,两平衡等效,达新平衡状态时B 的体
2
积分数与原平衡相同,故D正确;
故选:D。
7(2021·山西·侯马市第一中学校高二期中)相同温度下,体积相等的两个恒容绝热密闭容器中发生可逆反
应:N(g)+3H(g) 2NH (g) ΔH=-92.6 kJ·mol。实验测得起始、平衡时的有关数据如下表所示
2 2 3
起始时各物质的物质的量/mol 达平衡时体系能量的变化
容器编号
N H NH 放出热量:
2 2 3
① 1 3 0 23.15 kJ
② 0 0 2 吸收热量:QkJ
下列叙述正确的是
A.容器①、②中反应的平衡常数相等
B.平衡时两个容器中NH 的体积分数相等
3
C.Q+23.15=92.6D.平衡时两容器N 的物质的量浓度①>②
2
【答案】D
【解析】A.该反应为放热反应,容器为恒容绝热容器,①向正反应方向进行,温度升高,②向逆反应方
向进行,温度降低,平衡常数只受温度的影响,两容器温度不同,因此化学平衡常数也不相同,故A错误;
B.容器为恒容绝热容器,因此这两个平衡不属于等效平衡,即平衡是两个容器中氨气的体积分数不相等,
故B错误;
C.如果这个两容器为恒温恒容,则这两个平衡为等效平衡,即存在Q+23.15=92.6,但这两个容器为恒容
绝热容器,这两个平衡不属于等效平衡,因此Q+23.15≠92.6,故C错误;
D.该反应为放热反应,①反应向正反应方向进行,温度升高,氮气的转化率降低,②反应向逆反应方向
进行,温度降低,氨气的转化率降低,因此平衡时两容器氮气的物质的量的浓度①>②,故D正确;
答案为D。
8.如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M,N两个容器中均发生反应:
。保持温度不变向M、N中各通入1 mol X和2 mol Y的混合气体,初始时M、N
的容积相同。下列说法正确的是
A.x不论何值,平衡时M、N中的平均相对分子质量都相等
B.若 ,达到平衡后X的体积分数关系:
C.若 ,Z的物质的量关系:
D.若 ,达到平衡后Y的转化率:
【答案】C
【解析】M、N中起始量、体积、温度均相同,M保持体积不变,N保持压强不变,对应N来说,若
x=3,与A为等效平衡;若x>3,由于反应后气体体积增大,N容器建立的平衡相当于恒温恒容下建立的
平衡扩大容器体积,压强减小,平衡正向移动;若x<3,由于反应后气体体积减小,N容器建立的平衡相
当于恒温恒容下建立的平衡缩小容器体积,压强增大,平衡正向移动。
A.若x=3,M、N中平衡状态相同,平衡时M、N中的平均相对分子质量都相等,若x>3或<3,两者的
平衡状态不同,平衡时M、N中的平均相对分子质量不等,故A错误;B.若x=3,由于反应前后气体体积不变,N容器建立的平衡与恒温恒容下建立的平衡等效,所以达到平衡
后A的体积分数关系为:φ(M)=φ(N),故B错误;
C.若x<3,由于反应后气体体积减小,N容器建立的平衡相当于恒温恒容下建立的平衡缩小容器体积,
压强增大,平衡正向移动,Z的物质的量增大,所以Z的物质的量关系为: ,故C正确;
D.若x>3,由于反应后气体体积增大,N容器建立的平衡相当于恒温恒容下建立的平衡扩大容器体积,
压强减小,平衡正向移动,Y的转化率增大,所以达到平衡后Y的转化率关系为: ,故D错
误。答案选C。
9.在一个固定体积的密闭容器中,加入2mol A和1mol B发生反应: 2A(g)+B(g) 3C(g)+D(g) 达到
平衡时, C的浓度为n mol·L-1. 若维持容器的体积和温度不变,按下列各种配比为起始物质, 达到平衡后,
C的浓度仍为n mol·L-1的是
A.4mol A + 2mol B
B.2mol A + 1mol B + 3mol C + 1mol D
C.3mol A + 1mol B
D.1mol A + 0.5mol B + 1.5mol C + 0.5mol D
【答案】D
【解析】若维持体积和温度不变,改变加入的起始物质的配比,达平衡后,C的浓度仍为n mol/L,则与原
平衡为等效平衡,反应前后气体的物质的量不同,按化学计量数完全转化到方程式的左边,满足
n(A)=2mol,n(B)=1mol即可:
A.开始加入4 mol A 和2 mol B,等效为在原平衡的基础在加入2molA、1molB,与原平衡相比,平衡正
向移动,平衡时C的浓度大于nmol/L,故不A符合;
B.开始加入2 mol A+1 mol B+3 molC+1 mol D,完全转化到方程式的左边,可以得到4 mol A 和2 mol
B,平衡时C的浓度大于nmol/L,故B不符合;
C.开始加入3 mol A+1 mol B,等效为在原平衡的基础上加入1molA,与原平衡相比,平衡正向移动,平
衡时C的浓度大于nmol/L,故C不符合;
D.开始加入1 mol A+0.5 mol B+1.5 mol C+0.5 mol D,完全转化到方程式的左边,可以得到2mol A 和1
mol B,与原平衡等效,平衡时C的浓度等于nmol/L,故D符合;
故选:D。
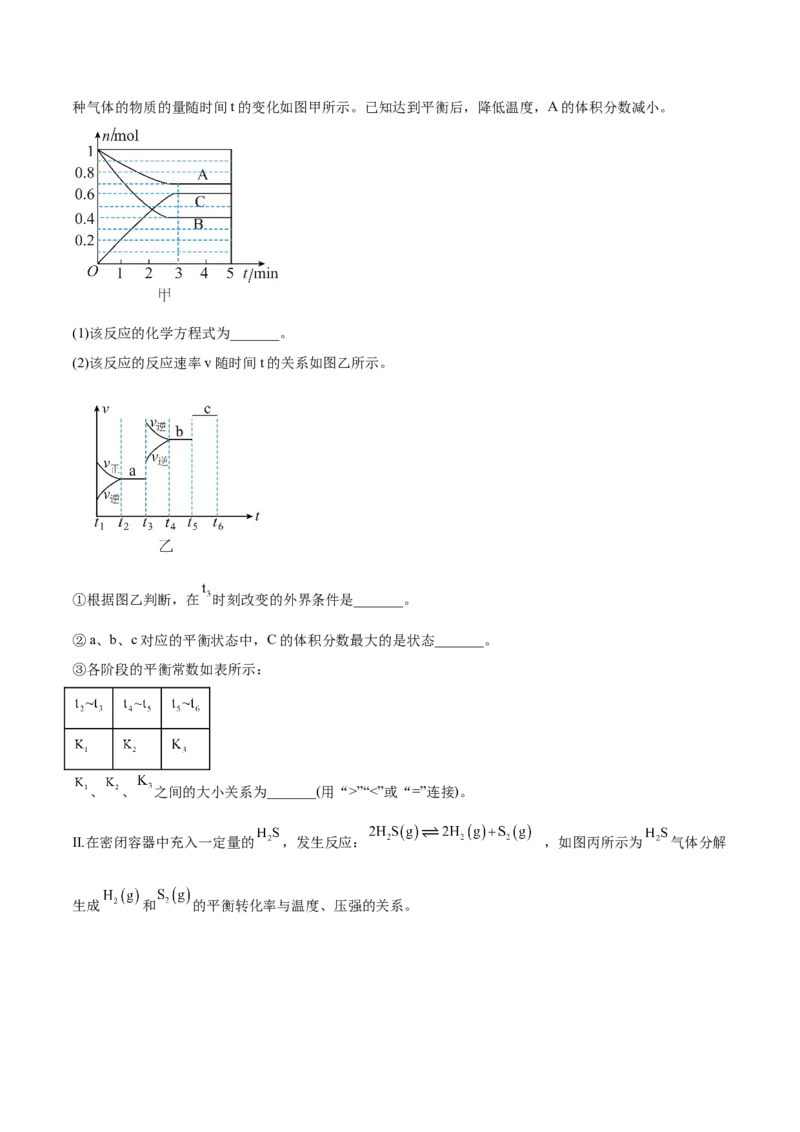
10.(2021·内蒙古·包头市第四中学高二期中)Ⅰ.一定条件下,在容积为5 L的密闭容器中,A、B、C三种气体的物质的量随时间t的变化如图甲所示。已知达到平衡后,降低温度,A的体积分数减小。
(1)该反应的化学方程式为_______。
(2)该反应的反应速率v随时间t的关系如图乙所示。
①根据图乙判断,在 时刻改变的外界条件是_______。
②a、b、c对应的平衡状态中,C的体积分数最大的是状态_______。
③各阶段的平衡常数如表所示:
、 、 之间的大小关系为_______(用“>”“<”或“=”连接)。
Ⅱ.在密闭容器中充入一定量的 ,发生反应: ,如图丙所示为 气体分解
生成 和 的平衡转化率与温度、压强的关系。(3) _______(填填“>”“<”或“=”)0。
(4)图丙中压强( 、 、 )由大到小的顺序为_______。
(5)如果想进一步提高 的转化率,除改变温度、压强外,还可以采取的措施有_______。
【答案】(1)
(2) 升高温度 a
(3)>
(4)
(5)及时分离出产物
【解析】(1)根据图像可知,达到平衡时A的物质的量减小了:1mol-0.7mol=0.3mol,B的物质的量减小
为:1mol-0.4mol=0.6mol,C的物质的量增加,增加的物质的量为:0.6mol,所以A、B、C的物质的量变
化之比为:0.3mol:0.6mol:0.6mol=1:2:3,该反应的化学方程式为: ;故答案为:
;
(2)①根据图像可知:t 时正逆反应速率同时增大,且逆反应速率大于正反应速率,说明平衡向着逆向移
3
动,若增大压强,平衡向着正向移动,由于该反应为放热反应,升高温度后平衡向着逆向移动,所以t 时
3
升高了温度;故答案为:升高了温度;
②根据图像变化可知,在t~t 时反应向着正向移动,A转化率逐渐增大,直至t~t 时反应达到平衡状态,
1 2 2 3
A转化率达到最大;而t~t 时升高了温度,平衡向着逆向移动,A的转化率逐渐减小,直至t~t 时A的
3 4 4 5
转化率达到最低;而t~t 时正逆反应速率同时增大且相等,说明平衡没有移动,A的转化率不变,与t~
5 6 4
t 时相等,所以A的转化率最大的时间段是:t~t,A的转化率最大时C的体积分数最大,此时间段为t
5 2 3 2
~t,即为a点;a、b、c三点中,C的体积分数最大的是a。故答案为:a;
3
③反应A+2B 2C ΔH<0,温度升高平衡向着逆反应方向移动,化学平衡常数减小,所以温度越高,化学
平衡常数越小⇌;t~t、t~t、t~t 时间段的温度关系为:t~t=t~t>t~t,所以化学平衡常数大小关系
2 3 3 4 4 5 3 4 4 5 2 3为:K>K =K 。故答案为:K>K =K ;
1 2 3 1 2 3
(3)恒压条件下,温度升高,HS的转化率升高,即升高温度平衡正向移动,则ΔH> 0;故答案为:>;
2
(4)2HS(g) 2H(g)+S (g) ΔH=+169.8kJ•mol-1,反应是气体体积增大的反应,温度不变,压强增大平
2 2 2
衡逆向进行,HS的转化率减小,则压强关系为:图中压强(p、p、p)的大小顺序为p>p>p。故答案为:
2 1 2 3 3 2 1
p>p>p;
3 2 1
(5)进一步提高HS的转化率,除改变温度、压强外,还可以采取的措施有及时分离出产物,故答案为:
2
及时分离出产物。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育