文档内容
第五章 化工生产中的重要非金属元素
实验活动5 不同价态含硫物质的转化
分层作业
基础达标
1.关于反应HSO +NaSO =Na SO +SO ↑+HO所涉及的物质,下列说法错误的是(
2 4 2 3 2 4 2 2
)
A.浓HSO 能与SO 发生氧化还原反应 B.NaSO 容易被空气中的O 氧化变质
2 4 2 2 3 2
C.浓硫酸与铜在常温下反应生成SO D.SO 是导致酸雨的主要有害污染物
2 2
2.一密闭试管中装有 ,加入少量 稀溶液,震荡后没有明显现象。那么溶液中S
元素存在的主要形式为( )
A.S2- B.HS C.S D.SO
2
3.在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.SO CaSO CaSO
2 3 4
B.Fe Fe O FeCl
2 3 3
C.HCl(aq) Cl Ca(ClO)
2 2
D.Cu (OH) CO CuO CuCl (aq)
2 2 3 2
4.已知物质X在一定条件下能发生如图所示转化。下列说法错误的是( )
A.反应①②③均为氧化还原反应 B.X可能与 反应
C.物质A可以是 或 D.若不考虑反应③,X也可以是有机物
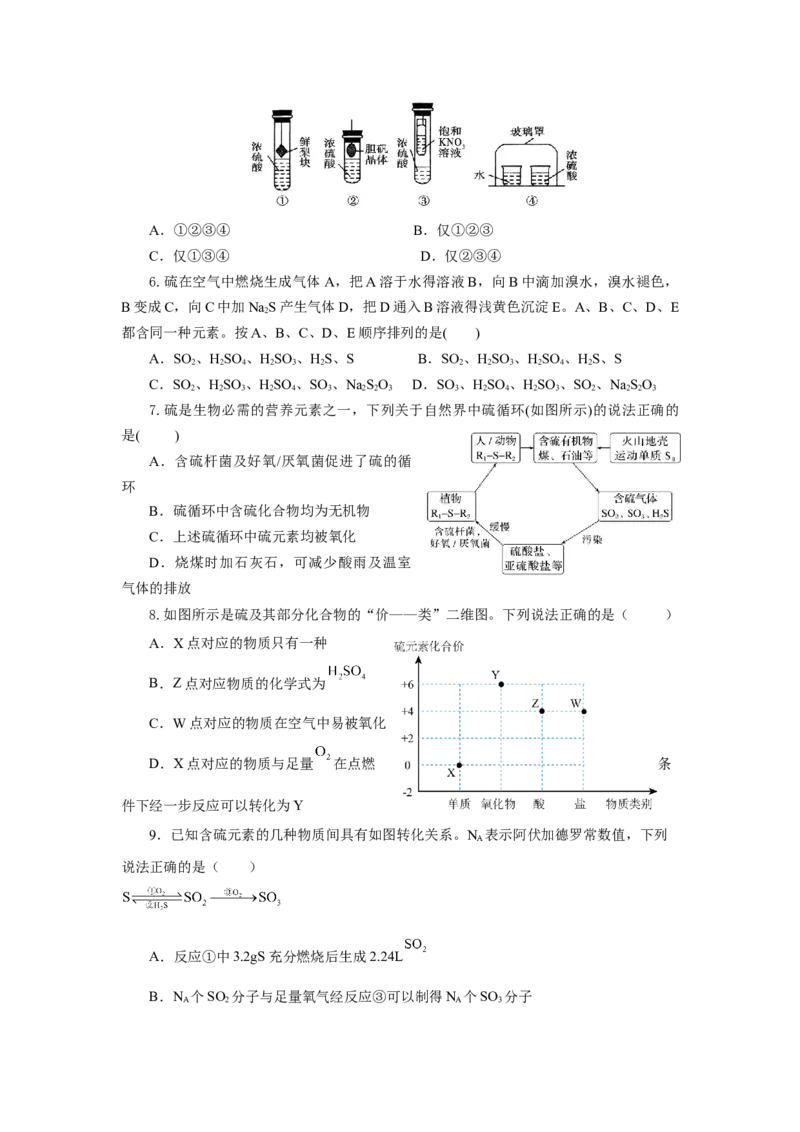
5.在实验探究课上,同学们积极思考,共设计出如图所示四种实验方案用以验证浓硫
酸的吸水性,其中在理论上可行的是 ( )A.①②③④ B.仅①②③
C.仅①③④ D.仅②③④
6.硫在空气中燃烧生成气体A,把A溶于水得溶液B,向B中滴加溴水,溴水褪色,
B变成C,向C中加NaS产生气体D,把D通入B溶液得浅黄色沉淀E。A、B、C、D、E
2
都含同一种元素。按A、B、C、D、E顺序排列的是( )
A.SO 、HSO 、HSO 、HS、S B.SO 、HSO 、HSO 、HS、S
2 2 4 2 3 2 2 2 3 2 4 2
C.SO 、HSO 、HSO 、SO 、NaSO D.SO 、HSO 、HSO 、SO 、NaSO
2 2 3 2 4 3 2 2 3 3 2 4 2 3 2 2 2 3
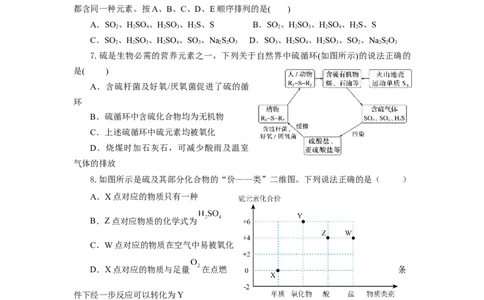
7.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)的说法正确的
是( )
A.含硫杆菌及好氧/厌氧菌促进了硫的循
环
B.硫循环中含硫化合物均为无机物
C.上述硫循环中硫元素均被氧化
D.烧煤时加石灰石,可减少酸雨及温室
气体的排放
8.如图所示是硫及其部分化合物的“价——类”二维图。下列说法正确的是( )
A.X点对应的物质只有一种
B.Z点对应物质的化学式为
C.W点对应的物质在空气中易被氧化
D.X点对应的物质与足量 在点燃 条
件下经一步反应可以转化为Y
9.已知含硫元素的几种物质间具有如图转化关系。N 表示阿伏加德罗常数值,下列
A
说法正确的是( )
A.反应①中3.2gS充分燃烧后生成2.24L
B.N 个SO 分子与足量氧气经反应③可以制得N 个SO 分子
A 2 A 3C.反应②中若转移2N 个电子,生成1.5molS
A
D.只要氧气过量,硫可以一步转化为SO
3
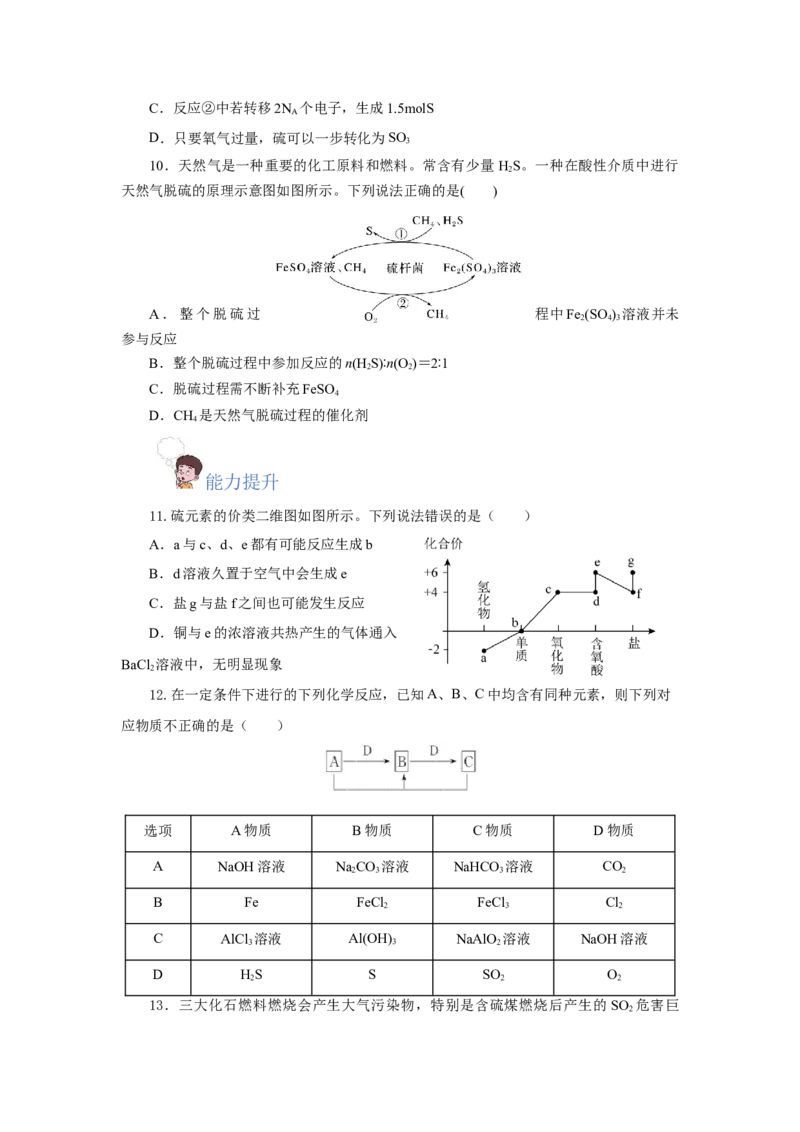
10.天然气是一种重要的化工原料和燃料。常含有少量 HS。一种在酸性介质中进行
2
天然气脱硫的原理示意图如图所示。下列说法正确的是( )
A.整个脱硫过 程中Fe (SO ) 溶液并未
2 4 3
参与反应
B.整个脱硫过程中参加反应的n(H S)∶n(O )=2∶1
2 2
C.脱硫过程需不断补充FeSO
4
D.CH 是天然气脱硫过程的催化剂
4
能力提升
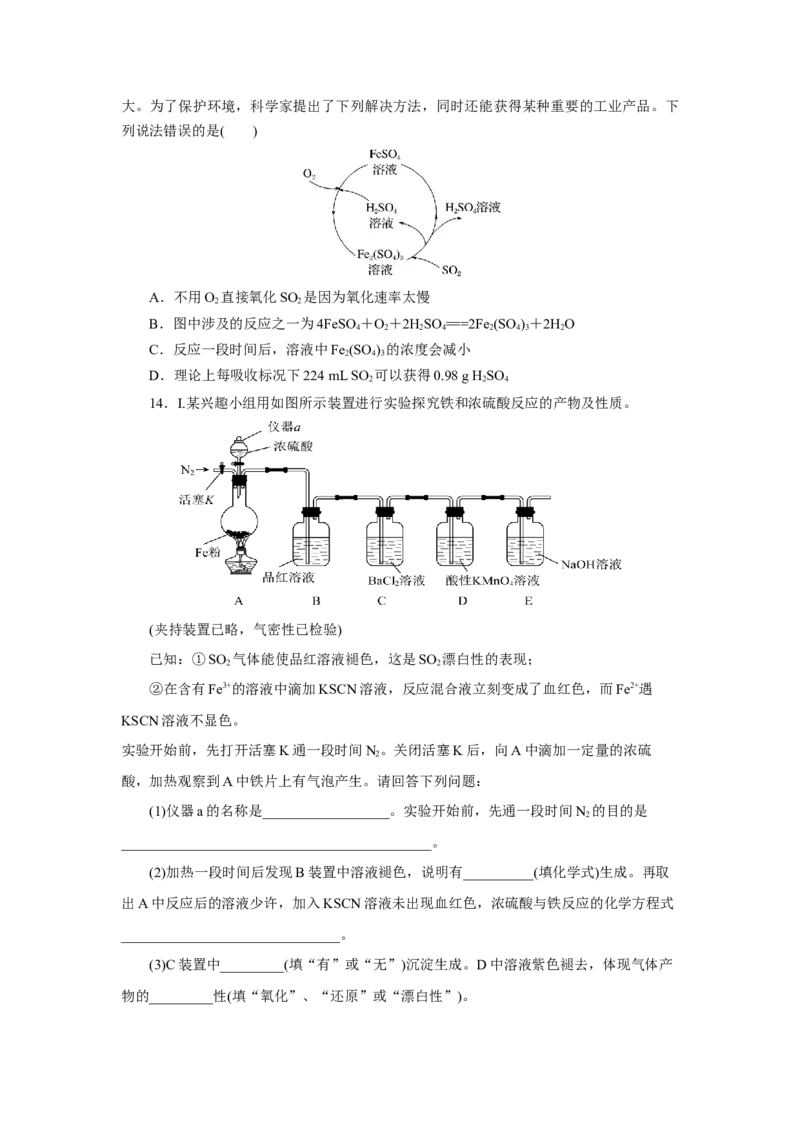
11.硫元素的价类二维图如图所示。下列说法错误的是( )
A.a与c、d、e都有可能反应生成b
B.d溶液久置于空气中会生成e
C.盐g与盐f之间也可能发生反应
D.铜与e的浓溶液共热产生的气体通入
BaCl 溶液中,无明显现象
2
12.在一定条件下进行的下列化学反应,已知A、B、C中均含有同种元素,则下列对
应物质不正确的是( )
选项 A物质 B物质 C物质 D物质
A NaOH溶液 NaCO 溶液 NaHCO 溶液 CO
2 3 3 2
B Fe FeCl FeCl Cl
2 3 2
C AlCl 溶液 Al(OH) NaAlO 溶液 NaOH溶液
3 3 2
D HS S SO O
2 2 2
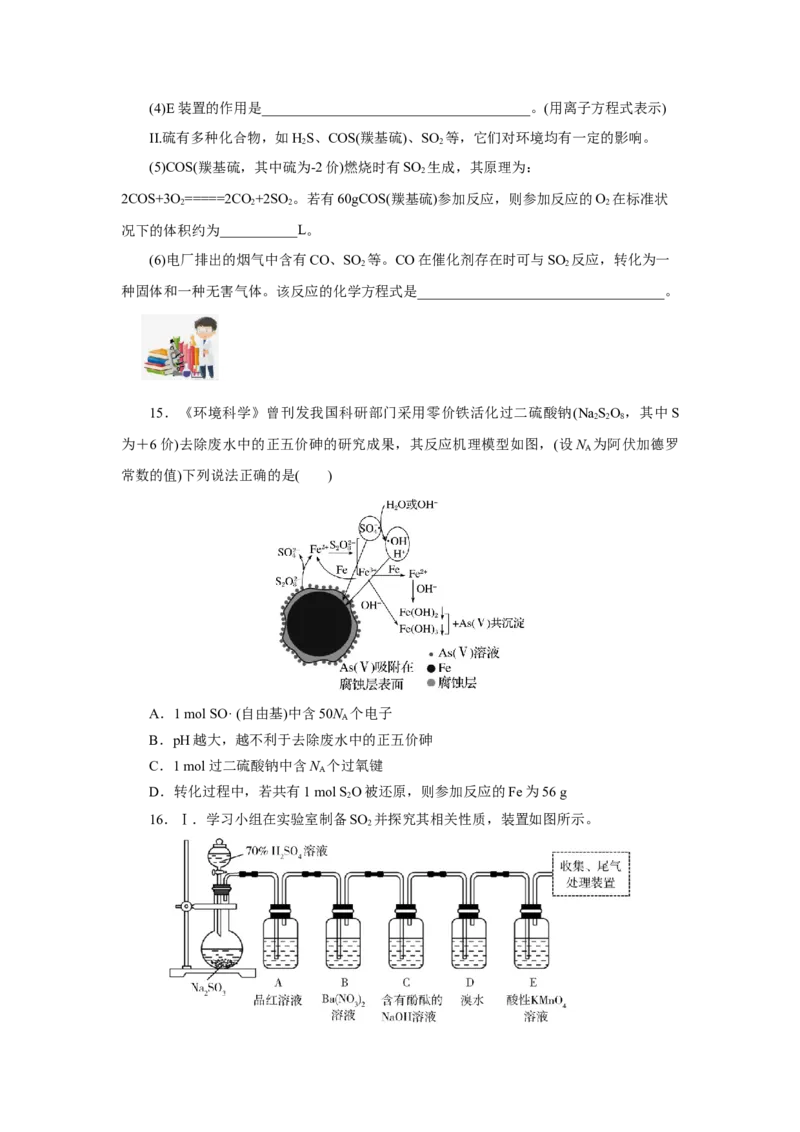
13.三大化石燃料燃烧会产生大气污染物,特别是含硫煤燃烧后产生的 SO 危害巨
2大。为了保护环境,科学家提出了下列解决方法,同时还能获得某种重要的工业产品。下
列说法错误的是( )
A.不用O 直接氧化SO 是因为氧化速率太慢
2 2
B.图中涉及的反应之一为4FeSO +O+2HSO ===2Fe (SO )+2HO
4 2 2 4 2 4 3 2
C.反应一段时间后,溶液中Fe (SO ) 的浓度会减小
2 4 3
D.理论上每吸收标况下224 mL SO 可以获得0.98 g H SO
2 2 4
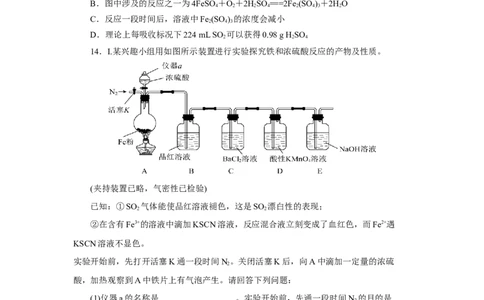
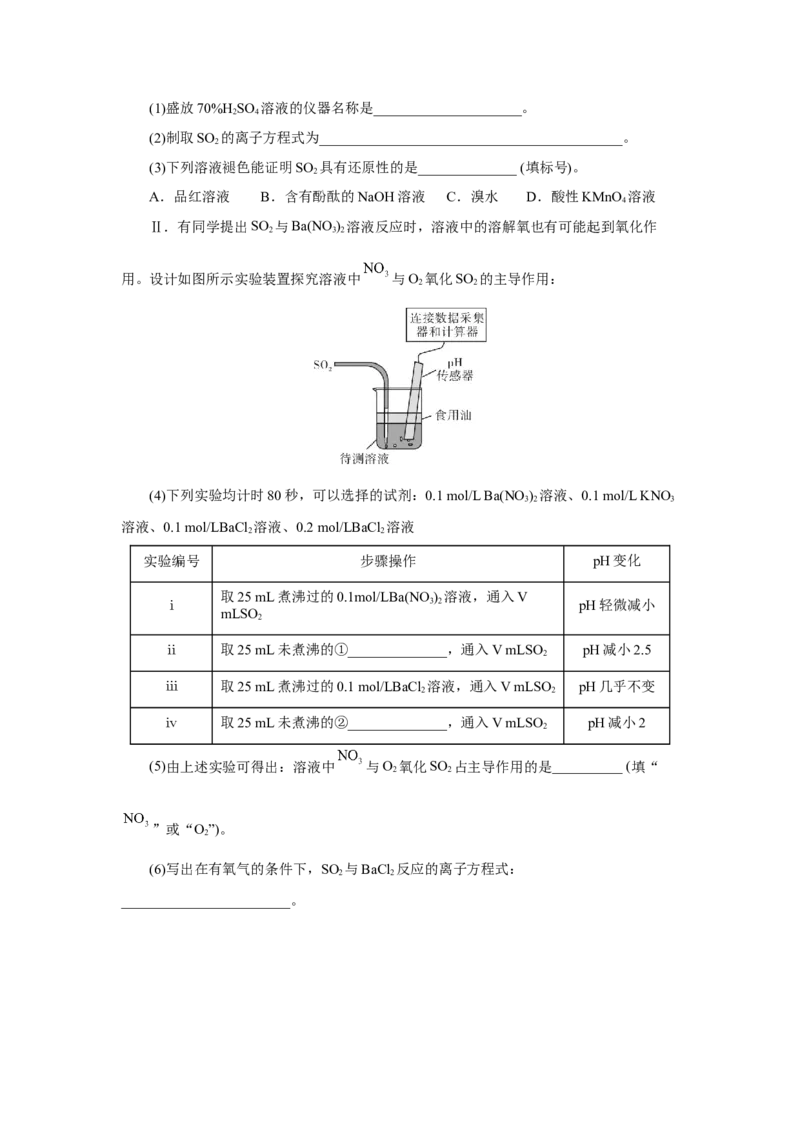
14.I.某兴趣小组用如图所示装置进行实验探究铁和浓硫酸反应的产物及性质。
(夹持装置已略,气密性已检验)
已知:①SO 气体能使品红溶液褪色,这是SO 漂白性的表现;
2 2
②在含有Fe3+的溶液中滴加KSCN溶液,反应混合液立刻变成了血红色,而Fe2+遇
KSCN溶液不显色。
实验开始前,先打开活塞K通一段时间N。关闭活塞K后,向A中滴加一定量的浓硫
2
酸,加热观察到A中铁片上有气泡产生。请回答下列问题:
(1)仪器a的名称是__________________。实验开始前,先通一段时间N 的目的是
2
____________________________________________。
(2)加热一段时间后发现B装置中溶液褪色,说明有__________(填化学式)生成。再取
出A中反应后的溶液少许,加入KSCN溶液未出现血红色,浓硫酸与铁反应的化学方程式
_______________________________。
(3)C装置中_________(填“有”或“无”)沉淀生成。D中溶液紫色褪去,体现气体产
物的_________性(填“氧化”、“还原”或“漂白性”)。(4)E装置的作用是______________________________________。(用离子方程式表示)
II.硫有多种化合物,如HS、COS(羰基硫)、SO 等,它们对环境均有一定的影响。
2 2
(5)COS(羰基硫,其中硫为-2价)燃烧时有SO 生成,其原理为:
2
2COS+3O =====2CO+2SO。若有60gCOS(羰基硫)参加反应,则参加反应的O 在标准状
2 2 2 2
况下的体积约为___________L。
(6)电厂排出的烟气中含有CO、SO 等。CO在催化剂存在时可与SO 反应,转化为一
2 2
种固体和一种无害气体。该反应的化学方程式是___________________________________。
直击高考
15.《环境科学》曾刊发我国科研部门采用零价铁活化过二硫酸钠(Na SO ,其中S
2 2 8
为+6价)去除废水中的正五价砷的研究成果,其反应机理模型如图,(设N 为阿伏加德罗
A
常数的值)下列说法正确的是( )
A.1 mol SO· (自由基)中含50N 个电子
A
B.pH越大,越不利于去除废水中的正五价砷
C.1 mol过二硫酸钠中含N 个过氧键
A
D.转化过程中,若共有1 mol S O被还原,则参加反应的Fe为56 g
2
16.Ⅰ.学习小组在实验室制备SO 并探究其相关性质,装置如图所示。
2(1)盛放70%H SO 溶液的仪器名称是_____________________。
2 4
(2)制取SO 的离子方程式为___________________________________________。
2
(3)下列溶液褪色能证明SO 具有还原性的是______________ (填标号)。
2
A.品红溶液 B.含有酚酞的NaOH溶液 C.溴水 D.酸性KMnO 溶液
4
Ⅱ.有同学提出SO 与Ba(NO ) 溶液反应时,溶液中的溶解氧也有可能起到氧化作
2 3 2
用。设计如图所示实验装置探究溶液中 与O 氧化SO 的主导作用:
2 2
(4)下列实验均计时80秒,可以选择的试剂:0.1 mol/L Ba(NO ) 溶液、0.1 mol/L KNO
3 2 3
溶液、0.1 mol/LBaCl 溶液、0.2 mol/LBaCl 溶液
2 2
实验编号 步骤操作 pH变化
取25 mL煮沸过的0.1mol/LBa(NO ) 溶液,通入V
ⅰ 3 2 pH轻微减小
mLSO
2
ⅱ 取25 mL未煮沸的①______________,通入V mLSO pH减小2.5
2
ⅲ 取25 mL煮沸过的0.1 mol/LBaCl 溶液,通入V mLSO pH几乎不变
2 2
ⅳ 取25 mL未煮沸的②______________,通入V mLSO pH减小2
2
(5)由上述实验可得出:溶液中 与O 氧化SO 占主导作用的是__________ (填“
2 2
”或“O”)。
2
(6)写出在有氧气的条件下,SO 与BaCl 反应的离子方程式:
2 2
________________________。