文档内容
人教版 高中化学 选择性必修 第三册 知识点
第一章 有机化合物的结构特点与研究方法
一、有机化合物中碳原子的成键特点
1、碳原子有4个价电子,能与其他原子形成4个共价键,碳碳之间的结合
方式有单键、双键或三键;多个碳原子之间可以相互形成长短不一的碳
链和碳环,碳链和碳环也可以相互结合,所以有机物结构复杂,数量庞
大。
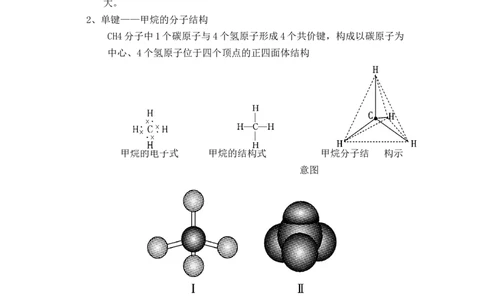
2、单键——甲烷的分子结构
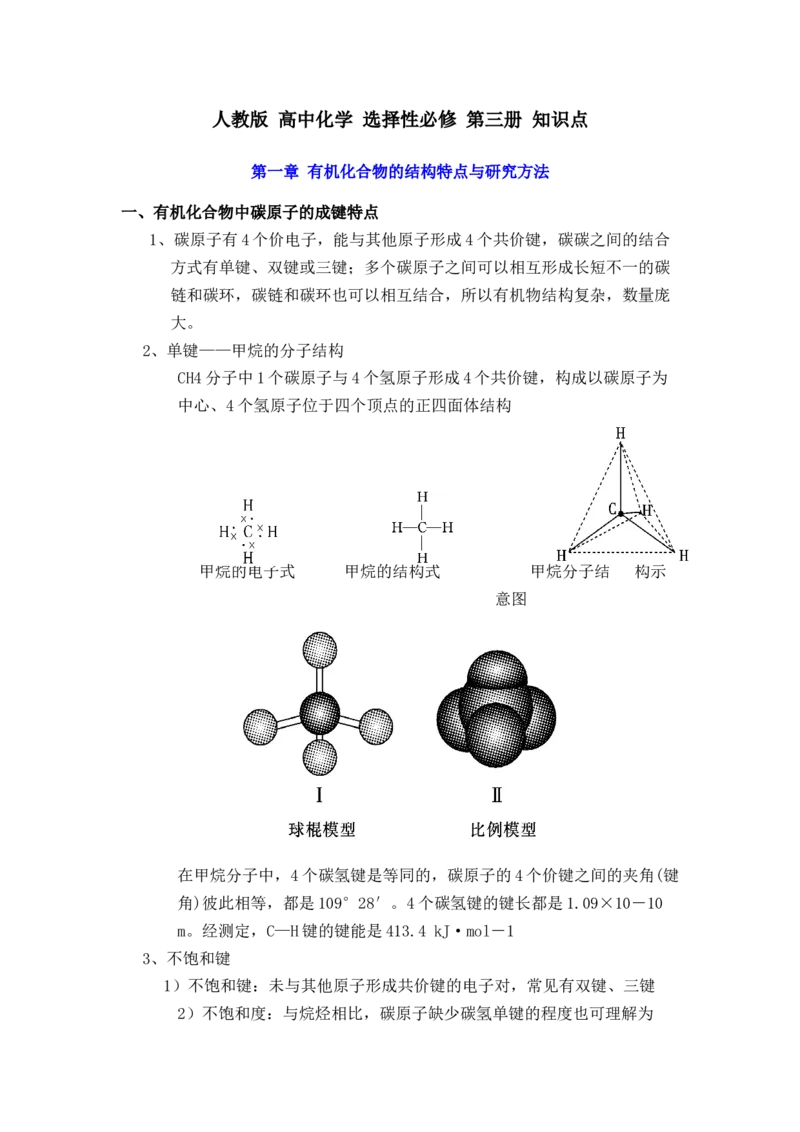
CH4分子中1个碳原子与4个氢原子形成4个共价键,构成以碳原子为
中心、4个氢原子位于四个顶点的正四面体结构
甲烷的电子式 甲烷的结构式 甲烷分子结 构示
意图
在甲烷分子中,4个碳氢键是等同的,碳原子的4个价键之间的夹角(键
角)彼此相等,都是109°28′。4个碳氢键的键长都是1.09×10-10
m。经测定,C—H键的键能是413.4 kJ·mol-1
3、不饱和键
1)不饱和键:未与其他原子形成共价键的电子对,常见有双键、三键
2)不饱和度:与烷烃相比,碳原子缺少碳氢单键的程度也可理解为缺氢程度
3)不饱和度(Ω)计算*
a、烃CxHy的不饱和度的计算
与碳原子以单键直连的卤族原子或无碳基视为氢原子
b、根据结构计算
一个双键或环相当于一个不饱和度
一个三键相当于两个不饱和度
一个碳氧双键相当于一个不饱和度
二 、有机化合物的同分异构现象
1、同分异构
化合物具有相同的分子式,但具有不同的结构的现象叫做同分异构。具
有同分异构现象的化合物互称为同分异构体。它是有机物种类繁多的重
要原因之一。同分异构体之间的转化是化学变化。同分异构体的特点是
分子式相同,结构不同,性质不同
2.同分异构的种类
(1)碳链异构:由于碳链骨架不同,产生的异构现象称为碳链异构。烷烃中的
同分异构体均为碳链异构。如有三种同分异构体,即正戊烷,异戊烷,新戊烷。
(2)位置异构:指官能团或取代基在碳链上的位置不同而造成的异构。如
1-丁烯与2-丁烯、1-丙醇与2-丙醇。
(3)官能团异构:指官能团不同而造成的异构,如乙醇和二甲醚,葡萄糖
和果糖。(4)其他异构:顺反异构、对映异构(也叫手性异构)等中学化学极少涉
及。
3.同分异构体的书写规律
(1)烷烃(只可能存在碳异构)的书写规律:主链由长到短,支链由整到
散,位置由心到边,排列临、间、对。
(2)按照碳链异构→位置异构→顺反异构→官能团异构的顺序书写,也可
按官能团异构→碳链异构→位置异构→顺反异构的顺序书写,不管按哪种方法
书写都必须防止漏写和重写。
(3)若遇到苯环上有三个取代基时,可先定两个的位置关系是邻或间或对,
然
后再对第三个取代基依次进行定位,同时要注意哪些是与前面重复的。
4.同分异构体数目的判断方法
(1)记忆法:
①凡只含一个碳原子的分子均无异构;
②丁烷、丁炔、丙基、丙有2种;
③戊烷、戊炔有3种;
④丁基、丁烯(包括顺反异构)、C8H10(芳烃)有4种;
⑤己烷、C7H8O(含苯环)有5种;
⑥C8H8O2的芳香酯有6种;
⑦戊基、C9H12(芳烃)有8种。
(2)基元法:将有机物看成由基团连接而成,由基团的异构数目可推断有
机物的异构体数目。例如:丁基有4种,丁醇、戊醛、戊酸都有4种。
(3)替代法将有机物中的不同原子或基团进行等同转换。
例如:一氯乙烷有一个氯原子,五个氢原子,一氯乙烷只有一种结构,
假设将氯乙烷中的Cl原子转换为H原子,而H原子转化为Cl原子,其情况和一
氯乙烷完全相同,故五氯乙烷也只有一种结构。(4)等效氢法:等效氢指在有机物分子中处于相同位置的氢原子。等效氢
任一原子若被相同取代基取代所得产物都为同一物质。判断方法有:
①同一碳原子上连接的氢原等效
②同一碳原子上接的-中H原子等效
③同一分子中处于轴对称位置的氢原子等效。
3、常见异类异构
具有相同C原子数的异类异构有:
a、烯烃与环烷烃(CnH2n)
b、炔烃、二烯烃和环烯烃(CnH2n-2)
c、苯的同系物、二炔烃和四烯烃等(CnH2n-6)
d、饱和一元醇和醚、烯醇和烯醚等(CnH2n+2O)
e、饱和一元醛和酮、烯醛和烯酮等(CnH2nO)
f、饱一元羧酸、饱和一元酯和饱和一元羟醛等(CnH2nO2)
g、苯酚同系物、芳香醇和芳香醚(CnH2n-6O)
h、氨基酸和硝基化合物(CnH2n+1NO2)
三 、有机化合物分子结构的表示方法
1、有机物结构的各种表示方法
种类 实例 含义
乙烯C2H4、 用元素符号表示物质分子组成的式子,可反映出一个
化学式
戊烷C5H12 分子中原子的种类和数目
最简式 乙烷CH3、 表示物质组成的各元素原子最简整数比的式子,由最
(实验式) 烯烃CH2 简式可求最简式量
乙烯
用“·”或“×”表示电子,表示分子中各原子最外
电子式
层电子成键情况的式子
乙烯
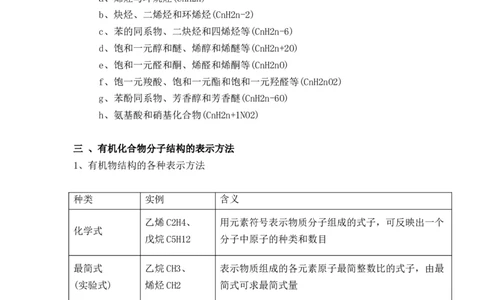
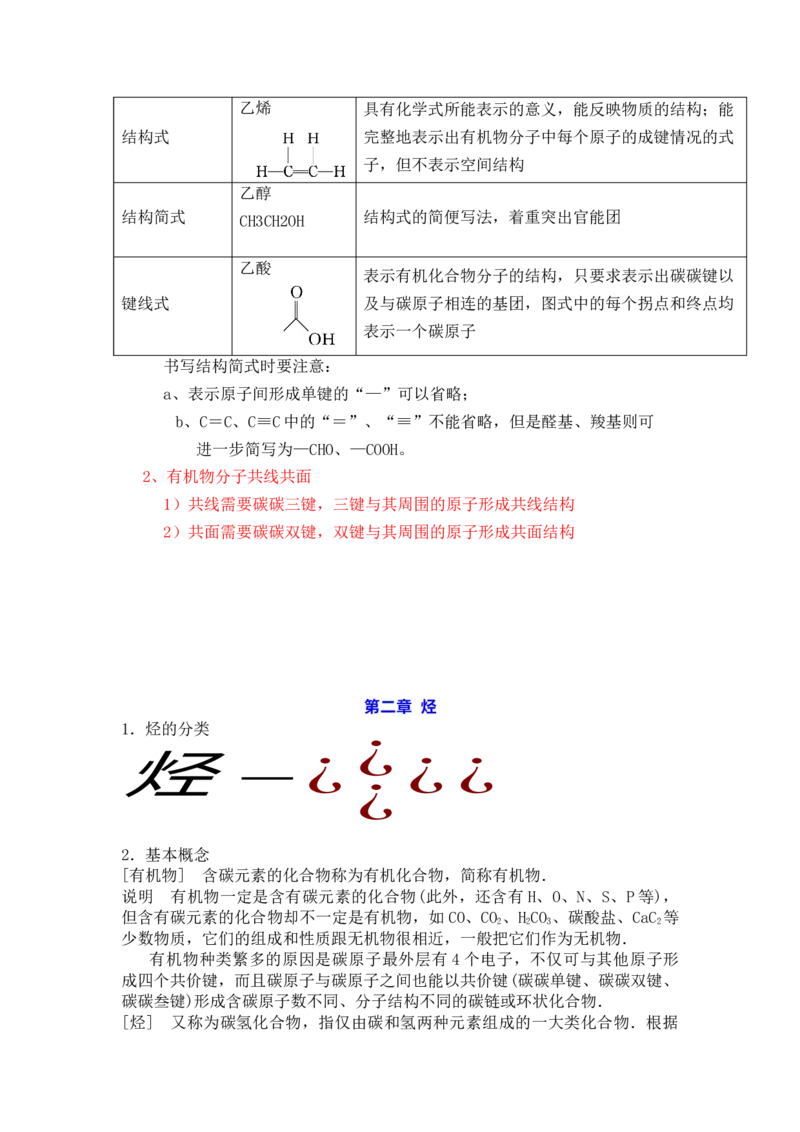
小球表示原子,短棍表示共价键,用于表示分子的空
球棍模型
间结构(立体形状)
用不同体积的小球表示不同的原子大小,用于表示分
比例模型
乙烯 子中各原子的相对大小及结合顺序乙烯 具有化学式所能表示的意义,能反映物质的结构;能
结构式 完整地表示出有机物分子中每个原子的成键情况的式
子,但不表示空间结构
乙醇
结构简式 结构式的简便写法,着重突出官能团
CH3CH2OH
乙酸
表示有机化合物分子的结构,只要求表示出碳碳键以
键线式 及与碳原子相连的基团,图式中的每个拐点和终点均
表示一个碳原子
书写结构简式时要注意:
a、表示原子间形成单键的“—”可以省略;
b、C=C、C≡C中的“=”、“≡”不能省略,但是醛基、羧基则可
进一步简写为—CHO、—COOH。
2、有机物分子共线共面
1)共线需要碳碳三键,三键与其周围的原子形成共线结构
2)共面需要碳碳双键,双键与其周围的原子形成共面结构
第二章 烃
1.烃的分类
¿
烃−¿ ¿ ¿
¿
2.基本概念
[有机物] 含碳元素的化合物称为有机化合物,简称有机物.
说明 有机物一定是含有碳元素的化合物(此外,还含有H、O、N、S、P等),
但含有碳元素的化合物却不一定是有机物,如CO、CO 、H CO 、碳酸盐、CaC 等
2 2 3 2
少数物质,它们的组成和性质跟无机物很相近,一般把它们作为无机物.
有机物种类繁多的原因是碳原子最外层有 4个电子,不仅可与其他原子形
成四个共价键,而且碳原子与碳原子之间也能以共价键(碳碳单键、碳碳双键、
碳碳叁键)形成含碳原子数不同、分子结构不同的碳链或环状化合物.
[烃] 又称为碳氢化合物,指仅由碳和氢两种元素组成的一大类化合物.根据结构的不同,烃可分为烷烃、烯烃、炔烃、芳香烃等.
[结构式] 用一根短线代表一对共用电子对,并将分子中各原子用短线连接起
来,以表示分子中各原子的连接次序和方式的式子.如甲烷的结构式为:
乙烯的结构式为:
H-C-H H H H-C=C-H
[结构简式] 将有机物分子的结构式中的“C—C”键和“C—H”键省略不写所
得的一种简式.如丙烷的结构简式为CH CH CH ,乙烯的结构简式
3 2 3
为CH =CH ,苯的结构简式为 等.
2 2
[烷烃] 又称为饱和链烃.指分子中碳原子与碳原子之间都以 C—C单键(即1
个共用电子对)结合成链状,且碳原子剩余的价键全部跟氢原子相结合的一类烃.
“烷”即饱和的意思.CH 、CH CH 、CH CH CH ……等都属于烷烃.烷烃中最简
4 3 3 3 2 3
单的是甲烷.
[同系物] 结构相似,在分子组成上相差一个或若干个CH 原子团的有机物,互
2
称同系物.
说明 判断有机物互为同系物的两个要点;①必须结构相似,即必须是同一类
物质.例如,碳原子数不同的所有的烷烃(或单烯烃、炔烃、苯的同系物)均互
为同系物.由于同系物必须是同一类物质,则同系物一定具有相同的分子式通
式,但分子式通式相同的有机物不一定是同系物.由于同系物的结构相似,因
此它们的化学性质也相似.②在分子组成上相差一个或若干个CH 原子团.由于
2
同系物在分子组成上相差CH 原子团的倍数,因此同系物的分子式不同.
2
由同系物构成的一系列物质叫做同系列(类似数学上的数列),烷烃、烯烃、炔
烃、苯的同系物等各自为一个同系列.在同系列中,分子式呈一定规律变化,
可以用一个通式表示.
[取代反应] 有机物分子里的原子或原子团被其他原子或原子团所代替的反应,
叫做取代反应.根据有机物分子里的原子或原子团被不同的原子或原子团[如-
X(卤原子)、-NO (硝基),-SO H(磺酸基),等等]所代替,取代反应又分为卤
2 3
代反应、硝化反应、磺化反应,等等.
①卤代反应.如:
CH + C1 → CH C1 + HCl(反应连续进行,可进一步生成CH C1 、CHCl 、CCl )
4 2 3 2 2 3 4
(一NO 叫硝基)
2
②硝化反应.如:
③磺化反应.如:(一SO H叫磺酸基)
3
[同分异构现象与同分异构体]
化合物具有相同的分子式,但具有不同的结构式的现象,叫做同分异构现象.
具有同分异构现象的化合物互为同分异构体.
说明 同分异构体的特点:①分子式相同,相对分子质量相同,分子式的通式
相同.但相对分子质量相同的化合物不一定是同分异构体,因为相对分子质量
相同时分子式不一定相同.同分异构体的最简式相同,但最简式相同的化合物
不一定是同分异构体,因为最简式相同时分子式不一定相同.②结构不同,即
分子中原子的连接方式不同.同分异构体可以是同一类物质,也可以是不同类
物质.当为同一类物质时,化学性质相似,而物理性质不同;当为不同类物质
时,化学性质不同,物理性质也不同.[烃基] 烃分子失去一个或几个氢原子后剩余的部分.烃基的通式用“R-”表
示.例如:-CH (甲基)、-CH CH (乙基)、-CH=CH (乙烯基)、-C H 或f 今
3 2 3 2 6 5
胃(苯基)等.烷基是烷烃分子失去一个氢原子后剩余的原子团,其通式为-
CnH2n+1.烃基是含有未成对电子的原子团,例如,
-CH 的电子式为
3
1 mol-CH 中含有9 mol电子.
3
[不饱和烃] 分子里含有碳碳双键(C=C)或碳碳叁键(C≡C)的烃,双键碳原子
或叁键碳原子所结合的氢原子数少于烷烃分子中的氢原子数,还可再结合其他
的原子或原子团.不饱和烃包括烯烃、炔烃等.
[加成反应] 有机物分子里的双键或叁键两端的碳原子与其他原子或原子团直
接结合生成新的化合物的反应,叫做加成反应.
说明 加成反应是具有不饱和键的物质的特征反应.不饱和键上的两个碳原子
称为不饱和碳原子,加成反应总是发生在两个不饱和碳原子上.加成反应能使
有机分子中的不饱和碳原子变成饱和碳原子.烯烃、炔烃、苯及其同系物均可
发生加成反应,例如:
(1,2-二溴乙烷)
(1,2-二溴乙烯)
(1,1,2,2-四溴乙烷)
[聚合反应] 聚合反应又叫做加聚反应.是由相对分子质量小的化合物分子(即
单体)互相结合成相对分子质量大的高分子(即高分子化合物)的反应.
说明 加聚反应是合成高分子化合物的重要反应之一.能发生加聚反应的物质
一定要有不饱和键.加聚反应的原理是不饱和键打开后相互连接成很长的链.
例如:
(聚乙烯)
(聚氯乙烯)
[烯烃] 分子中含有碳碳双键(C=C键)的一类不饱和烃.根据烃分子中所含碳
碳双键数的不同,烯烃又可分为单烯烃(含一个C=C键)、二烯烃(含两个C=C
键)等.烯烃中最简单的是乙烯.
[炔烃] 分子中含有碳碳叁键(C≡C键)的一类不饱和烃.炔烃中最简单的是乙
炔.
[芳香烃] 分子中含有一个或多个苯环的碳氢化合物,叫做芳香烃,简称芳烃.
苯是最简单、最基本的芳烃.
[石油的分馏] 是指用蒸发和冷凝的方法把石油分成不同沸点范围的蒸馏产物
的过程.
说明 ①石油的分馏是物理变化;②石油的分馏分为常压分馏和减压分馏两种
常压分馏是指在常压(1.0l×l05Pa)时进行的分馏,主要原料是原油,主要产品
有溶剂油、汽油、煤油、柴油和重油.减压分馏是利用“压强越小,物质的沸
点越低”的原理,使重油在低于常压下的沸点就可以沸腾,而对其进一步进行
分馏.
[石油的裂化和裂解] 裂化是在一定条件下,将相对分子质量较大、沸点较高
的烃断裂为相对分子质量较小、沸点较低的烃的过程.在催化剂作用下的裂化,
又叫做催化裂化.例如:C16H34 C8H18 + C8H16
裂解是采用比裂化更高的温度,使石油分馏产品中的长链烃断裂成乙烯、丙烯
等短链烃的加工过程.裂解是一种深度裂化,裂解气的主要产品是乙烯.
[煤的干馏] 又叫做煤的焦化.是将煤隔绝空气加强热使其分解的过程.
说明 ①煤的干馏是化学变化;
②煤干馏的主要产品有焦炭、煤焦油、焦炉气(主要成分为氢气、甲烷等)、粗
氨水和粗苯.
[煤的气化和液化]
(1)煤的气化.
①概念:把煤中的有机物转化为可燃性气体的过程.
②主要化学反应: C(s) + O (g) CO (g)
2 2
⑧煤气的成分、热值和用途比较:
煤气种类 低热值气 中热值气 高热值气(合成天然气)
CO + 3H C H +
生成条件 碳在空气中燃烧 碳在氧气中燃烧 2 4
H O
2
CO、H 、相当量
成 分 2 CO、H 、少量CH 主要是CH
的N 2 4 4
2
热值较高,可短
距离输送.可用
热值较低.用作
特点和用 作居民使用的煤 热值很高,可远距离输
冶金、机械工业
途 气,也可用作合 送
的燃料气
成氨、甲醇的原
料等
(2)煤的液化.
①概念:把煤转化成液体燃料的过程.
②煤的液化的途径:
a.直接液化:把煤与适当的溶剂混合后,在高温、高压下(有时还使用催化剂),
使煤与氢气作用生成液体燃料.
b.间接液化:如图3—11—1所示.
3.烷烃、烯烃的命名
[烷烃的命名]
①习惯命名法.当烷烃分子中所含碳原子数不多时,可用习惯命名法.其命名
步骤要点如下:a.数出烷烃分子中碳原子的总数.碳原子总数在10以内的,
从1~10依次用甲、乙、丙、丁、戊、己、庚、辛、壬、癸来表示.b.当烷烃
分子中无支链时,用“正”表示,如:CH3CH2CH2CH3叫正丁烷;当烷烃分子中
含“CHa--CH--”结构时,用
②系统命名法.
步骤:a.选主链.选择支链最多且含碳原子数最多的碳链作主链,并称“某
烷”;b.定起点.选择离最简单的支链(即含碳原子数最少)最近的一端作为主
链的起点,并使取代基的编号数之和最小;c.取代基,写在前,注位置,短线
连;d.相同取代基要合并.不同取代基,不论其位次大小如何,简单在前,复杂在后.
[烯烃的命名] 在给烯烃命名时,要始终注意到C=C键所在的位置:①选择含
有C=C在内的最长碳链作主链(注:此时主链上含碳原子数不一定最多);②从
离C=C键最近的一端开始给主链碳原子编号;⑧在“某烯”字样前用较小的阿
拉伯数字“1、2…”给烯烃编号.其余与烷烃的命名方法相同.例如:
CH3--CHz--'<3--<3H2--K3H3
,l
CHc
其名称为2—乙基—l—丁烯.
4.同分异构体的有关知识
[同分异构体的熔点、沸点高低的规律]
①当为脂肪烃的同分异构体时,支链越多(少),沸点越低(高);②当为含两个
侧链的苯的同系物时,侧链相隔越远(近),沸点越高(低).
[同分异构体的种类]
①有机物类别异构,???如烷烃与烯烃为两类不同的有机物;②碳链异构(苯
环上有邻、间、对位三种异构);③官能团位置异构(在“烃的衍生物”中将学
习到).
[同分异构体的书写规律]
①同分异构体的书写规律:要准确、完全地写出同分异构体,一般按以下顺序
规律进行书写:类别异构 + 碳链异构一位置异构.
②碳链异构(烷烃的同分异构体)的书写技巧:a.先写出不含支链的最长碳链;
b.然后写出少1个碳原子的主链,将余下的1个碳原子作支链加在主链上,并
依次变动支链位置;c.再写出少2个碳原子的主链,将余下的2个碳原子作为
一个乙基或两个甲基加在主链上,并依次变动其位置(注意不要重复);d.以此
类推,最后分别在每个碳原子上加上氢原子,使每个碳原子有4个共价键.
说明 a.从上所述可归纳为:从头摘、挂中间,往端移、不到边,先甲基、后
乙基,先集中、后分散,变换位、不能同.b.在书写烯烃或炔烃的同分异构体
时,只要在碳链异构的基础上依次变动碳碳双键或碳碳叁键位置即可.
[烃的同分异构体种数的确定方法]
①等效氢法.烃分子中同一种类的氢原子称为等效氢原子.有机分子中有
几种不等效氢原子,其氢原子被一种原子或原子团取代后的一取代物就有几种
同分异构体.
等效氢原子的一般判断原则:a.位于同一碳原子上的H原子为等效H原子.
如CH 中的4个H原子为等效H原子.b.位于同一C原子上的甲基上的H原子为
4
等效H原子.如新戊烷(CH ) C上的12个H原子为等效H原子.c.同一分子中
3 4
处于对称位置或镜面对称位置上的 H原子为等效H原子.对于含苯环结构的分
子中等效H原子的种数的判断,应首先考虑苯环所在平面上是否有对称轴,若
没有,则还应考虑是否有垂直于苯环平面的对称轴存在,然后根据对称轴来确
定等效H原子的种数.
②换元法.换元法是要找出隐含在题目中的等量关系,并将所求对象进行
恰当地转换.例如,已知正丁烷的二氯代物有6种同分异构体,则其八氯代物
的同分异构体有多少种?正丁烷C H 。的二氯代物的分子式为 C H Cl ,八氯代
4 10 4 8 2
物的分子式为C H Cl ,变换为C Cl H ,很显然,两者的同分异构体数是相同的,
4 2 8 4 8 2
均为6种.[同分异构体与同位素、同素异形体、同系物的比较]
同位素 同素异形体 同系物 同分异构体
适用对
原子 单质 有机物 有机物
象
①结构相似的同一类
①分子式相同②结构
判断依 ①原子之间②质子数 ①单质之间②属于同 物质②符合同一通式
不同③不一定是同类
据 相同,中子数不同 一种元素 ③相对分子质量不同
物质
(相差14n)
化学性质相似;物理
化学性质可能相似,
化学性质相同;物理 化学性质相同;物理 性质不同(熔点、沸
性 质 也可能不同;物理性
性质有差异 性质不同 点、密度呈规律性变
质不同
化)
红磷与白磷;金刚石 甲烷与乙烷;乙烯与 戊烷有正、异、新戊
实 例 H、T、D
与石墨 丙烯 烷三种
5.甲烷、乙烯、乙炔及苯的比较
烃的种
甲 烷 乙 烯 乙 炔 苯
类
分子式 CH C H C H C H
4 2 4 2 2 6 6
结构简
CH =CH CH≡CH
式 2 2
直线形,键角为
平面结构,键角为 平面正六边形,键
正四面体,键角为 180°,分子中所
120°,分子中所 角为120°,分子
109°28′,由极 有的原子均处于同
有的原子均处于同 中6个碳原于完全
分子结 性键形成的非极性 一直线上(也必处
一平面内.分子中 相同(6个碳键的键
构特点 分子.与C原子共 于同一平面内).
含C—H极性键和C 长、键能、键角相
平面的H原子最多 分子中含C—H极
—C非极性键.是 同).12个原子均
只有2个 性键和C—C非极
非极性分子 处于同一平面上
性键
无色、有特殊气味
的液体,有毒,不
无色、无味的气 无色、稍有气味的 纯乙炔是五色、无
物理性 溶于水,密度比水
体,极难溶于水, 气体,难溶于水, 味的气体,密度比
质 小,熔点、沸点
密度比空气小 密度比空气略小 空气小,微溶于水
低.用冰冷却苯,
苯凝结为无色晶体
含碳的
质
75 85.7 92 92
量分
数%
燃烧现 火焰较明亮,带黑
火焰不明亮 火焰明亮,带浓烟 火焰明亮,带浓烟
象 烟兼有烷烃和烯烃的
①性质稳定,不能
性质:①取代反
与强酸、强碱、酸
应.与X 发生卤代
性KMnO 溶液反 化学性质活泼①加 化学性质活泼①加 2
4 反应,与浓HNO 发
应;②与纯X 发生 成反应:与X 、 成反应:与X 、 3
2 2 2 生硝化反 应,
一系列取代反应, HX、H 、H O等加 HX、H 、H O等加
2 2 2 2 与 浓H SO 发生磺
化学性 生成CH X、 成,能使溴水褪色 成,能使溴水褪 2 4
3 化反应;②加成反
质 CH X 、CHX 、CX 的 ②氧化反应:能使 色.如:
2 2 3 4 应.例如在催化剂
混合物;③热分 酸性KMnO 溶液褪 ②氧化反应:能使
4 Ni和加热的条件
解:9u 高温 色③加聚反应: 酸性KMnO 溶液褪
4 下,苯与H 加成得
—(隔绝空气)— nCH =CH 催化剂 色 2
2 2 到环己烷:③苯不
C+2H2(注:X为卤
能使酸性KMnO 溶
素) 4
液褪色
工业制
煤的干馏 石油裂解 煤的干馏
法
主要用 气体燃料,制炭 合成酒精,制聚乙 氧炔焰,制氯乙烯 合成纤维、橡胶、
途 黑、氯仿等 烯等 等 染料等
5.甲烷、乙烯、乙炔及苯的比较
6.烷烃、烯烃、炔烃及苯的同系物的比较
烃 的
烷 烃 烯 烃 炔 烃 苯的同系物
类别
分子
CnH2n+2 CnH2n CnH2n-2 CnH2n-6
式通
(n≥1) (n≥2) (n≥2) (n≥6)
式
分子中C原子间均 分子中含C=C 分子中含C≡C 分子中只含一个苯
分子 以C-C单键连接 键,其中的一个键 键,其中有两个键 环,苯环的侧链是
结构 成链状;碳链为锯 键能较低,易断 键能较低,易断 烷基(CnH2n-),
特点 齿形;C-C键可旋 裂;C=C键不能旋 裂,C≡C键不能旋 苯环与侧链相互影
转 转 转 响
①加成反应 ①取代反应
主要 ①取代反应 ①加成反应
化学 ②加聚反应 ②加成反应
反应 ②裂化反应 ②氧化反应
③氧化反应 ③氧化反应
碳碳
键的
C-C>苯环中的碳碳键>C=C>C≡C
键长
比较
物理
①常温时,烃分子中碳原子数≤4个时为气体;②烃不溶于水,气态或液态烃的
性质
密度比水小(浮在水面上),③各类烃中,随分子中碳原子数增多,熔点、沸点升
的规
高,密度增大
律
7.烃的基本实验
[甲烷与氯气的取代反应]①反应原理:
(一氯甲烷)
(二氯甲烷)
(氯仿)
(四氯化碳)
②实验现象及解释:
a.量筒内壁中出现油状液体(生成的CH Cl 、CHCl 、CCl 为不溶于水的液体);
2 2 3 4
b.量筒内水面上升(反应后气体总体积减小且生成的HCl气体易溶于水);
c.水槽中有晶体析出(生成的HCl气体溶于水后使NaCl溶液过饱和).
③应注意点:a.不要将混合气体放在日光直射的地方,以免引起爆炸;b.反
应产物是两种气体(HCl、CH Cl)和三种液体(CH Cl 、CHCl 、CCl )的混合物.
3 2 2 3 4
[乙烯的实验室制法]
①反应原理:
CH CH OH CH=CH ++H O
3 2 2 2
②所需主要仪器和用品:酒精灯,圆底烧瓶,温度计,双孔橡胶塞,碎瓷片.
③发生装置:液+液二 气体型装置.与制C1 、HCl气体的发生装置相似,只
2
需将制C1 、HCl气体装置中的分液漏斗改为温度计即可.
2
④收集方法:排水法(不能用排空气法,因为乙烯与空气的密度很接近).
⑤反应液中无水酒精与浓H SO 的体积比为1∶3.应首先向烧瓶中加入酒精,再
2 4
慢慢地注入浓H SO (类似于浓H SO 加水稀释)。使用过量浓H SO ,可提高乙烯
2 4 2 4 2 4
的产率,增加乙烯的产量.
⑥浓H SO 的作用:催化剂和脱水剂.
2 4
⑦温度计水银球放置位置:必须插入反应液中(以准确测定反应液的温度).
⑧发生的副反应:
2CH CH OH C H OC H + H O
3 2 2 5 2 5 2
(乙醚)
因此,在实验室加热制乙烯时,应迅速使温度上升到170℃,以减少乙醚的生
成,提高乙烯的产量。
C H OH + 4H SO (浓)= 4SO ↑+ CO ↑+ C↓+ 7H O
2 5 2 4 2 2 2
在加热过程中,反应液的颜色由无色变为棕色,甚至变为黑褐色.这是因为浓
H SO 具有强氧化性,将部分乙醇氧化为炭.由于有上述两个副反应发生,所以
2 4
在制得的乙烯中会混有CO 、SO 等杂质气体,其中SO 也能使酸性KMnO 溶液或
2 2 2 4
溴水褪色,因此,在做乙烯的性质实验之前,应首先将气体通过碱石灰或碱液
以除去SO .
2
⑨在圆底烧瓶中加入碎瓷片的目的:防止液体受热时产生暴沸.
[乙炔的实验室制法]
①反应原理:CaC + 2H O → Ca(OH) ↓ + CH≡CH↑
2 2 2
②装置:固 + 液 → 气体型装置,与制H 、CO 等气体的发生装置相同.用排
2 2
水集气法收集乙炔.
③所需主要仪器;分液漏斗,平底烧瓶(或大试管、广口瓶、锥形瓶等),双孔
橡胶塞.
④不能用启普发生器的原因:a.碳化钙与水的反应较剧烈,使用启普发生器难
于控制反应速率;b.反应过程中放出大量热,易使启普发生器炸裂;c.反应生成的Ca(OH) 为浆状物,易堵塞导管.
2
⑤注意事项:a.为减缓反应速率,得到平稳的乙炔气流,可用饱和 NaCl溶液
代替水,用块状电石而不用粉末状的电石.b.为防止反应产生的泡沫堵塞导管,
应在导气管口附近塞上少量棉花.c.电石中混有CaS、Ca P 等杂质,它们也跟
3 2
水反应生成H S、
2
PH 等气体,因此,用电石制得的乙炔(俗称电石气)有特殊臭味.把混有上述混
3
合气体的乙炔气通过盛有CuSO 溶液的洗气瓶,可除去H S、PH 等杂质气体.
4 2 3
[石油的分馏]
①原理:根据石油中所含各种烃的沸点不同,通过加热和冷凝的方法,将石油
分为不同沸点范围的蒸馏产物.
②使用的玻璃仪器:酒精灯,蒸馏烧瓶(其中有防止石油暴沸的碎瓷片),温度
计,冷凝管,尾接管,锥形瓶.
③温度计水银球位置:蒸馏烧瓶支管口(用以测定蒸气的温度).
④冷凝管中水流方向:由下往上(原因:水能充满冷凝管,水流与蒸气流发生对
流,起到充分冷凝的效果).
⑤注意点:a.加热前应先检查装置的气密性.b.石油的分馏是物理变化.c.
石油的馏出物叫馏分,馏分仍然是含有多种烃的混合物.
8.有关烃的计算类型
[烃的分子式的确定方法]
①先求烃的最简式和相对分子质量,再依;(最简式的相对分子质量)n=相对分
子质量,求得分子式.
说明 a.已知C、H元素的质量比(或C、H元素的质量分数,或燃烧产物的量),
均可求出该烃的最简式.
b.求有机物相对分子质量的常见公式:
▲有机物的摩尔质量=m/n
分子中某元素原子个数×相对原子质量
有机物的摩尔质量=
或 该元素的质量分数
▲气态有机物的相对分子质量=标准状况下该气体密度×22.4
▲ 有机物混合气体的平均相对分子质量=W总/n总
0 0
或=M 1 ⋅x 1 0 +M 2 ⋅x 2 0 + ……
▲通过相对密度求算:M =D·M ,即ρ /ρ =M /M .
未知 已知 A B A B
注:①也可先求出相对分子质量,再根据各元素的质量分数和相对分子质量直
接求得分子式.
②依各类烃的通式和相对分子质量(或分子中所含电子的总数)求算.
③商余法:烃的相对分子质量/12 → 商为C原子数,余数为H原子数.
注意 一个C原子的质量等于12个H原子的质量.
C H C H
例 某烃的相对分子质量为128,则该烃的分子式为 9 20或 10 8.
④平均值法:平均值法适用于混合烃的有关计算,它是根据各组分的某种平均
值来推断烃分子式的解题方法.平均值法特别适用于缺少数据而不能直接求解
的计算.平均值法有:平均摩尔质量法、平均碳原子法、平均氢原子法和平均
分子式法等.[烃的燃烧计算]
①烃燃烧的通式.
a.完全燃烧时(O 充足):CxHy + (x +y/4)O →xCO + y/ 2H O
2 2 2 2
b.不完全燃烧时(O 不充足):
2
a+x y
+
CxHy + ( 2 4 )O →aCO + (x−a)CO + y/ 2H O
2 2 2
②不同烃完全燃烧时耗O 量的比较.
2
x+y
a.物质的量相同时:( 4)的值愈大,耗O 量愈多.
2
b,质量相同时:
CH y y
y
▲将CxHy变换为
x
则 x值越大(小),耗O
2
量越多(少); x值相同,耗O
2
量相同.
▲最简式相同,耗 O 量相同.最简式相同的有:(CH)n——C H 与 C H 等;
2 2 2 6 6
(CH )n——烯烃与环烷烃.
2
c.最简式相同的烃,不论以何种比例混合,只要混合物的总质量一定,则耗 O
2
量一定.
③烃完全燃烧时,烃分子中 H原子数与反应前后气体的物质的量(或压强或体
积)的关系.
a.t≥100℃时(水为气体):
CxHy(g) + (x+y/4)O →xCO (g) + y/ 2H O(g)
2 2 2
1 (x+y/4) x y/ 2
∵V =1+x+y/4 V =x +y/ 2 ∴V -V =1-y/4
前 后 前 后
当V =V 时,y=4;
前 后
当V >V 时,y<4;
前 后
当V <V 时,y>4;
前 后
由此可见,烃CxHy完全燃烧前后气体体积的变化只与烃分子中的 H原子数有关,
而与C原子数无关(因此,在计算烃完全燃烧时,要验算耗O 量).
2
规律:
▲若燃烧前后气体的体积不变,
则y=4.具体的烃有CH 、C H 、C H 及其混合物.
4 2 4 3 4
▲若燃烧后气体的体积减小,则y<4.只有C H 符合这一情况.
2 2
▲若燃烧后气体的体积增大,则y>4.用体积增量法来求算具体是哪一种烃.
b.t<100℃时(水为液体):
反应后气体的体积较反应前恒减小,用体积减量法确定具体的CxHy:
CxHy(g) + (x+y/4)O →xCO (g) + y/ 2H O(aq) 气体体积减少
2 2 2
2 (x+y/4) x 1+y/4第三章 烃的衍生物
1.烃的衍生物
[烃的衍生物的比较]
分子结构特
类别 官能团 分 类 主要化学性质
点
①取代反应(水解反应):
①氟烃、氯烃、溴 R-X+H O
2
卤 碳-卤键(C 烃;②一卤烃和多 R-OH + HX
卤原子
代 - X) 有 极 卤烃; ③饱和卤 ②消去反应:
(-X)
烃 性,易断裂 烃、不炮和卤烃和 R-CH -CH X + NaOH
2 2
芳香卤烃
RCH=H + NaX + H O
2 2
①取代反应:
a.与Na等活泼金属反应;b.与HX反
①脂肪醇(包括饱
应,c.分子间脱水;d.酯化反应
和醇、不饱和
②氧化反应:
- OH 在 非 醇);②脂环醇(如
醇 苯环碳原子 环己醇)③芳香醇 2R-CH OH + O
2 2
上 (如苯甲醇),④一 2R-CHO+2H O
2
均为羟基 元醇与多元醇(如 ③消去反应,
(-OH) 乙二醇、丙三醇)
CH CH OH
3 2
CH =H ↑+ H O
2 2 2
- OH 直 接 ①易被空气氧化而变质;②具有弱酸
连在苯环碳 性③取代反应
一元酚、二元酚、
酚 原上.酚类
三元酚等
中均含苯的 ④显色反应
结构
①加成反应(与H 加成又叫做还原反
2
①脂肪醛(饱和醛
分子中含有 应):R-CHO+H R-CH OH
醛基 和不饱和醛);② 2 2
醛 醛基的有机 ②氧化反应:a.银镜反应;b.红色
(-CHO) 芳香醛;③一元醛
物 沉淀反应:c.在一定条件下,被空气
与多元醛
氧化
①脂肪 酸与芳香 ①具有酸的通性;②酯化反应
酸;②一元酸与多
分子中含有
羧基 元酸;③饱和羧酸
羧酸 羧基的有机
(-COOH) 与不饱和羧酸;④
物
低级脂肪酸与高级
脂肪酸
水解反应:
①饱和一元酯:
RCOOR′+ H O
2
羧 CnH2n+lCOOCmH2m+
酯基 (R 为烃基或 RCOOH + R'OH
酸 1
H RCOOR′+ NaOH
酯 ②高级脂肪酸甘油
原子,R′ RCOONa + R'OH
酯③聚酯④环酯
只 能 为 烃 (酯在碱性条件下水解较完全)
基)
2.有机反应的主要类型
反应类型 定 义 举例(反应的化学方程式)有机物在一定条件下,从
C H OH CH =H ↑+ H O
一个分子中脱去一个小分 2 5 2 2 2
消去反应 子(如H O、HBr等)而生成
2
不饱和(含双键或叁键)化
合物的反应
苯酚与含 Fe3+的溶液作
苯酚的显色反
用,使溶液呈现紫色的反
应
应
CH≡CH + H CH =H
2 2 2
有机物分子得到氢原子或
还原反应 CH =H + H CH CH
失去氧原子的反应 2 2 2 3 3
R—CHO + H R-CH OH
2 2
燃烧或被
2CH CH OH + O 2CH CHO + 2H O
空气中的 3 2 2 3 2
氧
O 氧化 2CH CHO + O 2CH COOH
2 3 2 3
化 有机物分子得到氧原子或
CH CHO + 2Ag(NH ) OH
反 银镜反应 失去氢原子的反应 3 3 2
CH COONH +2Ag↓+ 3NH ↑+ H O
应 3 4 3 2
红色沉淀 CH CHO + 2Cu(OH) CH COOH + Cu O↓+
3 2 3 2
反应 2H O
2
在NaOH水溶液的条件下, R-CH X + H O RCH OH + HX
卤代烃的 2 2 2
卤代烃与水作用,生成醇
水解反应
和卤化氢的反应
取
酸(无机含氧酸或羧酸)与
代 RCOOH + R'CH OH
酯化反应 醇作用,生成酯和水的反 2
反 RCOOCH R′+ H O
应 2 2
应
在酸或碱存在的条件下, RCOOR′+ H O RCOOH + R'OH
酯的水解 2
酯与水作用生成醇与酸的 RCOOR′+ NaOH → RCOONa + R'OH
反应
反应
3.同分异构体的有关知识
[同分异构体的熔点、沸点高低的规律]
①当为脂肪烃的同分异构体时,支链越多 ( 少 ) ,沸点越低 ( 高 ) ;②当为含两个
侧链的苯的同系物时,侧链相隔越远 ( 近 ) ,沸点越高 ( 低 ) .
[同分异构体的书写规律]
①同分异构体的书写规律:要准确、完全地写出同分异构体,一般按以下顺序
规律进行书写:类别异构 + 碳链异构一位置异构.
②碳链异构(烷烃的同分异构体)的书写技巧:a.先写出不含支链的最长碳链;
b.然后写出少1个碳原子的主链,将余下的1个碳原子作支链加在主链上,并
依次变动支链位置;c.再写出少2个碳原子的主链,将余下的2个碳原子作为
一个乙基或两个甲基加在主链上,并依次变动其位置(注意不要重复);d.以此
类推,最后分别在每个碳原子上加上氢原子,使每个碳原子有4个共价键.
说明 a.从上所述可归纳为:从头摘、挂中间,往端移、不到边,先甲基、后
乙基,先集中、后分散,变换位、不能同.b.在书写烯烃或炔烃的同分异构体
时,只要在碳链异构的基础上依次变动碳碳双键或碳碳叁键位置即可.
[烃的同分异构体种数的确定方法]
①等效氢法.烃分子中同一种类的氢原子称为等效氢原子.有机分子中有
几种不等效氢原子,其氢原子被一种原子或原子团取代后的一取代物就有几种同分异构体.
等效氢原子的一般判断原则:a.位于同一碳原子上的H原子为等效H原子.
如CH 中的4个H原子为等效H原子.b.位于同一C原子上的甲基上的H原子为
4
等效H原子.如新戊烷(CH ) C上的12个H原子为等效H原子.c.同一分子中
3 4
处于对称位置或镜面对称位置上的 H原子为等效H原子.对于含苯环结构的分
子中等效H原子的种数的判断,应首先考虑苯环所在平面上是否有对称轴,若
没有,则还应考虑是否有垂直于苯环平面的对称轴存在,然后根据对称轴来确
定等效H原子的种数.
②换元法.换元法是要找出隐含在题目中的等量关系,并将所求对象进行
恰当地转换.例如,已知正丁烷的二氯代物有6种同分异构体,则其八氯代物
的同分异构体有多少种?正丁烷C H 。的二氯代物的分子式为 C H Cl ,八氯代
4 10 4 8 2
物的分子式为C H Cl ,变换为C Cl H ,很显然,两者的同分异构体数是相同的,
4 2 8 4 8 2
均为6种.
4.烷烃、烯烃、炔烃及苯的同系物的比较
烃的类 烷 烃 烯 烃 炔 烃 苯的同系物
别
分子式 CnH2n+2 CnH2n CnH2n-2 CnH2n-6
通式
(n≥1) (n≥2) (n≥2) (n≥6)
分子中 C 原子间 分子中含 C=C 分 子 中 含 C≡ C 分子中只含一个苯环,
均以 C-C 单键连 键,其中的一个 键,其中有两个键 苯环的侧链是 烷基
分子结
接成链状;碳链 键键能较低,易 键能较低,易断 (CnH2n-),苯环与侧
构特点
为锯齿形;C-C 断裂;C=C键不 裂,C≡C键不能旋 链相互影响
键可旋转 能旋转 转
①加成反应 ①取代反应
主要化 ①取代反应 ①加成反应
②加聚反应 ②加成反应
学反应
②裂化反应 ②氧化反应
③氧化反应 ③氧化反应
碳碳键
的键长 C-C>苯环中的碳碳键>C=C>C≡C
比较
物理性 ①常温时,烃分子中碳原子数≤4个时为气体;②烃不溶于水,气态或液态烃的密
质的规 度比水小(浮在水面上),③各类烃中,随分子中碳原子数增多,熔点、沸点升高,
律 密度增大
5.有关烃的计算类型
[烃的分子式的确定方法]
①先求烃的最简式和相对分子质量,再依;(最简式的相对分子质量)n=相对分
子质量,求得分子式.
说明 a.已知C、H元素的质量比(或C、H元素的质量分数,或燃烧产物的量),
均可求出该烃的最简式.
b.求有机物相对分子质量的常见公式:
▲有机物的摩尔质量=m/n
分子中某元素原子个数×相对原子质量
有机物的摩尔质量=
或 该元素的质量分数
▲气态有机物的相对分子质量=标准状况下该气体密度×22.4
▲ 有机物混合气体的平均相对分子质量=W总/n总0 0
或=M 1 ⋅x 1 0 +M 2 ⋅x 2 0 + ……
▲通过相对密度求算:M =D·M ,即ρ /ρ =M /M .
未知 已知 A B A B
注:①也可先求出相对分子质量,再根据各元素的质量分数和相对分子质量直
接求得分子式.
②依各类烃的通式和相对分子质量(或分子中所含电子的总数)求算.
③商余法:烃的相对分子质量/12 → 商为C原子数,余数为H原子数.
注意 一个C原子的质量等于12个H原子的质量.
C H C H
例 某烃的相对分子质量为128,则该烃的分子式为 9 20或 10 8.
子法、平均氢原子法和平均分子式法等.
[烃的燃烧计算]
①烃燃烧的通式.
a.完全燃烧时(O 充足):CxHy + (x +y/4)O →xCO + y/ 2H O
2 2 2 2
b.不完全燃烧时(O 不充足):
2
a+x y
+
CxHy + ( 2 4 )O →aCO + (x−a)CO + y/ 2H O
2 2 2
②不同烃完全燃烧时耗O 量的比较.
2
x+y
a.物质的量相同时:( 4)的值愈大,耗O 量愈多.
2
b,质量相同时:
CH y y
y
▲将CxHy变换为
x
则 x值越大(小),耗O
2
量越多(少); x值相同,耗O
2
量相同.
▲最简式相同,耗 O 量相同.最简式相同的有:(CH)n——C H 与 C H 等;
2 2 2 6 6
(CH )n——烯烃与环烷烃.
2
c.最简式相同的烃,不论以何种比例混合,只要混合物的总质量一定,则耗 O
2
量一定.
③烃完全燃烧时,烃分子中 H原子数与反应前后气体的物质的量(或压强或体
积)的关系.
a.t≥100℃时(水为气体):
CxHy(g) + (x+y/4)O →xCO (g) + y/ 2H O(g)
2 2 2
1 (x+y/4) x y/ 2
∵V =1+x+y/4 V =x +y/ 2 ∴V -V =1-y/4
前 后 前 后
当V =V 时,y=4;
前 后
当V >V 时,y<4;
前 后
当V <V 时,y>4;
前 后
由此可见,烃CxHy完全燃烧前后气体体积的变化只与烃分子中的 H原子数有关,
而与C原子数无关(因此,在计算烃完全燃烧时,要验算耗O 量).
2
规律:
▲若燃烧前后气体的体积不变,
则y=4.具体的烃有CH 、C H 、C H 及其混合物.
4 2 4 3 4
▲若燃烧后气体的体积减小,则y<4.只有C H 符合这一情况.
2 2
▲若燃烧后气体的体积增大,则y>4.用体积增量法来求算具体是哪一种烃.b.t<100℃时(水为液体):
反应后气体的体积较反应前恒减小,用体积减量法确定具体的CxHy:
CxHy(g) + (x+y/4)O →xCO (g) + y/ 2H O(aq) 气体体积减少
2 2 2
2 (x+y/4) x 1+y/4
6.有机物的分离和提纯方法
(1)有机物的分离与提纯的原则:分离是把混合物各组分经过化学变化而设法分
开,得到混合前的物质.提纯是除去物质中混有的少量杂质.
①加入试剂时,不容易引入新的杂质;
②所用试剂最好只与杂质起反应,而不与所需提纯的物质起反应;
③反应后的其他生成物必须和所需提纯的物质易分离;
④有机物的分离与提纯不能用合成转化的方法.
(2)常见有机物的分离、提纯方法:
①洗气法.将气体混合物中的杂质气体用溶液吸收除去.例如,除去气态烷烃
中混有的气态烯烃(或炔烃),可将混合气体通过盛有溴水的洗气瓶.
②分液法.根据有机物在水中的溶解性、酸碱性等性质上的差异,把两种相互
混溶的有机物中的一种转变为可溶于水的物质,另一种仍不溶于水,从而达到
分离与提纯的目的.a.若杂质易溶于水而被提纯物不溶于水,则直接加入水后
用力振荡,使杂质转入水层中,用分液漏斗分离.b.若杂质与被提纯物都不溶
于水,则先使杂质与某种试剂反应,使其转化为易溶于水的物质后再分离.
③蒸馏(分馏)法.
a.对沸点差别大的有机物,可直接进行蒸馏提纯与分离;
b.混合物中各组分的沸点相差不大时,则加入某种物质,使其中一种组分转化
为高沸点、难挥发性物质后再进行蒸馏.例如,分离乙醇与乙酸的混合液时,
先向其中加入固体NaOH,使乙酸转化生成高沸点的CH COONa,蒸馏出乙醇后,
3
再加入浓H SO ,使CH COONa转化为CH COOH,再经蒸馏得到乙酸.
2 4 3 3第四章 生物大分子
生物大分子的组成特点及多样性的原因:
名称 基本单位 化学通式 聚合方式 多样性的原因
①葡萄糖数目不同
多糖 葡萄糖 ②糖链的分支不同
C H O
6 12 6 ③化学键的不同
①氨基酸数目不同
②氨基酸种类不同
R
蛋白质 氨基酸 脱水缩合 ③氨基酸排列次序不
NH C COOH 同
2
④肽链的空间结构
H
①核苷酸数目不同
核酸
②核苷酸排列次序不
(DNA和 核苷酸
同
RNA)
③核苷酸种类不同
生物大分子的结构与功能:
物质结构与性能的关系间题, 是辩证思维的重要命题之一。而分子生物学
正是研究生物大分子的各种结构—化学结构、几何空间结构及分子内部各基因
相互作用的本质与其宏观的化学性质、物理性质及生物学活性间相互联系的科
学。经典的化学结构理论指出物质的内部结构完全决定了它的典型化学反应性
能, 同时也决定了许多其它方面的性能反过来, 通过这些典型化学性能的研究,
原则上也能定出化学结构, 甚至主体结构的一些轮廓蛋白质分子是由 20种氨基
酸构成的, 但氨基酸和蛋白质的性能有很大的差别, 蛋白质分子具有运输、保
护、运动、催化等生命物质的功能。比如, 血红蛋白是机体血液中运输氧气的
蛋白, 组成皮肤的胶原蛋白, 具有保护作用。 肌肉的运动是靠肌球蛋白和肌动
蛋白的滑动来实现,肌体中成千上万种的生理生化反应是靠一种特殊的蛋白质—
酶来催化等, 而氨基酸分子则没有这些功能, 这说明当分子与分子以某种分工
结合时, 就会表现出原有的分子不曾有的崭新性质和功能, 绝不是它的组成成
份简单的加和。再如, 核酸是由四种核昔酸构成, 核苷酸是小分子物质, 并不
表现出任何生命物质的特征, 一且这些小分子结合成核酸分子, 其性质就出现
了从无生命物质向生命物质的飞跃。氨基酸和蛋白质、核昔酸和核酸的结构与功能的不同, 是由组成大分子的
小分子的数量、连接方式及小分子间的相互作用引起的, 蛋白质分子中, 由于
个别氨基酸的改变或排列顺序的差异, 就可影响其肽链的折叠, 从而影响其生
物功能。DNA分子中,若有一个核苷酸发生改变, 或增、减一个核苷酸, 就可引
起基因突变, 使生物的某些特性或性状发生改变例如, 镰刀型贫血病,是由于病
人血红素分子β-链的第六位谷氨酸被撷氨酸代替所引起的, 这种氨基酸的改
变归根到底是由于编码这种蛋白质的基因突变引起的, 结果使患者的红血球在
氧气缺乏时呈镰刀状, 易胀破发生溶血, 运氧机能降低, 引起头昏、胸闷等贫
血症状。
生物大分子的结构有平面结构和立体结构, 象蛋白质在完成其生物功能时
一般是以立体构象存在的,若加上某些变性因子, 使其立体结构变成线型的平面
结构, 则生物功能就完全丧失。如蛋白质在溶液中若温度上升到60℃以上, 生
物活性便逐渐丧失, 直至完全丧失。在蛋白质分子构象研究中发现, 具备三级
结构的蛋白质分子都具有近似球形或椭球状的物理外形, 常称它们为球蛋白。
球蛋白的分子结构有一些规律:(1)球蛋白结构组织具有严密的层次体系:一
级结构,二级结构,超二级结构,三级结构,四级结构。(2)结构具有明显的
择优性, 这表现在每个层次上。最低层次的择优性表现在L一氨基酸占绝对优
势;二级结构的螺旋全是右手的,β一折叠大部分是反平行的; 四级结构具有
明显的对称组合优势, 蛋白质分子结构具有择优性这样一个重要特点, 与生命
现象作为物质高级运动形式趋于有序化密切相关。(3)所有球蛋白结构都有一
疏水内核, 并且密堆积成致密的球状结构。这种结构对蛋白质折叠的能力学研
究和结构预测具有重要意义。(4)高度的专一性与高度灵活性的协调统一。现
已测出来的结构都显示出, 同类蛋白质分子, 具有基本相同的三级结构特征。
不同种类的蛋白质分子, 具有完全不同的三级结构特征,但另一方面, 对同一
蛋白质的不同状态的结构研究表明,在正常生理过程中, 这种高度专一的三级结
构并不一成不变的, 而是发生一些构象变化。如血红蛋白在与氧的结合过程中,
其分子的三、四级结构都要发生改变, 在第一个氧与血红蛋白结合后, 使分子
的构象发生改变, 有利于第二个氧与血红蛋白结合, 同样第二个氧结合后, 分
子结合第三、第四个氧的能力就增加, 这是蛋白质分子高度专一性与高度灵活
性协调统一的表现。以上可以看出, 任何物质系统的结构, 都是空间结构随时间而变化, 是空
间结构和时间结构的统一,稳定结构和可变结构的统一。物质系统的结构, 是系
统具有整体性和层次性的基础和前提。
物质系统的结构, 往往总是与其功能紧密联系的。功能是物质系统所具有
的, 在内部与外部关系中表现出来的行为特性、作用、能力和功效等。结构与
功能的关系是结构是功能的基础, 功能是结构的表现。但结构与功能又是相互
对立、相互作用的, 即不是单值对应, 有同构异功, 异构同功等情形。生物大
分子正是从辩证的角度反应了结构与功能的关系, 如在动物体内某些生化过
程中, 蛋白质分子的某些肽链链必须先按特定的方式断裂, 然后才呈现生物活
性, 这是蛋白质分子的结构与功能高度统一性的表现。在酶的调节控制中, 比
较早就发现了许多酶都有一个无活性的前体, 经专一的水解酶作用切去一肽段,
而转变成有活力的物质。象胰蛋白酶的前体在肠激酶的作用下, 从氨基末端切
掉六个氨基酸残基, 才变成具有生活性的胰蛋白酶。另外,生物大分子在执行其
生物功能时, 其结构是在不断地发生变化的。如酶在作用于底物时, 受底物的
诱导, 酶的构象就要发生变化, 使酶变得适宜与底物结合, 从而作用于底物,
这也是结构与功能高度统一的表现但在酶分子中有同功酶, 这些酶能够催化同
一种化学反应, 而酶蛋白本身的分子结构、组成都有所不同。象乳酸脱氢酶同
功酶, 它们的分子结构各不相同, 但都能进行催化反应, 这是异构同功现象。
在机体内, 一般的酶所催化的反应都是可逆的, 既可催化正反应的进行, 也可
催化逆反应的进行, 说明酶的功能不是一种,具有同构异功作用。这充分说明结
构与功能不是单值决定的。
从上述可以看出, 结构与功能本来就是相通的,结构通过系统包含了功能,
功能也通过系统包含了结构。在一定条件下, 结构变化之因含导致功能变化之
果, 同样, 功能变化之因亦必导致结构变化之果。
第五章 合成高分子
一、有机高分子化合物
1.概念:由许多小分子化合物通过共价键结合成的,相对分子质量很高(104~106)的一类化合物。
2.特点
(1)相对分子质量很大,由于高分子化合物都是混合物,其相对分子质量只是一
个平均值。
(2)合成原料都是低分子化合物。
(3)每个高分子都是由若干个重复结构单元组成的。
3.与高分子化合物有关的概念
(1)单体:能够进行聚合反应形成高分子化合物的低分子化合物。
(2)链节:高分子化合物中化学组成相同、可重复的最小单位。
(3)聚合度:高分子链中含有链节的数目,通常用n表示。
(4)聚合物的平均相对分子质量=链节的相对质量×n。
有机高分子化合物与低分子有机物的区别
有机高分子化合物 低分子有机物
相对分子质量 高达10000以上 1000以下
相对分子质量的数值 平均值 明确数值
分子的基本结构 若干重复结构单元组成 单一分子结构
性质 物理、化学性质有较大差别
二、加成聚合反应
1.概念:一定条件下,由含有不饱和键的化合物分子以加成反应形式结合成高
分子化合物的反应,简称加聚反应。
2.常见的加聚反应
(1)丙烯酸加聚
(1)加聚反应的特点①单体必须是含有双键、三键等不饱和键的化合物。例如,烯、二烯、炔、醛
等含不饱和键的有机物。
②发生加聚反应的过程中没有副产物(小分子化合物)产生,只生成高聚物。
③聚合物链节的化学组成跟单体的化学组成相同,聚合物的相对分子质量为单
体相对分子质量的整数倍。
(2)加聚产物的书写
加聚反应本质上是加成反应,在书写加聚产物时要把原来不饱和碳上的原子或
原子团看作支链,写在主链的垂直位置上。如:
方法点拨——加聚产物确定单体的方法
(1)凡链节的主链只有两个碳原子(无其他原子)的聚合物,其合成单体必为一种,
将两个半键闭合即可。
(2)凡链节的主链有四个碳原子(无其他原子),且链节无双键的聚合物,其单体
必为两种,在正中央划线断开,然后两个半键闭合即可。
(3)凡链节的主链中只有碳原子,并存在碳碳双键结构的聚合物,其规律是“有
双键,四个碳;无双键,两个碳”,划线断开,然后将半键闭合即单双键互换。
三、缩合聚合反应
1.概念:一定条件下,具有两个或多个官能团的单体相互结合成高分子化合物,
同时有小分子(如H2O、NH3、HCl等)生成的反应称为缩合聚合反应,简称缩聚
反应。
2.常见的缩聚反应
(1)羟基酸缩聚
(3)氨基酸缩聚(1)缩聚反应的特点
①缩聚反应的单体通常是具有双官能团(如—OH、—COOH、—NH2、—X及活泼
氢原子等)或多官能团的小分子。
②缩聚反应生成聚合物的同时,还有小分子副产物(如H2O、NH3、HCl等)生成。
③所得聚合物链节的化学组成与单体的化学组成不同。
(2)书写缩聚反应方程式及产物的注意事项
①书写缩聚物的结构简式时,要在方括号外侧写出链节余下的端基原子或原子
团,而加聚物的端基不确定,通常用横线“—”表示。如
方法点拨——缩聚产物单体的推断
(1)若链节中含有以下结构,HO—ROH、 ,其单
体 必 为 一 种 , 如 HO— CH2CH2OH 的 单 体 为 HO— CH2CH2— OH ,
的单体为 ,方法是去中括号和n即
为单体。
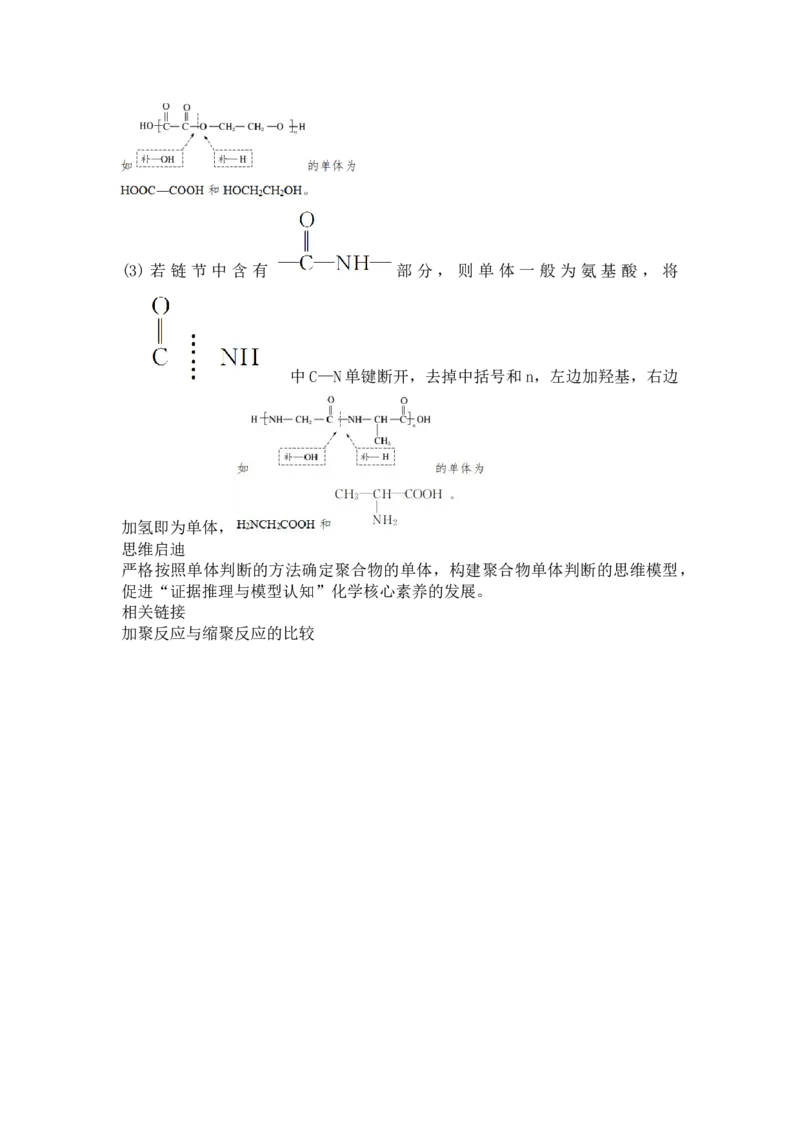
(2)若链节中含有 部分,则单体一般为氨基酸,将 中C—O
单 键 断 开 , 去 掉 中 括 号 和 n , 左 边 加 羟 基 , 右 边 加 氢 即 为 单 体 ,(3) 若 链 节 中 含 有 部 分 , 则 单 体 一 般 为 氨 基 酸 , 将
中C—N单键断开,去掉中括号和n,左边加羟基,右边
加氢即为单体,
思维启迪
严格按照单体判断的方法确定聚合物的单体,构建聚合物单体判断的思维模型,
促进“证据推理与模型认知”化学核心素养的发展。
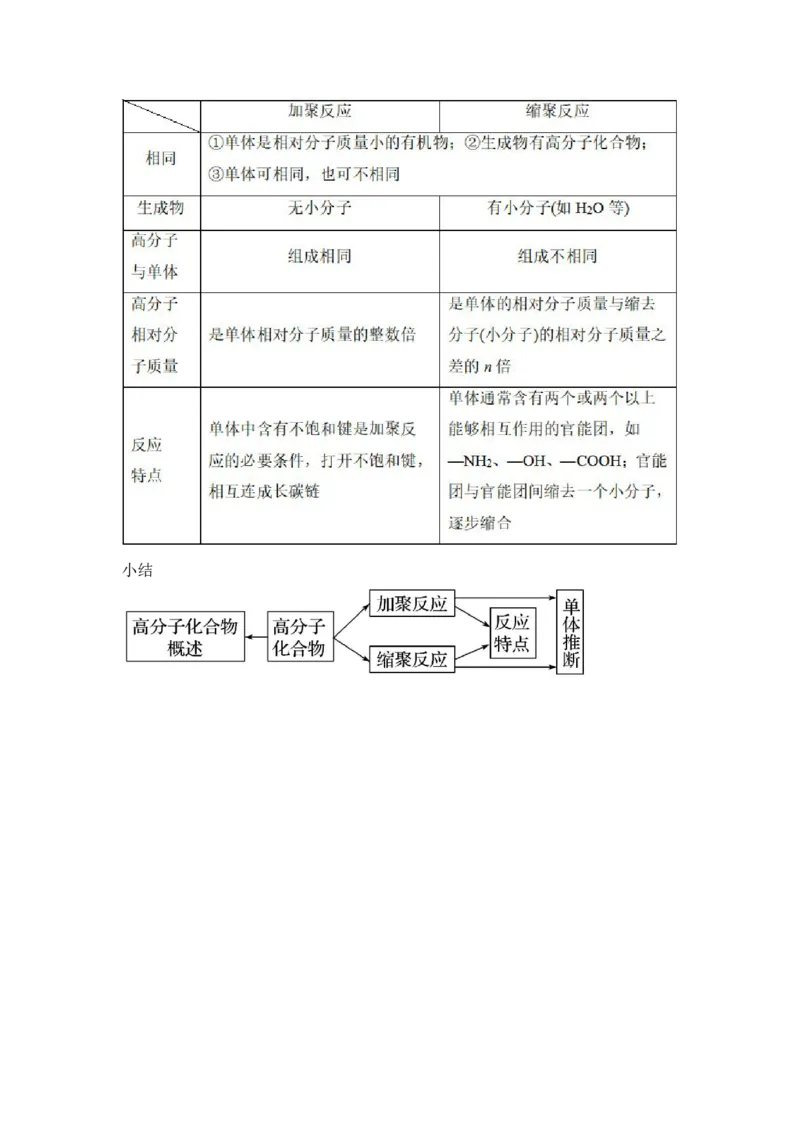
相关链接
加聚反应与缩聚反应的比较小结