文档内容
2022-2023 学年上学期期末考试模拟卷(一)
高二化学
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 K-39 Mn-55
一、单项选择题:本题共16小题。每小题3分,共48分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.实施垃圾分类,节约使用资源是社会文明水平的重要体现,废旧铅蓄电池属于
A.厨余垃圾 B.可回收物
C.有害垃圾 D.其他垃圾
2.物质的变化伴随能盘的变化,下列属于吸热反应的是
A.氢原子和氯原子形成 键 B.生石灰吸水
C.镁条与稀盐酸反应 D.木炭与水反应生成CO和H
2
3.下列离子方程式正确的是
A.碳酸钠水解:
B.硫氢化钠水解:
C.制 胶体:
D.硫酸铝溶液与偏铝酸钠溶液反应:
4.一定温度下,对于可逆反应N (g)+3H (g) 2NH (g)(正反应放热)的下列叙述,不能说明反应已达化
2 2 3
学平衡状态的是
A.恒容容器内混合气体的密度不再变化
B.NH 的生成速率与H 的生成速率之比为2∶3
3 2
C.恒压容器内混合气体的总物质的量不再变化
D.单位时间内断裂amolN≡N键,同时断裂6amolN—H键
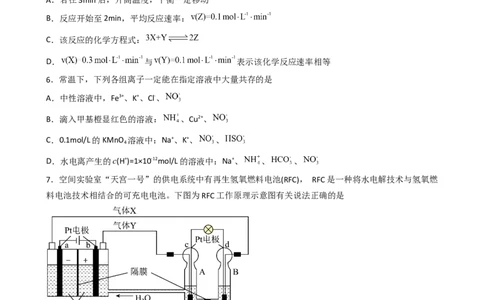
5.某温度下,在2L恒容密闭容器中,X、Y、Z三种气态物质的物质的量变化曲线如图所示,下列有关说
法中错误的是
学学科科网网((北北京京))股股份份有有限限公公司司A.若在3min后,升高温度,平衡一定移动
B.反应开始至2min,平均反应速率:
C.该反应的化学方程式:
D. 与 表示该化学反应速率相等
6.常温下,下列各组离子一定能在指定溶液中大量共存的是
A.中性溶液中,Fe3+、K+、Cl-、
B.滴入甲基橙显红色的溶液: 、Cu2+、
C.0.1mol/L的KMnO 溶液中:Na+、K+、 、
4
D.水电离产生的c(H+)=1×10-12mol/L的溶液中:Na+、 、 、
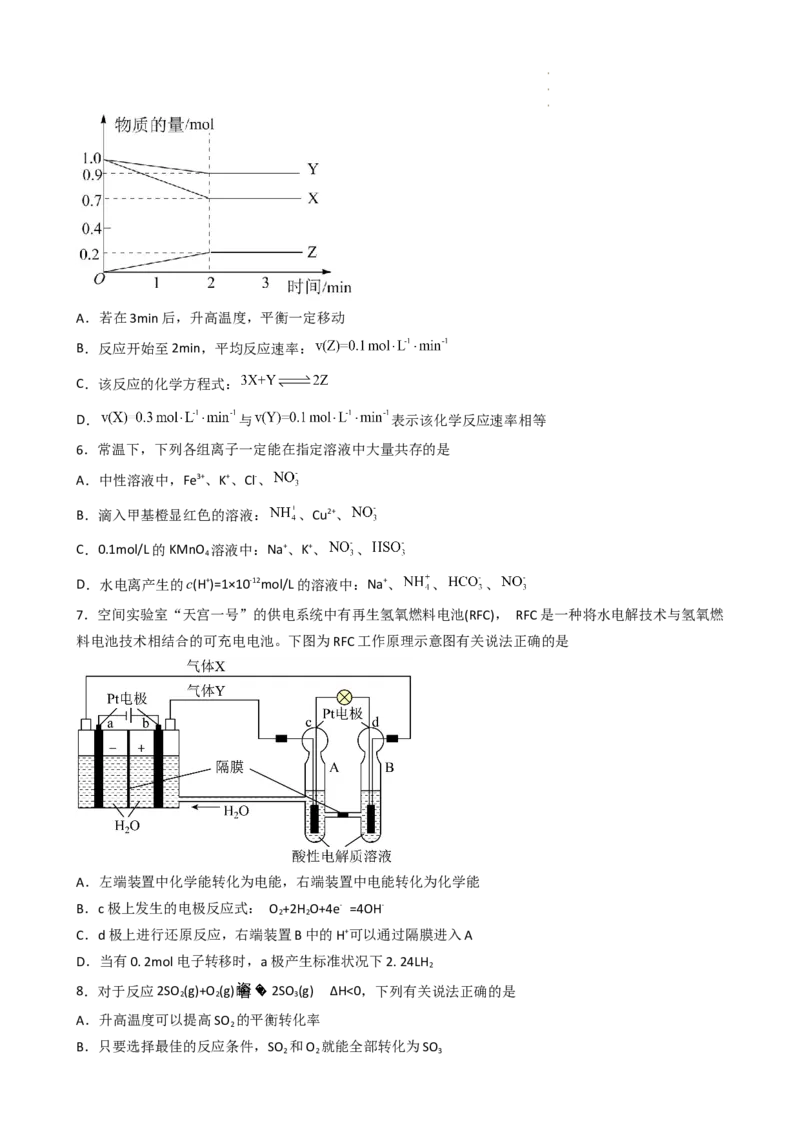
7.空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC), RFC是一种将水电解技术与氢氧燃
料电池技术相结合的可充电电池。下图为RFC工作原理示意图有关说法正确的是
A.左端装置中化学能转化为电能,右端装置中电能转化为化学能
B.c极上发生的电极反应式: O +2H O+4e- =4OH-
2 2
C.d极上进行还原反应,右端装置B中的H+可以通过隔膜进入A
D.当有0. 2mol电子转移时,a极产生标准状况下2. 24LH
2
8.对于反应2SO (g)+O (g) 2SO (g) ΔH<0,下列有关说法正确的是
2 2 3
A.升高温度可以提高SO 的平衡转化率
2
B.只要选择最佳的反应条件,SO 和O 就能全部转化为SO
2 2 3
学学科科网网((北北京京))股股份份有有限限公公司司C.加入催化剂可以降低反应的活化能,增加活化分子百分数
D.提高 的值可增大O 的转化率
2
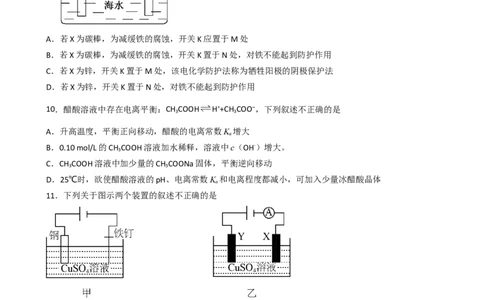
9.利用如图装置模拟铁的电化学防护。下列说法正确的是
A.若X为碳棒,为减缓铁的腐蚀,开关K应置于M处
B.若X为碳棒,为减缓铁的腐蚀,开关K置于N处,对铁不能起到防护作用
C.若X为锌,开关K置于M处,该电化学防护法称为牺牲阳极的阴极保护法
D.若X为锌,开关K置于N处,对铁不能起到防护作用
10.醋酸溶液中存在电离平衡:CH COOH H++CH COO⁻,下列叙述不正确的是
3 3
A.升高温度,平衡正向移动,醋酸的电离常数K 增大
a
B.0.10 mol/L的CH COOH溶液加水稀释,溶液中c(OH-)增大。
3
C.CH COOH溶液中加少量的CH COONa固体,平衡逆向移动
3 3
D.25℃时,欲使醋酸溶液的pH、电离常数K 和电离程度都减小,可加入少量冰醋酸晶体
a
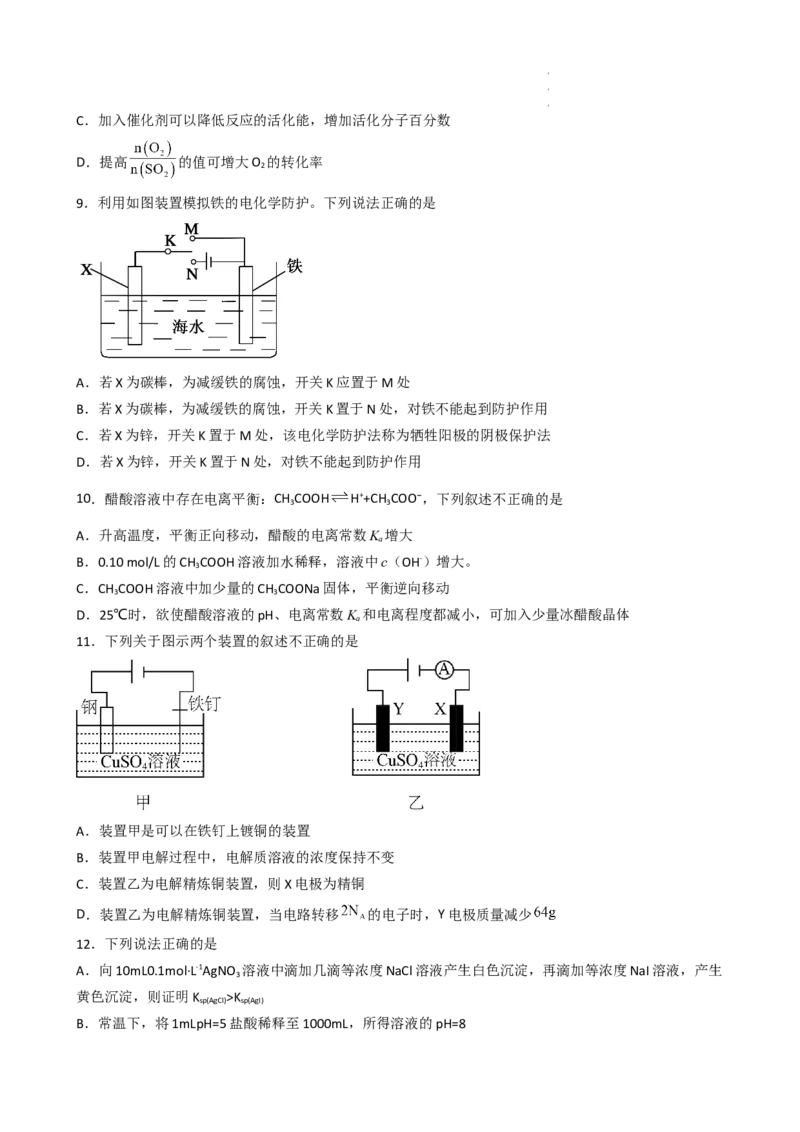
11.下列关于图示两个装置的叙述不正确的是
A.装置甲是可以在铁钉上镀铜的装置
B.装置甲电解过程中,电解质溶液的浓度保持不变
C.装置乙为电解精炼铜装置,则X电极为精铜
D.装置乙为电解精炼铜装置,当电路转移 的电子时,Y电极质量减少
12.下列说法正确的是
A.向10mL0.1mol·L-1AgNO 溶液中滴加几滴等浓度NaCl溶液产生白色沉淀,再滴加等浓度NaI溶液,产生
3
黄色沉淀,则证明K >K
sp(AgCl) sp(AgI)
B.常温下,将1mLpH=5盐酸稀释至1000mL,所得溶液的pH=8
学学科科网网((北北京京))股股份份有有限限公公司司C.常温下,pH=2的盐酸和醋酸,c(H+)前者大于后者
D.常温下,当水电离出的c(H+)为1×10-13mol·L-1时,此溶液的pH可能为1或13
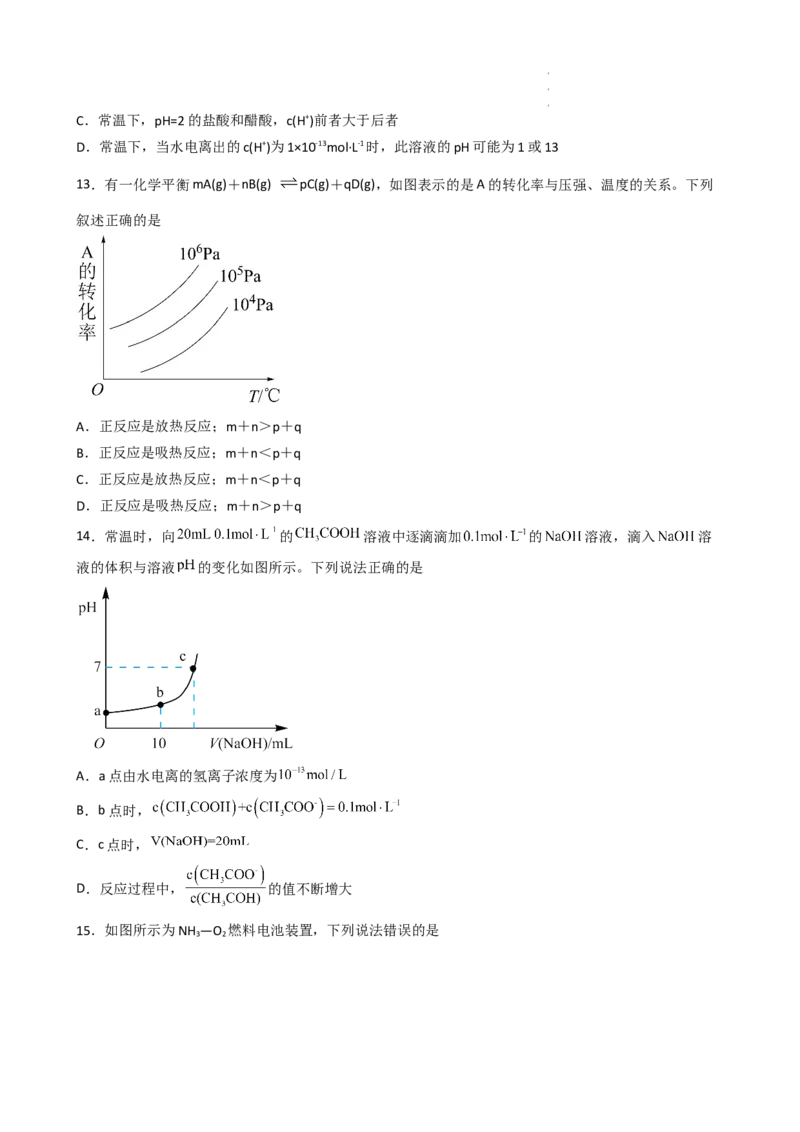
13.有一化学平衡mA(g)+nB(g) pC(g)+qD(g),如图表示的是A的转化率与压强、温度的关系。下列
叙述正确的是
A.正反应是放热反应;m+n>p+q
B.正反应是吸热反应;m+n<p+q
C.正反应是放热反应;m+n<p+q
D.正反应是吸热反应;m+n>p+q
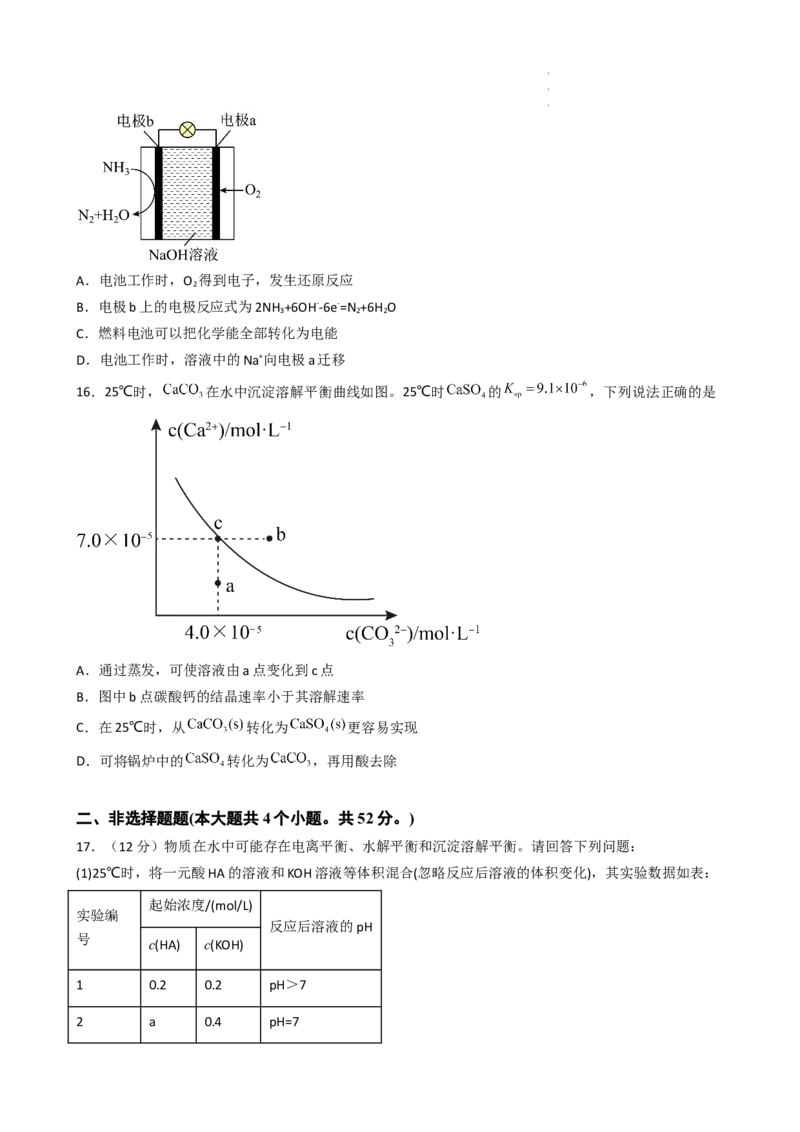
14.常温时,向 的 溶液中逐滴滴加 的 溶液,滴入 溶
液的体积与溶液 的变化如图所示。下列说法正确的是
A.a点由水电离的氢离子浓度为
B.b点时,
C.c点时,
D.反应过程中, 的值不断增大
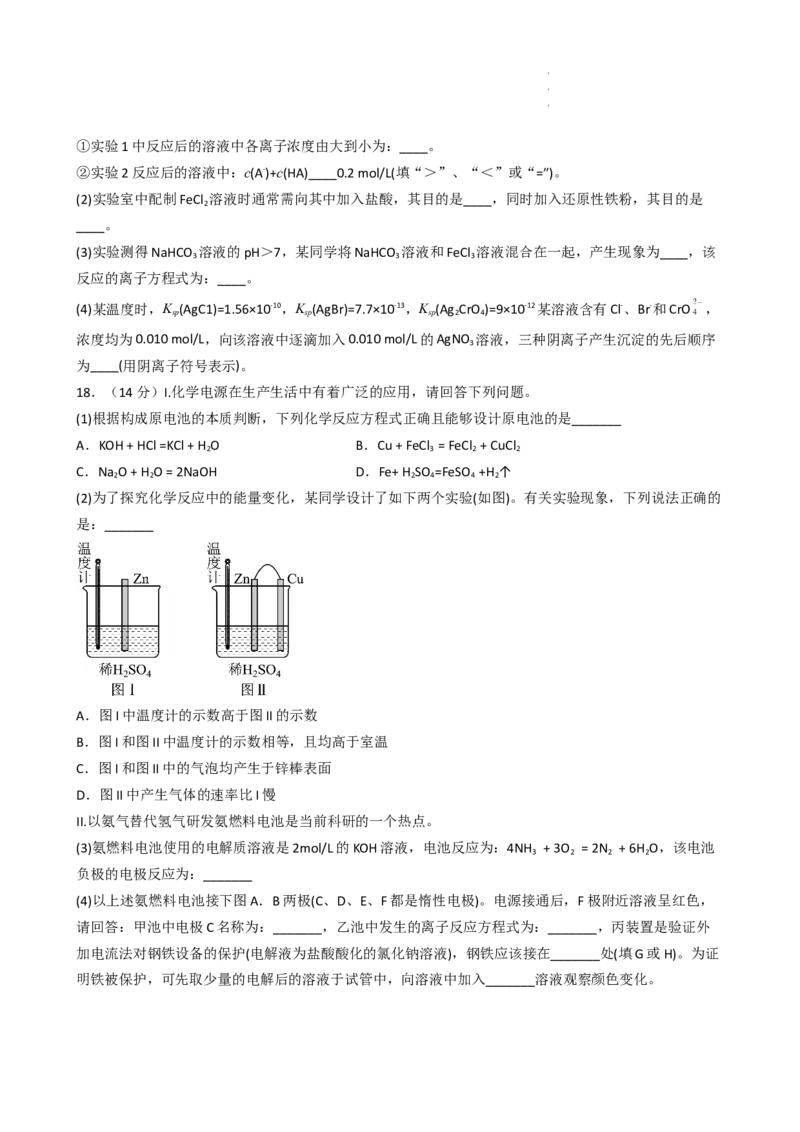
15.如图所示为NH —O 燃料电池装置,下列说法错误的是
3 2
学学科科网网((北北京京))股股份份有有限限公公司司A.电池工作时,O 得到电子,发生还原反应
2
B.电极b上的电极反应式为2NH +6OH--6e-=N +6H O
3 2 2
C.燃料电池可以把化学能全部转化为电能
D.电池工作时,溶液中的Na+向电极a迁移
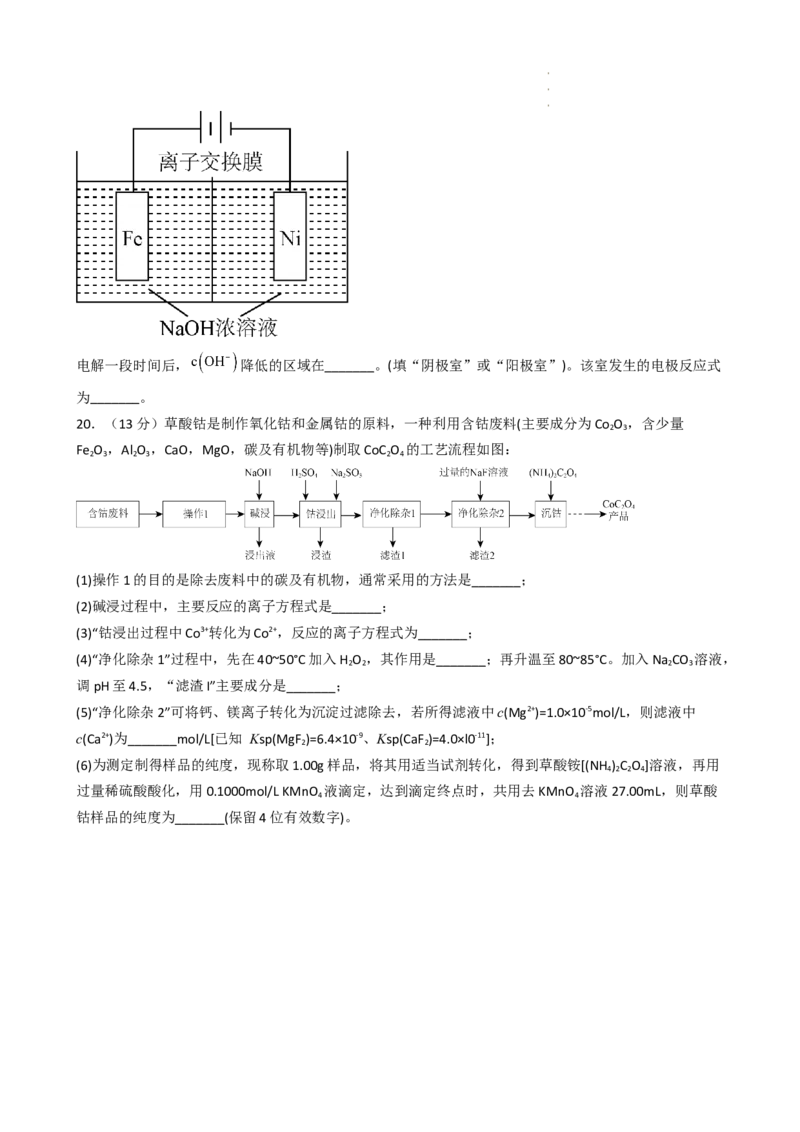
16.25℃时, 在水中沉淀溶解平衡曲线如图。25℃时 的 ,下列说法正确的是
A.通过蒸发,可使溶液由a点变化到c点
B.图中b点碳酸钙的结晶速率小于其溶解速率
C.在25℃时,从 转化为 更容易实现
D.可将锅炉中的 转化为 ,再用酸去除
二、非选择题题(本大题共4个小题。共52分。)
17.(12分)物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。请回答下列问题:
(1)25℃时,将一元酸HA的溶液和KOH溶液等体积混合(忽略反应后溶液的体积变化),其实验数据如表:
起始浓度/(mol/L)
实验编
反应后溶液的pH
号
c(HA) c(KOH)
1 0.2 0.2 pH>7
2 a 0.4 pH=7
学学科科网网((北北京京))股股份份有有限限公公司司①实验1中反应后的溶液中各离子浓度由大到小为:____。
②实验2反应后的溶液中:c(A-)+c(HA)____0.2 mol/L(填“>”、“<”或“=”)。
(2)实验室中配制FeCl 溶液时通常需向其中加入盐酸,其目的是____,同时加入还原性铁粉,其目的是
2
____。
(3)实验测得NaHCO 溶液的pH>7,某同学将NaHCO 溶液和FeCl 溶液混合在一起,产生现象为____,该
3 3 3
反应的离子方程式为:____。
(4)某温度时,K (AgC1)=1.56×10-10,K (AgBr)=7.7×10-13,K (Ag CrO )=9×10-12某溶液含有Cl-、Br-和CrO ,
sp sp sp 2 4
浓度均为0.010 mol/L,向该溶液中逐滴加入0.010 mol/L的AgNO 溶液,三种阴离子产生沉淀的先后顺序
3
为____(用阴离子符号表示)。
18.(14分)I.化学电源在生产生活中有着广泛的应用,请回答下列问题。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是_______
A.KOH + HCl =KCl + H O B.Cu + FeCl = FeCl + CuCl
2 3 2 2
C.Na O + H O = 2NaOH D.Fe+ H SO =FeSO +H ↑
2 2 2 4 4 2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关实验现象,下列说法正确的
是:_______
A.图I中温度计的示数高于图II的示数
B.图I和图II中温度计的示数相等,且均高于室温
C.图I和图II中的气泡均产生于锌棒表面
D.图II中产生气体的速率比I慢
II.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:4NH + 3O = 2N + 6H O,该电池
3 2 2 2
负极的电极反应为:_______
(4)以上述氨燃料电池接下图A.B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,
请回答:甲池中电极C名称为:_______,乙池中发生的离子反应方程式为:_______,丙装置是验证外
加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在_______处(填G或H)。为证
明铁被保护,可先取少量的电解后的溶液于试管中,向溶液中加入_______溶液观察颜色变化。
学学科科网网((北北京京))股股份份有有限限公公司司19.(13分)甲醇是一种可再生能源,由 制备甲醇可能涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
(1)反应Ⅱ的 _______。反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为 、 、 ,则 _______(用 、 表
示)。
(2)反应Ⅰ能自发进行的条件是_______(填“较低温度”“较高温度”或“任何温度”)。
(3)下表是反应Ⅲ: 在不同温度下化学平衡常数(K)
温度/℃ 250 300 350
平衡常数(K) 2.04 0.27 0.012
某温度下,将 和 充入2L的密闭容器中,充分反应后达平衡时,
①测得 ,则 的转化率是_______,此时的温度为_______。
②要提高 的转化率,可以采取的措施是_______。
A.升温 B.恒容充入 C.恒容充入 D.分离出甲醇
③在此条件下,不可作为判断反应Ⅲ达到平衡状态的标志是_______。
A.混合气体的密度不再变化 B.生成 的同时生成
C.混合气体的平均相对分子质量不再变化 D.甲醇的百分含量不再变化
(4)由 制备甲醇还需要氢气。工业上用电解法制取 ,同时获得氢气,原理如下图。
学学科科网网((北北京京))股股份份有有限限公公司司电解一段时间后, 降低的区域在_______。(填“阴极室”或“阳极室”)。该室发生的电极反应式
为_______。
20.(13分)草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分为Co O ,含少量
2 3
Fe O ,Al O ,CaO,MgO,碳及有机物等)制取CoC O 的工艺流程如图:
2 3 2 3 2 4
(1)操作1的目的是除去废料中的碳及有机物,通常采用的方法是_______;
(2)碱浸过程中,主要反应的离子方程式是_______;
(3)“钴浸出过程中Co3+转化为Co2+,反应的离子方程式为_______;
(4)“净化除杂1”过程中,先在40~50°C加入H O ,其作用是_______;再升温至80~85°C。加入Na CO 溶液,
2 2 2 3
调pH至4.5,“滤渣I”主要成分是_______;
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=1.0×10-5mol/L,则滤液中
c(Ca2+)为_______mol/L[已知 Ksp(MgF )=6.4×10-9、Ksp(CaF )=4.0×l0-11];
2 2
(6)为测定制得样品的纯度,现称取1.00g样品,将其用适当试剂转化,得到草酸铵[(NH ) C O ]溶液,再用
4 2 2 4
过量稀硫酸酸化,用0.1000mol/L KMnO 液滴定,达到滴定终点时,共用去KMnO 溶液27.00mL,则草酸
4 4
钴样品的纯度为_______(保留4位有效数字)。
学学科科网网((北北京京))股股份份有有限限公公司司学学科科网网((北北京京))股股份份有有限限公公司司