文档内容
第五章 化学生产中的重要非金属元素
实验活动4 用化学沉淀法去除粗盐中的杂质离子
【学习目标】1.通过联系旧知,讨论交流,认识化学沉淀法去除粗盐中的Ca2+、Mg2
+和SO基本原理和方法。
2.通过实验操作、问题探究,熟练掌握溶解、过滤、蒸发等化学实验基本操作,认识
化学方法在物质分离和提纯中的重要作用。
【学习重点】用化学沉淀法对粗盐进行提纯
【学习难点】粗盐精制原理及实验方案设计
【课前预习】
旧知回顾:1.过滤:过滤是分离 过滤 常用的方法,主要用于除去液体中的 固
体和液体不溶性物质 。玻璃仪器有 烧杯、漏斗、玻璃棒 。
【注意】一贴 滤纸紧贴漏斗内壁 ;
二低 滤纸低于漏斗口,液面低于滤纸边缘 ;
三靠 烧杯紧靠玻璃棒,玻璃棒紧靠三层滤纸处,漏斗下端紧靠烧杯内壁 。
2.蒸发:玻璃棒不断搅拌的目的是 加快蒸发,防止液体局部温度过高而造成飞溅
。当 出现较多量固体 时停止加热,利用余热使滤液蒸干。
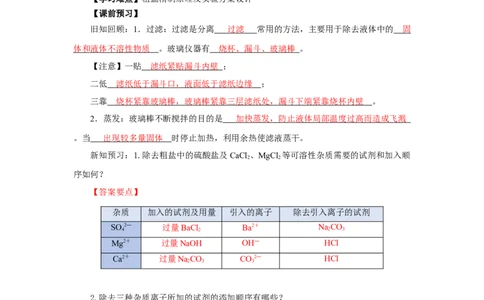
新知预习:1.除去粗盐中的硫酸盐及CaCl 、MgCl 等可溶性杂质需要的试剂和加入顺
2 2
序如何?
【答案要点】
杂质 加入的试剂及用量 引入的离子 除去引入离子的试剂
SO 2― 过量BaCl Ba2+ NaCO
4 2 2 3
Mg2+ 过量NaOH OH― HCl
Ca2+ 过量NaCO CO2― HCl
2 3 3
2.除去三种杂质离子所加的试剂的添加顺序有哪些?
【答案要点】过量BaCl 、过量NaOH、过量NaCO、过滤、适量盐酸
2 2 3
过量NaOH、过量BaCl 、过量NaCO、过滤、适量盐酸
2 2 3
过量BaCl 、过量NaCO、过量NaOH、过滤、适量盐酸(BaCl 必须在NaCO 前面)
2 2 3 2 2 3
【课中探究】
情景导入:观看视频—氯化钠与海水
一、物质的分离和提纯
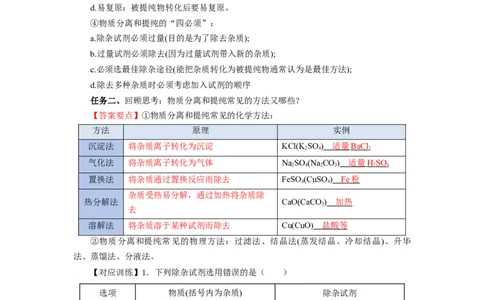
活动一、物质的分离和提纯的概念及原则任务一、讨论交流:物质分离和提纯的基本概念、原则及注意事项分别是什么?
【答案要点】①物质的分离:将混合物的各种物质彼此分开,最终获得几种纯净物的
过程。即A和B的混合物通过某种分离方法最终得到纯净的A和纯净的B 的过程。
②物质的提纯:将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除
杂。
③物质分离和提纯的“四原则”:
a.不增:提纯过程中不增加新的杂质;
b.不减:不减少被提纯物;
c.易分离:被提纯物与杂质容易分离;
d.易复原:被提纯物转化后要易复原。
④物质分离和提纯的“四必须”:
a.除杂试剂必须过量(目的是为了除去杂质);
b.过量试剂必须除去(因为过量试剂带入新的杂质);
c.必须选最佳除杂途径(能把杂质转化为被提纯物通常认为是最佳方法);
d.除去多种杂质时必须考虑加入试剂的顺序
任务二、回顾思考:物质分离和提纯常见的方法又哪些?
【答案要点】①物质分离和提纯常见的化学方法:
方法 原理 实例
沉淀法 将杂质离子转化为沉淀 KCl(KSO ) 适量 BaCl
2 4 2
气化法 将杂质离子转化为气体 NaSO (Na CO) 适量 H SO
2 4 2 3 2 4
置换法 将杂质通过置换反应而除去 FeSO (CuSO ) Fe 粉
4 4
杂质受热易分解,通过加热将杂质除
热分解法 CaO(CaCO) 加热
3
去
溶解法 将杂质溶于某种试剂而除去 Cu(CuO) 盐酸等
②物质分离和提纯常见的物理方法:过滤法、结晶法(蒸发结晶、冷却结晶)、升华
法、蒸馏法、分液法。
【对应训练】1.下列除杂试剂选用错误的是( )
选项 物质(括号内为杂质) 除杂试剂
A CO 气体(HCl气体) 饱和碳酸氢钠溶液
2
B FeCl 溶液(FeCl ) 过氧化氢溶液
3 2
C Al O 固体(Fe O 固体) 氢氧化钠溶液
2 3 2 3
D MnO 固体(KCl固体) 蒸馏水
2
A.A B.B C.C D.D
【答案】C【解析】A.盐酸的酸性强于碳酸,CO 中混有HCl,常采用通入饱和碳酸氢钠溶液,
2
故A不符合题意;B.加入过氧化氢,将Fe2+氧化成Fe3+,不引入新杂质,能够完成实验目
的,故B不符合题意;C.氧化铝为两性氧化物,氧化铁为碱性氧化物,加入氢氧化钠溶
液,氧化铝与氢氧化钠生成可溶的偏铝酸钠,而氧化铁不与氢氧化钠反应,不能达到实验
目的,故C符合题意;D.MnO 不溶于水,KCl可溶于水,因此可采用加水溶液,过滤,
2
除去KCl,能达到实验目的,故D不符合题意;答案为C。
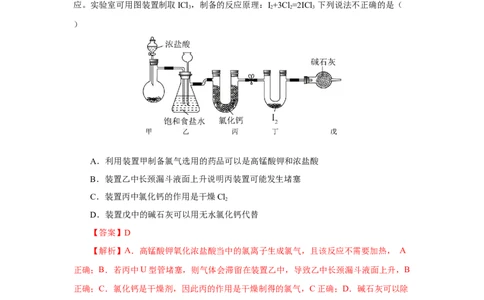
2.三氯化碘(ICl )在药物合成中用途非常广泛,其熔点为33℃,沸点为73℃,遇水易反
3
应。实验室可用图装置制取ICl ,制备的反应原理:I+3Cl=2ICl 下列说法不正确的是(
3 2 2 3
)
A.利用装置甲制备氯气选用的药品可以是高锰酸钾和浓盐酸
B.装置乙中长颈漏斗液面上升说明丙装置可能发生堵塞
C.装置丙中氯化钙的作用是干燥Cl
2
D.装置戊中的碱石灰可以用无水氯化钙代替
【答案】D
【解析】A.高锰酸钾氧化浓盐酸当中的氯离子生成氯气,且该反应不需要加热, A
正确;B.若丙中U型管堵塞,则气体会滞留在装置乙中,导致乙中长颈漏斗液面上升,B
正确;C.氯化钙是干燥剂,因此丙的作用是干燥制得的氯气,C正确;D.碱石灰可以除
去多余的氯气,无水氯化钙不能除去氯气,故装置戊中的碱石灰不可以用无水氯化钙代
替,D错误;故本题选D。
活动二、物质的分离和提纯的常用实验操作方法—过滤与蒸发
任务一、过滤实验操作的概念、原理、适用范围、主要仪器及注意事项分别是什么?
【答案要点】①概念:利用物质溶解性的差异,将液体和不溶于液体的固体分离开来
②原理:物质溶解性的差异
③适用范围:适用于固液混合物的分离。一般情况下,是一种物质易溶于水,另一种
物质难溶于水④主要仪器:铁架台(含铁圈)、烧杯、漏斗、滤纸
⑤装置图:
⑥注意事项:一贴:滤纸紧贴漏斗内壁,中间不留有气泡;
二低:滤纸上边缘低于漏斗边缘,液面低于滤纸边缘;
三靠:倾倒液体的烧杯紧靠玻璃棒,玻璃棒末端紧靠三层滤纸处,漏斗的下端尖口紧
靠盛接滤液的烧杯内壁
【注意】①若滤液浑浊,需更换滤纸,重新过滤,直至溶液澄清透明为止
②浑浊的原因可能是:滤纸破损、滤液超过滤纸边缘、仪器不干净
任务二、蒸发实验操作的概念、原理、适用范围、主要仪器及注意事项分别是什么?
【答案要点】①概念:在蒸发皿中不断加热,蒸发溶剂,使溶液浓缩,从而析出晶体
的过程。
②适用范围:适用于分离溶液中的溶质。
③主要仪器:铁架台(含铁圈)、酒精灯、蒸发皿、玻璃棒。
④装置图:
⑤注意事项:a.行蒸发时,液体量不得超过蒸发皿容积的2/3,以免加热时液体溅出
b.在加热过程中,要用玻璃棒不断搅拌液体,防止因局部温度过热,造成液体飞溅
c.当蒸发皿中出现较多固体时,应停止加热,利用余热蒸干
d.取下未冷却的蒸发皿时,要放在石棉网上
【注意】①结晶是使溶质从溶液中以晶体状态析出的过程,是分离、提纯固体物质的
重要方法之一
②结晶的方法有蒸发结晶(物质溶解度随温度变化不大的物质,如:NaCl)和冷却结
晶(溶解度随温度下降而显著降低的物质,如:KNO)两种。
3
【对应训练】1.在进行“用化学沉淀法去除粗盐中的杂质离子”的实验中,下列说法
不正确的是( )
A.过滤时需用到的玻璃仪器有:烧杯、玻璃棒、漏斗
B.蒸发结晶时当蒸发皿中出现较多固体时,停止加热
C.按照实验操作顺序玻璃棒的作用依次为:引流、搅拌、搅拌
D.加入除杂的试剂顺序可以是NaOH、BaCl 、NaCO,过滤后再加适量盐酸
2 2 3
【答案】C【解析】A.过滤时需要用到的玻璃仪器有烧杯、玻璃棒、漏斗,A正确;B.蒸发结
晶时,当蒸发皿中出现较多固体时,即停止加热,用余热将剩余水分蒸干,B正确;C.用
化学沉淀法除去粗盐中的杂质离子,步骤包括粗盐溶解,加沉淀剂,过滤,调节pH,蒸发
结晶等,玻璃棒的作用依次为搅拌、引流、搅拌,C错误;D.加入除杂的试剂顺序可以
是先加NaOH除去镁离子,再加BaCl 除去硫酸根离子,加入碳酸钠除去钙离子和过量的
2
钡离子,过滤后加适量盐酸中和NaOH和碳酸钠,D正确;故答案选C。
2.为提纯下列物质(括号内的物质为杂质),所选用的方法正确的是( )
A.HCl(HS):通入酸性KMnO 溶液中洗气
2 4
B.CO(SO ):通入溴水溶液中洗气
2 2
C.AlCl 溶液(FeCl ):加入过量的NaOH溶液过滤
3 3
D.NO (NO):通入NaOH溶液中洗气
2
【答案】B
【解析】A.HCl和HS都能与酸性KMnO 溶液反应,A错误;B.SO 能与溴水发生
2 4 2
氧化还原反应而CO 不能,CO 中的SO 可以用溴水除去,B正确;C.AlCl 溶液中含有
2 2 2 3
FeCl ,加入过量的NaOH溶液生成NaAlO ,过滤后得到NaAlO 溶液,C错误;D.NO 与
3 2 2 2
NaOH溶液反应,NO (NO)通入NaOH溶液,除去NO ,D错误;故选B。
2 2
二、粗盐的提纯原理与方法
实验用品:
试管、托盘天平、量筒、酒精灯、铁架台、试管架、橡胶塞、乳胶管、胶头滴管、玻
璃导管、石棉网(或陶土网)、玻璃棒、药匙、棉花、镊子、火柴。
粗盐、蒸馏水、0.1 mol/L BaCl 溶液、20% NaOH溶液、饱和NaCO 溶液、6 mol/L盐
2 2 3
酸、pH试纸
活动一、用化学沉淀法去除粗盐中的杂质离子
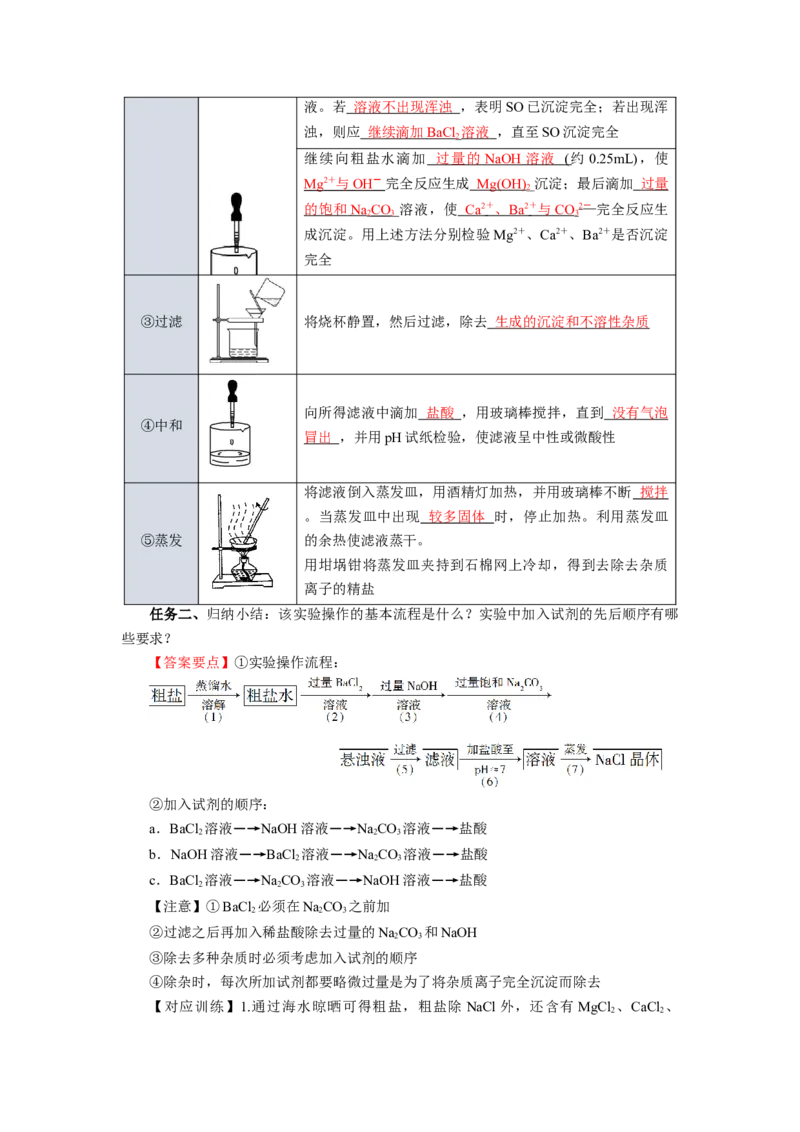
任务一、利用提供的实验用品,结合教材P29页【实验步骤】,分小组完成下表实
验,并填写表格内容:
实验步骤 实验装置 实验操作
①溶解 用托盘天平称取5g粗盐,放入100mL 烧杯中,然后加入
20mL水,用玻璃棒 搅拌 ,使粗盐全部溶解,得到粗盐水
向粗盐水中滴加过量的 BaCl 溶液(约2~3mL),使 SO 与
2
②沉淀
Ba 2 + 完全反应生成 Ba SO 沉淀 ,将烧杯静置
4
静置后,沿烧杯壁向上层清液中继续滴加2~3滴BaCl 溶
2液。若 溶液不出现浑浊 ,表明SO已沉淀完全;若出现浑
浊,则应 继续滴加 BaC l 溶液 ,直至SO沉淀完全
2
继续向粗盐水滴加 过量的 NaOH 溶液 (约 0.25mL),使
Mg 2 + 与 OH - 完全反应生成 Mg(OH ) 沉淀;最后滴加 过量
2
的饱和 N aCO 溶液,使 C a 2 + 、 B a 2 + 与 CO 2- 完全反应生
2 3 3
成沉淀。用上述方法分别检验Mg2+、Ca2+、Ba2+是否沉淀
完全
③过滤 将烧杯静置,然后过滤,除去 生成的沉淀和不溶性杂质
向所得滤液中滴加 盐酸 ,用玻璃棒搅拌,直到 没有气泡
④中和
冒出 ,并用pH试纸检验,使滤液呈中性或微酸性
将滤液倒入蒸发皿,用酒精灯加热,并用玻璃棒不断 搅拌
。当蒸发皿中出现 较多固体 时,停止加热。利用蒸发皿
⑤蒸发 的余热使滤液蒸干。
用坩埚钳将蒸发皿夹持到石棉网上冷却,得到去除去杂质
离子的精盐
任务二、归纳小结:该实验操作的基本流程是什么?实验中加入试剂的先后顺序有哪
些要求?
【答案要点】①实验操作流程:
②加入试剂的顺序:
a.BaCl 溶液―→NaOH溶液―→NaCO 溶液―→盐酸
2 2 3
b.NaOH溶液―→BaCl 溶液―→NaCO 溶液―→盐酸
2 2 3
c.BaCl 溶液―→NaCO 溶液―→NaOH溶液―→盐酸
2 2 3
【注意】①BaCl 必须在NaCO 之前加
2 2 3
②过滤之后再加入稀盐酸除去过量的NaCO 和NaOH
2 3
③除去多种杂质时必须考虑加入试剂的顺序
④除杂时,每次所加试剂都要略微过量是为了将杂质离子完全沉淀而除去
【对应训练】1.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl 、CaCl 、
2 2NaSO 以及泥沙等杂质,粗盐精制的实验流程如下。下列说法不正确的是( )
2 4
A.在第①步中使用玻璃棒搅拌可加速粗盐溶解
B.第⑤步操作是过滤
C.第②③④⑥步通过加入化学试剂除杂,加入试剂顺序为:NaOH溶液→NaCO 溶
2 3
液→BaCl 溶液→稀盐酸
2
D.除去MgCl 的方程式为:MgCl +2NaOH===Mg(OH) ↓+2NaCl
2 2 2
【答案】C
【解析】加入过量的氢氧化钠可以将镁离子沉淀,加入过量的氯化钡可以将硫酸根离
子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入碳酸钠要放在加入氯化钡之后,这样
碳酸钠会除去反应剩余的氯化钡,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离
子和碳酸根离子,所以正确的顺序为:NaOH、BaCl 、NaCO 或BaCl 、NaOH、NaCO,
2 2 3 2 2 3
NaCO 要在BaCl 的后面加,C错误。
2 3 2
2.海盐经溶解、过滤后仍含有可溶性杂质 Ca2+、Mg2+、SO,为了得到纯净的NaCl,
下列试剂(均过量)的滴加顺序及操作顺序不合理的是( )
A.BaCl 溶液→NaOH溶液→NaCO 溶液→过滤→稀盐酸→蒸发结晶
2 2 3
B.Ba(OH) 溶液→NaCO 溶液→过滤→稀盐酸→蒸发结晶
2 2 3
C.NaCO 溶液→NaOH溶液→BaCl 溶液→过滤→稀盐酸→蒸发结晶
2 3 2
D.BaCl 溶液→NaCO 溶液→NaOH溶液→过滤→稀盐酸→蒸发结晶
2 2 3
【答案】C
【解析】粗盐提纯时,所加的试剂有NaOH溶液(除去Mg2+)、BaCl 溶液(除去SO)、
2
NaCO 溶液(除去Ca2+和过量的Ba2+),过滤后,加入稀盐酸(除去过量的OH-、CO2-),
2 3 3
注意NaCO 溶液一定要在BaCl 溶液之后加入,稀盐酸在过滤后加入,故 A、D项正确,
2 3 2
C项错误;加入过量的Ba(OH) 溶液,可除去SO、Mg2+,再加入过量的NaCO 溶液,除
2 2 3
去Ca2+和过量的Ba2+,过滤后,向滤液中加入稀盐酸,除去过量的CO2-和OH-,蒸发结
3
晶得到纯净的NaCl,B项正确。
活动二、问题与讨论
任务一、问题探究:(1)在实验操作②中为什么依次加入的试剂都要略微过量?实验
操作④中加入盐酸的目的是什么?
【答案要点】①实验操作②中所加试剂过量是为了将杂质离子完全沉淀而除去。
②实验操作④中加入盐酸是为了除去滤液中过量的OH-(或调节溶液的pH)和CO。
(2)粗盐水中加入氯化钡溶液使SO沉淀而除去,如何检验SO是否沉淀完全?
【答案要点】静置后,沿烧杯壁向上层清液中继续滴加2~3滴氯化钡溶液,若溶液不
出现浑浊,说明SO已沉淀完全。(3)第③步过滤和第④步加入盐酸的操作顺序能否颠倒?为什么?
【答案要点】先过滤再加入盐酸的操作顺序不能颠倒。若在过滤前加入稀盐酸,会使
生成的沉淀溶解,产生新的杂质。
任务二、归纳总结:除去粗盐中可溶性杂质的一般思路和方法分别是什么?要注意哪
些问题?
【答案要点】①思路和方法:选择除杂试剂,依据是将可溶性杂质转化成沉淀、水或
气体等易分离的物质,尽可能不引入新杂质;安排试剂的用量(一般过量)和添加顺序,
依据是过量的试剂必须靠后面添加的试剂除去。
②需要注意的问题:a.洗涤沉淀的操作:向漏斗中加蒸馏水至没过沉淀,待水自然流
下,重复操作2~3次。
b.过滤操作不可用玻璃棒搅拌漏斗内的物质,以免划破滤纸。
c.检验沉淀是否洗涤干净的操作:检验沉淀是否洗涤干净的操作:取最后一次洗涤液
进行检验(事先要确定沉淀中含有的离子,选择合适的试剂进行检验)。
d.检验沉淀是否完全的方法:检验沉淀是否完全的方法:取(或向)上层清液中继续
滴加原沉淀剂,若无沉淀产生则沉淀完全。
【对应训练】1.有关粗盐(主要含NaCl,杂质为BaCl 、MgCl )提纯的描述错误的是
2 2
( )
A.将粗盐溶于水得到无色溶液,边搅拌边适当加热能加快溶解的速率
B.提纯时需要的除杂试剂有NaCO 溶液、NaOH溶液,稀盐酸
2 3
C.加入除杂试剂时,必须先加入稀盐酸后加入NaCO 溶液
2 3
D.该提纯过程中未涉及氧化还原反应
【答案】C
【解析】A.溶解时搅拌或适当升温都能加快溶解的速率,故将粗盐溶于水得到无色
溶液,边搅拌边适当加热能加快溶解的速率,A正确;B.提纯时需要的除杂试剂有
NaCO 溶液除去BaCl 、NaOH溶液除去MgCl ,稀盐酸除去过量的NaCO 和NaOH,B正
2 3 2 2 2 3
确;C.根据除杂的基本要求可知,加入NaCO 溶液除去BaCl 、NaOH溶液除去MgCl ,
2 3 2 2
过滤产生的沉淀后加入稀盐酸以除去过量的NaCO 溶液和NaOH溶液,C错误;D.该提
2 3
纯过程中涉及的反应有:NaCO+BaCl =BaCO ↓+2NaCl,
2 3 2 3
MgCl +2NaOH=Mg(OH)↓+2NaCl,NaCO+2HCl=2NaCl+H O+CO↑,
2 2 2 3 2 2
NaOH+HCl=NaCl+H O,故未涉及氧化还原反应,D正确;
2
故答案为:C。2.下列说法正确的是( )
A.向某溶液中滴加少量AgNO 溶液,有白色沉淀产生,溶液中一定含有Cl-
3
B.向某溶液中加入一定量的稀硫酸,产生的气体使澄清石灰水变浑浊,溶液中一定
含有SO 或CO
C.氯气使湿润的红纸条褪色,说明氯气具有漂白性
D.SO 使酸性高锰酸钾褪色,表现了SO 的还原性
2 2
【答案】D
【解析】A.向某溶液中滴加少量AgNO3溶液,有白色沉淀产生,溶液中可能含有
Cl-、CO、SO等离子中的一种或几种,故A错误;B.向某溶液中加入一定量的稀硫酸,
产生的气体使澄清石灰水变浑浊,溶液中可能含有SO、CO、HSO、HCO等离子中的一种
或几种,故B错误;C.氯气使湿润的红纸条褪色,是氯气和水反应生成的次氯酸有强氧
化性,能使有色物质褪色,不能说明氯气具有漂白性,故C错误;D. SO2使酸性高锰酸
钾褪色,是SO 被高锰酸钾溶液氧化,高锰酸钾被还原成无色的离子,表现了SO2的还原
2
性,故D正确;故答案为:D。
【课后巩固】1.下列有关分析中,错误的是( )
A.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
B.“青蒿一握,以水二升渍,绞取汁”,该青蒿素的提取过程属于化学变化
C.1964年我国自行制造的第一颗原子弹爆炸成功,原子弹爆炸涉及物理变化
D.“方家以磁石磨针锋,则能指南”,中国古代磨制磁石制造指南针属于物理变化
【答案】B
【解析】A.由描述可知,铁与硫酸铜反应生成铜和硫酸亚铁,属于置换反应,A正
确;B.此过程为萃取,没有新物质生成,属于物理变化,B错误;C.原子弹爆炸涉及化
学变化和物理变化,C正确;D.中国古代磨制磁石制造指南针,过程中没有新物质生
成,属于物理变化,D正确;故选B。
2.下列说法正确的是( )
A.通过焰色试验可以鉴别碳酸钠中是否含有碳酸钾
B.向溶液中滴加盐酸酸化的BaCl 溶液,产生白色沉淀,则原溶液中一定有SO
2
C.向溶液中滴加AgNO,产生白色沉淀,则原溶液中一定有Cl-
3
D.向溶液中滴加盐酸,产生使澄清石灰水变浑浊的无色无味的气体,则原溶液中一定有CO
【答案】A
【解析】A.钾的焰色为紫色,钠的焰色为黄色,因此可用焰色实验鉴别碳酸钠中是
否含碳酸钾,故A正确;B.若原溶液中含银离子,加盐酸酸化的氯化钡也会生成白色沉
淀,不一定是硫酸根存在,应先加盐酸酸化,无现象后再加氯化钡,故B错误;C.能与
银离子沉淀的还有碳酸根、硫酸根等,不一定是氯离子,故C错误;D.能与盐酸反应生
成二氧化碳气体的还可以是碳酸氢根离子,故D错误;故选:A。
3.粗食盐水中常含有少量Ca2+、Mg2+、 杂质离子,实验室提纯粗食盐水制取食盐
的流程如下,过程III中,用到的分离方法是( )
A.吸附 B.加热蒸发 C.过滤 D.冷却结晶
【答案】B
【解析】食盐溶解度受温度影响小,加热蒸发食盐溶液得到食盐晶体,所以过程III
中,用到的分离方法是加热蒸发,故选B。
4.下列实验中,所选装置不合理的是( )
A.粗盐提纯,选①和②
B.用CCl 提取碘水中的碘,选③
4
C.从Br 的CCl 溶液中分离出Br ,选④
2 4 2
D.用NaOH溶液吸收Cl 选⑤
2
【答案】C
【解析】A.粗盐提纯的步骤有溶解、过滤、蒸发、结晶,①是过滤、②是蒸发,所
以选①和②,故A正确;B.碘易溶于CCl ,CCl 不溶于水,用CCl4萃取碘水中的碘,所
4 4
以选③,故B正确;C.Br 和CCl 是互溶液体,用蒸馏法分离Br2和CCl ,④装置缺少温
2 4 4度计,故C错误;D.氢氧化钠和氯气反应生成氯化钠、次氯酸钠和水,用NaOH溶液吸
收Cl,防止污染,选装置⑤,故D正确;选C。
2
5.下列有关实验操作的说法,不正确的是( )
A.铁离子的检验:向含Fe3+溶液中加入KSCN溶液,溶液颜色变红
B.检验溶液中的Na+:取一根洁净的铂丝,放在酒精灯火焰上灼烧至与火焰颜色一
致,然后蘸取少量试液,置于火焰上灼烧,若火焰呈黄色,则含有Na+
C.在配制100mL1.00mol ▪L-1的氯化钠溶液时,容量瓶不能用作溶解物质的容器
D.粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶
【答案】D
【解析】A.Fe3+与KSCN溶液作用产生血红色溶液,故常用向溶液中加入KSCN溶
液,溶液颜色变红来进行铁离子的检验,A正确;B.钠的焰色反应为黄色,由操作和现
象可知含有Na+,B正确; C.容量瓶不能用作溶解或者稀释物质、物质反应和长期贮存
溶液的容器,C正确;D.粗盐的提纯试验中,滤液在蒸发皿中加热蒸发结晶,而不是在
坩埚中加热蒸发,D错误;故答案为:D。
6.粗盐含有少量的 MgCl ,CaCl ,NaSO 等杂质,为了将杂质除干净得到精盐,对
2 2 2 4
粗盐溶液分别进行如下操作①加入过量的 NaOH 溶液、②加入过量的 NaCO 溶液、③
2 3
加入过量的BaCl 溶液、④过滤、⑤加入过量的稀盐酸、⑥蒸发。下列操作的先后顺序错
2
误的是( )
A.②③①④⑤⑥ B.③④②④①④⑤⑥
C.①③②④⑤⑥ D.③④①②④⑤⑥
【答案】A
【解析】①加过量NaOH溶液,Mg2+发生反应,生成Mg(OH) 沉淀和氯化钠;②加过
2
量NaCO 溶液,与CaCl 和③中过量BaCl 溶液发生反应,生成CaCO 沉淀和BaCO 沉淀
2 3 2 2 3 3
和氯化钠;③加入过量BaCl 溶液,与NaSO 发生反应,生成BaSO 沉淀和NaCl;④过
2 2 4 4
滤,滤出前面生成的沉淀及泥沙;⑤加适量盐酸,与①中过量NaOH溶液和②中过量
NaCO 溶液发生反应,生成氯化钠、水和二氧化碳气体;因此操作中应依次加入过量的氯
2 3
化钡、碳酸钠、氢氧化钠,过滤后加适量盐酸然后蒸发除水;正确的操作顺序为
③④②④①④⑤⑥、①③②④⑤⑥或③④①②④⑤⑥故选A。
7.NH MnPO ·2H O是一种活性催化剂,易溶于水,其溶解度随着温度升高而显著增
4 4 2
大。一种制备NH MnPO ·2H O的方法如下:
4 4 2下列叙述正确的是( )
A.“溶解”中加入盐酸的目的是加快溶解
B.“合成”中加入氨水过量,会生成酸式盐
C.“系列操作”需要酒精灯、蒸馏烧瓶等仪器
D.采用“重结晶”可提纯产品
【答案】D
【解析】A.氢氧化锰难溶于水,氯化锰溶于水后部分水解生成氢氧化锰,加入盐
酸,可抑制锰离子水解,A错误;B.加入氨水,中和盐酸,氨水较多,会生成碱式盐,B
错误;C.依题意,磷酸锰铵晶体易溶于水,根据溶解度与温度关系,分离操作是蒸发浓
缩、降温结晶、过滤、洗涤、干燥,不需要蒸馏烧瓶,C错误;D.采用重结晶方法可以
提纯磷酸锰铵结晶水合物,D正确;故选D。
8.为了除去粗盐中的Ca2+、Mg2+、SO 、泥沙等杂质,进行下列五项操作:①过滤
②加过量NaOH溶液 ③加适量HCl ④加过量NaCO 溶液 ⑤加过量BaCl 溶液 ⑥溶
2 3 2
解 ⑦蒸发,回答下列问题:
(1)以上五项操作的步骤为:
⑥→①→②→_______→_______→_______→_______→⑦,_______。其中加入BaCl 溶液
2
发生的离子反应方程式为:______________________________,加入过量NaCO 溶液的目
2 3
的是__________________________________。
(2)关于上述过程,错误的是_____________________
A.溶解粗盐时,加水越多越好
B.NaOH溶液不可用KOH溶液替代
C.滤去沉淀以后,将滤液移至坩埚内加热蒸发
D.当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干
E.将制得的晶体转移到过滤器中用大量水进行洗涤
(3)NaCl的焰色反应为_______色,验证提纯后的NaCl固体中不含KCl的操作及现象
是:
____________________________________________________________________________。
【答案】(1) ⑥→①→②→⑤→④→①→③→⑦ Ba2++SO=BaSO ↓
4除去Ca2+以及加入的过量Ba2+
(2)ACE
(3) 黄 用洁净的铂丝蘸取样品后在酒精灯上灼烧,透过蓝色钴玻璃观察不到
紫色火焰,说明不含KCl
【解析】(1)粗盐样品含有 Ca2+、Mg2+、SO、泥沙等杂质,加入过量氢氧化钠溶液
的目的是除去Mg2+;加入过量的BaCl ,可以将硫酸根离子除去,但是会引入Ba2+杂质离
2
子;加入过量的NaCO 溶液的目的除去杂质Ca2+,和加入的过量Ba2+;过滤,将得到的沉
2 3
淀全部滤出,得到的滤液是含有氯化钠、碳酸钠、氢氧化钠等的混合物,加入足量的盐
酸,可以出去碳酸根离子、氢氧根离子等杂质离子,最后即可获得较为纯净的氯化钠,所
以操作的步骤为:⑥→①→②→⑤→④→①→③→⑦。加入BaCl 溶液发生的离子反应方
2
程式为:Ba2++SO=BaSO ↓。加入过量NaCO 溶液的目的是除去Ca2+以及加入的过量
4 2 3
Ba2+。
(2)A.溶解时,若加入太多水,则蒸发时就需要大量时间,A错误;B.NaOH溶
液不可用KOH溶液替代,否则会引入新的杂质离子K+,B正确;C.滤去沉淀以后,将滤
液移至蒸发皿加热浓缩,C错误;D.蒸发时,有少量液体剩余就应该停止加热,D正确;
E.晶体应用少量水洗涤,否则会导致晶体溶于水损失,E错误;故选ACE。
(3)NaCl的焰色反应为黄色。用焰色反应验证提纯后的NaCl固体中不含KCl,操作
及现象是:用洁净的铂丝蘸取样品后在酒精灯上灼烧,透过蓝色钴玻璃观察不到紫色火
焰,说明不含KCl。