文档内容
第五章 化工生产中的重要非金属元素
实验活动4 用化学沉淀法去除粗盐中的杂质离子
分层作业
基础达标
1.中国传统文化对人类文明贡献巨大,古代文献中记载了古代化学研究成果。下列关
于文献记载内容的说法正确的是( )
A.《周礼》中“煤饼烧蛎房成灰”(蛎房即牡蛎壳),“灰”的主要成分为CaCO
3
B.《本草纲目》中记载:“此即地霜也,所在山泽,冬月地上有霜,扫取以水淋
汁,后乃煎炼而成”,文中对硝酸钾的提取涉及溶解、蒸发、结晶操作
C.《抱朴子》中“丹砂(HgS)烧之成水银,积变又还成丹砂”描述的是升华和凝华过
程
D.《梦溪笔谈》中“熬胆矾铁釜,久之亦化为铜”,与化学反应无关
【答案】B
【解析】A.牡蛎壳的主要成分为CaCO ,CaCO 灼烧生成CaO,则“灰”的主要成
3 3
分为CaO,故A错误;B.“扫取以水淋汁,后乃煎炼而成”是指扫取后用水溶解,然后
加热蒸发结晶得到硝酸钾晶体,涉及溶解、蒸发、结晶操作,故B正确;C.“丹砂(HgS)
烧之成水银”即HgS发生分解反应生成水银,“积变又还成丹砂”即Hg和S又反应生成
HgS,两过程中均有新物质生成,为化学变化,而“升华”、“凝华”为物理变化,故C
错误;D.“熬胆矾铁釜,久之亦化为铜”是铁与硫酸铜发生置换反应生成硫酸亚铁和
铜,过程中有新物质生成,为化学变化,故D错误;故答案选B。
2.利用图中实验装置进行的相应实验,能达到实验目的的是( )
A.利用图1和图4所示装置进行粗盐提纯
B.利用图2所示装置除去 中混有的HClC.利用图3所示装置进行乙醇萃取碘水中的碘
D.利用图4所示装置提纯 胶体
【答案】A
【解析】A.粗盐中含不溶性和可溶性杂质,粗盐中的不溶性杂质需要过滤出去,可
溶性杂质通过化学方法转变成沉淀后过滤除去,所得食盐水通过蒸发结晶得到NaCl晶体,
则利用图1和图4所示装置进行粗盐提纯,A正确;B.二氧化碳和氯化氢气体都能和饱和
碳酸钠溶液反应,应把图2所示装置中的饱和碳酸钠换成饱和碳酸氢钠、即可除去CO 中
2
混有的HCl,B错误;C.乙醇和水互溶,故不能用乙醇萃取碘水中的碘,C错误;D.胶
体和溶液都能透过滤纸,故不能用过滤的方法提纯Fe(OH) 胶体,应用渗析,D错误;答
3
案选A。
3.下列说法正确的是( )
A.通过焰色试验可以鉴别碳酸钠中是否含有碳酸钾
B.向溶液中滴加盐酸酸化的BaCl 溶液,产生白色沉淀,则原溶液中一定有SO
2
C.向溶液中滴加AgNO,产生白色沉淀,则原溶液中一定有Cl-
3
D.向溶液中滴加盐酸,产生使澄清石灰水变浑浊的无色无味的气体,则原溶液中一
定有CO
【答案】A
【解析】A.钾的焰色为紫色,钠的焰色为黄色,因此可用焰色实验鉴别碳酸钠中是
否含碳酸钾,故A正确;B.若原溶液中含银离子,加盐酸酸化的氯化钡也会生成白色沉
淀,不一定是硫酸根存在,应先加盐酸酸化,无现象后再加氯化钡,故B错误;C.能与
银离子沉淀的还有碳酸根、硫酸根等,不一定是氯离子,故C错误;D.能与盐酸反应生
成二氧化碳气体的还可以是碳酸氢根离子,故D错误;故选:A。
4.下列分离混合物的实验方法中不正确的是( )
A.分离乙酸(沸点77.1 ℃)与某种液态有机物(沸点120 ℃)的混合物-蒸馏
B.从含有少量NaCl的KNO 溶液中提取KNO-热水溶解、降温结晶、过滤
3 3
C.用CCl 萃取碘水中的碘,液体分层后-下层液体从下口放出,上层液体从上口倒出
4
D.将溴水中的溴转移到有机溶剂中-加入乙醇萃取
【答案】D【解析】A.两种有机物互溶且沸点相差较大,则选择蒸馏法分离,A正确;B.NaCl
和KNO 的溶解度受温度影响变化程度不同,则从含有少量NaCl的KNO3溶液中提取
3
KNO3可采取热水溶解、降温结晶、过滤的方法,B正确;C.分液时,下层液体从下口放
出,上层液体从上口倒出,C正确;D.乙醇与水互溶,则乙醇不能萃取溴水中的溴,D错
误;故选:D。
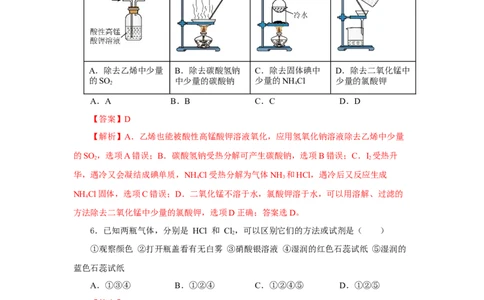
5.下列装置能达到除杂目的的是( )
A.除去乙烯中少量 B.除去碳酸氢钠 C.除去固体碘中 D.除去二氧化锰中
的SO 中少量的碳酸钠 少量的NH Cl 少量的氯酸钾
2 4
A.A B.B C.C D.D
【答案】D
【解析】A.乙烯也能被酸性高锰酸钾溶液氧化,应用氢氧化钠溶液除去乙烯中少量
的SO ,选项A错误;B.碳酸氢钠受热分解可产生碳酸钠,选项B错误;C.I 受热升
2 2
华,遇冷又会凝结成碘单质,NH Cl受热分解为气体NH 和HCl,遇冷后又反应生成
4 3
NH Cl固体,选项C错误;D.二氧化锰不溶于水,氯酸钾溶于水,可以用溶解、过滤的
4
方法除去二氧化锰中少量的氯酸钾,选项D正确;答案选D。
6.已知两瓶气体,分别是 HCl 和 Cl,可以区别它们的方法或试剂是( )
2
①观察颜色 ②打开瓶盖看有无白雾 ③硝酸银溶液 ④湿润的红色石蕊试纸 ⑤湿润的
蓝色石蕊试纸
A.①③④ B.①②④ C.①②④⑤ D.①②⑤
【答案】C
【解析】①Cl 为黄绿色气体,而氯化氢无色,可以通过观察气体颜色鉴别二者,故①
2
符合题意;②氯化氢极易溶于水,打开瓶盖后有白雾,而Cl 不具有此性质,打开瓶盖看有
2
无白雾可鉴别二者,故②符合题意;③HCl和Cl 都能够与硝酸银溶液反应生成氯化银沉
2
淀,无法用硝酸银溶液鉴别二者,故③不符合题意;④HCl不能使红色石蕊试纸变色,而
Cl 能够使湿润的红色石蕊试纸褪色,可以据此鉴别二者,故④符合题意;⑤湿润的蓝色石
2
蕊试纸遇Cl 先变红后褪色,湿润的蓝色石蕊试纸遇HCl只变红,故可以用湿润的蓝色石
2蕊试纸来区别Cl 和HCl,故⑤符合题意;故答案选C。
2
7.现有四组分散系:①汽油和水形成的混合物;②含有泥沙的食盐水;③溶有碘(I)
2
的酒精溶液;④乙二醇和丙三醇的混合溶液(乙二醇和丙三醇的部分物理性质见下表)。
物质 熔点/℃ 沸点/℃ 密度/g·cm−3 溶解性
乙二醇 -11.5 198 1.11 易溶于水和乙醇
丙三醇 17.9 290 1.26 能跟水、酒精以任意比互溶
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )
A.③―d―蒸发结晶 B.②―b―过滤
C.①―c―分液 D.④―a―蒸馏
【答案】A
【解析】A.③溶有碘(I2)的酒精溶液中分离I2和酒精,二者的沸点不同,可采用蒸馏
方法分离,使用的仪器是蒸馏烧瓶a,A错误;B.②含有泥沙的食盐水中泥沙难溶于水,
可通过过滤的方法分离除去,使用的仪器是漏斗,B正确;C.①汽油和水是互不相溶的两
层液体物质,分离可使用分液方法,使用的仪器是c分液漏斗,C正确;D.④乙二醇和丙
三醇是互溶的沸点不同的液体有机物,可根据二者沸点不同,采用蒸馏方法,使用的仪器
是蒸馏烧瓶a,D正确;故合理选项是A。
8.下列分离混合物的实验方法中不正确的是( )
A.分离乙酸(沸点77.1 ℃)与某种液态有机物(沸点120 ℃)的混合物-蒸馏
B.从含有少量NaCl的KNO 溶液中提取KNO-热水溶解、降温结晶、过滤
3 3
C.用CCl 萃取碘水中的碘,液体分层后-下层液体从下口放出,上层液体从上口倒出
4
D.将溴水中的溴转移到有机溶剂中-加入乙醇萃取
【答案】D
【解析】A.两种有机物互溶且沸点相差较大,则选择蒸馏法分离,A正确;B.NaCl
和KNO3的溶解度受温度影响变化程度不同,则从含有少量NaCl的KNO3溶液中提取
KNO 可采取热水溶解、降温结晶、过滤的方法,B正确;C.分液时,下层液体从下口放
3出,上层液体从上口倒出,C正确;D.乙醇与水互溶,则乙醇不能萃取溴水中的溴,D错
误;故选:D。
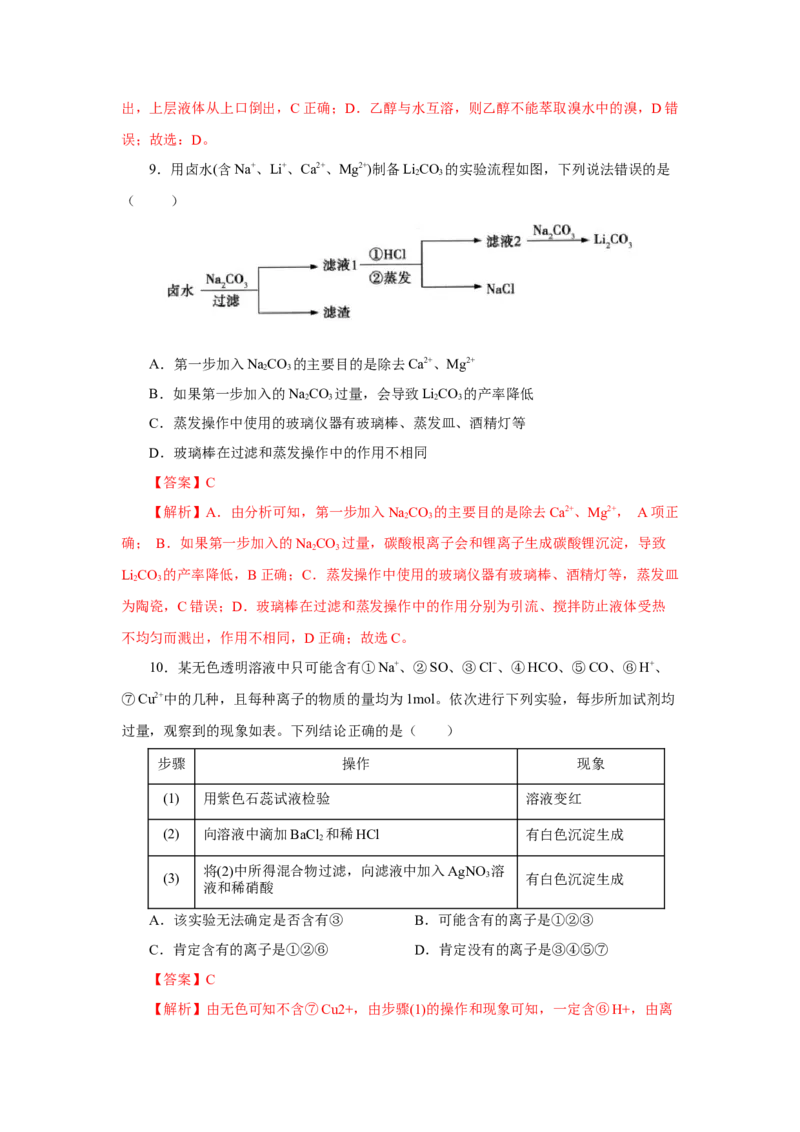
9.用卤水(含Na+、Li+、Ca2+、Mg2+)制备LiCO 的实验流程如图,下列说法错误的是
2 3
( )
A.第一步加入NaCO 的主要目的是除去Ca2+、Mg2+
2 3
B.如果第一步加入的NaCO 过量,会导致LiCO 的产率降低
2 3 2 3
C.蒸发操作中使用的玻璃仪器有玻璃棒、蒸发皿、酒精灯等
D.玻璃棒在过滤和蒸发操作中的作用不相同
【答案】C
【解析】A.由分析可知,第一步加入NaCO 的主要目的是除去Ca2+、Mg2+, A项正
2 3
确; B.如果第一步加入的NaCO 过量,碳酸根离子会和锂离子生成碳酸锂沉淀,导致
2 3
LiCO 的产率降低,B正确;C.蒸发操作中使用的玻璃仪器有玻璃棒、酒精灯等,蒸发皿
2 3
为陶瓷,C错误;D.玻璃棒在过滤和蒸发操作中的作用分别为引流、搅拌防止液体受热
不均匀而溅出,作用不相同,D正确;故选C。
10.某无色透明溶液中只可能含有①Na+、②SO、③Cl−、④HCO、⑤CO、⑥H+、
⑦Cu2+中的几种,且每种离子的物质的量均为1mol。依次进行下列实验,每步所加试剂均
过量,观察到的现象如表。下列结论正确的是( )
步骤 操作 现象
(1) 用紫色石蕊试液检验 溶液变红
(2) 向溶液中滴加BaCl 和稀HCl 有白色沉淀生成
2
将(2)中所得混合物过滤,向滤液中加入AgNO 溶
(3) 3 有白色沉淀生成
液和稀硝酸
A.该实验无法确定是否含有③ B.可能含有的离子是①②③
C.肯定含有的离子是①②⑥ D.肯定没有的离子是③④⑤⑦
【答案】C
【解析】由无色可知不含⑦Cu2+,由步骤(1)的操作和现象可知,一定含⑥H+,由离子共存可知,不含④HCO、⑤CO;由步骤(2)中可知白色沉淀为硫酸钡,则一定含SO;
(3)中白色沉淀为AgCl,但(2)中引入氯离子,由操作和现象不能判断是否含氯离子,由于
每种离子的物质的量均为1mol,由电荷守恒可知,还一定含①Na,则一定不含日③Cl-。
A.根据上述分析,一定不含③,A错误;B.根据上述分析,一定含①②⑥,一定不含
③④⑤⑦,B错误;C.根据上述分析,肯定含有的离子是①②⑥,C正确;D.根据上述
分析,肯定没有的离子有③④⑤⑦,,D错误;
能力提升
11.下列实验目的对应的实验操作正确的是( )
选项 实验目的 实验操作
检验溶液中是否含 向待测液中滴加BaCl 溶液,若出现沉淀,再滴加
A 2
有SO 稀盐酸,观察沉淀是否溶解
检验溶液中是否含 向待测液中滴加过量硝酸,再滴加AgNO 溶液,观
B 3
有Cl- 察是否出现白色沉淀
检验溶液中是否含 向待测液中加入一定量NaOH溶液,观察是否出现
C
有Mg2+ 白色沉淀
检验溶液中是否含 向待测液中加入过量稀盐酸,观察是否生成使澄清
D
有CO 石灰水变浑浊的无色无味气体
A.A B.B C.C D.D
【答案】B
【解析】A.检验溶液中是否含有SO,应先向溶液中滴加盐酸,若无现象,再滴加氯
化钡,有白色沉淀,则证明含有硫酸根,故A不符合题意;B.检验溶液中是否含有Cl
-,向待测液中滴加过量硝酸,再滴加AgNO 溶液,观察是否出现白色沉淀,有白色沉
3
淀,则含有氯离子,反之则无,故B符合题意;C.检验溶液中是否含有Mg2+,向待测液
中加入一定量NaOH溶液,观察是否出现白色沉淀,溶液中有铝离子也能出现白色沉淀,
故C不符合题意;D.向待测液中加入过量稀盐酸,观察是否生成使澄清石灰水变浑浊的
无色无味气体,不能检验溶液中是否含有CO,碳酸氢根也是这样的现象,故D不符合题
意。综上所述,答案为B。
12.以软锰矿(主要成分是MnO ,含有SiO、Fe O 等杂质)制备高性能的磁性材料碳
2 2 3 4
酸锰(MnCO )的基本工业流程如图:
3下列说法错误的是( )
A.浸锰过程中存在Fe O+SO+4H+=3Fe2++2H O
3 4 2 2
B.滤渣I中主要成分为SiO
2
C.氧化过程的目的只是将过量的SO 消耗
2
D.沉锰过程发生的反应为Mn2++2 =MnCO↓+CO ↑+H O
3 2 2
【答案】C
【解析】由流程可知软锰矿形成矿浆,通入足量的SO ,发生反MnO +SO=MnSO ,
2 2 2 4
Fe O+SO+4H+=3Fe2++SO+2H O,SiO 不反应,过滤,滤渣I为SiO,滤液含有Mn2+、
3 4 2 2 2 2
Fe2+,加入MnO 氧化亚铁离子,反应为2Fe2++MnO+4H+=2Fe3++2H O+Mn2+,调节pH,沉
2 2 2
淀铁离子,过滤,滤渣II为氢氧化铁,向滤液中加入碳酸氢铵溶液,生成MnCO 沉淀,过
3
滤得到的滤渣中主要含有MnCO ,反应为Mn2++2HCO=MnCO↓+CO ↑+H O,通过洗涤、
3 3 2 2
烘干得到MnCO 晶体,据此分析解题。A.由分析可知,浸锰过程中存在
3
Fe O+SO+4H+=3Fe2++ +2H O,A正确;B.由分析可知,滤渣I中主要成分为SiO,B正
3 4 2 2 2
确;C.由分析可知,氧化过程的目的主要是将Fe2+氧化为Fe3+,以便以后步骤中调节pH
值来沉淀除去,也能将过量的SO 消耗,C错误;D.有分子可知,沉锰过程发生的反应为
2
Mn2++2HCO=MnCO↓+CO ↑+H O,D正确;故答案为:C。
3 2 2
13.钛酸锶(SrTiO )常作电子陶瓷材料和人造宝石。实验室制备原理如下:
3
(1)
(2) 。
某小组利用图1和图2装置完成反应(1),再灼烧滤渣制备钛酸锶。下列说法错误的是
( )A.仪器A的名称是球形冷凝管 B.热水浴的优点是受热均匀和便于控制温度
C.利用图2抽滤时用玻璃棒搅拌 D.灼烧时需要选择坩埚承载固体
【答案】C
【解析】A.根据仪器构造可知,上述仪器A的名称为球形冷凝管,A正确;B.热水
浴与酒精灯加热相比,受热均匀,且便于控制温度,B正确;C.抽滤时不能用玻璃棒搅
拌,防止划破滤纸,导致过滤失败,C错误;D.坩埚耐高温,可用于灼烧固体,D正确;
故选C。
14.海水提纯精盐的过程是用化学沉淀法去除粗盐中的杂质离子Ca2+、Mg2+和SO,请
完成下题:
(1)下面是粗盐提纯的部分操作步骤,请补充③处实验步骤:
①用天平称取5.0g粗盐,放入100ml烧杯中,然后加入20mL蒸馏水,用玻璃棒搅
拌,使粗盐全部溶解,得到粗盐水。
②向粗盐水中滴加过量的BaCl 溶液,使SO与Ba2+完全反应生成BaSO 将烧杯静置。
2 4
③ ___________________________________________________________
④向粗盐水中滴加过量的NaOH溶液,使Mg2+与OH-完全反应生成Mg(OH) 沉淀,然
2
后滴加过量的饱和NaCO 溶液,使Ca2+、Ba2+与CO 完全反应生成沉淀。
2 3
⑤…
(2)有学生设计出如下粗盐提纯工艺流程图
①上述流程图中③处加入的试剂是 ______________ _ 。(填名称)
②写出流程中③处发生的离子反应方程式 _______________________ _,___________________________ 。
(3)方案评价
化学沉淀法中沉淀剂BaCl 和NaCO 加入的顺序能否交换? 。(填“能”或
2 2 3
“否”)
【答案】(1)沿烧杯壁向上层清液继续滴加2~3滴BaCl 溶液,若不出现浑浊,则表明
2
SO沉淀完全,若出现沉淀,则继续滴加BaCl 溶液,直至SO沉淀完全
2
(2) 稀盐酸 H++OH-=H O 2H++CO=H O+CO↑
2 2 2
(3)否
【解析】在粗盐除杂工艺中,粗盐溶解、过滤后加入过量的BaCl 溶液,生成BaSO
2 4
沉淀而除去SO,此时溶液中含有Na+、Ca2+、Mg2+、Ba2+和Cl-,再加入过量NaCO 溶液,
2 3
生成沉淀BaCO 和CaCO 而除去Ca2+和Ba2+,再加入过量的NaOH溶液,生成沉淀
3 3
Mg(OH) 而除去Mg2+,最后再加入适量的HCl除去过量的NaOH和NaCO,最后得到精
2 2 3
盐。
(1)滴加过量的BaCl 溶液除去SO后还要检验SO是否除干净,因此接下来操作是沿
2
烧杯壁向上层清液继续滴加2 3滴BaCl 溶液,若不出现浑浊,则表明SO沉淀完全,若
2
出现沉淀,则继续滴加BaCl 溶液,直至SO沉淀完全;
2
(2)①由分析可知上述流程图中③处加入的试剂是稀盐酸;
②流程中③中加入适量的稀盐酸除去过量的NaOH和NaCO,其发生的离子反应方程
2 3
式为H++OH-=H O和2H++CO=H O+CO↑;
2 2 2
(3)沉淀法中沉淀剂BaCl 和NaCO 加入的顺序不能交换,后加入NaCO 溶液不但
2 2 3 2 3
可以除去粗盐中Ca2+,还可以除去前面加入过量的Ba2+,若交换顺序,则无法除去Ba2+。
直击高考
15.(NH )SO 是一种常见的化肥,其溶解度随着温度的升高而增大,某工厂用石膏、
4 2 4
NH 、HO和CO 制备(NH )SO 的工艺流程如图:
3 2 2 4 2 4下列说法正确的是( )
A.通入NH 和CO 的顺序可以互换
3 2
B.操作2为将滤液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得(NH )SO
4 2 4
C.步骤②中反应的离子方程式为
D.通入的NH 和CO 均应过量,且工艺流程中CO 可循环利用
3 2 2
【答案】B
【解析】A.由于CO 微溶于水,NH 易溶于水,应先通入足量NH ,使溶液呈碱性,
2 3 3
然后再通入适量CO,反应的化学方程式为
2
,通入NH 和CO 的顺序不可以互换,选
3 2
项A错误;B.向硫酸钙悬浊液中通入足量的氨气,使溶液呈碱性,再通入适量的二氧化
碳利于反应的进行,硫酸钙与氨气、水和二氧化碳反应生成了硫酸铵和碳酸钙沉淀。操作
2是溶液中得到溶质固体的过程,需要蒸发浓缩、冷却结晶、过滤、洗涤、干燥等,可得
(NH )SO ,选项B正确;C.硫酸钙与氨气、水和二氧化碳反应生成了硫酸铵和碳酸钙沉
4 2 4
淀,物质发生的主要化学反应为 ,反应的
离子方程式为 ,选项C错误;D.反应过
程中二氧化碳参与反应生成硫酸铵和碳酸钙,碳酸钙分解生成二氧化碳,工艺流程中产生
的CO 可循环利用,通入足量NH ,通适量二氧化碳,否则碳酸钙溶解,选项D错误。答
2 3
案选B。
16.草木灰中含有可溶性钾盐(主要成分是 、 、 )。骉学生按下列操
作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结
晶。
(1)由草木灰提取钾盐并检验钾元素的存在,下列实验操作中正确的是
___________。(2)为检验草木灰中的其它离子,取少量晶体溶于水,并把溶液分成三份,完成以下
实验报告(在横线上填写相关的内容):
实验步骤 实验现象 实验结论
I. 取第一份溶液和适量稀盐酸加入试管中,把
澄清的石灰水加入烧杯中
________,澄
证明含有碳酸根
清的石灰水变
离子
浑浊
证明含有硫酸根
II.取第二份溶液,先后滴加_______和_______ ________
离子
III.取第三份溶液加入过量 溶液,过滤,
有_______生
证明含有氯离子
除去 和 ,再滴加 溶液和稀硝
成
酸
(3)步骤III所得的结论,你认为是否正确?为什么?
____________________________
(4)写出步骤II有关现象的化学方程式
_________________________________________、
_________________________________________。
【答案】(1)ABCD
(2)有无色气泡产生 稀盐酸 氯化钡溶液 气泡产生、生成白色沉淀(或先
加氯化钡溶液后加稀盐酸,看到白色沉淀生成,沉淀部分溶解) 白色沉淀
(3)否,步骤III中引入氯离子,干扰实验,应选硝酸钡
(4) (或
、 、)
【解析】检验溶液中的离子,需要根据离子的性质检验,CO可与H+反应生成CO 气
2
体,故可用盐酸检验CO;SO一般用Ba2+检验,但需要排除CO、Cl-等的干扰;Cl-一般用
Ag+检验,K+只能用颜色反应检验,以此来解析;(1)由草木灰提取押盐并检验钾元素存
在,需要溶解,过滤,蒸发操作,ABC均合理,且D是透过蓝色钴玻璃观察钾焰色反应操
作,钾的焰色反应,必须透过蓝色钴玻璃观察,故D也合理,所以ABCD均合理;故选
ABCD。(2)溶液检验草木灰中的离子,取第一份溶液,加盐酸有气泡产生,发生反应
CO+2H+=CO ↑+H O,证明含有碳酸根离子;取第二份溶液,先滴加稀盐酸,有气泡产生,
2 2
后加氯化钡溶液,有气泡若生成白色沉淀,含硫酸根离子;取第三份溶液加入过量BaCl
2
溶液,过滤,除去SO和CO,再滴加AgNO 溶液和稀硝酸,有白色沉淀生成,为AgCl,
3
证明含有氯离子;(3)否,步骤Ⅲ中引入氯离子,干扰实验,应选硝酸钡,用氯化钡则不
合理;(4)碳酸钾和稀盐酸反应生成氯化钾、二氧化碳和水,反应的方程式为:
KCO+2HCl=2KCl+H O+CO↑,加入氯化钡与硫酸钾反应生成硫酸钡和氯化钾,反应的方
2 3 2 2
程式为:KSO +BaCl =BaSO ↓+2KCl;
2 4 2 4