文档内容
第五章 化学生产中的重要非金属元素
实验活动5 不同价态含硫物质的转化
【学习目标】1.通过旧知回顾、讨论交流,进一步认识含不同价态硫元素的物质可以
相互转化,并能设计实验进行探究和验证,加深对硫及其化合物性质的认识和理解。
2.通过实验探究、归纳总结,应用氧化还原反应的原理实现不同价态含硫物质的转
化,提升实验探究和实验设计能力,培养科学探究精神。
【学习重点】实验探究不同价态含硫物质的转化关系
【学习难点】利用氧化还原反应原理理解不同价态含硫物质的转化
【课前预习】
旧知回顾:以金属单质Ca和非金属单质C为例,如何实现各类物质的转化,写出相
应的化学方程式。
①转化关系模型:
②化学方程式:
新知预习:利用氧化还原反应原理,如何实现不同价态含硫物质的转化?请举例说
明。
①转化关系模型:
②转化关系实例(化学方程式):
情境导入:观看视频—不同价态含硫物质的转化(见PPT视频)
一、常见含硫物质的转化
活动一、相同和不同价态含硫物质的转化
任务一、根据氧化还原反应原理,结合元素价态规律及物质类别和性质,思考常见含
硫化合物的转化有何特点和规律?
①不同价态含硫物质相互转化关系如图:
②相同价态含硫物质间的转化可表示为:
③含硫物质的转化小结:
【注意】任务二、讨论交流:根据上述含硫化合物的转化关系,回答不同价态含硫物质的转化
有何规律?
①邻位价态规律:
②互不反应规律:
③归中规律:
④连续氧化规律:
【对应训练】1.硫在自然界中的循环过程如下图所示,下列说法不正确的是( )
A.石油和煤等化石燃料中含有硫元素
B.大气中的二氧化硫只来源于火山喷发产生的气体
C.地壳中的硫元素常以硫化物和硫酸盐的形式存在
D.动植物遗体被微生物分解后,可产生SO和SO
2
2.有下列两种转化途径,某些反应条件和产物已省略。下列有关说法不正确的是(
)
途径① S HSO 途径② S SO SO HSO
2 4 2 3 2 4
A.途径①反应中体现了浓硝酸的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O 浓度来降低成本
2
C.由途径①和②分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol e-
2 4
D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相
对小且原子利用率高
活动二、设计实验探究不同价态含硫物质的转化
任务一、讨论交流:如何设计实验验证不同价态含硫物质的转化?
①实验探究:
②设计思路:
③设计原则:
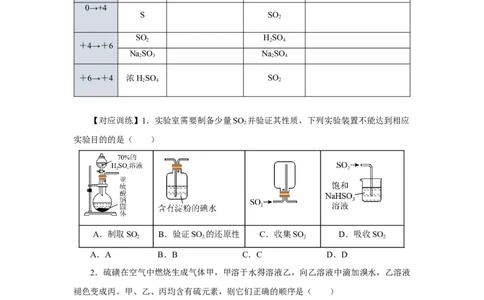
任务二、结合硫元素的化合价,思考依据氧化还原反应原理,如何通过实验验证不同
价态含硫物质转化的发生?并填写表格内容。转化前的 预测转化后的
转化目标 选择试剂 实验现象
含硫物质 含硫物质
HS
2
-2→0
S
NaS
2
HS
2
0→-2 S
NaS
2
0→+4
S SO
2
SO HSO
2 2 4
+4→+6
NaSO NaSO
2 3 2 4
+6→+4 浓HSO SO
2 4 2
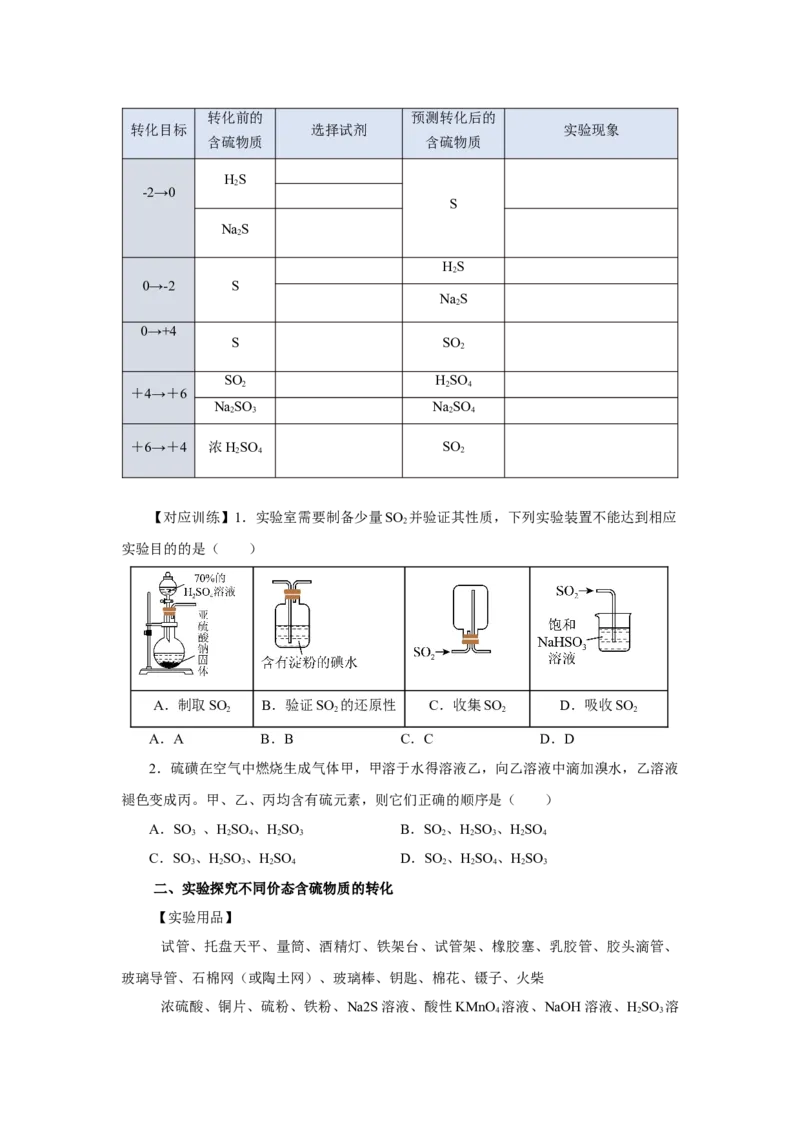
【对应训练】1.实验室需要制备少量SO 并验证其性质,下列实验装置不能达到相应
2
实验目的的是( )
A.制取SO B.验证SO 的还原性 C.收集SO D.吸收SO
2 2 2 2
A.A B.B C.C D.D
2.硫磺在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,乙溶液
褪色变成丙。甲、乙、丙均含有硫元素,则它们正确的顺序是( )
A.SO 、HSO 、HSO B.SO 、HSO 、HSO
3 2 4 2 3 2 2 3 2 4
C.SO 、HSO 、HSO D.SO 、HSO 、HSO
3 2 3 2 4 2 2 4 2 3
二、实验探究不同价态含硫物质的转化
【实验用品】
试管、托盘天平、量筒、酒精灯、铁架台、试管架、橡胶塞、乳胶管、胶头滴管、
玻璃导管、石棉网(或陶土网)、玻璃棒、钥匙、棉花、镊子、火柴
浓硫酸、铜片、硫粉、铁粉、Na2S溶液、酸性KMnO 溶液、NaOH溶液、HSO 溶
4 2 3液、品红溶液。
活动一、实验探究不同价态含硫物质的转化
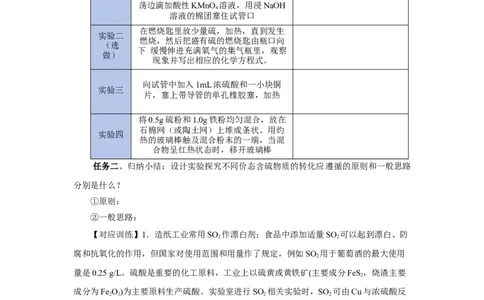
任务一、利用提供的实验用品,结合教材P30页【实验步骤】,完成下表中的三个实
验,并填写表格内容。
实验 操作 现象
在一支试管中加入1mL Na S溶液,边振
2
荡边滴加HSO 溶液,用浸NaOH溶液的
2 3
棉团塞住试管口
实验一
在一支试管中加入1mL Na S溶液,边振
2
荡边滴加酸性KMnO 溶液,用浸NaOH
4
溶液的棉团塞住试管口
在燃烧匙里放少量硫,加热,直到发生
实验二
燃烧,然后把盛有硫的燃烧匙由瓶口向
(选
下 缓慢伸进充满氧气的集气瓶里,观察
做)
现象并写出相应的化学方程式。
向试管中加入1mL浓硫酸和一小块铜
实验三
片,塞上带导管的单孔橡胶塞,加热
将0.5g硫粉和1.0g铁粉均匀混合,放在
石棉网(或陶土网)上堆成条状。用灼
实验四
热的玻璃棒触及混合粉末的一端,当混
合物呈红热状态时,移开玻璃棒
任务二、归纳小结:设计实验探究不同价态含硫物质的转化应遵循的原则和一般思路
分别是什么?
①原则:
②一般思路:
【对应训练】1.造纸工业常用SO 作漂白剂;食品中添加适量SO 可以起到漂白、防
2 2
腐和抗氧化的作用,但国家对使用范围和用量作了规定,例如SO 用于葡萄酒的最大使用
2
量是0.25 g/L。硫酸是重要的化工原料,工业上以硫黄或黄铁矿(主要成分FeS,烧渣主要
2
成分为Fe O)为主要原料生产硫酸。实验室进行SO 相关实验时,SO 可由Cu与浓硫酸反
2 3 2 2
应制得。下列有关物质的性质与用途不具有对应关系的是( )
A.SO 具有还原性,可用作葡萄酒抗氧化剂 B.SO 具有氧化性,可用作纸浆漂白
2 2
剂
C.SO 是酸性氧化物,可用氢氧化钠溶液吸收D.浓硫酸有吸水性,可作气体干燥剂
2
2.有一瓶可能部分被氧化的NaSO 溶液,某同学取少量此溶液,滴入 Ba(NO ) 溶
2 3 3 2
液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。下述有关此实验的
结论正确的是( )
A.NaSO 已部分被空气中的氧气氧化
2 3B.加入 Ba(NO ) 溶液后,生成的沉淀中一定含有BaSO
3 2 4
C.加足量硝酸后的白色沉淀一定是BaSO
4
D.此实验能确定NaSO 是否部分被氧化
2 3
活动二、问题与讨论
任务一、问题探究:(1)在上述实验中,含硫物质中硫元素的价态发生了怎样的变
化?
转化前的含硫物质 转化后的含硫物质 价态变化
NaS
2
HSO
2 3
HSO
2 4
S
(2)实验1中用浸有NaOH溶液的棉花团塞住试管口的作用是什么?
(3)铁粉与硫粉在空气中混合燃烧时,可能发生哪些反应?设计实验实现硫元素的价
态+4→+6的变化的实验方案,写出反应原理及必要的实验操作、现象。
任务二、应用探究:某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体
的成分。该小组成员将气体通入澄清石灰水中,发现澄清石灰水变浑浊,持续通入,发现
浑浊又变澄清,由此该小组成员对该气体的成分提出猜想。
[ 提 出 猜 想 ] 猜 想 1 : _______________________ ; 猜 想 2 :
___________________________;
猜想3:__________________________________________。
为了验证猜想,该小组设计实验加以探究。
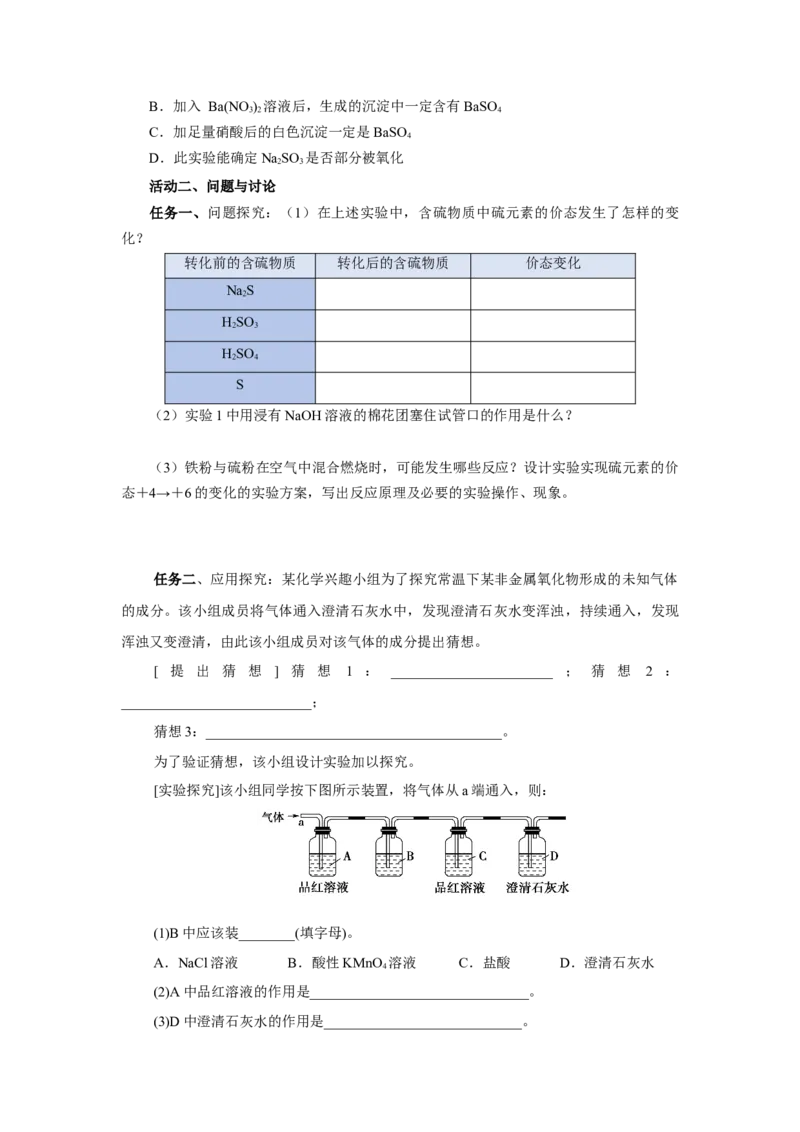
[实验探究]该小组同学按下图所示装置,将气体从a端通入,则:
(1)B中应该装________(填字母)。
A.NaCl溶液 B.酸性KMnO 溶液 C.盐酸 D.澄清石灰水
4
(2)A中品红溶液的作用是_______________________________。
(3)D中澄清石灰水的作用是____________________________。通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
[ 得 出 结 论 ](4) 由 上 述 现 象 , 该 小 组 同 学 确 认 该 气 体 为
____________________________。
【对应训练】1.根据SO 通入不同溶液中实验现象,所得结论不正确的是( )
2
溶液 现象 结论
A 氯水 黄绿色溶液褪色 SO 有还原性
2
B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D NaSiO 溶液 产生胶状沉淀 酸性:HSO >H SiO
2 3 2 3 2 3
A.A B.B C.C D.D
2.如图是足量的铜与浓硫酸反应的实验装置。已知浓硫酸(浓度为18 mol·L-1)为50
mL。下列有关判断正确的是( )
A.装置B中盛装的是浓硫酸,作用是干燥SO
2
B.装置C为安全瓶,防止装置D中的液体倒吸入装置B中
C.品红溶液可检验生成的SO ,碱性棉球的作用是吸收空气中的酸性气体
2
D.充分反应后,被还原的硫酸少于0.45 mol
【课后巩固】1.硫元素在自然界中的循环如图所示,下列说法错误的是( )
A.硫是组成某些蛋白质的生命元素
B.地壳中化合态的硫主要以硫化物和硫酸盐的
形式存在
C.硫粉在过量的纯氧中燃烧可以生成SO
3
D.化石燃料的燃烧以及含硫矿物的冶炼是大气
SO 污染的主要来源
2
2.盛有氯化钡稀溶液的甲、乙两试管分别通入SO 至饱和,若向甲试管中加入足量双
2氧水,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是( )
A.甲、乙两试管都有白色沉淀生成 B.甲、乙两试管都没有白色沉淀生成
C.甲试管没有白色沉淀生成而乙试管有 D.甲试管有白色沉淀生成而乙试管没有
3.元素及其化合物的转化关系是化学学习的重要内容之一,下列各组物质的转化关
系,不能均由一步反应实现的是( )
A. B.Fe→FeCl →Fe(OH) →Fe(OH)
2 2 3
C.Na→NaO→NaO→NaCO D.
2 2 2 2 3
4.在硫酸的工业生产过程中,SO 的吸收过程是在吸收塔中进行的,吸收塔里还装入
3
了大量瓷环。下列有关说法错误的是( )
A.从①处通入SO 整个吸收操作采取逆流的形式
3
B.从②处喷下98.3%的浓硫酸,瓷环的作用是增大接触面
积
C.从③处导出的气体只含有少量的SO ,可直接排入空气
2
中
D.从④处流出的是可用水或稀硫酸稀释的浓硫酸
5.在实验室进行铁粉和硫粉混合加热的实验,产物又进行了系列实验,流程如下。下
列说法正确的是( )
A.气体A和D含有同一物质,且均为
氧化产物
B.硫元素一共参加了2个氧化还原反应 C.沉淀F为黄色单质
D.若固体B中加浓硫酸,发生反应时被氧化的和被还原的均为同一种元素
6.固态单质甲及其化合物之间的转化如图所示(某些产物及反应条件略去)。下列分析
错误的是( )
A.甲在空气中燃烧产生淡蓝色火焰
B.工业上乙→丙的条件是:高温、高压、催化剂
C.乙和丙的相对分子质量比为4:5
D.戊既有还原性又有氧化性
7.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a可与O 反应直接生成c
2
B.b既可被氧化,也可被还原C.可向HO 中加入b制得d
2 2
D.可存在b→c→d→b的转化关系
8.“价一类”二维图是预测物质性质的重要思维工具。如图是硫元素的常见化合价与
部分物质类别的对应关系:
(1)图中X、Y、Z三种物质中,属于电解质的是__________________(用化学式表示)。
(2) 的电离方程式为_____________________________________________。
(3)硫代硫酸钠 俗称海波。从类别的角度分析,其属于_______(填标号)。
A.盐 B、碱 C.
酸 D.氧化物
从价态的角度分析, _______(填标号)
A.只有氧化性 B.既有氧化性又有还原性 C.只有
还原性
(4)Z的浓溶液可用铝质容器储存的原因是
_______________________________________。
(5)从物质的性质分析,Y不可用_____________进行干燥(填标号)。
A.浓硫酸 B.碱石灰 C.PO
2 5
固体