文档内容
第二章 分子结构与性质
第一节 共价键
第1课时 共价键
基础过关练
题组一 共价键的形成与特征
1.下列不属于共价键成键因素的是( )
深度解析
A.电子在两原子核之间高概率出现
B.未成对电子必须配对
C.成键后体系能量降低,趋于稳定
D.两原子核体积大小要适中
2.共价键具有饱和性和方向性,下列有关叙述不正确的是 ( )
A.共价键的饱和性是由成键原子的未成对电子数决定的
B.共价键的方向性与成键原子的轨道的伸展方向有关
C.共价键的饱和性决定了各种原子形成分子时相互结合的数量关系
D.共价键的饱和性与原子轨道的重叠程度有关
3.对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了8电子的
结构。则一个三硫化四磷分子中含有的共价键个数是( )
A.7 B.9
C.19 D.不能确定
4.下列说法正确的是( )
A.若把H S分子写成H S分子,违背了共价键的饱和性
2 3
B.H O+的存在说明共价键不具有饱和性
3
C.所有共价键都有方向性
D.两个原子轨道发生重叠后,电子仅存在于两核之间
题组二 σ键和π键5.(2020江苏徐州一中高二月考)下列分子中存在π键的是( )
A.H B.Cl C.N D.HCl
2 2 2
6.(2020云南昭通高二期末)下列分子中,既含有σ键,又含有π键的是( )
A.CH B.HCl
4
C.CH CH D.F
2 2 2
7.下列对σ键的认识不正确的是( )
A.σ键不属于共价键,是另一种化学键
B.s-s σ键与s-p σ键的对称性相同
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
8.具有下列电子排布式的原子中,不能形成π键的是( )
A.1s22s22p63s23p4 B.1s22s22p3
C.1s22s22p63s1 D.1s22s22p2
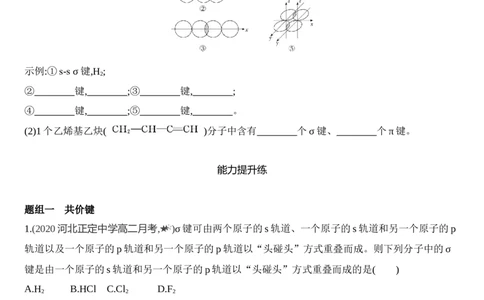
9.下列对分子中σ键重叠方式的分析不正确的是( )
A B C D
H HCl Cl ClF
2 2
两个原子的s 氢原子的s轨道和氯原 一个氯原子的s轨道和另一个 氯原子的p轨道和氟原
轨道重叠 子的p轨道重叠 氯原子的p轨道重叠 子的p轨道重叠
10.下列分子中既有σ键,又有π键的是( )
①HCl ②H O ③N ④H O ⑤C H ⑥C H
2 2 2 2 2 4 2 2
A.①②③ B.③④⑤⑥
C.①③⑥ D.③⑤⑥
11.下列说法正确的是( )
深度解析
A.σ键强度小,容易断裂,而π键强度较大,不易断裂B.共价键都具有方向性
C.π键是由两个原子的p轨道“头碰头”重叠形成的
D.两个原子之间形成共价键时,最多有一个σ键
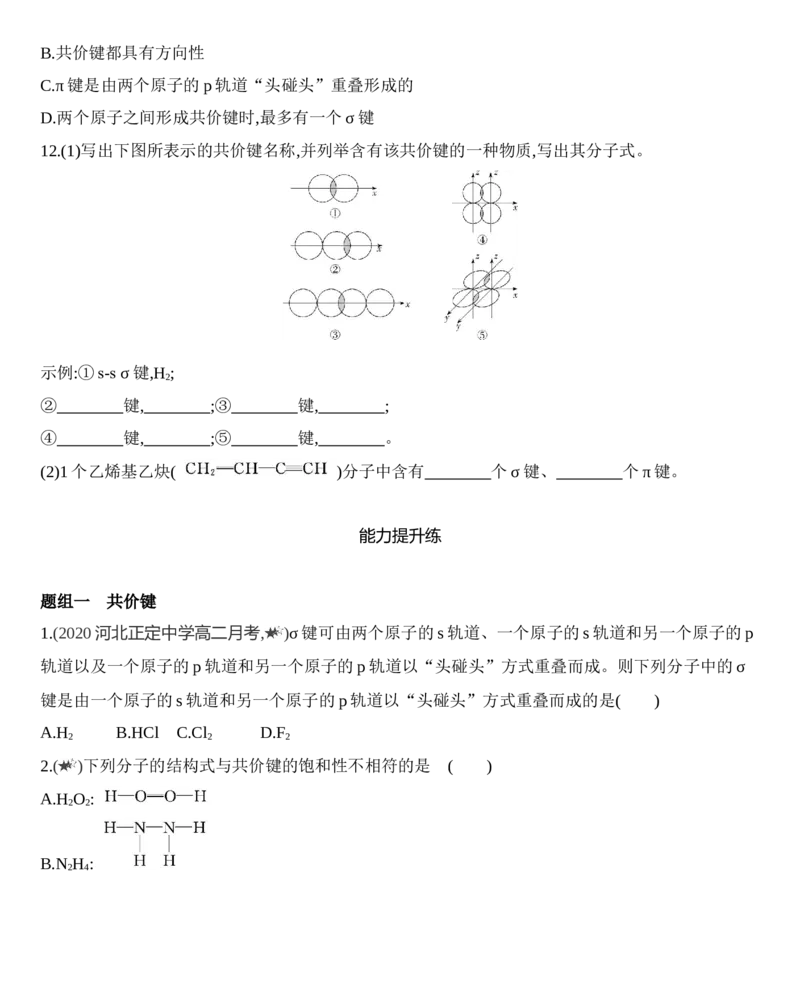
12.(1)写出下图所表示的共价键名称,并列举含有该共价键的一种物质,写出其分子式。
示例:①s-s σ键,H ;
2
② 键, ;③ 键, ;
④ 键, ;⑤ 键, 。
(2)1个乙烯基乙炔( )分子中含有 个σ键、 个π键。
能力提升练
题组一 共价键
1.(2020河北正定中学高二月考, )σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p
轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠而成。则下列分子中的σ
键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠而成的是( )
A.H B.HCl C.Cl D.F
2 2 2
2.( )下列分子的结构式与共价键的饱和性不相符的是 ( )
A.H O :
2 2
B.N H :
2 4C.C H SH:
2 5
D.SiHCl :
3
3.( )下列说法正确的是( )
A.1 mol C H 分子中含有(3n+1)mol共价键
n 2n+2
B.Na O 和Na O固体中阳离子与阴离子的数目比相同,化学键类型也相同
2 2 2
C.只含有非金属元素的化合物中只有共价键
D.电负性之差小于1.7的两种元素的原子间一定形成共价键
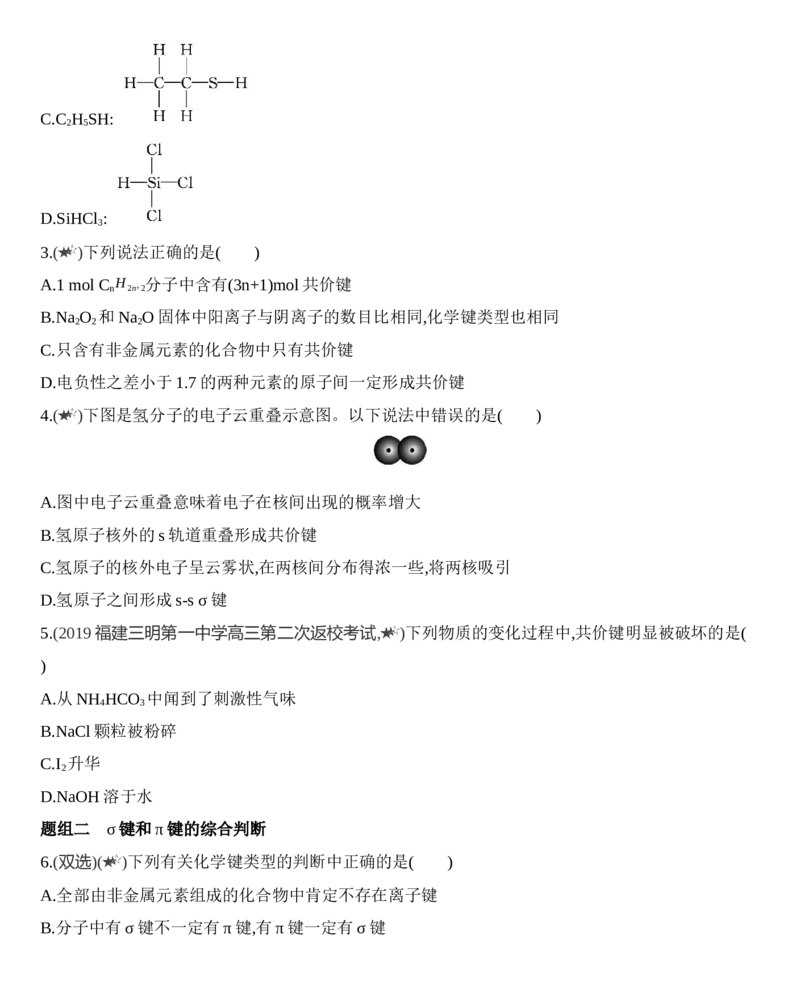
4.( )下图是氢分子的电子云重叠示意图。以下说法中错误的是( )
A.图中电子云重叠意味着电子在核间出现的概率增大
B.氢原子核外的s轨道重叠形成共价键
C.氢原子的核外电子呈云雾状,在两核间分布得浓一些,将两核吸引
D.氢原子之间形成s-s σ键
5.(2019福建三明第一中学高三第二次返校考试, )下列物质的变化过程中,共价键明显被破坏的是(
)
A.从NH HCO 中闻到了刺激性气味
4 3
B.NaCl颗粒被粉碎
C.I 升华
2
D.NaOH溶于水
题组二 σ键和π键的综合判断
6.(双选)( )下列有关化学键类型的判断中正确的是( )
A.全部由非金属元素组成的化合物中肯定不存在离子键
B.分子中有σ键不一定有π键,有π键一定有σ键C.已知乙炔的结构式为 ,则1个乙炔分子中存在2个σ键(C—H键)和3个π键(
键)
D.乙烷分子中只存在σ键,即C—H键和C—C键均为σ键
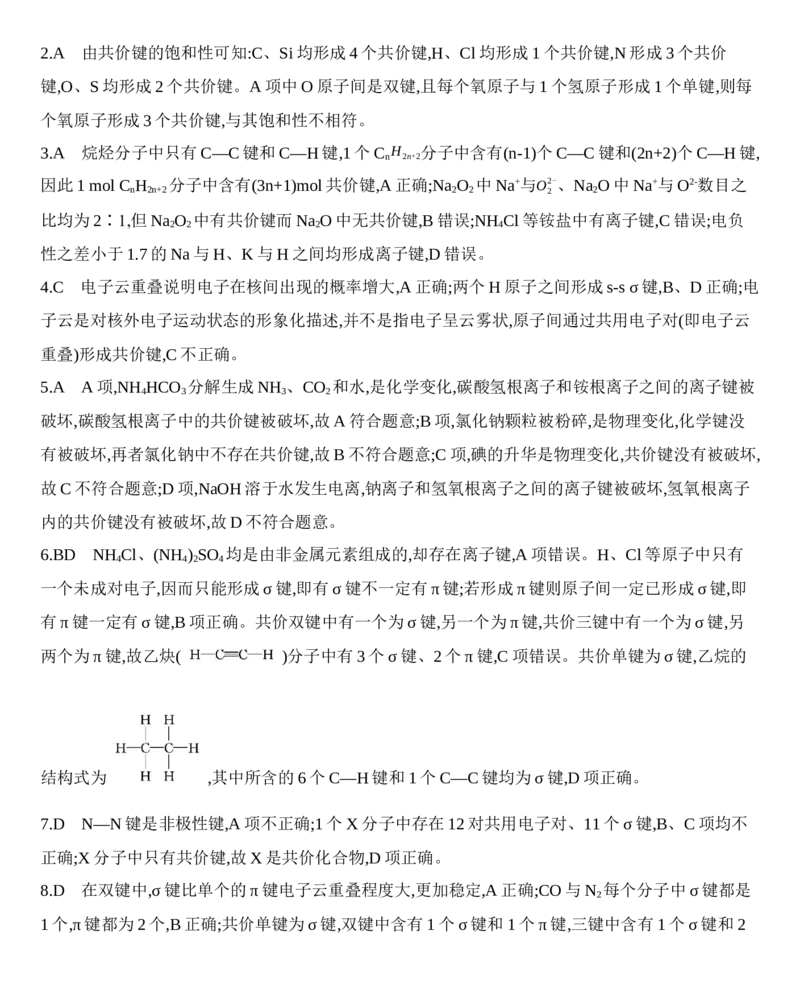
7.( )化合物X是一种新型锅炉水除氧剂,其结构式为 ,设N 为阿伏加德罗常
A
数的值。下列说法中正确的是( )
A.X分子中只有极性键,没有非极性键
B.1个X分子中的共用电子对数目为11
C.1 mol X分子中所含的σ键数目为10N
A
D.X是共价化合物
8.(2019吉林扶余第一中学高二下第一次月考, )下列关于共价键的说法不正确的是( )
A.在双键中,σ键比π键稳定
B.N 与CO分子中σ键和π键个数对应相等
2
C.两个原子形成共价键时至少有1个σ键
D.HCHO分子中σ键与π键个数比为2∶1
9.( )由前10号元素组成的物质T和X,有如图所示的转化关系。X不稳定,易分解。设N 为阿伏加
A
德罗常数的值,下列有关说法正确的是( )
A.为使该转化成功进行,Y可以是酸性KMnO 溶液
4
B.等物质的量的T、X分子中含有π键的数目均为N
A
C.X分子中含有的σ键个数是T分子中含有的σ键个数的2倍
D.T分子中只含有极性键,X分子中既含有极性键又含有非极性键
10.( )有三种物质AC 、B C 、AD ,在常温下分别为气体、固体和液体。元素A的最高正价和最低
2 2 2 4
负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B C ;
2 2
元素D的负一价阴离子的电子层结构与氩原子相同。则:(1)A、B、C、D元素的名称分为 、 、 、 。
(2)AD 分子中含有的σ键类型为 (填“s-s”“s-p”或“p-p”)σ键。
4
(3)D的负一价阴离子的电子排布式为 ,B C 属于 (填“离子”或“共价”)化合物。
2 2
基础过关练
1.D 2.D 3.B 4.A 5.C 6.C 7.A 8.C
9.C 10.D 11.D
1.D 共价键的成因是当成键原子相互靠近时,原子轨道发生重叠,自旋状态相反的未成对电子形成共
用电子对,两原子核间的电子云密度增大,体系的能量降低。
特别提醒 (1)s轨道与s轨道形成σ键时,电子并不是只在两核间运动,只是在两核间出现的概率增大。
(2)形成共价键的两种元素电负性差值较小,一般电负性差值小于1.7。如H(2.1)与Cl(3.0),电负性差值
为0.9,二者形成共价键。
(3)形成共价键时,成键的两个原子的原子核都吸引共用电子对,使之处于平衡状态,体系能量降低。
2.D 一般地,原子的未成对电子一旦配对成键,就不再与其他原子的未成对电子配对成键了,故共价键
的饱和性由原子的未成对电子数决定,共价键的饱和性也就决定了各种原子形成分子时相互结合的数
量关系,故A、C正确,D错误;形成共价键时,原子轨道重叠的程度越大,共价键越稳定,原子轨道都有一
定的形状,要达到最大重叠,共价键必然有方向性,故B正确。
3.B 三硫化四磷分子中没有不饱和键,且各原子的最外层均已达到了8电子的结构,P可形成3个共
价键,S可形成2个共价键,因此一个三硫化四磷分子中含有的共价键个数为3×4+2×3=9。
2
4.A S原子有两个未成对电子,根据共价键的饱和性,形成的氢化物为H S,A项对;H O能结合1个
2 2
H+形成H O+,不能说明共价键不具有饱和性,B项错;H 分子中的H—H键没有方向性,C项错;两个原子
3 2
轨道发生重叠后,电子只是在两核之间出现的概率大,D项错。
5.C 氢气分子中只存在σ键,故A错误;氯气分子中只存在σ键,故B错误;氮气分子的结构式为
,1个分子中存在1个σ键和2个π键,故C正确;氯化氢分子中只存在σ键,故D错误。
6.C CH 中只存在C—H键,仅含σ键;HCl中只存在H—Cl键,仅含σ键;CH CH 中含C—H键和
4 2 2
键,C—H键为σ键, 键中既有σ键又有π键;F 中只含F—F键,仅含σ键。
27.A A项,σ键属于共价键;B项,s-s σ键与s-p σ键都属于σ键,对称性相同;C项,分子中含有共价键,则
至少含有一个σ键;D项,一般π键容易断裂,而σ键不易断裂,所以含有π键的化合物与只含σ键的化
合物的化学性质不同。
8.C 根据电子排布式可知四种原子分别是S、N、Na、C,其中Na是活泼金属,在化学反应中易失去
最外层的一个电子,形成离子键,而π键是共价键的一种,S、N、C均能形成π键。
9.C A项,H 分子中两个原子的1s轨道重叠,正确;B项,HCl分子中氢原子的1s轨道和氯原子的3p轨
2
道重叠,正确;C项,Cl 分子中两个氯原子的3p轨道重叠,错误;D项,ClF分子中氯原子的3p轨道和氟原
2
子的2p轨道重叠,正确。
10.D 一个N 分子中有一个σ键,两个π键;一个C H 分子中有五个σ键,一个π键;一个C H 分子中
2 2 4 2 2
有三个σ键,两个π键;HCl、H O、H O 分子中只有σ键。
2 2 2
11.D 一般σ键比π键更稳定,A项错误;s-s σ键无方向性,B项错误;原子轨道以“头碰头”方式相互
重叠形成的共价键为σ键,C项错误;两个原子之间形成共价键时,单键为σ键,双键和三键中都只有一
个σ键,D项正确。
特别提醒 π键原子轨道重叠程度比σ键小,一般π键没有σ键牢固,在反应中比较活泼。
12.答案 (1)②s-p σ HCl ③p-p σ Cl ④p -p π N ⑤p -p π N (2)7 3
2 z z 2 y y 2
解析 (1)①②③为原子轨道“头碰头”重叠形成σ键,④⑤为原子轨道“肩并肩”重叠形成π键。(2)
单键都是σ键, 键中含1个π键, 键中含1个σ键,2个π键;由分子结构可知有7个σ键,3
个π键。
能力提升练
1.B 2.A 3.A 4.C 5.A 6.BD 7.D 8.D
9.A
1.B A项,H 中的σ键是两个氢原子的s轨道重叠而成的;B项,HCl中的σ键是氢原子的s轨道和氯原
2
子的p轨道重叠而成的;C项,Cl 中的σ键是两个氯原子的p轨道以“头碰头”方式重叠而成的;D
2
项,F 中的σ键是两个氟原子的p轨道以“头碰头”方式重叠而成的。
22.A 由共价键的饱和性可知:C、Si均形成4个共价键,H、Cl均形成1个共价键,N形成3个共价
键,O、S均形成2个共价键。A项中O原子间是双键,且每个氧原子与1个氢原子形成1个单键,则每
个氧原子形成3个共价键,与其饱和性不相符。
3.A 烷烃分子中只有C—C键和C—H键,1个C H 分子中含有(n-1)个C—C键和(2n+2)个C—H键,
n 2n+2
因此1 mol C H 分子中含有(3n+1)mol共价键,A正确;Na O 中Na+与O2-、Na O中Na+与O2-数目之
n 2n+2 2 2 2 2
比均为2∶1,但Na O 中有共价键而Na O中无共价键,B错误;NH Cl等铵盐中有离子键,C错误;电负
2 2 2 4
性之差小于1.7的Na与H、K与H之间均形成离子键,D错误。
4.C 电子云重叠说明电子在核间出现的概率增大,A正确;两个H原子之间形成s-s σ键,B、D正确;电
子云是对核外电子运动状态的形象化描述,并不是指电子呈云雾状,原子间通过共用电子对(即电子云
重叠)形成共价键,C不正确。
5.A A项,NH HCO 分解生成NH 、CO 和水,是化学变化,碳酸氢根离子和铵根离子之间的离子键被
4 3 3 2
破坏,碳酸氢根离子中的共价键被破坏,故A符合题意;B项,氯化钠颗粒被粉碎,是物理变化,化学键没
有被破坏,再者氯化钠中不存在共价键,故B不符合题意;C项,碘的升华是物理变化,共价键没有被破坏,
故C不符合题意;D项,NaOH溶于水发生电离,钠离子和氢氧根离子之间的离子键被破坏,氢氧根离子
内的共价键没有被破坏,故D不符合题意。
6.BD NH Cl、(NH ) SO 均是由非金属元素组成的,却存在离子键,A项错误。H、Cl等原子中只有
4 4 2 4
一个未成对电子,因而只能形成σ键,即有σ键不一定有π键;若形成π键则原子间一定已形成σ键,即
有π键一定有σ键,B项正确。共价双键中有一个为σ键,另一个为π键,共价三键中有一个为σ键,另
两个为π键,故乙炔( )分子中有3个σ键、2个π键,C项错误。共价单键为σ键,乙烷的
结构式为 ,其中所含的6个C—H键和1个C—C键均为σ键,D项正确。
7.D N—N键是非极性键,A项不正确;1个X分子中存在12对共用电子对、11个σ键,B、C项均不
正确;X分子中只有共价键,故X是共价化合物,D项正确。
8.D 在双键中,σ键比单个的π键电子云重叠程度大,更加稳定,A正确;CO与N 每个分子中σ键都是
2
1个,π键都为2个,B正确;共价单键为σ键,双键中含有1个σ键和1个π键,三键中含有1个σ键和2个π键,则两个原子形成共价键时至少有1个σ键,C正确;1个HCHO分子中含有2个单键和一个双键,
则σ键与π键个数之比为3∶1,D错误。
9.A 由题图可知,T为HCHO,X不稳定,易分解,则X为H CO ,Y为氧化剂,可以选择酸性KMnO 溶
2 3 4
液,A项正确;等物质的量并不一定是1 mol,B项错误;1个X分子中含有的σ键个数为5,1个T分子中
含有的σ键个数为3,C项错误;T、X分子中均只含有极性键,无非极性键,D项错误。
10.答案 (1)碳 钠 氧 氯 (2)p-p (3)1s22s22p63s23p6 离子
解析 (1)火焰呈黄色,说明有钠元素,则淡黄色固体为Na O ,所以元素B为Na,元素C为O。由“元素
2 2
D的负一价阴离子的电子层结构与氩原子相同”知,D为Cl。由“元素A的最高正价和最低负价的绝
对值相等”,可知A为ⅣA族元素,又由于常温下AC 是气体,AD 是液体,所以AC 是二氧化碳(ⅣA
2 4 2
族元素中Si及其以下元素形成的氧化物常温下均为固体),AD 是CCl ,即A是C(碳)。(2)CCl 中只有
4 4 4
σ键,且其类型为p-p σ键。