文档内容
第一章 物质及其变化
第 2节 离子反应
2.1 电解质的电离
“电解质的电离 离子反应”是高中化学必修课程中概念原理类的内容,是高中一年级全体学
生都要学习的重点知识。该内容教学可安排两课时。第1课时的重点是:形成认识化学反应的微观
视角,认识酸、碱、盐等电解质在水溶液中或熔融状态下能发生电离,构建酸碱盐的概念。课时 2
的重点是:通过实验事实认识离子反应及其发生的条件,通过书写离子方程式认识化学反应的本质。
1、教学目标
(1) 通过溶液能否导电的实验认识生活中和化学中的导电现象。
(2) 通过导电和不导电的现象将化合物再次进行分类,建立电解质的概念。
(3) 通过NaCl溶液(或熔融)导电实验的认识,初步建立电离过程的认识
模型。
(4) 通过对酸碱盐的电离过程的认识,构建酸碱盐的概念,纠偏迷思概念。
2、评价目标
(1) 通过对导电现象的交流与点评,诊断并发展学生实验探究的水平(定性
水平、定量水平)。
(2) 通过对具体电解质和非电解质的判断和分析,诊断并发展学生对电解质
概念的认识进阶水平(内涵角度、外延角度)。
(3) 通过对具体电解质电离过程的交流和分析,诊断并发展学生对导电本质
原因的认知进阶水平(物质水平,微粒水平)。
(4) 通过对酸碱盐的电离过程分析和交流,诊断并发展学生对酸碱盐概念的
认识水平(感性认识、理性认识)。
重点:1.电解质
2.电离方程式
难点:电离概念的形成过程印发学案,准备演示实验器材药品、制作多媒体课件
【引入】在我们学习过的化学反应中,有许多是在水溶液中进行的,如酸碱盐之间的反应,那么酸
碱盐溶于水后发生什么变化?水溶液中这些物质之间的反应有什么特点呢?
【板书】一、电解质的电离
【创设情境】生活常识告诉我们,给电器设备通电时,湿手操作容易发生触电事故,这是为什么?
【实验探究】实验1-2
【投影】导电性实验
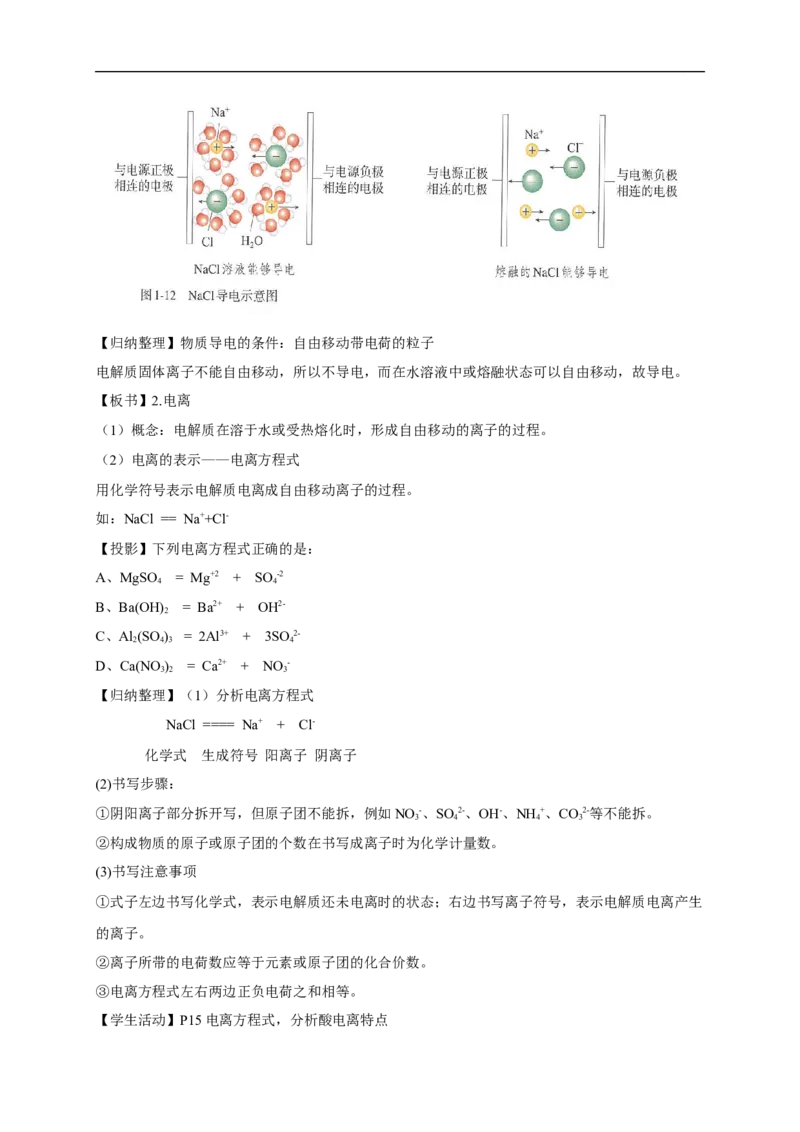
【归纳整理】干燥的氯化钠、硝酸钾等固体不导电,而他们的水溶液或熔融状态下导电,我们把这
些物质称为电解质。
【板书】1.电解质:在水溶液中或熔融状态下能够导电的化合物。
【投影展示】上述状态下不导电的化合物是非电解质。
例如:HSO 、NaOH、KNO 等,都是电解质。
2 4 3
酸、碱、盐、部分金属氧化物和水是电解质。
酒精、苯、二氧化碳等是非电解质
【归纳整理】
混合物 电解质 :酸、碱、盐、水、活泼金属氧化物
物质 化合物
纯净物 非电解质:乙醇、蔗糖等大部分有机物
单质
既不是电解质,也不是非电解质
【思考讨论】(1)铁丝和盐酸能导电,所以二者是电解质,液态硫酸不导电,所以硫酸是非电解质,
对吗?并分析。
(2)1 mol/L的NaCl溶液和1 mol/L的FeCl 溶液的导电能力相同吗?
3
(3)SO 属于化合物,溶于水也能导电,SO 属于电解质吗?
2 2
【归纳整理】①单质、混合物既不是电解质,也不是非电解质。电解质、非电解质都是化合物。
②电解质导电须有外界条件:水溶液或熔融状态。
③电解质因本身离解成自由离子而导电。某些化合物,像SO 、CO、NH ,它们的水溶液虽能导电,
2 2 3
但它们不是电解质。
④某些难溶于水的化合物。如BaSO 、AgCl等,由于它们的溶解度太小,难测其水溶液的导电性,
4但这些难溶于水的化合物和部分金属的氧化物,它们在熔融状态都是能够导电的,所以是电解质
⑤酸、碱、大多数盐、活泼金属的氧化物(NaO 、Al O )都是电解质;除电解质外的化合物都是
2 2 3
非电解质,如大多数有机物和非金属氧化物等。
【学生活动】解决情境问题
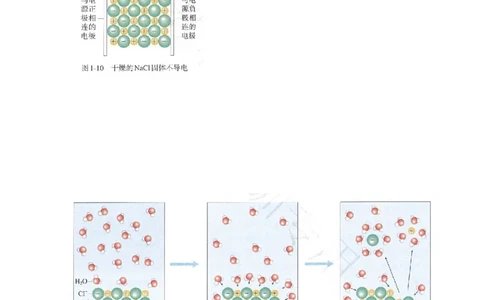
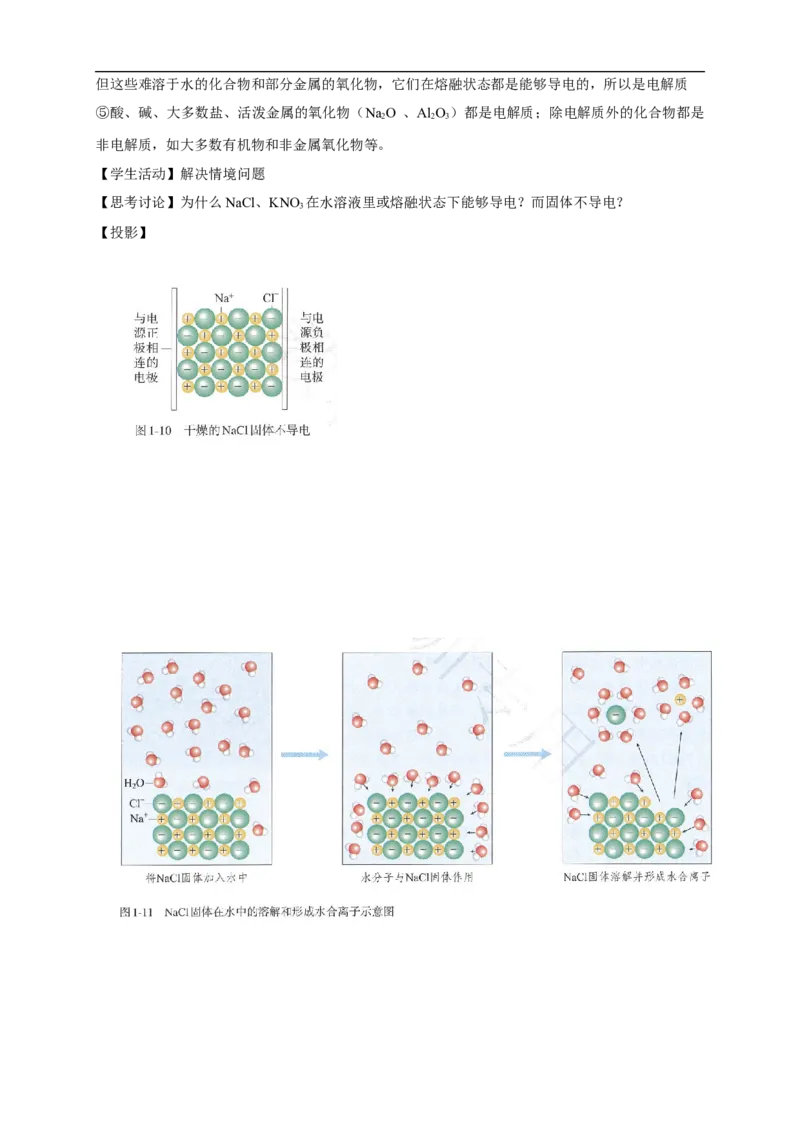
【思考讨论】为什么NaCl、KNO 在水溶液里或熔融状态下能够导电?而固体不导电?
3
【投影】【归纳整理】物质导电的条件:自由移动带电荷的粒子
电解质固体离子不能自由移动,所以不导电,而在水溶液中或熔融状态可以自由移动,故导电。
【板书】2.电离
(1)概念:电解质在溶于水或受热熔化时,形成自由移动的离子的过程。
(2)电离的表示——电离方程式
用化学符号表示电解质电离成自由移动离子的过程。
如:NaCl == Na++Cl-
【投影】下列电离方程式正确的是:
A、MgSO = Mg+2 + SO -2
4 4
B、Ba(OH) = Ba2+ + OH2-
2
C、Al (SO ) = 2Al3+ + 3SO 2-
2 4 3 4
D、Ca(NO ) = Ca2+ + NO -
3 2 3
【归纳整理】(1)分析电离方程式
NaCl ==== Na+ + Cl-
化学式 生成符号 阳离子 阴离子
(2)书写步骤:
①阴阳离子部分拆开写,但原子团不能拆,例如NO -、SO 2-、OH-、NH +、CO2-等不能拆。
3 4 4 3
②构成物质的原子或原子团的个数在书写成离子时为化学计量数。
(3)书写注意事项
①式子左边书写化学式,表示电解质还未电离时的状态;右边书写离子符号,表示电解质电离产生
的离子。
②离子所带的电荷数应等于元素或原子团的化合价数。
③电离方程式左右两边正负电荷之和相等。
【学生活动】P15电离方程式,分析酸电离特点【板书】3.酸:电离时生成的阳离子全部是H+的化合物。
【思考讨论】P15
【归纳整理】碱:电离时生成的阴离子全部是OH-的化合物。
【课堂小结】1.电解质:在水溶液里或熔融状态下能够导电的化合物。
非电解质:在水溶液里和熔融状态下均不导电的化合物。
2电离及电离方程式
3. 酸、碱的实质。
1、定性:从质的方面分析事物,把握研究对象的本质,经过分析综合、比较、抽象和概括,
揭示事物间的相互关系;
定量:分析一个研究对象所包含的数量关系或具备性质间的数量关系,研究结果用“数量”加
以描述。
2、概念都有内涵和外延,即其涵义和适用范围。认知过程包括,感性认识和理性认识。
3、学生在学习本节内容时,缺乏对导电的认识。生活中导电的实际例子不多,导致学生无法
清晰的认识导电,同时由于知识的欠缺,导致学生无法从微观角度认识导电的原因,这是在讲解过
程中出现的一个障碍,因此需要设计相应的实验让学生认识溶液能导电的事实,也应设计相应的环
节让学生从微观的角度认识导电的本质。