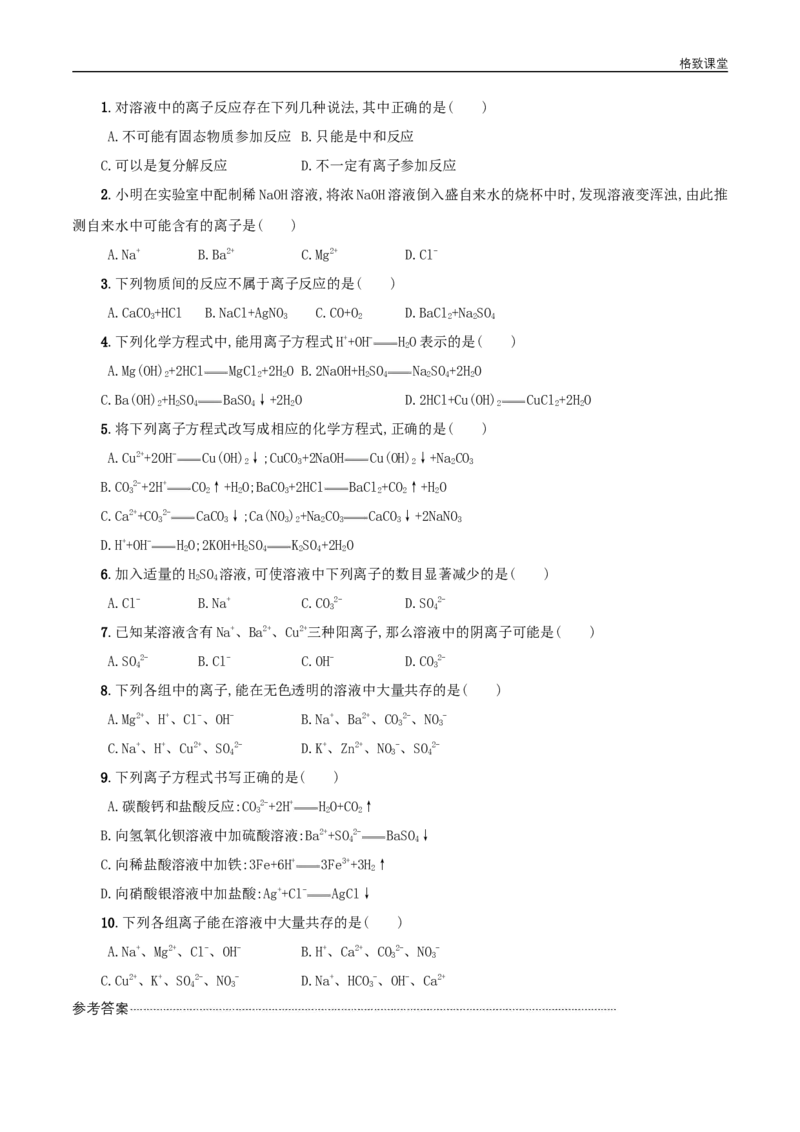文档内容
格致课堂
第一章 物质及其变化
第 2节 离子反应
2.2 离子反应
1.了解离子反应的本质。
2.正确书写离子方程式。
3.初步掌握离子共存的判断方法。
重点:1.离子反应的含义及其发生的条件
2.离子方程式的书写
难点:离子方程式的书写
复分解反应及发生条件
二、离子反应
1.定义: 。
【实验探究】
实验 向盛有2mL Na SO 稀溶液的试管中加入2mL BaCl 稀溶液,观察现象并分析。
2 4 2
分析
现象
NaSO 和BaCl 的电离方程
2 4 2 混合前两种溶液中离子 混合后溶液中离子
式
原因
【交流·研讨1】
BaCl 溶液与CuSO 溶液混合后发生了怎样的反应?
2 4
现象分析:
(1)混合前,溶液中各存在哪些离子?格致课堂
(2)混合后,宏观上看到什么现象?
(3)发生反应的化学方程式是 。
(4)反应的实质是 。
2.离子方程式
定义: 。
【交流·研讨2】
如何正确书写一个离子反应的离子方程式呢?
书写四步: 。
。
。
。
【练习】
1.完成下列离子方程式:
(1)CuSO+NaOH——
4
(2)CaCO+HCl——
3
(3)CuO+HNO——
3
(4)CO+NaOH——
2
(5)Fe+CuSO——
4
2.请写出①稀硫酸和氢氧化钠溶液;②稀硝酸和氢氧化钾溶液反应的化学方程式和离子方程式。
【小结】离子反应发生的条件:
随堂检测格致课堂
1.对溶液中的离子反应存在下列几种说法,其中正确的是( )
A.不可能有固态物质参加反应 B.只能是中和反应
C.可以是复分解反应 D.不一定有离子参加反应
2.小明在实验室中配制稀NaOH溶液,将浓NaOH溶液倒入盛自来水的烧杯中时,发现溶液变浑浊,由此推
测自来水中可能含有的离子是( )
A.Na+ B.Ba2+ C.Mg2+ D.Cl-
3.下列物质间的反应不属于离子反应的是( )
A.CaCO+HCl B.NaCl+AgNO C.CO+O D.BaCl+NaSO
3 3 2 2 2 4
4.下列化学方程式中,能用离子方程式H++OH- HO表示的是( )
2
A.Mg(OH)+2HCl MgCl+2HO B.2NaOH+HSO NaSO+2HO
2 2 2 2 4 2 4 2
C.Ba(OH)+HSO BaSO↓+2HO D.2HCl+Cu(OH) CuCl+2HO
2 2 4 4 2 2 2 2
5.将下列离子方程式改写成相应的化学方程式,正确的是( )
A.Cu2++2OH- Cu(OH)↓;CuCO+2NaOH Cu(OH)↓+NaCO
2 3 2 2 3
B.CO2-+2H+ CO↑+HO;BaCO+2HCl BaCl+CO↑+HO
3 2 2 3 2 2 2
C.Ca2++CO2- CaCO↓;Ca(NO)+NaCO CaCO↓+2NaNO
3 3 3 2 2 3 3 3
D.H++OH- HO;2KOH+HSO KSO+2HO
2 2 4 2 4 2
6.加入适量的HSO 溶液,可使溶液中下列离子的数目显著减少的是( )
2 4
A.Cl- B.Na+ C.CO2- D.SO2-
3 4
7.已知某溶液含有Na+、Ba2+、Cu2+三种阳离子,那么溶液中的阴离子可能是( )
A.SO2- B.Cl- C.OH- D.CO2-
4 3
8.下列各组中的离子,能在无色透明的溶液中大量共存的是( )
A.Mg2+、H+、Cl-、OH- B.Na+、Ba2+、CO2-、NO-
3 3
C.Na+、H+、Cu2+、SO2- D.K+、Zn2+、NO-、SO2-
4 3 4
9.下列离子方程式书写正确的是( )
A.碳酸钙和盐酸反应:CO2-+2H+ HO+CO↑
3 2 2
B.向氢氧化钡溶液中加硫酸溶液:Ba2++SO2- BaSO↓
4 4
C.向稀盐酸溶液中加铁:3Fe+6H+ 3Fe3++3H↑
2
D.向硝酸银溶液中加盐酸:Ag++Cl- AgCl↓
10.下列各组离子能在溶液中大量共存的是( )
A.Na+、Mg2+、Cl-、OH- B.H+、Ca2+、CO2-、NO-
3 3
C.Cu2+、K+、SO2-、NO- D.Na+、HCO-、OH-、Ca2+
4 3 3
参考答案格致课堂
学习过程
二、1.有离子参加或生成的反应
【实验探究】
实验 向盛有2mL Na SO 稀溶液的试管中加入2mL BaCl 稀溶液,观察现象并分析。
2 4 2
分析
现象
NaSO 和BaCl 的电离方程
2 4 2 混合前两种溶液中离子 混合后溶液中离子
式
NaSO=2Na++SO2- Na+ Cl-
2 4 4
白 色
Na+ 、Ba2+ SO 2- Cl-
沉淀 4
BaCl =Ba2++2Cl-
2
化学反应方程式是 NaSO + BaCl == BaSO ↓+ 2NaCl
2 4 2 4
原因
反应的实质是 Ba2++ SO 2-==BaSO ↓
4 4
【交流·研讨1】
(1)Cu2+、SO2—、Ba2+、Cl-。
4
(2)有白色沉淀生成。
(3)CuSO+BaCl BaSO↓+CuCl
4 2 4 2
(4)Ba2++SO2— BaSO↓
4 4
2.用实际参加反应的离子的符号来表示离子反应的式子
【交流·研讨2】
一写:写出正确的化学方程式
二拆:把易溶于水、易电离的物质拆写成离子形式,难溶于水、难电离的物质(如水)以及气体、单质、
氧化物等用化学式表示
三删:删去方程式两边不参加反应的离子
四查:是否符合质量守恒、是否符合电荷守恒、是否符合客观事实、离子的改写是否正确
【练习】
1.(1)Cu2++2OH- Cu(OH)↓
2
(2)2H++CaCO Ca2++HO+CO↑
3 2 2
(3)2H++CuO Cu2++HO
2
(4)2OH-+CO CO2-+HO
2 3 2
(5)Fe+Cu2+ Fe2++Cu
2.HSO+2NaOH NaSO+2HO
2 4 2 4 2
OH-+H+ HO
2
KOH+HNO KNO+HO
3 3 2格致课堂
OH-+H+ HO
2
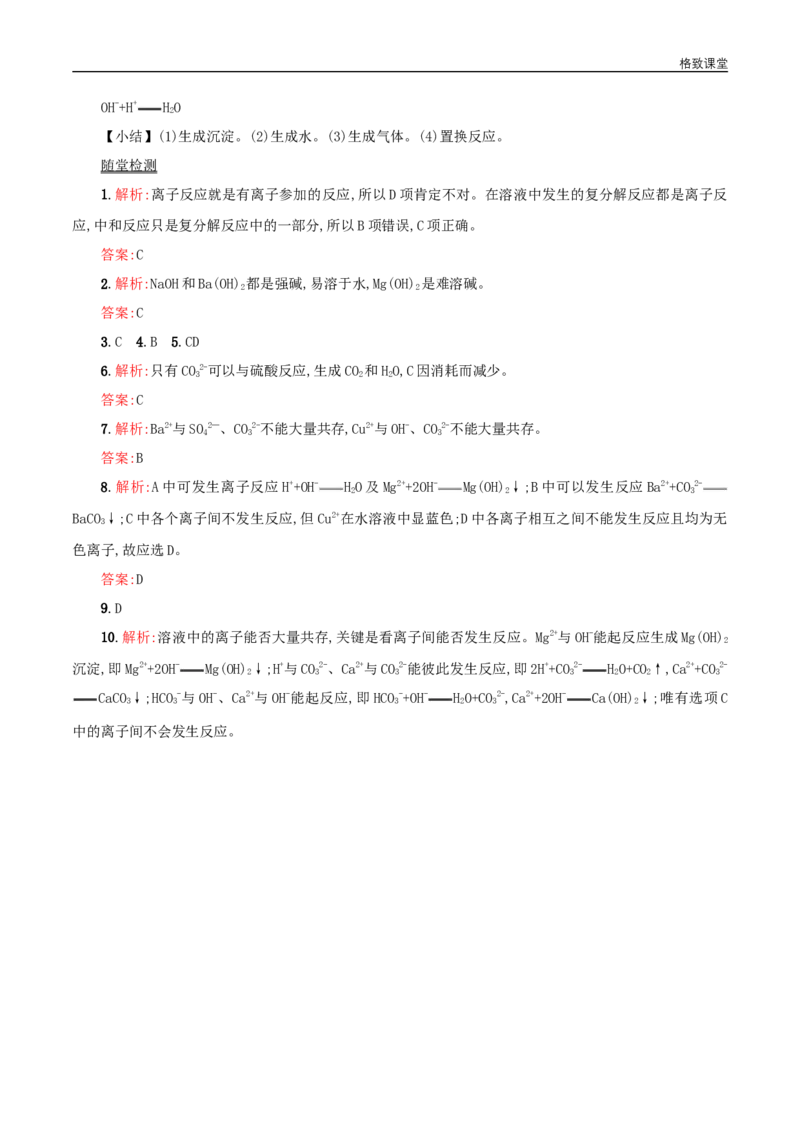
【小结】(1)生成沉淀。(2)生成水。(3)生成气体。(4)置换反应。
随堂检测
1.解析:离子反应就是有离子参加的反应,所以D项肯定不对。在溶液中发生的复分解反应都是离子反
应,中和反应只是复分解反应中的一部分,所以B项错误,C项正确。
答案:C
2.解析:NaOH和Ba(OH) 都是强碱,易溶于水,Mg(OH) 是难溶碱。
2 2
答案:C
3.C 4.B 5.CD
6.解析:只有CO2-可以与硫酸反应,生成CO 和HO,C因消耗而减少。
3 2 2
答案:C
7.解析:Ba2+与SO2—、CO2-不能大量共存,Cu2+与OH-、CO2-不能大量共存。
4 3 3
答案:B
8.解析:A中可发生离子反应H++OH- HO及Mg2++2OH- Mg(OH)↓;B中可以发生反应Ba2++CO2-
2 2 3
BaCO↓;C中各个离子间不发生反应,但Cu2+在水溶液中显蓝色;D中各离子相互之间不能发生反应且均为无
3
色离子,故应选D。
答案:D
9.D
10.解析:溶液中的离子能否大量共存,关键是看离子间能否发生反应。Mg2+与OH-能起反应生成Mg(OH)
2
沉淀,即Mg2++2OH- Mg(OH)↓;H+与CO2-、Ca2+与CO2-能彼此发生反应,即2H++CO2- HO+CO↑,Ca2++CO2-
2 3 3 3 2 2 3
CaCO↓;HCO-与OH-、Ca2+与OH-能起反应,即HCO-+OH- HO+CO2-,Ca2++2OH- Ca(OH)↓;唯有选项C
3 3 3 2 3 2
中的离子间不会发生反应。